Какими препаратами лечат цитомегаловирус у ребенка
ЦИТОМЕГАЛОВИРУС (CMV/ЦМВ)
• ЧТО ТАКОЕ ЦМВ?
• КАК ЛЕЧАТ ЦМВ?
• МОЖНО ЛИ ЧТО-ТО СДЕЛАТЬ ДЛЯ ПРОФИЛАКТИКИ ЦМВ?
• КАК МНЕ ВЫБРАТЬ ЛЕЧЕНИЕ ОТ ЦМВ?
• ИТОГ
Как лечат ЦМВ?
Первые методы лечения ЦМВ требовали ежедневных внутривенных инъекций. У большинства людей был постоянный медицинский катетор, вставленный в ключицу или руку. Людям приходилось принимать лекарства против ЦМВ всю жизнь.
Способы лечения ЦМВ невероятно улучшились за последние несколько лет. Сейчас существует семь видов лечения, одобренных Управлением по контролю за продуктами и лекарствами (FDA, США).
Сильные антиретровирусные препараты (АРВ) могут улучшить иммунную систему. Пациенты могут прекратить прием лекарств от ЦМВ, если уровень CD4 клеток у них поднимается от 100 до 150 и держится на этом уровне (и выше) в течение трех месяцев. Однако, есть два особых случая:
1. Синдром иммунного восстановления может вызвать воспаление в глазах людей, инфицированных ВИЧ, даже если у них раньше и не было ЦМВ. Стандартный способ лечения –добавить препарат от ЦМВ к схеме АРВ препаратов пациента.
2. Если уровень CD4 падает ниже 50, риск возникновения заболевания вызванного ЦМВ значительно возрастает.
Можно ли что-то сделать для профилактики ЦМВ?
Ганцикловир был одобрен для предупреждения (профилактики) ЦМВ. Однако, многие врачи не прописывают его. Они не хотят прибавлять до 12 капсул ежедневно к схеме своих пациентов. Кроме того, не очевидно то, что это приносит пользу. Два больших исследования пришли к разным выводам. В конце концов, АРВ препараты поддерживают уровень CD4 клеток у большинства людей на уровне, которого достаточно, чтобы не заболеть ЦМВ.
Как мне выбрать лечение от ЦМВ
Есть несколько проблем, которые необходимо рассмотреть выбирая лечение от заболевания, вызванного ЦМВ:
Ваше зрение под угрозой?
Возможно вам придется предпринять быстрые действия, чтобы спасти свое зрение
Насколько оно (лечение) эффективно?
Внутривенное введение ганцикловира –наиболее эффективное из всех видов лечения ЦМВ. Имплантанты очень эффективны для остановки воспаления сетчатки. Однако, они действуют только в том глазу, куда были имплантированы.
Какова форма применения?
Таблетки наиболее легкий способ. Внутривенные уколы подразумевают иголки или катетор, в который могут проникнуть инфекции (. ). Глазные инъекции означают введение иглы прямо в глаз. Для того чтобы вставить имплантанты, которые действуют от 6 до 8 месяцев, нужна операция длительностью примерно час.
Это местная или системная терапия?
Местная терапия действует только на глаза. При ЦМВ воспаление сетчатки может прогрессировать стремительно и привести к слепоте. Именно поэтому, при первых же признаках появления, его начинают лечить очень агрессивно. С помощью новейших инъекций и имплантантов лекарство помещается прямо в глаз и оказывает наиболее сильное воздействие на ретинит.
ЦМВ также может проявиться в других частях организма. Чтобы контролировать ЦМВ во всем организме, вам нужна системная (общая) терапия. Это могут быть внутривенные инъекции или таблетки вальганцикловира.
Каковы побочные эффекты?
Некоторые препараты против ЦМВ могут повредить вашим почкам или костному мозгу. В таком случае могут понадобиться дополнительные препараты. Они вводятся с помощью капельницы, что может занять долгое время. Обсудите побочные эффекты лечения ЦМВ со своим врачом.
А что говорят рекомендации (директивы)?
Недавно несколько изданий рекомендаций для профессионалов рекомендовали вальганцикловир в качестве предпочтительного лечения для пациентов, у которых не стоит риск немедленной потери зрения.
ИТОГ
Прием АРв препаратов, вероятно, лучший способ предотвратить появление ЦМВ. Если ваш уровень CD4 ниже 100, поговорите со своим врачом о профилактике ЦМВ и регулярном глазном тестировании. Если у вас низкий уровень CD4 и вы испытываете любые проблемы со зрением, немедленно обратитесь по этому поводу к своему врачу!
Лекарство, вводимое непосредственно в глаз позволяет контролировать развитие воспаления сетчатки, вызванного ЦМВ. С учетом появления новейших лекарств для лечения ЦМВ, вы можете избежать ежедневных уколов и вставленных катеторов.
Большинство людей могут совершенно спокойно прекратить прием препаратов от ЦМВ, если уровень их CD4 клеток поднялся со 100 до 150 при приеме АРВ –терапии.
Методы лечения цитомегаловируса у детей и взрослых
Цитомегаловирусная инфекция относится к семейству герпесвирусов. Заболевание протекает латентно у здоровых людей, но весьма опасно для пациентов с иммунодефицитом (ВИЧ-инфицированных, принимающих иммуносупрессоры после трансплантации органов и тканей). Врожденная цитомегаловирусная инфекция может привести к серьезным патологиям и даже смерти. После инфицирования вирус остается в организме на протяжении всей жизни и способен к реактивации в любое время, что может вызвать развитие мукоэпидермоидной карциномы и других злокачественных образований. Вот почему так важно своевременно сдать анализ крови на антитела к цитомегаловирусу во время беременности.
Причины и симптомы заболевания
Заражение происходит при непосредственном контакте с носителем инфекции или больным через различные биологические жидкости: кровь, сперму, слюну, влагалищные выделения, мочу, грудное молоко. Еще один путь передачи инфекции – от матери к плоду во время беременности. При инфицировании плода может развиться врожденная цитомегалия.
У пациентов с нормальным иммунитетом ЦМВ-инфекция через 30-60 суток после заражения часто проявляется мононуклеозоподобным синдромом. Могут отмечаться слабость, лихорадка, боль в мышцах. После выработки антител против вируса симптомы заболевания исчезают, но вирус остается в организме в неактивной форме.
У пациентов с ослабленным иммунитетом цитомегаловирусная инфекция вызывает поражение легких, поджелудочной железы, печени, почек и других органов. Внутриутробное инфицирование плода чревато развитием серьезного заболевания – врожденной цитомегалии.
Симптомы цитомегалии:
- увеличение селезенки, печени;
- хориоретинит;
- пневмония;
- тугоухость;
- аномалии развития зубов.
Вирус Эпштейна-Барр тоже относится к семейству герпесвирусов. Симптомы поражения вирусом Эпштейна-Барр у мужчин:
- повышение температуры тела;
- воспаление миндалин;
- увеличение лимфоузлов на шее, затылке, в паховой области.
Что значит положительный цитомегаловирус IgG
Наличие антител IgM к цитомегаловирусу у женщин при отрицательном IgG говорит о недавнем инфицировании и начале развития болезни. Положительный результат анализа на определение антител IgG и IgM свидетельствует об острой стадии заболевания.
Обнаружен цитомегаловирус при беременности – что делать
Как лечить цитомегаловирус? Вирусоносительство и мононуклеозоподобный синдром у пациентов с нормальным иммунитетом обычно не требуют лечения. Терапию назначают при выявлении генерализованных форм инфекции. Поскольку применяемые для лечения цитомегаловируса препараты достаточно токсичные, их назначают только по жизненным показаниям. Для профилактики цитомегаловирусной инфекции, развивающейся на фоне иммунодепрессивной терапии, назначают иммуноглобулин антицитомегаловирусный (один или в сочетании с противовирусным препаратом). Это позволяет предупредить ухудшение состояния и снизить риск летального исхода.
Если обнаружен цитомегаловирус при беременности, то для профилактики передачи вируса плоду проводят десенсибилизирующую и общеукрепляющую терапию. Назначают иммуномодуляторы, витамины. В качестве специфического средства применяют нормальный человеческий иммуноглобулин. Число мертворождений при такой схеме лечения снижается в пять раз. Препараты с выраженным противовирусным действием токсичны, а потому не применяются для лечения ЦМВ-инфекции у беременных.
Лечение цитомегаловируса у детей проводят с использованием специфических иммуноглобулинов и противовирусных препаратов. Эффективным средством для лечения ЦМВ-инфекции признан ганцикловир – пуриновый ациклический нуклеозид. Однако препарат обладает высокой токсичностью, поэтому его не применяют для лечения цитомегаловируса у новорожденных. В других возрастных группах ганцикловир назначают только при непосредственной угрозе жизни ребенка. Применение препарата оправдано при подтвержденном диагнозе и наличии четких показаний.
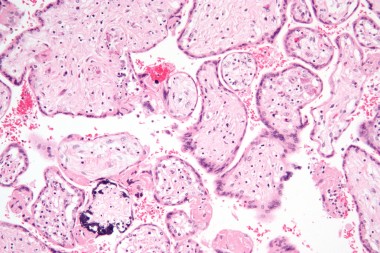
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
И. Я. Извекова 1 , доктор медицинских наук, профессор
М. А. Михайленко
Е. И. Краснова, доктор медицинских наук, профессор
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование

До 80% всех людей на свете инфицированы цитомегаловирусом, но у большинства с ним нет хлопот. Если только речь не идет об иммунодефицитах, беременности и внутриутробном развитии.
Цитомегаловирусная (ЦМВ) инфекция - вирусное заболевание, которое связано с заражением человека цитомегаловирусом. Этот возбудитель относят к герпесвирусам 5 типа, он широко распространен в популяции. 50–80% всех людей в мире инфицированы ЦМВ. Однажды заразившись, человек инфицирован навсегда, но для здоровых это не опасно. Вирус повышает свою активность, только если происходит снижение иммунитета. Это частая ситуация при ВИЧ-инфекции или при приеме иммунодепрессивных (снижающих иммунитет) препаратов.
Если женщина впервые заразилась цитомегаловирусной инфекцией во время беременности, это может привести к серьезной патологии плода.
Причины и факторы риска
Цитомегаловирус передается через близкий физический контакт человека с человеком. Это может происходить через жидкости организма:
- слюну
- кровь (в том числе при переливании крови и трансплантации органов)
- грудное молоко
- семенную жидкость и вагинальный секрет.
Во время беременности заражение происходит через плаценту или непосредственно во время родов.
Инфицирование возможно при поцелуе или при контакте с предметами, на которых есть частички слюны или мочи больного человека. Основная часть людей заражается в детстве, обычно в яслях или детском саду, т.е. там, где есть много контактов между детьми. Реже инфицирование происходит в возрасте 10-35 лет.
Что происходит при ЦМВ
Первая встреча с вирусом чаще всего протекает бессимптомно. Только в 2% случаев отмечают симптомы, похожие на ОРВИ (повышение температуры тела, лихорадка, боль в горле, боли в суставах и мышцах, увеличение лимфатических узлов). У людей с нормальным иммунитетом инфекция обычно не вызывает серьезных осложнений.
Гораздо опаснее врожденная цитомегаловирусная инфекция. Чаще всего беременные женщины получают ЦМВ от больных детей младшего возраста. Различные врожденные патологии диагностируют у 10% детей, инфицированных во время внутриутробного развития. Вирус существенно увеличивает риск преждевременных родов, задержки внутриутробного развития, спонтанного прерывания беременности.
Первичное инфицирование матери во время беременности связано с большим риском для плода (30–50%). В результате 10–15% детей могут иметь нарушения слуха или зрения, судороги, замедление внутриутробного развития, микроцефалию (уменьшение размера мозга). После рождения возможны неврологические симптомы, задержка умственного и физического развития, поражение печени, которое чаще всего проявляется желтухой, увеличение селезенки.
Симптомы ЦМВ
Существует несколько видов патологий, которые вызывает цитомегаловирусная инфекция. У здоровых людей заболевание может себя вообще ничем себя не проявлять и человек может даже не узнать, что заразился. Реже болезнь протекает в виде острой цитомегаловирусной инфекции, по симптомам напоминающей инфекционный мононуклеоз:
- увеличение лимфатических узлов
- температура тела выше 38 градусов
- слабость, утомляемость, отсутствие аппетита
- боль в мышцах и суставах
- сильная боль в горле, воспаление миндалин
- головная боль.
Как правило, выздоровление наступает за 2 недели.
В тяжелых случаях возможны поражение печени, желтуха, боли в грудной клетке, кашель, одышка, диарея, боли в животе.
У больных с иммунодефицитом цитомегаловирусная инфекция протекает более тяжело, так как вирус быстро распространяется по организму и вызывает:
- поражение центральной нервной системы с возможными судорогами, возникновением комы
- тяжелую диарею
- пневмонию, затруднения дыхания
- ретинит (поражение сетчатки)
- гепатит (поражение печени).
У новорожденных, которые внутриутробно заразились ЦМВ, могут быть:
- желтуха
- пневмония
- мелкоточечная пурпурная сыпь
- увеличение печени и селезенки
- низкий вес при рождении
- маленький размер головы.
Диагностика ЦМВ
Заподозрить инфекцию можно по общему анализу крови, где уровень лимфоцитов превышает 50%, и атипичные лимфоциты составляют до десятой части всех этих клеток крови.
Точную диагностику цитомегаловирусной инфекции обычно проводят с помощью анализа биологических жидкостей методом ПЦР (полимеразной цепной реакции) или ИФА (иммуноферментного анализа). Другие способы диагностики, как, например, выращивание культуры ЦМВ, в настоящее время почти не применяют. ПЦР определяет наличие специфических для ЦМВ участков ДНК в образцах слюны, грудного молока и т.д. ИФА позволяет определить антитела к цитомегаловирусу в сыворотке крови. Как правило, оценивают наличие иммуноглобулинов - IgG и IgM. Высокий уровень IgM (иммуноглобулинов класса М) в крови больного обычно свидетельствует о первичном инфицировании. При реактивации вируса количество IgM также может расти, но не так сильно, как в первый раз. Если определяют иммуноглобулины класса G (IgG), то встреча организма с ЦМВ уже не первая; эти антитела остаются на всю жизнь. Их количество может расти при активации вируса. Расшифровка результатов анализов ведется врачом, так как появление специфичных антител к вирусу может отставать от заражения до 4 недель.
Цитомегаловирус относят к группе герпесвирусов, и, если в организме присутствует вирус Эпштейна-Барр (тоже из семейства герпесвирусов), результат может быть ложноположительным.
Для диагностики поражения печени проводят определение уровня билирубина, АСТ, АЛТ.
Лечение
Пациенты с нормальным иммунитетом специфического лечения не требуют. Болезнь проходит самостоятельно, как и ОРВИ, в течение нескольких недель.
Если беспокоит высокая температура, сильная боль в мышцах, то применяют противовоспалительные препараты: парацетамол или ибупрофен. Важно пить большое количество жидкости, это не только уменьшит симптомы болезни, но и позволит избежать обезвоживания.
Пациентам с иммунодефицитами назначают противовирусные препараты. Эти лекарства не могут полностью удалить ЦМВ из организма и вылечить от инфекции, но способны замедлить размножение вируса. Схема лечения цитомегаловирусной инфекции у больных с ослабленной иммунной системой может включать в себя:
- ганцикловир
- валганцикловир
- фоскарнет
- цидофовир (не зарегистрирован в РФ).
Противовирусные препараты имеют побочные эффекты, поэтому лечение требует медицинского контроля. Принимают противовирусные средства не менее 14 дней.
Новорожденных с ЦМВ-инфекцией лечат в специализированных отделениях перинатальных центров, где проводят противовирусную терапию ганцикловиром или валганцикловиром. После выписки таким малышам нужен постоянный контроль зрения и слуха, наблюдение у невролога.
Профилактика ЦМВ
Специфическая профилактика цитомегаловирусной инфекции отсутствует. Эффективной и безопасной вакцины против ЦМВ пока не существует. Вирус передается при половых контактах, поцелуях, совместном использовании столовых приборов, игрушек, зубных щеток. Поэтому соблюдение общих правил гигиены, мытье рук с мылом перед приготовлением еды, после похода в туалет или смены подгузника поможет предотвратить заражение. При контакте с биологическими жидкостями (спермой, мочой) необходимо использовать резиновые перчатки.
Уязвимым группам пациентов - например, принимающим иммунодепрессанты после пересадки органов или беременным - нужно более тщательно соблюдать гигиенические правила. По возможности нужно избегать контакта с маленькими детьми (особенно до 5 лет) и тем более не целовать их, не есть с ними из одной посуды.
Перед трансплантацией органов или переливанием крови проводят исследование ЦМВ-статуса потенциального донора.
Осложнения
Первичное заражение при беременности приводит к нарушению внутриутробного развития, микроцефалии, поражению печени, легких, центральной нервной системы плода. У новорожденных детей с симптомами поражения органов и систем в 30% случаев возможен летальный исход. У 40–90% из них имеются неврологические нарушения (задержка умственного развития, потеря слуха, нарушения зрения, эпилепсия).
У больных с ВИЧ-инфекцией цитомегаловирус может быть причиной следующих осложнений:
- хориоретинит (сочетанное воспаление сосудистой оболочки и сетчатки глаза)
- панкреатит, гепатит, колит
- синдром Гийена-Барре
- энцефалиты
- поражение периферических нервов
- воспаление легких вирусной природы
- поражение сердечной мышцы
- поражение кожи.
Редко осложнения бывают и у здоровых людей. Чаще всего это диарея, боль в животе и мышцах.
Аннотация научной статьи по клинической медицине, автор научной работы — Кочкина Светлана Сергеевна, Ситникова Елена Павловна
Цель исследования оценка эффективности лечения генерализованной цитомегаловирусной инфекции (ЦМВИ) у детей грудного возраста комбинацией ганцикловира и препарата ВИФЕРОН®. Материалы и методы. Пролечено 52 ребенка первых месяцев жизни с генерализованной ЦМВИ. Пациенты распределены на 3 группы: в 1-ю вошли 25 детей, получавших ганцикловир в течение 14-21 дня, затем ИФН-a-2b в комплексе с антиоксидантами витаминами Е и С (ВИФЕРОН®); 2-ю группу составили 17 пациентов, получавших только ганцикловир ; в 3-ю группу включили 1 0 детей, у которых применяли только симптоматическое лечение ЦМВИ: гепатопротекторы, антибиотики широкого спектра действия (цефтриаксон, ампициллины) в возрастных дозировках. Терапию проводили под контролем вирусной нагрузки в сыворотке крови на 14-й и 21-й день от начала лечения . Пациентам 1-й группы при уменьшении клинических проявлений ЦМВИ и снижении вирусной нагрузки до 104-103 копий/мл на 14-21-й день назначали ректальные суппозитории ИФН-a-2b (ВИФЕРОН®) 150 000 МЕ по оригинальной схеме. Результаты. В 1-й группе у всех детей в течение 3-6 мес. происходила элиминация вируса из крови и ликвора. Рецидива ЦМВИ не отмечалось. У детей 2-й группы наблюдалось снижение вирусной нагрузки, но элиминации вируса из крови, ликвора не происходило. У больных 3-й группы вирусная нагрузка оставалась на том же уровне, а у 1 пациента увеличилась на 102 копий/мл. Заключение. Сочетанное использование комбинированной противовирусной терапии ганцикловиром и ИФН-a-2b в комплексе с антиоксидантами витаминами Е и С (ВИФЕРОН®) способствует элиминации вируса из крови и ликвора, переводу и удержанию его в неактивном состоянии, что предотвращает развитие осложнений. Предлагаемый способ лечения ЦМВИ может успешно использоваться в стационарных и в амбулаторных условиях.
Похожие темы научных работ по клинической медицине , автор научной работы — Кочкина Светлана Сергеевна, Ситникова Елена Павловна
The Method of Treatment of Generalized Cytomegalovirus Infection in Infants
Materials and methods. 52 children of the first months of life were treated with generalized CMV. Patients are divided into 3 groups: the first included 25 children who received ganciclovir for 14-21 days, then IFN-a-2b in combination with antioxidants vitamins E and C (VIFERON®); The second group consisted of 1 7 patients receiving only ganciclovir ; in the third group included 1 0 children who had only symptomatic treatment of CMVI: hepatoprotectors, broad-spectrum antibiotics (ceftriaxone, ampicillins) at age dosages. Therapy was carried out under the control of viral load in the blood serum on the 14th and 21 st day from the start of treatment . Patients of the 1 st group with a decrease in the clinical manifestations of CMV and a decrease in the viral load to 1 04-1 03 copies/ml on the 14-21 day were prescribed rectal suppositories of IFN-a-2b (VIFERON®) 150 000 IU according to the original scheme. Results. In the 1 st group, all children during 3-6 months had an elimination of the virus from the blood and liquor. Relapse of CMV was not observed. Children of the second group had a decrease in the viral load was observed, but the elimination of the virus from the blood, the cerebrospinal fluid did not occur. Patients of the 3rd g roup had the viral load remained at the same level, it increased by 1 02 copies/ml at one patient. The conclusion. Using of combined antiviral therapy with ganciclovir and IFN-a-2b in combination with antioxidants vitamins E and C (VIFERON®) promotes elimination of the virus from blood and liquor, transferring and keeping it in an inactive state, which prevents the development of complications. The proposed method for treatment of CMV can be successfully used in inpatient and outpatient settings.
генерализованной цитомегаловирусной инфекции у детей грудного возраста
С. С. Кочкина, Е. П. Ситникова
Цель исследования — оценка эффективности лечения генерализованной цитомегаловирусной инфекции (ЦМВИ) у детей грудного возраста комбинацией ганцикловира и препарата ВИФЕРОН®.
Материалы и методы. Пролечено 52 ребенка первых месяцев жизни с генерализованной ЦМВИ. Пациенты распределены на 3 группы: в 1-ю вошли 25 детей, получавших ганцикловир в течение 14—21 дня, затем — ИФН-а-2Ь в комплексе с антиокси-дантами витаминами Е и С (ВИФЕРОН®); 2-ю группу составили 17 пациентов, получавших только ганцикловир; в 3-ю группу включили 1 0 детей, у которых применяли только симптоматическое лечение ЦМВИ: гепатопротекторы, антибиотики широкого спектра действия (цефтриаксон, ампициллины) в возрастных дозировках. Терапию проводили под контролем вирусной нагрузки в сыворотке крови на 14-й и 21-й день от начала лечения. Пациентам 1-й группы при уменьшении клинических проявлений ЦМВИ и снижении вирусной нагрузки до 104— 103 копий/мл на 14—21-й день назначали ректальные суппозитории ИФН-а-2Ь (ВИФЕРОН®) 150 000 МЕ по оригинальной схеме.
Результаты. В 1-й группе у всех детей в течение 3—6 мес. происходила элиминация вируса из крови и ликвора. Рецидива ЦМВИ не отмечалось. У детей 2-й группы наблюдалось снижение вирусной нагрузки, но элиминации вируса из крови, лик-вора не происходило. У больных 3-й группы вирусная нагрузка оставалась на том же уровне, а у 1 пациента увеличилась на 102 копий/мл.
Заключение. Сочетанное использование комбинированной противовирусной терапии ганцикловиром и ИФН-а-2Ь в комплексе с антиоксидантами витаминами Е и С (ВИФЕРОН®) способствует элиминации вируса из крови и ликвора, переводу и удержанию его в неактивном состоянии, что предотвращает развитие осложнений. Предлагаемый способ лечения ЦМВИ может успешно использоваться в стационарных и в амбулаторных условиях.
Ключевые слова: цитомегаловирусная инфекция, лечение, дети грудного возраста, ИФН-а-2Ь (ВИФЕРОН®), ганцикловир
The Method of Treatment of Generalized Cytomegalovirus Infection in Infants
S. S. Kochkina, E. P. Sitnikova
Yaroslavl State Medical University of the Ministry of Health of Russia, Yaroslavl, Russia
Purpose of the study. Evaluation of the effectiveness of treatment of generalized cytomegalovirus infection (CMVI) in infants with a combination of ganciclovir and
Materials and methods. 52 children of the first months of life were treated with generalized CMV. Patients are divided into 3 groups: the first included 25 children who received ganciclovir for 14—21 days, then — IFN-а^Ь in combination with antioxidants vitamins E and C (VIFERON®); The second group consisted of 1 7 patients receiving only ganciclovir; in the third group included 1 0 children who had only symptomatic treatment of CMVI: hepatoprotectors, broad-spectrum antibiotics (ceftriaxone, ampicillins) at age dosages. Therapy was carried out under the control of viral load in the blood serum on the 1 4th and 21st day from the start of treatment. Patients of the 1 st group with a decrease in the clinical manifestations of CMV and a decrease in the viral load to 1 04—1 03 copies/ml on the 1 4—2 1 day were prescribed rectal suppositories of IFN^-2b (VIFERON®) 1 50 000 IU according to the original scheme.
Results. In the 1 st group, all children during 3—6 months had an elimination of the virus from the blood and liquor. Relapse of CMV was not observed. Children of the second group had a decrease in the viral load was observed, but the elimination of the virus from the blood, the cerebrospinal fluid did not occur. Patients of the 3rd group had the viral load remained at the same level, it increased by 1 02 copies/ml at one patient.
The conclusion. Using of combined antiviral therapy with ganciclovir and IFN^-2b in combination with antioxidants vitamins E and C (VIFERON®) promotes elimination of the virus from blood and liquor, transferring and keeping it in an inactive state, which prevents the development of complications. The proposed method for treatment of CMV can be successfully used in inpatient and outpatient settings. Keywords: cytomegalovirus infection, treatment, infants, IFN^-2b (VIFERON®), ganciclovir
Svetlana S. Kochkina, Ph.D., Associate Professor of the Department of Infectious Diseases, Epidemiology and Pediatric Infections, Yaroslavl State Medical University of the Ministry of Health of Russia; +7 (920) 1 0-67-46; sema7476@mail.ru
Интерес к изучению цитомегаловирусной инфекции (ЦМВИ) не ослабевает последние десятилетия. Это связано с ее широким распространением и поражением иммуносупрессивных групп населения, в том числе беременных женщин, новорожденных и грудных детей. По данным Кистеневой Л.Б. и соавт. (2014), в Москве среди женщин репродуктивного
возраста инфицированность ЦМВ составляет от 87,6 до 91,6% [1]. В настоящее время доказано нейро-тропное, эпителитропное, гепатотропное и кардио-тропное действие цитомегаловируса, что объясняет генерализованный характер заболевания и полиморфизм клинической картины у новорожденных и грудных детей [2, 3].
Следует заметить, что в настоящее время ни один из методов лечения не позволяет полностью избавиться от цитомегаловируса, который при попадании в организм человека остается в нем навсегда. Поэтому целью лечения ЦМВИ является устранение симптомов острой формы заболевания и удержание вируса в неактивном состоянии [1, 4]. В России специфическая терапия ЦМВИ проводится только после верификации диагноза и должна подтверждаться данными клинических, иммунологических, вирусологических исследований.
При этом единые подходы к лечению генерализованных форм ЦМВИ у детей первого года жизни до сих пор отсутствуют. Согласно зарубежным рекомендациям [5, 6], с 2013 года при развитии у новорожденного манифестной врожденной ЦМВИ, протекающей с вовлечением ЦНС и/или органными поражениями, назначается ганцикловир внутривенно капельно из расчета 6 мг/кг каждые 12 часов не менее 42 дней, под контролем гематологических, печеночных и почечных показателей. В дальнейшем при возможности переходят на пе-роральную форму валганцикловира в дозе 16—20 мг/кг каждые 1 2 часов, в течение 6 месяцев. В Белоруссии при выявлении врожденной генерализованной ЦМВИ согласно стандартам лечения назначается ганцикловир в дозе 6 мг/кг каждые 12 часов в течение 21 дня [7].
В России ведущими специалистами перинатальной медицины предложен проект Клинических рекомендаций по диагностике, лечению и профилактике врожденной цитомегаловирусной инфекции, в котором с учетом мирового опыта и прогностической важности этиотроп-ной терапии при врожденной генерализованной ЦМВИ рекомендовано применение ганцикловира или ванган-цикловира [8].
Ганцикловир (Цимевен, CYMEVENE®, F. Hoffmann-La Roche Ltd, Швейцария) — синтетический аналог дезок-сигуанозина, который подавляет размножение вирусов герпеса. Вирусологическое действие ганцикловира обусловлено подавлением синтеза вирусной ДНК двумя путями — конкурентное ингибирование встраивания де-зоксигуанозинтрифосфата в ДНК под действием ДНК-полимеразы и включение ганцикловиртрифосфата в вирусную ДНК, приводящего к прекращению удлинения вирусной ДНК или очень ограниченному ее удлинению. Применение ганцикловира возможно только с 12 лет, назначать препарат детям более раннего возраста рекомендуется в том случае, если польза от лечения превышает существенный риск [9].
Известный метод лечения ЦМВИ цитотектом/неоци-тотектом (антицитомегаловирусным иммуноглобулином человека) [2, 3] является эффективным, но дорогостоящим. Описано при цитомегаловирусной инфекции применение иммуноглобулинов (пентаглобина), а также ацик-ловира внутривенно капельно в дозе 5—10 мг на кг массы тела каждые 8 ч, продолжительность курса составляет 5—10 дней [2], однако элиминации вируса при таком лечении не происходит.
Особый интерес вызывает терапия ЦМВИ интерфе-ронами (ИФН), поскольку противовирусный эффект —
Целью исследования была оценка эффективности лечения генерализованной цитомегаловирусной инфекции у детей грудного возраста комбинацией ганцикловира и препарата ВИФЕРОН® (патент на изобретение № 2602953 от 27 октября 2016 г.).
Материалы и методы исследования
Исследование проводили на базе Инфекционной клинической больницы № 1 г. Ярославля и Областного перинатального центра с 2008 по 2017 гг. Критериями включения пациентов в исследование были возраст до 2 мес., постоянное проживание в Ярославле и Ярославской области, установленный диагноз генерализованной ЦМВИ. В исследование было включено 52 ребенка. Получено информированное согласие родителей на проведение специфической терапии. Диагноз ЦМВИ устанавливали на основании клинико-анам-нестических и лабораторных данных: обнаружения ДНК ЦМВ в сыворотке крови, ликворе, слюне, моче; количественного определения ЦМВ в сыворотке крови методом полимеразной цепной реакции (ПЦР); наличия aнти-ЦМВ IgM, анти-ЦМВ IgG в сыворотке крови методом иммуноферментного анализа (ИФА), результатов биохимического анализа крови (уровень билирубина, АСТ, АЛТ, щелочной фосфатазы). Проводили УЗИ паренхиматозных органов и слюнных желез. Все дети осмотрены специалистами: оториноларингологом, неврологом, при необходимости — гематологом; наблюдались инфекционистом, неонатологом и иммунологом.
Все пациенты взяты в исследование в возрасте до 2 мес., преобладали мальчики — 32 (61,5%), девочек
Лечение и профилактика широкого спектра вирусных и вирусно-бактериальных инфекций (ОРИ, в том числе грипп, герпесвирусные и урогенитальные инфекции, вирусные гепатиты В, С и О).
Разрешен детям с первых дней жизни Оригинальная формула ВИФЕРОН®, соче-
и будущим мамам - с 14 недели тающая интерферон а-2Ь и антиоксиданты,
беременности обеспечивает высокую противовирусную
V Сочетается с другими противовирусными активность препарата и антибактериальными препаратами
Читайте также:
- Как создать вирус как creeper
- Профилактика вирусной инфекции у человека 2020
- Можно ли делать прививку кокав при гриппе
- Гепатит в опасаться нужно
- Тесты на ацетон и на ротавирус
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции

