Интерферон подавляет вирус гриппа

Сегодня постоянно увеличивается арсенал лекарственных средств, используемых при гриппе и ОРВИ, отличающийся разнообразием и охватывающий всевозможные способы влияния на инфекционный процесс. Он включает химиопрепараты этиотропного действия, средства для им-мунокорригирующей, патогенетической и симптоматической терапии (табл. 1.).
Сюда же относятся и антибиотики широкого спектра действия для профилактики постгриппозных бактериальных осложнений [6].
Следует отметить значительный вклад академика АМН СССР А.А. Смородинцева, академиков О.И. Киселева, профессора Н.П. Чижова, а также многих других сотрудников НИИ гриппа СЗО РАМН в разработку противовирусных препаратов и стратегии их применения при ОРВИ и гриппе. Казалось бы, совокупность указанных средств должна существенно снизить заболеваемость ОРВИ и гриппом, но, как считает академик О.И. Киселев, нет оснований быть удовлетворенными результатами клинического применения этих препаратов, поскольку не обеспечивается радикальный эффект, в результате ОРВИ и грипп, продолжают оставаться малоконтролируемыми инфекциями [6].
Основные препараты для лечения и профилактики гриппа и ОРВИ (Киселев О.И. с соавт., 2010)
Группы
лекарственных средств
Блокаторы ионного канала
Специфический шаперон ГА
Ингибиторы NP- белка
Включение синтеза
эндогенных интерферонов
Циклоферон, кагоцел, амиксин
Средства для снятия
Эуфиллин, кленил, аскорил,
беротек, пульмикорт
Адаптогены, витамины С, В, Е, А
Противовирусные препараты - вещества, обладающие антивирусной активностью, представлены этиотропными средствами (химиопрепараты - истинные химические соединения различных классов); патогенетическими лекарственными средствами являются препараты неспецифического действия - интерфероны, их индукторы и частично иммунотропные препараты [4].
Существует несколько способов контроля вирусных инфекций. Неспецифический тип контроля, обеспечиваемый препаратами неспецифического действия (интерфероны, их индукторы и иммунотропные препараты), является наиболее эффективным, его антивирусный спектр очень широкий, но длительность эффекта короткая. Специфический тип контроля обеспечивается вакцинацией против основных заболеваний, согласно национальному календарю прививок, его эффективность и длительность эффекта высокая, но спектр узкий. Химический тип контроля реализуется химиопрепаратами, активность узкая, длительность высокая [6, 17].
Химиопрепараты при лечении заболеваний верхних дыхательных путей
Химиопрепараты являются средством этиотропной терапии заболеваний дыхательных путей, поэтому основным показателем их клинической пригодности служит химиотерапевтический индекс (отношение специфической эффективности к токсичности). К основным недостаткам антивирусных химиопрепаратов относятся узкий спектр действия и формирование резистентных вирусных штаммов, что сводит на нет эффективность терапии. Резистентность обусловлена мутациями в том вирусном белке, который является мишенью действия для препарата. Лекарственная устойчивость является результатом изменений наследственных свойств вирусов и развивается при многократном применении препаратов [5, 14].
Применения только этиотропных средств при повышенной заболеваемости (эпидемии) гриппом и ОРВИ недостаточно, что показал сезон повышенной заболеваемости гриппом 2009/10 гг. (табл. 2).
Максимальный клинический эффект при лечении гриппа и других ОРВИ, не-гриппозной этиологии может быть получен при сочетанном применении химиопрепаратов с препаратами неспецифического действия либо использовании только препаратов патогенетической направленности - интерферонов их индукторов и иммуномодуляторов, обладающих противовирусной активностью.
Эпидемобстановка в России 2009 г.
(по материалам конгресса по инфекционным болезням, 30 марта 2010 г)
Грипп А/H1N1/09 - 35-66,7%
ГриппА/H3N2, H1/N1 - 1% Грипп В - 0,5%; Парагрипп - 0,5%; Аденовирус - 7,2%; РС-вирус - 1,3%
Харитонова В.Ф. (2010)
РС-вирус - 43,1%; Аденовирус - 18,3%; Парагрипп - 31%; РС+парагрипп - 7,9%
Романцов М.Г. (2010),
Вирус гриппа А (H1N1)/09 и H3N2, 14% и 4%; Вирус Парагриппа (11%),
Адено- и РС-вирус (по 4%)
Вопрос о назначении антибиотиков при респираторных инфекциях и гриппе остается спорным. При неосложненных формах респираторных инфекций антибиотики не назначают, поскольку они повышают риск возникновения побочных эффектов и способствуют распространению лекарственной устойчивости. Местное назначение антибактериальных препаратов показано лицам с хроническими заболеваниями (синуситы, риниты, отиты). Респираторные заболевания опасны своими осложнениями, поэтому настороженность врачей при лечении больных гриппом чрезвычайно важна [4, 5, 15].
Роль интерферона и его индукторов при респираторных заболеваниях у детей
Ведущую роль в защите против респираторных вирусов играют интерфероны 1-го и 2-го типа (ИФН-альфа/бета и ИФН - гамма). Неодинаковая способность индуцировать интерферон связана с особенностями иммунопатогенеза детей. Иммунный ответ при ОРВИ реализуется в четырех вариантах, различающихся выраженностью и динамикой неспецифической иммуномодуляции (ответ ФГА в РБТЛ) и уровнем продукции цитокинов (ИФН-альфа/бета и гамма, ИЛ-1 и ТНФ), специфического антителообразования. В периоде выздоровления отмечается прирост ИФН альфа/бета и гамма соответственно на + 3,8 и 6,3 МЕ/мл при снижении исходно повышенного синтеза цитокинов. У детей в возрасте от 1 года до 7 лет синтез главного медиатора клеточной формы иммунного ответа - ИФН-гамма снижен, а период выздоровления сопровождается усиленной его продукцией. Аналогичная тенденция отмечена при индукции ТNF и ИЛ-1, оказывающих цитотоксическое действие на клетки, инфицированные вирусом, ингибируя при этом репродукцию вирусов [5].
В группе часто болеющих детей с атопией предпочтительнее применять индукторы интерферона, поскольку удается избежать дополнительной сенсибилизации, а синтез индуцированного интерферона находится под контролем организма.
У часто болеющих детей, не страдающих бронхиальной астмой, высокая продукция ИЛ-4 сопровождается высокой продукцией ИФН-гамма. В приступном периоде бронхиальной астмы выявлена низкая продукция ИФН-альфа и -гамма, а уже через 3 недели отмечалась выраженная стимуляция продукции интерферона. У часто болеющих детей после очередного ОРВИ наблюдали сочетание высокой продукции ИЛ-4 и интерферона-гамма, уровень последнего был повышен и в периоде ремиссии, а у больных группы сравнения указанные показатели значимо не менялись [11].
В исследованиях Н.В. Минаевой (2006) изучен цитокиновый профиль (ИЛ-1, ИФН-гамма, ИЛ-4) 392 детей дошкольного возраста с аллергической патологией. Отмечено повышение уровня ИЛ-1 в 20 раз выше нормы, отражая сочетание аллергического и инфекционного воспаления. Уровень интерферона гамма составил 58,8 (при колебаниях от 47,5 до 131,4 при норме до 25 пг/мл). Установлена корреляционная связь средней силы между ИЛ-1 и ИФН-гамма (r=0,48). После проведения иммунореабилитационных мероприятий (циклоферон, ацикловир) уровень ИФН-гамма снизился в 1,5 раза, составив 38,3 при норме до 25 пг/мл [12, 13].
Увеличение уровня интерферон-гамма при одновременном снижении уровня ИЛ-4, под влиянием проводимой терапии (циклоферон+гриппозная инактивированная вакцина) с целью профилактики ОРВИ и гриппа указывает на активацию Th1 ответа, являясь благоприятным фактором для прогноза заболевания.
Е.А. Лыкова, с соавт. (2001) показала, что у детей с осложненным течением ОРВИ наблюдается значительное снижение способности к индукции альфа- и гамма-ИФН. Способность к индукции альфа- и гамма-ИФН при положительной динамике инфекционного процесса заметно увеличивается, а сывороточный интерферон превышает допустимые значения. Улучшение параметров интерферонового ответа в процессе терапии свидетельствует о восстановлении адаптивного иммунного ответа макроорганизма. Способность к индукции интерферонов у реконвалесцентов ОРВИ ниже, чем у детей с вегето-сосудистой дистонией, что объясняет возникновение реинфекции и бактериальных осложнений при текущей вирусной инфекции [10].
Таким образом, отмечается индукция уровня альфа-интерферонов у детей в возрасте до 4-х лет под воздействием как антигенного раздражителя (вирус), так и под воздействием лекарственных средств, включая и индукторы эндогенного интерферона. Представляется закономерным включение индукторов интерферона 1-и 2-го типа (к которым относится циклоферон) в комплексное лечение неосложненных и осложненных ОРВИ.
Возможности применения индукторов интерферона в детской практике с учетом иммунного ответа
Индукторы интерферона обладают универсально широким диапазоном антивирусной активности (этиотропное действие) и выраженным иммуномодулирующим эффектом, не обладают антигенностью, синтез эндогенного интерферона сбалансирован, контролируется организмом, предотвращая побочные эффекты, характерные для экзогенно вводимых интерферонов. Однократное введение индуктора приводит к длительной циркуляции эндогенного интерферона (при введении циклоферона - до 72 часов, а при введении амиксина - 48 часов, кагоцела - до 5 суток) [4,6-17].
В детской практике применяется амиксин - низкомолекулярный индуктор интерферона, относится к классу флуоренонов. Обладает противовирусным и иммуномодулирующим действием, ингибирует трансляцию вирусспецифических белков в инфицированных клетках, вследствие чего подавляется репликация вируса. Сегодня на фармацевтическом рынке имеется дженерик амиксина - лавомакс. Применяется в детской практике у детей старше 7 лет. Побочные явления - аллергические реакции, диспептические явления, кратковременный озноб. На фармацевтическом рынке России появился КагОцел, полимер на основе целлюлозы. КагОцел - поздний индуктор интерферона, вызывает синтез эндогенных ИНФ-α/β и ИФН-γ с пиком активности через 24-48 часов с последующей циркуляцией до 4-5 дней. Умеренный эффект препарата на индукцию альфа-интерферона (+8 МЕ/мл) и несколько ниже эффект на синтез гамма-инферферона (+4,8 МЕ/мл) 17.
Одним из важных направлений формирования полноценного иммунного ответа является регуляция синтеза ИФН-g. Продукция ИФН-g Th1 осуществляется благодаря стимуляции ИФН-g-индуци-рующими цитокинами - ИЛ-12, ИЛ-2 и ФНО-a. ИЛ-18, являясь потенциальным индуктором синтеза ИФН-g, выступает в роли синергиста ИЛ-12, и оба цитокина лидируют в быстрой активации моноцит/макрофа-гальной системы посредством стимуляции выработки ИФН-g, который стимулируется циклофероном. В ряде случаев размножение вирусов подавляется дефектными частицами - дефект-интерферирующие частицы (ДИ-частицы), препятствующие нормальной репродукции вируса, подавляя цитоцидное действие вируса. Накопление достаточного количества ДИ-частиц в инфицированном организме приводит к самоограничению инфекции. Дефектные частицы сохраняют цитокин- и интерферон (ИФН)-индуцирующие свойства, стимулируя неспецифический иммунитет [17].
Показана [17] нормализация показателей клеточного иммунитета и концентрации иммуноглобулина А (при комбинированном применении циклоферона и биовестин-лакто); показано увеличение числа детей, не болевших ОРВИ в течение 3-6 месяцев после приема препаратов, обеспечив снижение повторных ОРВИ и осложнений, снижение кратности (в 2,2 раза) и длительности острых эпизодов (на 2,7дня) ОРВИ, уменьшение проявлений синдрома лимфоаденопатии, астенического синдрома, осложненного течения заболевания, восстановление нормальной флоры слизистых оболочек носа и зева. И.В. Сарвилиной [20] отмечено снижение ОРВИ в 4,1 раза и уменьшение длительности обострения ОРЗ в 1,7 раз, а также частоты развития аллергии в 4,6 раза. В исследованиях [18, 21] показана эпидемиологическая эффективность циклоферона (индекс эффективности 2,9 при колебаниях от 2,4 до 3,4, при показателе защиты от 58,5 до 67,1%), отмечено снижение уровня заболеваемости в 2,9 раза. Число заболевших, получавших циклоферон, составило 6%, наблюдалось легкое течение ОРВИ, число пропущенных дней по болезни в пересчете на 1 ребенка составило 4,8 дня. Среди детей, не получавших средств неспецифической профилактики, уровень заболеваемости составил 58%, при заболеваемости в 19% у детей, получавших гриппол. Показано снижение заболеваемости ОРВИ и гриппом (в 2,4 - 4,4 раза) в организованных коллективах, как у детей, так и у подростков. При проведении курса циклоферона наблюдается смена структуры ОРВИ среди заболевших, увеличиваются легкие (в 4,3 и более раза), уменьшаются тяжелые и осложненные формы заболеваний. У детей с бронхиальной астмой выявлено снижение в 1,4 раза обострений заболевания и в 1,9 раза частоты ОРВИ у больных детей.
Применяя циклоферон для профилактики ОРЗ и гриппа, Е.И.Кондратьева [7] показала, что препарат, обладая цитопротективным действием на слизистую оболочку полости носа, снижает степень деструкции плоского и цилиндрического эпителия, повышает содержание лизоцима, увеличивает уровень s- IgA в слюне.
Микоплазменная инфекция актуальна в связи с формированием рецидивирующих и хронических заболеваний органов дыхания, оказывает цитопатическое действие на клетки эпителия респираторного тракта, изменяя их метаболическую активность, нарушая эвакуаторную функцию. Возбудитель способствует формированию затяжного и/или рецидивирующему течению воспалительного процесса. При включении циклоферона в терапию микоплазменной инфекции сокращается лихорадочный период, интоксикация, уменьшается длительность катарального симптома, бронхиальной обструкции (в среднем на 3-1,6 дней). Улучшение клинической симптоматики происходит на фоне усиления макрофагальной активности, активации синтеза интерферона (в 1,5-1,9 раза), снижения уровня TNF, нарастания концентрации иммуноглобулина А, включая и секреторный его компонент, у 67-87 % пациентов [8].
Н.В. Минаевой [12,13] изучены особенности аллергопатологии у детей с синдромом нарушения противоинфекционной защиты, и разработана схема лечебно-реабилитационных мероприятий, основанная на этиоиммунопатогенетических принципах, с применением циклоферона. Применение циклоферона в комплексе с ацикловиром у детей с аллергической патологией и синдромом нарушения противоинфекционной защиты снижает в 1,7 раза уровень острой заболеваемости, уменьшает в 1,9-2,6 раза рецидивирование хронической герпесвирусной инфекции, долю детей с ЛОР-патологией, нормализуя показатели иммунитета. Детям с манифестацией герпесвирусной инфекции, риском активации или высокой активностью противовирусного иммунитета рекомендуется терапия ацикловиром и циклофероном. При отсутствии манифестных форм ВПГ-инфекции или высоких титров антител к ВПГ рекомендуется лечение только циклофероном.
У детей раннего возраста на отягощенном преморбитном фоне нарушения иммунного реагирования обусловлены инфицированием вирусами простого герпеса (1 и 2 типы), цитомегаловирусом. Частота выявления антител к герпесвирусам составила 77,4%. Циклоферон обеспечивает гладкое течение постинфекционного периода, предотвращая развитие осложненных форм инфекции, способствует укорочению длительности периода интоксикации и лихорадки. Циклоферон нормализует Т-клеточный иммунный ответ и купирует общеинфекционный синдром. При бронхолегочных осложнениях ОРВИ циклоферон нормализует уровень АКТГ и кортизола и поддерживает на нижней границе нормы концентрации ТТГ и Т3, повышая активность АКТГ, снижая повышенный уровень соматотропного гормона (СТГ). Наблюдается легкое течение заболевания без развития осложнений, быстрое купирование лихорадки и интоксикации [1, 14].
Нами проведена вакцинация часто болеющих детей с рецидивирующими заболеваниями верхних и нижних дыхательных путей, дивакциной против кори и паротита (в возрасте 1,76±0,35 лет) с применением циклоферона. В поствакцинальном периоде у 2 (7,1 %) детей отмечена пневмония, остальные 26 (92,8 %) детей переносили вакцинацию бессимптомно, а течение поствакцинального процесса у них было гладким. При первичном введении вакцины происходил прирост антител к кори и паротиту с 14 дня от начала вакцинации, а выработка антител продолжалась в период от 45 до 60 дня после вакцинации. Без применения препарата прироста антител на этих же сроках у часто болеющих детей не происходило. При ревакцинации отмечен прирост (в 3-4 раза) титров антител к 45 дню. По данным предыдущих исследований, проводимых нами, до 15 % часто болеющих детей после ревакцинации остаются с низкими титрами антител, а наслоение интеркуррентных заболеваний отмечалось более чем у 30 % детей [17].
В период повышенного подъема заболеваемости гриппом A/H1N1(sw)/09/04 осенью 2009 года проведена оценка эффективности циклоферона как лечебного (150 человек) и профилактического средства для экстренной профилактики (86 человек). Циклоферон при своевременно начатом лечении обеспечивал минимизацию синдрома интоксикации, ликвидацию катарального синдрома (к 5 дню). Снижение температурной реакции отмечено на 2-е сутки, а ее нормализация наступала к 4-м суткам приема препарата, без использования антибактериальных средств. Защита от гриппа и ОРВИ наблюдалась у 76,5% у медицинских работников, контактирующих с больными гриппом и ОРВИ в осенний период 2009 года [19].
Из иммунотропных препаратов, обладающих интерферониндуцирующей активностью, остановимся на иммунофане, бронхомунале, рибомуниле, ИРС-19 и иммунориксе (пидотимоде). Мишенью для препаратов являются фагоцитарные клетки. Препараты повышают функциональную активность фагоцитов, синтез провоспалительных цитокинов, а имунорикс усиливает активность естественных (натуральных) киллеров. Препараты рекомендуются для коррекции иммунного дисбаланса, профилактики и лечения инфекционно-воспалительных заболеваний ЛОР-органов у детей 17.
Таким образом, список противовирусных лекарственных препаратов, разрешенных для применения в детской практике, постоянно расширяется, эти препараты занимают достойное место, обеспечивая улучшение качества оказания медицинской помощи детям.
Список литературы

АМИКСИН ® — современное противовирусное и иммуностимулирующее средство; способствует образованию в организме четырех видов интерферонов (альфа, бета, гамма и лямбда).
Узнать подробнее про АМИКСИН ® …


Противовирусные препараты с иммуностимулирующей активностью могут рекомендоваться как при лечении гриппа, так и других ОРВИ. С их помощью можно сократить сроки болезни и предотвратить развитие осложнений.

Прием противовирусного препарата АМИКСИН ® возможен на любой стадии простуды и гриппа по рекомендации врача.
Как принимать препарат?


В сезон простуды и гриппа прием противовирусных и иммуномодулирующих препаратов помогает снизить вероятность заболевания.

АМИКСИН ® — современный противовирусный и иммуномодулирующий препарат, используемый в комплексной терапии целого ряда вирусных инфекционных заболеваний, в том числе гриппа, ОРВИ и герпеса.
Подробнее о препарате…


Иммуномодулирующие препараты — одни из важных составляющих комплексной терапии гриппа и других ОРВИ.
Функции и механизм действия интерферона в человеческом организме
Интерферон — это белковая молекула, которая обеспечивает противовирусный иммунитет. При этом она обладает неспецифической активностью, то есть действуют не на возбудителя какого-то конкретного заболевания, а на все вирусные частицы в целом. Если сказать обобщенно, то интерферон — универсальный защитник организма, который начинает действовать еще до того, как в работу включатся остальные звенья иммунитета [1] . Препараты интерферона применяются даже в терапии онкологии: они подавляют опухолевый рост.
Клетки вырабатывают этот защитный белок в ответ на действие вирусов, бактерий, опухолевых клеток или продуктов их метаболизма. Стимулировать их выработку могут и лекарственные препараты — индукторы интерферона. Молекулы последних, попадая в кровь и межклеточную жидкость, связываются с рецепторами зараженных или поврежденных клеток. Они запускают сложный каскад реакций, приводящих к образованию специфических белков. В результате клетка перестает воспроизводить вирусные частицы, расщепляет их генетическую структуру, а поверхность этой клетки становится менее проницаемой для внутриклеточных паразитов.
Кроме действия на сами зараженные клетки, интерфероны стимулируют активность других звеньев иммунитета, контролируют воспалительную реакцию [2] и даже могут защитить организм от опухолей. Это свойство активно изучают и уже используют для борьбы с некоторыми видами рака [3] .
Молекулы интерферона отличаются между собой по генетической структуре, типу клеточных рецепторов, на которые они действуют, даже по участкам ДНК, которые кодируют их состав. Все интерфероны делят на 3 типа.
- К первому типу относят альфа-интерферон, который имеет 13 различных структурных вариантов, а также бета-, каппа-, эпсилон- и омега-.
- Второй тип представлен только одним типом, гамма-интерфероном.
- Относительно недавно, в 2002 году, был открыт и третий тип молекул, лямбда-. Это отдельное семейство интерферонов, которое отличается от всех предыдущих генетическим строением и даже типом рецепторов, с которыми они взаимодействуют. Но по своей биологической активности лямбда-интерфероны очень похожи на первый тип [4] .
Не стоит относиться к интерферонам как к панацее от всех бед. Во-первых, некоторые вирусы могут подавлять образование специфических белков внутри зараженных клеток, что значительно снижает эффективность противовирусной защиты.
Поэтому прежде чем начинать лечение препаратами интерферона, нужно внимательно изучить пользу и возможный вред от их приема.
Лекарственные средства на основе интерферона доказали свою эффективность [5] в лечении широкого круга заболеваний: герпетических инфекций, ВПЧ, острых и хронических форм вирусного гепатита, рассеянного склероза, волчанки, гриппа и многих других вирусных и бактериальных инфекций. Применяют интерферон и при терапии онкологических заболеваний, а также СПИДа. И это притом, что по меркам медицины открыли его совсем недавно. Это произошло в 1957 году при проведении опытов на мышах. Ученые обратили внимание, что животные, заразившиеся одним вирусом, становились невосприимчивы к другому вирусному заболеванию. Это явление было названо интерференцией, а вещества, которые ему способствовали — интерферонами. Оказалось, что интерфероны вырабатываются не только у мышей, но и у всех млекопитающих, в том числе у человека. Началось изучение возможности промышленного производства веществ, обладающих противовирусным эффектом.
Однако долгое время применение интерферонов было ограничено из-за несовершенства процедуры их получения. Выделять это вещество из крови человека-донора было сложно, дорого и неэффективно.
В 1980 году в Японии впервые использовали для производства интерферона специально выращенную культуру лимфобластных клеток. А в 1981 году в США вместо клеток человека использовали культуру дрожжевых грибков. С помощью генной инженерии в геном ввели ген, который кодирует производство молекулы интерферона. Это позволило значительно упростить производство препарата [8] .
По способу производства существует четыре основных разновидности этого препарата: лейкоцитарный, лимфобластоидный, рекомбинантный и пегилированный.
После получения такой препарат очищают и концентрируют. В него могут входить все виды интерферонов и другие биологически активные вещества. Это одновременно и плюс, и минус. Преимущество такого препарата — его высокий потенциал биологического действия. Недостаток — высокая вероятность побочных эффектов при внутримышечном введении.
Лимфобластоидный интерферон получают не от человека-донора, а из культуры лимфобластных клеток, которые также обрабатывают веществами, стимулирующими иммунный ответ. Такие препараты содержат определенное соотношение различных видов интерферона и не так часто вызывают побочные эффекты.
Пегилированные, или ПЭГ-интерфероны — это рекомбинантные белковые молекулы, соединенные с полиэтиленгликолем. Такое соединение увеличило срок действия интерферона в организме.
ПЭГ растворим в воде, не вступает в биологические реакции в организме и не вызывает иммунного ответа. При присоединении ПЭГ молекула интерферона значительно увеличивается в размерах. А это, в свою очередь, увеличивает период полувыведения препарата.
Объединить интерфероны в однородные группы по методу получения, формам выпуска и показаниям не получится. Каждый препарат имеет свои особенности применения, эффективность при определенных заболеваниях. В зависимости от степени очистки и других факторов какие-то препараты с одним и тем же видом иммуноглобулина могут применяться только местно, а какие-то можно использовать в виде инъекций.
Поэтому при выборе препарата интерферона стоит ориентироваться не только на общую характеристику группы веществ, но в первую очередь на рекомендации врача и инструкцию по применению конкретного препарата.
Интерферон в виде инъекций применяют при системных заболеваниях, таких как гепатит, опухоли или рассеянный склероз. Препарат в виде капель в нос подходит для лечения риносинуситов и профилактики ОРВИ. Капли в глаза помогут при конъюнктивите. Суппозитории можно использовать при многих заболеваниях, в том числе у детей. А гель подходит для смазывания носа или кожи.
Интерфероны защищают организм от вирусов, бактерий и опухолевых клеток. Они обладают сложным биологическим действием. Но современная медицина научилась создавать аналогичные вещества и использовать их. Однако подбор подходящего препарата — задача, которую может решить только врач.
Преимущества этого препарата — максимум выработки интерферона уже в первые сутки от начала приема и активация четырех видов интерферонов. Увеличение концентрации интерферонов в отдельных органах может достигаться уже через 4 часа.
Все индукторы интерферона обладают индивидуальными характеристиками, показаниями и противопоказаниями. Поэтому препарат нужно выбирать внимательно, только после прочтения инструкции. С особой осторожностью нужно подходить к выбору лекарства, если его нужно принимать детям. Для детей существуют отдельные формы выпуска.
И, конечно, никогда нельзя заниматься самолечением. Любые препараты нужно принимать только по согласованию с врачом.

А. С. Боткина, канд. мед. наук, доц. кафедры госпитальной педиатрии им. акад. В. А. Таболина ФГБОУ ВО им. Н. И. Пирогова Минздрава России, Москва
Резюме: актуальность проблемы респираторных вирусных заболеваний обусловлена их чрезвычайно широким распространением, зачастую тяжелым течением, возможностью развития жизнеугрожающих осложнений и высоким экономическим ущербом, наносимым обществу в целом. В статье в сравнительном аспекте рассматриваются различные лекарственные средства, используемые в комплексной терапии острых респираторных вирусных инфекций у детей.
Ключевые слова: респираторные инфекции, индукторы интерферона, иммуномодуляция, дети, Циклоферон®
Abstract: the urgency of the problem of respiratory viral diseases is due to their extremely high spread, often severe, the possibility of developing life-threatening complications and the high economic damage caused to society as a whole. The article in a comparative aspect discusses the various drugs, used for the prevention and treatment of acute respiratory viral infections in children.
Keywords: respiratory infections, interferon inductors, immunomodulation, children, Cycloferon®
Этиологическими факторами данной группы заболеваний являются около 300 эпителиотропных вирусов, из которых наиболее часто встречающимися у детей являются риновирусы, парагрипп, аденовирусы, грипп. В последние годы нарастает удельный вес таких возбудителей, как корона-, бока- и метапневмовирусы. Также ежегодно увеличивается доля различных микст-инфекций, вызывающих более тяжелое по течению респираторное заболевание, что существенно усложняет диагностику и лечение таких пациентов.
Клинические симптомы респираторных вирусных инфекций у детей во многом похожи и проявляются различной по степени тяжести и длительности лихорадкой, интоксикацией, катаральным синдромом и поражением дыхательных путей (табл. 1).
Таблица 1. Тропизм различных вирусов, вызывающих ОРВИ
| Вирус | Наиболее часто поражаемый орган |
| Гриппа | Трахея, носоглотка, сосуды |
| Парагриппа | Гортань |
| Аденовирус | Глотка, конъюнктива, кишечник |
| Риновирус | Полость носа |
| Реовирус | Носоглотка, кишечник |
| Коронавирус | Носоглотка, бронхи, кишечник |
| РС-вирус | Бронхиолы, альвеолы |
| Бокавирус | Носоглотка, кишечник |
| Метапневмовирус | Носоглотка, трахея, бронхи |
При гриппе на первый план выходит выраженный интоксикационный синдром и лихорадка, аденовирусная инфекция характеризуется болью в горле, конъюнктивитом, продуктивным кашлем, нередко - развитием обструктивного синдрома и болями в животе; при парагриппе часты ларингиты с развитием стеноза гортани, а при респираторно-синцитиальной инфекции -бронхит и/или бронхиолит с выраженным и длительным обструктивным синдромом. Однако различия симптоматики в зависимости от этиологии вирусного заболевания не всегда четко различимы, следовательно, практикующему врачу важно иметь в своем арсенале средства, одинаково эффективные для профилактики и лечения как гриппа, так и других ОРВИ.
Выбор метода лечения ОРВИ у детей зависит от возраста ребенка, клинической картины заболевания, выраженности симптомов, степени тяжести и наличия осложнений. Лечение обязательно должно включать режим, диету, медикаментозную и немедикаментозную терапию. Лекарственная терапия респираторных заболеваний у детей ориентирована на использование всего арсенала современных препаратов, отвечающих определенным критериям [3, 4]:
- высокая эффективность относительно большинства возбудителей;
- минимальный спектр побочных эффектов;
- отсутствие токсичности;
- сочетание противовирусного и иммуномодулирующего эффекта;
- наличие различных лекарственных форм;
- этиотропные, действующие на возбудителя заболевания;
- патогенетические (иммуномодулирующие), исправляющие нарушения системы иммунитета, возникающие и развивающиеся в процессе болезни;
- симптоматические, предназначенные для купирования отдельных симптомов заболевания.
Таблица 2. Механизм действия различных противовирусных препаратов, применяемых при ОРВИ
| Действие | Механизм действия | Препарат |
| Ингибиторы нейраминидазы | Конкурентно и избирательно ингибирует нейроминидазу, что нарушает проникновение вируса в здоровые клетки, тормозит выход вирионов из инфицированной клетки | Осельтамивир, занамивир |
| Блокатор М-йонного канала (адамантаны) | Блокирует специфические ионные М-2 каналы, что приводит к нарушению процесса дезинтеграции вириона и высвобождению рибонуклеопротеида | Ремантадин, орвирем |
| Блокатор слияния, индуктор ИФН | Ингибирует слияние липидной вирусной оболочки с клеточной мембраной | Арбидол |
| Ингибитор РНК и ДНК вирусов | Конкурентное подавление образования гуанозин трифосфата, приводящее к нарушению синтеза вирусных РНК и ДНК | Рибавирин |
Так, ингибиторы нейраминидазы обладают избирательной активностью только против вирусов гриппа типа А и В, эффективны при назначении не позднее 48 ч от начала клинических симптомов заболевания, оказывают раздражающее действие на слизистую оболочку респираторного и пищеварительного тракта, вызывают тяжелые аллергические реакции вплоть до развития токсического эпидермального некролиза, а также имеют высокую стоимость. Препараты из группы адамантинов также обладают избирательной активностью против вируса гриппа А, вызывают побочные эффекты со стороны желудочно-кишечного тракта в виде тошноты и рвоты, нервной системы, проявляющиеся галлюцинациями и психозом, аллергическими реакциями. Кроме того, все противовирусные препараты эффективны только при раннем их применении, не позже 24-48 ч и приводят к возникновению штаммов вирусов с низкой чувствительностью или резистентностью к терапии. Лекарственная устойчивость является результатом мутаций вирусов и развивается, как правило, при многократном использовании препарата [5, 6].
Основными патогенетически действующими группами препаратов являются интерфероны и их индукторы. Интерфероны - это группа биологически активных белков или гликопротеидов, синтезируемых клеткой в процессе защитной реакции на чужеродные агенты (экзогенные и/или эндогенные). Образование и действие интерферона составляет важнейший механизм врожденного (естественного) иммунитета. Доказано, что течение и исход вирусных инфекций во многом зависит от способности системы интерферона быстро реагировать на внедрение возбудителя [7]. Всего в настоящее время описано более 100 различных эффектов интерферонов, основными из которых являются:
- подавление роста внутри- и внеклеточных инфекционных агентов вирусной и невирусной (хламидии, простейшие, бактерии) природы;
- антипролиферативная активность;
- антитуморогенный эффект;
- антимутагенный эффект;
- антитоксическое действие;
- радиопротективный эффект;
- иммуномодулирующий эффект(подавление или усиление продукции антител, стимуляция макрофагов, усиление фагоцитоза и др.).
Рис. 1. Побочные эффекты препаратов интерферонового ряда 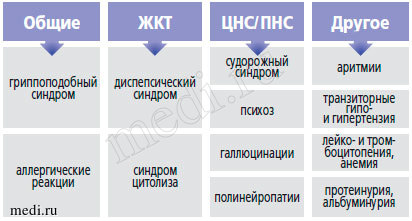
Таблица 3. Классификация индукторов интерферона (Ершов Ф.И., Романцов М.Г., Петров А.Ю., 2008)
| Химическая природа | Препарат |
| А. Синтетические соединения с основной интерферон-индуктивной активностью | |
| Низкомолекулярные: Флуореноны Акриданоны Олигопептиды Производное имидазо (4,5-С) квинолина | Амиксин Циклоферон® аллокин-альфа имиквимод |
| Полимеры (дс-РНК) | Полудан, полигуацил |
| Б. Природные соединения с основной интерферон-индуктивной активностью | |
| Полифенолы | Кагоцел, мегосин, саврац рагосин, гозалидон |
| Полимеры (дс-РНК) | Ридостин, ларифан |
| Производные флавонидов и аминокислот | протефлазид |
| В. Иммунотропные препараты с вторичной интерферон-индуктивной активностью | |
| Т-миметики | Тимоген, тактивин, изопринозин, гроприносин, иммунофан |
| Иммуномодуляторы бактериального происхождения - эубиотики | Лактобактерин, биоспорин |
| Вакциноподобные препараты | Бронхомунал, рибомунил, ИРС-19, уроваксом |
| Липополисахариды | Пирогенал, продигиозан |
| Производные нуклеиновых кислот | Натрия нуклеинат |
| Препараты пурина и пиримидина | Метилурацил, пентоксил |
| Производные бензимидазола | Дибазол |
| Производные индола | Арбидол |
| Растительные иммунокорректоры | Родиола розовая, экстракт эхинацеи |
| Г. Препараты других фармакологических групп с вторичной интерферон-индуктивной активностью | |
| Метилксантины | Теофиллин, эуфиллин, дипиридамол, кофеин |
| Производные изохинолина | Папаверин, дротавирин |
| Производные бензофурана | Кордарон |
| Производные хромена | Интеркордин |
Немаловажным является то, что образование эндогенного интерферона при введении его индукторов является более физиологичным процессом, чем повторное введение экзогенных интерферонов, которые, помимо побочных эффектов, быстро выводятся из организма и угнетают образование собственных (аутологичных) интерферонов по принципу отрицательной обратной связи, что может привести к формированию хронического инфекционного процесса в организме ребенка [10]. Имея основные свойства интерферона, его индукторы не обладают антигенностью и даже при однократном введении обеспечивают длительную циркуляцию синтезированных цитокинов на терапевтическом уровне. Стимулированный ими синтез эндогенного интерферона находится под контролем интерлейкинов и белков-репрессоров и не вызывает гиперинтерферонемии и развития связанных с ней побочных эффектов. Проведенные исследования показали, что индукторы интерферона обладают универсально широким диапазоном фармакологической активности, обладая одновременно прямым противовирусным и иммуномодулирующим действием. Введенные в организм индукторы интерферона стимулируют выработку эндогенного интерферона трех типов (α,β,γ) в разных пропорциях, что зависит от химической структуры индуктора. В зависимости от времени продукции интерферона в крови различают индукторы ранние (4-8 ч) и поздние (18-24 ч) [11].
Среди индукторов интерферона в профилактике и лечении ОРВИ у детей широко применяется препарат Циклоферон®, являющийся синтетическим производным акридонуксусной кислоты. Препарат повышает уровень интерферона α/β-типа в органах и тканях, содержащих лимфоидные элементы: в слизистой тонкого кишечника, селезенке, печени, легких, активирует стволовые клетки костного мозга, стимулируя образование гранулоцитов, преодолевает гематоэнцефалический барьер. Циклоферон® обладает чрезвычайно широким спектром биологической активности: прямым противовирусным, иммуномодулирующим и противовоспалительным действиями. Прямая противовирусная активность Циклоферона® доказана относительно различных респираторных вирусов и гриппа А и В, вируса простого герпеса 1-го и 2-го типов, цитомегаловируса, гепатитов В и С, клещевого энцефалита, вируса папилломы человека. Препарат нарушает репликацию вирусов, блокирует инкорпорацию вирусных ДНК и РНК в капсиды, что приводит к увеличению количества дефектных вирусных частиц и снижает вирус-индуцированный синтез белка в клетках. Иммунотропное действие препарата реализуется путем активации фагоцитов, Т-лимфоцитов и NK-клеток, нормализации баланса между CD4+- и СБ8+-клетками, снижении уровня В-лимфоцитов в периферической крови, с одновременным повышением синтеза высокоаффинных антител и индукции синтеза мРНК для ИФН-γ[12; 13]. Противовоспалительное действие Циклоферона® обусловлено ингибированием основных провоспалительных цитокинов (IL-1-p, IL-8, IL-10 и TNF-ot).
Циклоферон® относится к ранним индукторам интерферона, так как пик его выработки приходится на период от 4 до 8 ч с момента приема, что позволяет рекомендовать препарат для купирования вирусного заболевания на ранней стадии или в качестве экстренной профилактики. Кроме того, Циклоферон® хорошо сочетается с симптоматическими препаратами, вакцинами, химиопрепаратами, препаратами интерферона, усиливая действие последних и уменьшая побочные эффекты от их применения, что позволяет получить оптимальный фармакотерапевтический эффект. Исследование эффективности применения Циклоферона® в комплексном лечении ОРВИ у детей, проведенное Е.И. Кондратьевой, выявило более быстрое купирование симптомов интоксикации и выраженности катаральных явлений, обусловленное противовоспалительным и цитопротективным действием на слизистую оболочку дыхательных путей, а также увеличением уровня секреторного IgA. М.В. Гаращенко в своем исследовании отмечает почти 10-кратное уменьшение числа заболевших ОРВИ в период эпидемического подъема заболеваемости на фоне применения Циклоферона® (6 и 58% соответственно), а также более легкое течение и отсутствие осложнений [14; 15].
Помимо высокой эффективности, препарат отличается высоким профилем безопасности, который подтверждается отсутствием токсичности, аллергенности, мутагенности, хорошей растворимостью в биологических средах и проникновением в ткани, быстрым выведением из организма и отсутствием кумуляции [16].
Таким образом, широкий спектр биологической активности при низкой токсичности, наличие иммуномодулирующего действия позволяют рекомендовать Циклоферон® как препарат первой линии в лечении острых респираторных инфекций у детей. Для наибольшей эффективности рекомендуется начинать применять Циклоферон® как можно раньше, дополняя его препаратами направленного этиотропного действия и иммуномодуляторами, что обеспечит достижение оптимального фармакотерапевтического эффекта.
ЛИТЕРАТУРА
- Руководство по вирусологии. Вирусы и вирусные инфекции человека и животных / Под ред. Д.К. Львова. М.: МИА, 2013. 1200 с.
- Грипп и гриппоподобные инфекции, включая особо опасные формы гриппозной инфекции. Фундаментальные и прикладные аспекты изучения // Бюллетень проблемной комиссии / Под ред. В.И. Покровского, Д.К. Львова, О.И. Киселева, Ф.И. Ершова. СПб.: Роза мира, 2008. 109 с.
- Ершов Ф.И., Коваленко А.Л., Романцов М.Г. Вопросы лечения гриппа и ОРВИ у детей // Экспериментальная и клиническая фармакология. 2011. № 6. С. 41-45.
- Ющук Н.Д., Бокова Н.О., Знойко О.О. Оптимизация диагностических подходов в тактике ведения больных гриппом // Лечащий врач. 2012. № 10. С. 64-67.
- Ершов Ф.И., Романцов М.Г. Лекарственные средства, применяемые при вирусных заболеваниях: Руководство для врачей. М.: ГЭОТАР-Медиа, 2007.
- Fiore А.Е., Fry A., Shay. D. Antiviral agents for the treatment and chemoprophylaxis of infl uenza. Recommendations of the advisory committee on immunization practices (ACIP) // Recommendations and Reports, 60 (RR01): 1-24 (2011).
- Ершов Ф.И., Наровлянский А.Н. Основные итоги изучения системы интерферона к 2011 году // Интерферон-2011: Сборник научных статей. М., 2012. С. 14-34.
- Григорян С.С. Индукторы интерферона: итоги и перспективы // Интерферону - 50 лет: Юбилейный сборник, посвященный открытию интерферонов / Под ред. акад. РАМН проф. Ф.И. Ершова. М., 2007. С. 66-71.
- Романцов М.Г., Ершов Ф.И. Иммунный ответ при вирусных инфекциях // Часто болеющие дети: современная фармакотерапия. М.: ГЭОТАР-Медиа, 2009. С. 134-142.
- Лыткина И.Н., Малышев Н.А. Профилактика и лечение гриппа и острых респираторных вирусных инфекций среди эпидемиологически значимых групп населения // Лечащий врач. 2010. № 10. С. 66-69.
- Романцов М.Г. и др. Антиоксиданты и иммунотропные препараты в терапии больных туберкулезом легких // Врач. 2005. № 9. С. 66-67.
- Применение Циклоферона при социально значимых заболеваниях у детей и подростков. Новейший справочник практикующего врача-педиатра / Под ред. М.Г. Романцова, Л.Г. Горячевой. А.А. Шульдякова. СПб., 2010. 165 с.
- Исаков В.А. и др. Эффективность Циклоферона® в терапии и профилактике гриппа и ОРЗ // РМЖ. 2011. № 23. С. 1-8.
- Кондратьева Е.И. Экстренная неспецифическая профилактика ОРВИ и гриппа препаратом Циклоферон® у детей в эпидемический период // Вестник Санкт-Петербургской государственной медицинской академии им. И.И. Мечникова. 2005. № 1.
- Гаращенко М.В. Новые технологии в медикаментозной профилактике острых респираторных заболеваний у детей школьного возраста в условиях мегаполиса: Автореф. дис. . канд. мед. наук. М., 2007.
- Татаурщиков Н.С., Сепиашвили Р.И. Современные подходы к использованию иммуномодуляторов в аллергологической практике. М: Тактик-Студио, 2012. 39 с.
Читайте также:


