Иммунологическая память от гепатита в
Вакцинация является эффективным методом борьбы с инфекционными болезнями, представляющими угрозу для жизни. Благодаря массовой вакцинации, обеспечивающей коллективный иммунитет, многие инфекционные заболевания перестали представлять серьезную опасность. Однако антипрививочные настроения растут, а уровень вакцинации падает. Разберемся как работают вакцины, и почему прививаться всё-таки стоит.
Основу приобретённого иммунитета составляют Т-лимфоциты и В-лимфоциты. Оба типа лимфоцитов помогают защитить организм от чужеродных агентов, таких как бактерии, вирусы и токсины. Они свободно перемещаются через ткани организма, проходят через стенки кровеносных сосудов, и перемещаются между различными лимфатическими узлами по лимфатическим сосудами.
Т- и В-лимфоциты обеспечивают разный иммунный ответ на различные инфекции. Чужеродный агент может находится внутри клетки (например, вирус), и в таком случае убить нужно собственную клетку организма. Для этого работает клеточный иммунитет – активируются Т-лимфоциты. Если же патоген внеклеточный (например, бактерия), тогда В-лимфоциты вырабатывают антитела – белковые молекулы, растворенные в плазме крови. Такой тип иммунного ответа называется гуморальным (от лат. humor – жидкость).
Во время вакцинации в организм вводится специальные препараты – вакцины - формирующие иммунитет к определенным вирусам или микроорганизмам. В зависимости от состава вакцины стимулируют разный иммунный ответ.
Вакцины могут содержать живой, но ослабленный (аттенуированный) патоген. Этот тип вакцин используется для профилактики кори, краснухи, паротита, туберкулеза (БЦЖ).
Другой тип вакцин, содержащие убитые микробы (инактивированные). К ним относятся вакцины против гриппа, гепатита А, пневмококка, коклюша, бешенства.
Субъединичные вакцины представляют собой отдельные фрагменты микробов, которые также вызывают иммунный ответ. Они могут быть натуральными, полученными из микробов и очищенными (например, Пневмо-23) или изготовленными с помощью генной инженерии (например, вакцина от гепатита В).
Существуют вакцины в состав которых входят инактивированные микробные токсины. Они химически обработаны и не приводят к тем последствиям, которые вызвали бы настоящие токсины, однако стимулируют выработку антител против соответствующего токсина. Это, например, антистолбнячная и противодифтерийная вакцины.
В ходе иммунного ответа на антиген возбудителя формируется иммунологическая память. Ее материальные носители — клетки памяти. Способность формировать клетки памяти в ответ на контакт с антигеном является одним из наиболее кардинальных отличий адаптивного иммунитета от врожденного и, без сомнения, является главным преимуществом первого. Особенность клеток памяти состоит в том, что они не участвуют в иммунном ответе, в ходе которого они образовались (например, в первичном иммунном ответе). Но при повторном поступлении специфического для этих клеток патогена их реакция оказывается более быстрой, мощной и результативной, чем ответ наивных лимфоцитов. Присутствие в организме клеток памяти к антигенам возбудителей обеспечивает устойчивость к ним организма (собственно, наличие иммунитета).
Цель данного сообщения подчеркнуть насколько длинный, сложный процесс запуска иммунного ответа. Большое количество клеток должно оказаться в нужном месте и в нужное время. На развитие иммунной реакции требуется много времени. Антитела образуется на 8-10-е сутки от момента первой встречи с патогеном. А вот если уже существует иммунологическая память после проведенной вакцинации, процесс занимает 1-3 дня. В этом случае человек либо вовсе не заметит, что у него была опасная болезнь, либо перенесет её намного легче.
Люди часто опасаются побочных эффектов от прививок. Да, они есть. И как правило ограничены умеренно выраженными местными реакциями: покраснение, отек, боль в месте введения. Тяжелые побочные реакции, в том числе аллергические (о них отдельно) развиваются редко. Все вакцины проходят тщательное тестирование, несколько этапов исследований, прежде чем будут широко использоваться.
Наибольший риск для большинства людей - не получить вакцину и потенциально заболеть после контакта с возбудителем. Болезнь может быть намного хуже (иногда даже смертельна), чем потенциальные побочные эффекты вакцины.
Широчайшее распространение инфекционных заболеваний во все времена не только приводило к гибели многих миллионов людей, но и было основной причиной малой продолжительности жизни человека. С тех пор, как 219 лет назад Э. Дженнер сделал первые прививки от оспы, в мире не существует более эффективного способа предотвращать инфекционные болезни, чем профилактические прививки, иначе называемые вакцинацией (иммунизацией).
Сразу после рождения человек соприкасается с огромным количеством микроорганизмов. Чтобы противостоять им, организм "включает" механизмы естественного иммунитета, который начинает формироваться еще в утробе матери и устанавливается в первые годы жизни. Часть микроорганизмов не могут преодолеть этот барьер и поэтому не опасны для здорового организма.
Другая часть микроорганизмов не может быть остановлена этой преградой и, проникая в организм человека, вызывает заболевание и начинает битву с организмом. Исход этой схватки не всегда можно предугадать. Если организм все же окажется сильнее вируса или микроба, то болезнь будет подавлена, а в организме появится информация о способах борьбы с ними – специфический (приобретенный) иммунитет. Правда, в самой первой схватке организму могут быть нанесены серьезные повреждения - осложнения, иногда напоминающие о себе всю оставшуюся жизнь. При повторной встрече с вирусом приобретенный иммунитет уже будет иметь информацию о методах борьбы с ним и сможет без особых усилий будет защитить организм.
Смысл вакцинации заключается в том, что в организм человека вводятся вакцины – ослабленные или убитые возбудители различных инфекций (или искусственно синтезированные белки, которые идентичны белкам возбудителя).
Вся вакцинопрофилактика основана на существовании феномена иммунологической памяти.Благодаря ей удается искусственно формировать длительный, иногда пожизненный антиинфекционный иммунитет.
Иммунологическая память– способность организма давать ускоренную иммунологическую реакцию на повторное введение антигена.
После введения вакцины появляются защитные специфические антитела (иммуноглобулины). Они обнаруживаются не сразу, а только на 5-7 день, затем их количество быстро нарастает к 10-12 дню, и максимально – к 20-22 дню. Затем число специфических антител убывает и через несколько месяцев не обнаруживается совсем или обнаруживается в низких титрах.
Но иммунологическая память сохраняется, ее носителями являются малые Т- и В-лимфоциты, специфически перестроенные при первичном ответе. Если возбудитель проникает вторично, то антитела появляются гораздо быстрее – уже через 1-2 дня – и в большем количестве, чем при первичном ответе.

Некоторые вакцины создают иммунитет с первого раза, другие приходится вводить повторно. Так называемая ревакцинация — мероприятие, направленное на поддержание иммунитета, выработанного предыдущими прививками.
Ослабленный возбудитель (получаемый из ослабленных или убитых микроорганизмов, продуктов их жизнедеятельности или из их антигенов, полученных генно-инженерным или химическим путём), попадая в тело человека, вызывает ответную реакцию организма для борьбы с вирусом. В результате этой борьбы организм вырабатывает антитела к данному вирусу, таким образом он получает опыт эффективного обезвреживания вируса (приобретенный иммунитет). Именно этот опыт будет впоследствии использоваться при встрече с аналогичным реальным возбудителем болезни – антитела остановят развитие заболевания в самом начале болезни или, в случае, если заражение все же произойдет, позволят организму справиться с вирусом без серьезных осложнений. Таким образом, вакцина является тренировочным испытанием организма для борьбы с определенным видом инфекции.
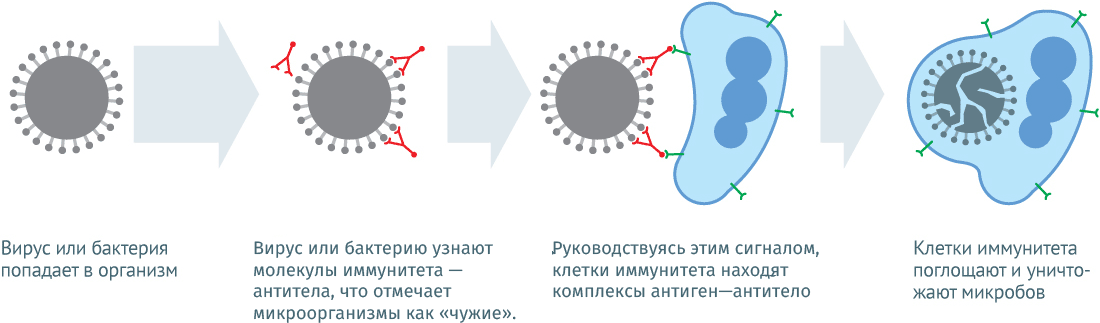
Вакцины стимулируют иммунную систему в той же степени, что и сам инфекционный агент, и потенциально могут дать более эффективную защиту против определенных патогенов. Наиболее важно, что защита, обусловленная вакцинацией, помогает миновать развитие осложнений, связанных с течением подобного заболевания. Польза вакцинации намного превышает этот показатель при развитии заболеваний, предупреждаемых вакцинацией.
Задать вопрос специалисту
Вопрос экспертам вакцинопрофилактики
Ребенку 1 г 10 мес. В 6 мес. была сделана прививка Инфанрикс-Гекса, две недели назад прививка корь-краснуха-паротит. Ребенок начал ходить в детский сад, сейчас узнала, что в группе есть дети, которым некоторое время назад сделали живую вакцину от полиомиелита.
Представляет ли пребывание с такими детьми опасность для моего ребенка?
Когда и какую можно сделать прививку от полиомиелита нам сейчас? У меня выбор: поставить комплексную АКДС Инфанрикс или только полиомиелит, можно ли сделать прививку от полиомиелита через две недели после Приорикса?
Отвечает Харит Сусанна Михайловна
Для защиты от любых форм полиомиелита ребенок должен иметь как минимум 3 прививки. При вакцинации других детей живой оральной вакциной против полиомиелита непривитые или не полностью привитые дети высаживаются из детского сада на 60 дней для предупреждения развития вакциноассоциированного полиомиелита.
Нет, через 2 недели вы не можете начать прививки, интервал между прививками не меньше 1 месяца. Вам нужно сделать как минимум 2 прививки против полиомиелита прежде, чем ребенок будет защищен от этой инфекции. Т.е если ребенок привит дважды, то только через 1 месяц после последней прививки выработается достаточный иммунитет. Лучше привиться 2-х кратно с интервалом в 1,5 месяца АКДС+ ИПВ(Пентаксим, ИнфанриксГекса), через 6-9 месяцев делается ревакцинация. АКДС+ИПВ/ОПВ(Пентаксим). Прививка против гепатита В у вас пропала, но если вы будете прививаться ИнфанриксГекса дважды с интервалом в 1,5 месяца, 3ю прививку против гепатита В можно сделать через 6 месяцев от первой. Рекомендую сделать полный курс вакцинации, поскольку ребенок посещает детский сад (организованный коллектив) и практически не имеет никакой защиты от опасных и тяжелых инфекций.
У меня вопрос несколько общего характера, но обращаюсь к вам, так как до сих пор не смог получить на него внятного ответа. Кому, на ваш взгляд, может быть выгодна кампания по дискредитации вакцинации и, в особенности, детской? Я не прошу, конечно же, назвать конкретных виновников, мне интереснее понять, какие стороны могут быть в этом заинтересованы? Или же это процесс спонтанный, сродни невежеству, не нуждающемуся в подпитке?
Мои знакомые врачи предполагают, что информационные вбросы о вреде прививок могут (в теории) заказывать производители лекарств, поскольку тем выгоднее, чтобы человек шёл в аптеку за рекламируемым по ТВ препаратом, а не делал прививку у врача. Но это было бы справедливо для вакцины (к примеру) от гриппа (по ТВ хватает рекламы противогриппозных препаратов). А как же тогда быть с вакциной БЦЖ, вакциной от гепатита? Такие-то препараты по ТВ не рекламируют. С такой же логикой можно было бы предположить, что "заинтересованная сторона" - производители вегетарианских товаров и витаминов, которые предлагают пичкать ими детей едва ли не с первых дней жизни, но и эта теория тоже представляется мне спорной. А вы что считаете по этому поводу?
Отвечает Полибин Роман Владимирович
Это вопрос, который, к сожалению, не имеет точного ответа, можно лишь предполагать. Понять мотивацию людей, выступающих против вакцинопрофилактики - метода, доказавшего свою безопасность и эффективность для профилактики инфекционных и, на сегодняшний день, некоторых неинфекционных болезней, достаточно сложно.
Существуют общества, фонды "антивакцинальщиков", которые зарабатывают на этом рейтинг, в т.ч. с использованием интернет-технологий (например посещаемость, просмотры сайтов, сообщения в форумах), а возможно и деньги. Возможно это лоббирование интересов со стороны гомеопатов, т.к. большинство гомеопатов высказываются негативно в отношении вакцинации, рекомендуя заменить эпидемиологически обоснованный метод – вакцинацию, на недоказанный - гомеопатию.
Моей дочери 13 лет и она не болела ветряной оспой. Хотим сделать прививку, правильно ли мы поступаем?
Отвечает Харит Сусанна Михайловна
Да, чем старше ребенок, тем, к сожалению, больше вероятность тяжелого течения ветряной оспы, А так как это девочка, то нужно подумать и о том, что если заболевают ветряной оспой во время беременности, то это приводит к тяжелой патологии плода.
Можно ли взрослому привиться от ротавируса, если каждый год болею этим, нет желчного пузыря, спасибо!
Отвечает Харит Сусанна Михайловна
Нет, смысла в вакцинации для взрослых нет. Взрослые не болеют очень тяжело, а задача вакцины против ротавируса – предотвратить тяжелые формы заболевания с обезвоживанием у младенцев. Потом на протяжении всей жизни все равно заболевания возможны, но в легкой форме. Возможно стоит поговорить с гастроэнтерологом о профилактических мерах, например, лечении биопрепаратами.
У нас медотвод до 3 лет. Родились недоношенными,повышен. ВЧД, ВПК, ОАК, дмжп, дмпп . В роддоме получили гепатит в и после бцж и манту в 1 год и все. После всего увиденного болезней страшных боимся получать прививки. Когда мы собирались получить прививки от кори в тот момент столько детей стали инвалидом (есть дети дальних родственников возраст начиная год и старшекласники). При наших болячках можно ли нам делать прививки? Какие анализы сдавать перед прививкой?
Отвечает Полибин Роман Владимирович
Для ребенка, особенно при наличии указанных состояний опасны не прививки, а инфекции. Для проведения вакцинации обязателен осмотр врача перед прививкой, клинический анализ крови, при необходимости – общий анализ мочи и осмотр врача специалиста, у которого наблюдается ребенок с имеющимися заболеваниями.
Что делает эта прививка? Как решается проблема с заражением столбняком.
Отвечает Харит Сусанна Михайловна
Прививка против столбняка защищает от развития заболевания. Заражение столбняком происходит путем попадания спор бактерий, находящихся в загрязненных землей предметах, в поврежденные ткани. Споры столбнячной палочки истребить невозможно, поэтому проблема с заболеванием решается путем плановой вакцинации.
Подскажите пожалйста, как лучше и более аргументировано ответить на мнение студента-медика и вообще любого медработника: "я не делаю прививку от гриппа, потому что не известно какой вирус будет в этом эпидсезон, а прививку от гриппа разрабатывают летом, когда еще на знают актуальные штаммы будущей эпидемии". Другими словами какая вероятность в % того, что тривакцина от гриппа, которой ппививают осенью "перекроет" актуальные штаммы вируса в наступающем эпидсезоне зимой с учетом того, что возможно появление одного или нескольких новых штаммов. Буду также благодарен, если Вы сбросите ссылки на первоисточники таких данных, чтобы мои слова были более убедительны.
Отвечает Полибин Роман Владимирович
Главными аргументами в необходимости профилактики гриппа являются сведения о высокой контагиозности, тяжести, многообразии осложнений этой инфекции. Грипп чрезвычайно не только для групп риска, но и для здоровых людей среднего возраста. Такое частое осложнение как пневмония протекает с развитием РДС и летальностью, достигающей 40%. В результате гриппа могут развиваться синдром Гудпасчера, Гийена-Барре, рабдомиолиз, синдром Рейе, миозит, неврологические осложнения и т.д. Причем среди умерших и лиц с тяжелыми осложнениями привитых людей не наблюдается!
Информацию о системе Глобального Надзора за гриппом можно найти на официальном сайте ВОЗ или сайте Европейского Региона ВОЗ.
JANGU BANATVALA 1 , PIERRE VAN DAMME 2 , STEPHAN OEHEN 3
1 Department of Microbiology, John Radcliffe Hospital, Oxford, UK
2 Centre for Evaluation of Vaccination, Department of Epidemiology, University of Antwerp, Antwerp, Belgium
3 University Hospital Zurich, Institute for Experimental Immunology, Zurich, Switzerland Продолжительный иммунитет к НВV-инфекции - в этом заинтересован каждый человек, врачи и медицинский персонал, занимающиеся вакцинацией, менеджеры, органы управления здравоохранением.
Продолжительный иммунитет означает, что в популяции будет поддерживаться иммунная защита от инфекции на достаточно высоком уровне, а также отпадет необходимость в проведении каких-либо промежуточных бустерных вакцинаций. В результате снижения заболеваемости и смертности от HBV-инфекции, снижения расходов на лечение заболевания и, конечно, снижения стоимости бустерных вакцинаций значительно возрастает экономическая выгода, связанная с существованием длительного иммунитета к инфекции.
Благодаря тому, что общедоступными становятся результаты долговременных исследований эффективности НВ-вакцин, а также накапливаются данные о взаимосвязи между иммуногенными свойствами вакцины, клеточным иммунитетом и иммунологической памятью, появилась возможность идентифицировать факторы, которые влияют на формирование иммунологической памяти к HBV-инфекции.
Иммуногенность первичной вакцинации позволяет прогнозировать и первичный и вторичный, анамнестический, ответ на НВ. Возможно, это имеет отношение и к иммунологической памяти и, как следствие, эффективности долговременной защиты от инфекции. Таким образом, напрашивается вывод, что использование высокоиммуногенных НВ вакцин создаст оптимальные условия для полноценного формирования иммунологической памяти и продолжительного иммунитета к HBV-инфекции.
Положение с НВ-вакцинацией в настоящее время
Финансовые проблемы заметно ограничивают использование НВ-вакцин. Несмотря на то, что снижение цены на НВ-вакцину в развивающихся странах с 20 USD до 3,0-5,0 USD за одну дозу сделало возможным массовое использование этой вакцины в детских иммунизационных программах, она по-прежнему остается дороже большинства других вакцин. В настоящее время во многих странах рекомендуется проводить периодические бустерные вакцинации даже иммунокомпетентных лиц, кроме того, бустерные дозы предусмотрены для иммунокопромитированных субъектов в случае снижения титра антител против поверхностного антигена HBV (анти-HBs) ниже 10 mlU/ml. Однако результаты научных исследований не подтверждают необходимости рутинной бустерной вакцинации для поддержания долговременной иммунологической защиты в этих популяциях. Как следствие были предложены новые рекомендации, суммированные в таблице 1. Они ограничивают круг лиц, нуждающихся в бустерной НВ-вакцинации, до иммунокомпромитированных групп риска, таких как пациенты, которым проводится гемодиализ, страдающие хронической почечной недостаточностью или заболеваниями печени и ВИЧ-позитивные субъекты. Повсеместное распространение новой концепции приведет к существенной экономии средств и в развитых, и, что наиболее важно, в развивающихся странах. Однако наряду с признанием отсутствия необходимости в бустерной вакцинации важно учитывать и те соображения, которые позволят оптимизировать первичный курс вакцинации.
Существуют также данные о возможности снижения числа доз первичного курса иммунизации с трех до двух без какого-либо ослабления эффективности НВ вакцинации. Такое сокращение количества доз, наряду с экономией, связанной с повышением доступности комбинированных вакцин, включающих НВ, окажет важнейшее влияние на расширение охвата прививками населения, необходимого для достижения цели глобального искоренения HBV-инфекции.
| Группы, в которых традиционно проводится бустерная НВ-вакцинация | Группы, в которых бустерная вакцинация предусмотрена новыми рекомендациями |
| Иммунокомпетентные лица
Медицинские работники и другие служащие с профессиональным риском заражения Группы повышенного риска Иммунокомпромитированные лица
| |
Что означает иммунитет к HBV?
Важно провести разграничение между защитой от субклинической и клинически выраженной инфекции. Клинически выраженная инфекция, которая может быть идентифицирована путем определения HBsAg и приводящая к клиническому заболеванию, после вакцинации не наблюдалась. Так называемая скрытая, или субклиническая, инфекция приводит к сероконверсии с появлением анти-HBs (антитела к ядерному НВ-антигену), протекает с транзиторной виремией и без выраженных симптомов, а также без заболевания. У индивидуумов, которые были ранее вакцинированы, но содержание анти-HBs значительно снизилось (до неопределяемого уровня), может произойти анамнестическое повышение содержания специфических антител за период менее 4 дней с момента вирусной "атаки". В то время, когда инфекция еще ограничивается небольшим количеством гепатоцитов, быстрое образование антител В-клетками памяти позволяет предотвратить распространение вируса и пресекает инфекцию до того, как появляется риск развития хронического вирусоносительства.
Иммунный ответ при естественном заражении HBV
Течение HBV-инфекции определяется сложным взаимодействием между различными составляющими антивирусного иммунного ответа хозяина. Гуморальный иммунный ответ, в ходе которого появляются нейтрализующие антитела к поверхностному антигену HBV (HBsAg), является необходимым условием эффективного клиренса вируса. Нейтрализующие антитела синтезируются активированными В-клетками. После заражения HBV невакцинированного человека протективные антитела появляются на 50-150-й день, в то время как цитопатические вирусы вызывают более быструю ответную реакцию (6-14-й день).
Клеточный иммунный ответ играет решающую роль в клиренсе HBV из инфицированных гепатоцитов. Вплоть до недавнего времени считалось, что это происходит исключительно в результате деструкции гепатоцитов цитотоксическими Т-клетками (CTL). Однако Т-хелперные клетки-индукторы вирус-специфических CTL играют еще и другую роль, состоящую в секреции нецитотоксических цитокинов: y-интерферона (IFNg) и фактора некроза опухолей-а (TNF-а), которые способны подавлять экспрессию вирусных генов и таким образом "лечить" инфицированные клетки.
Иммунный ответ, индуцированный НВ-вакцинацией
Большинство работ в этой области характеризует иммунный ответ на HBsAg, используемый в производстве рекомбинантных НВ-вакцин. Основные рекомбинантные НВ-вакцины, которые успешно используются с момента их внедрения в 1986 году, содержат дрожжевой HBsAg. Введение вакцины приводит к презентации HBsAg по классической схеме, то есть от антиген-презентирующих клеток (АПК) - Т-хелперным лимфоцитам (CD4), которые распознают антиген в комплексе с молекулами II класса МНС на АПК. Т-хелперные клетки запускают дифференцировку HBsAg-специфических В-лимфоцитов в быстро пролиферирующие анти-HBsAg иммуноглобулин (IgG)-продуцирующие клетки. Антиген-специфические В-клетки ответственны за продукцию анти-HBs (IgG). Вслед за первичным иммунным ответом образуются В- и Т-клетки памяти, которые способствуют стремительному протеканию последующих анамнестических реакций.
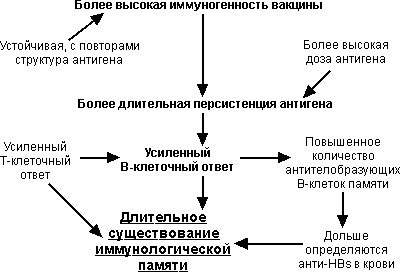
Влияние антигена на формирование иммунологической памяти:
- персистенция антигена играет важную роль в образовании антител-продуцирующих В-клеток памяти и, следовательно, в поддержания протективного уровня антител;
- персистенция антигена зависит от введенной дозы и возрастает с ее увеличением;
- нереплицирующиеся антигены с наиболее высоким числом повторов индуцируют наиболее сильный В-клеточный ответ
Зависимость гуморального иммунного ответа от Т-клеток привела к появлению работ, исследующих взаимосвязь между уровнем антител и лимфопролиферацией. Эксперименты с использование спот-фермент-связанного иммуносорбентного анализа (spot-ELISA), метода определения in vitro способности циркулирующих В-лимфоцитов продуцировать анти-HBs, продемонстрировали тесную корреляцию между продукцией анти-HBs IgG in vitro и иммунологической памятью (характеризуемой частотой В-клеток памяти). Статистически достоверная корреляция также была обнаружена между кинетикой и нарастанием содержания антител in vivo и Т-клеточным иммунным ответом in vitro.
Иммунологическая память
Механистической основой иммунологической памяти являются селективная экспансия и дифференцировка клонов антиген-специфических В- и Т-лимфоцитов. В то время как В-клеточный ответ - основной фактор иммунологической памяти, общепризнанным является факт, что наличие Т-клеток способствует В-клеточной персистенции и что "память" формируется в результате сложных взаимодействий В-, Т-, CTL-клеток памяти и комплексов антиген-антитело. Формирование иммунологической памяти - ключевая особенность специфического иммунного ответа, эту функцию выполняют В- и Т-лимфоциты памяти, синтезируемые в результате первичной антигенной стимуляции. Эти клетки сохраняют способность к быстрой пролиферации, дифференцировке и, в случае В-клеток памяти, быстрой продукции специфических антител при последующей встрече с идентичным антигеном. Иммунологическая память, таким образом, может рассматриваться как адаптивный иммунный ответ на антиген, который уже знаком иммунной системе. В обычных условиях вторичный иммунный ответ подразумевает продукцию сывороточных антител в более высокой концентрации и через более короткий промежуток времени по сравнению с первичным, кроме того, синтезируемые антитела обладают более высокой связывающей способностью. Для того чтобы понять, какие факторы оказывают воздействие на вакцин-индуцированную иммунологическую память, мы должны рассмотреть следующие иммунологические механизмы.
Персистенция иммунологической памяти к HBV
В то время как ответ CTL играет решающую роль в элиминации HBV из инфицированных гепатоцитов, гуморальный иммунный ответ ограничивает распространение инфекции путем нейтрализации вируса в крови, на слизистых и в экстраклеточном пространстве. Иммунологическая память к HBV, таким образом, фокусируется на быстром синтезе специфических антител. Имеющиеся данные говорят в пользу того, что иммунологическая память сохраняется после снижения содержания анти-HBs IgG ниже определяемого уровня. Действительно, анамнестический ответ, о котором судят по гуморальному ответу на бустерную вакцинацию, наблюдался у индивидуумов, у которых анти-HBs IgG не определялись на протяжении 28-31 месяца. Таким образом, снижение и практически исчезновение антител после первичной вакцинации не означает потери иммунитета, пока сохраняется иммунологическая память. Мощный Т-клеточный ответ также наблюдался спустя несколько лет после клинического разрешения острой HBV-инфекции.
В ходе испытания вакцин, а также в результате долговременных наблюдений за вакцинированными было показано, что иммунологическая память к НВ сохраняется в течение, по крайней мере, 5-12 лет.
Так как основная задача вакцинации в детском или подростковом возрасте состоит в формировании как можно более длительного иммунитета, используемая вакцина должна обладать оптимальными иммуногенными свойствами. Исследования вакцин-индуцированного иммунитета к НВ показывают, что вакцинация приводит к формированию иммунитета к инфекции и он сохраняется даже в том случае, когда антитела в крови уже не определяются. Предположение о том, что у адекватно вакцинированных лиц имеет место иммунологическое праймирование, подтверждается данными о том, что HBsAg-специфические лимфоциты памяти циркулируют в периферической крови вакцинированных людей, даже если у них к тому времени уже не обнаруживаются специфические антитела. Однако было показано, что гуморальный ответ на завершенный первичный курс вакцинации тесно коррелирует с будущей реакцией на ревакцинацию. Иммуногенность первичной вакцинации, таким образом, является ключевым фактором, определяющим силу последующего анамнестического ответа. Так как анамнестический гуморальный ответ зависит от В-клеток памяти, есть основания считать, что более сильный вторичный иммунный ответ является индикатором более мощного потенциала В-клеток памяти, который, в свою очередь, отражает иммуногенность первичного курса иммунизации.
Взаимодействие антигена, гуморального и клеточного иммунного ответа в формировании иммунологической памяти (упрощенная схема)
Исследования, в которых иммунологическая память оценивалась путем проведения бустерной вакцинации, не только демонстрируют наличие иммунологической памяти, но подтверждают последние рекомендации об отсутствии необходимости и бустерной дозы для поддержания иммунитета.
Перспективы
Дальнейшее изучение вопросов, связанных с проблемой иммунологической памяти, в будущем, несомненно, окажет влияние на политику вакцинации против HBV. Проведенные в этом направлении исследования уже позволили сделать выводы о том, что В-клетки обеспечивают существование долговременной иммунологической памяти и о синергии Т- и В-клеточных реакций, которые, безусловно, внесут свой вклад в понимание механизмов формирования долговременной иммунологической памяти. Необходимо продолжать наблюдения за группами вакцинированных против гепатита В людей, анализируя и клеточный, и гуморальный иммунитет. Также следует оценить эффект объединения НВ-вакцины с другими детскими вакцинами в комбинированных препаратах.
Существующие на сегодняшний день представления о роли первичного иммунного ответа в формировании иммунологической памяти подчеркивают важность гарантии полноценного иммунного ответа на первичный курс вакцинации. Это тем более важно в плане снижения количества доз вводимой вакцины.

Коллективная защита
Новая интеллектуальная система информации о защищенности россиян от инфекций позволит контролировать уровень сопротивляемости жителей разных регионов. С ее помощью также планируется корректировать Национальный календарь профилактических прививок, уточнять сроки и географию охвата населения вакцинацией.
В пилотном режиме система с 2018 года действует в девяти регионах России, в том числе в Москве, Подмосковье, Санкт-Петербурге, Крыму и Новосибирской области. У добровольцев разных возрастов берут анализы крови и определяют, антитела или антигены к каким заболеваниям содержатся в сыворотке. Вместе с анализами доброволец анонимно заполняет анкету, которая содержит некоторые социально-демографические данные о нем, например, пол и возраст. Результаты лабораторных исследований и анкетные данные специалисты заводят в геоинформационную систему Atlas, которая и помогает сделать вывод об общем иммунитете населения.
Бокс пробоподготовки (сортировка, маркировка, центрифугирование) в микробиологической лаборатории в Краснодарском крае

Внедрение мониторинга коллективного иммунитета планируют завершить во второй половине 2020 года. В списке уже более 20 заболеваний: это краснуха, ветряная оспа, туберкулез, гепатиты, энцефалит, менингококковая инфекция и другие.
Новый агент

Пока коронавирус 2019-nCoV — новый инфекционный агент. Он проник в человеческую популяцию не ранее ноября 2019 года, поэтому эффективного и специфического иммунитета у населения быть не может. Однако возможна иммунологическая память на другие родственные коронавирусы, отметил Владимир Гущин. Как она влияет на восприимчивость к 2019-nCoV, еще предстоит выяснить.
— Говоря о коллективном иммунитете и иммунологической памяти к 2019-nCoV, чрезвычайно важно понять, у скольких людей заболевание протекает в инаппарантной форме (без клинических признаков) и что происходит с иммунитетом к этому вирусу. Понимание механизмов формирования иммунологической памяти позволит подобрать средства противодействия и спланировать защиту населения, — отметил Владимир Гущин.
Бокс секвенирования ДНК (технология длинных чтений ДНК) в микробиологической лаборатории в Краснодарском крае
По его словам, для изучения иммунитета к 2019-nCoV понадобится инактивированный (безопасный) вирус или его антигены. При этом технически возможно оценивать как гуморальный иммунитет (защита посредством антител), так и клеточный (когда вся клетка участвует в реакции на вирус). Сейчас в Китае и других заинтересованных странах активно идут такие исследования.

Если говорить про изучение коллективного иммунитета к коронавирусу, то для его оценки, прежде всего, необходимо рассчитать уровень антител в крови, не позволяющий человеку заразиться. Для большинства инфекций, управляемых вакцинацией, он известен.
Также ученым нужно проанализировать образцы сывороток крови от больных и здоровых и создать стандарты, позволяющие количественно измерять защитный уровень антител. Наконец, предстоит рассчитать, сколько людей с защитным титром антител в популяции понадобится, чтобы уберечь всё население от коронавируса, особенно восприимчивых пациентов. Это и есть главное свойство коллективного иммунитета.
Когда новый коронавирус будет изучен, данные больных людей российским специалистам уже не понадобятся. Потребуется сыворотка крови здоровых, чтобы оценить, есть ли у них предварительно существующий иммунитет и какого он качества.
— Не исключено, что коронавирус станет чем-то обыденным, вроде кори, и мы будем прививаться от него. Если иммунитет окажется нестойким, то возможна повторная вакцинация. Чтобы это определить, и потребуется мониторинг коллективного иммунитета, — отметил Владимир Гущин.
Работа медиков реанимационного отделения больницы Чжуннань при Уханьском университете во время вспышки нового коронавируса
Вице-премьер РФ Татьяна Голикова 6 февраля заявила, что российские медики, прибывшие в Китай, до сих пор не получили живой штамм нового коронавируса. Без него нельзя разработать вакцину против 2019-nCoV.

— У нас огромное количество патогенных вирусов. При 2019-nCoV смертность составляет примерно 2%. Когда была вспышка той же атипичной пневмонии, она достигала 10–15%. Именно смертность, на мой взгляд, — главный критерий при выборе заболевания для исследования, — сказал парламентарий.
Депутат Госдумы, экс-руководитель Роспотребнадзора Геннадий Онищенко напомнил, что сама идея исследования коллективного иммунитета не новая. Что касается коронавируса, то, по его мнению, в ближайшие месяцы опасность нашей стране не грозит.
Карантин продолжается
Утром 6 февраля власти Китая заявили, что общее число зараженных новым коронавирусом превысило 28 тыс. человек, 563 больных скончались. Почти 4 тыс. пациентов находятся в тяжелом состоянии. 1,15 тыс. человек выздоровели и были выписаны из больниц.
Счетчик китайского издания South China Morning Post вечером 6 февраля сообщил о 28 403 случаях по всему миру. Из них 28 164 зарегистрированы в Китае. Всего вирус обнаружен в 26 странах.
Всемирная организация здравоохранения (ВОЗ) приняла решение созвать 11–12 февраля глобальный форум по вопросам изучения 2019-nCoV и разработки вакцины от него.
Читайте также: