Иммунодефицит при вирусе эпштейна

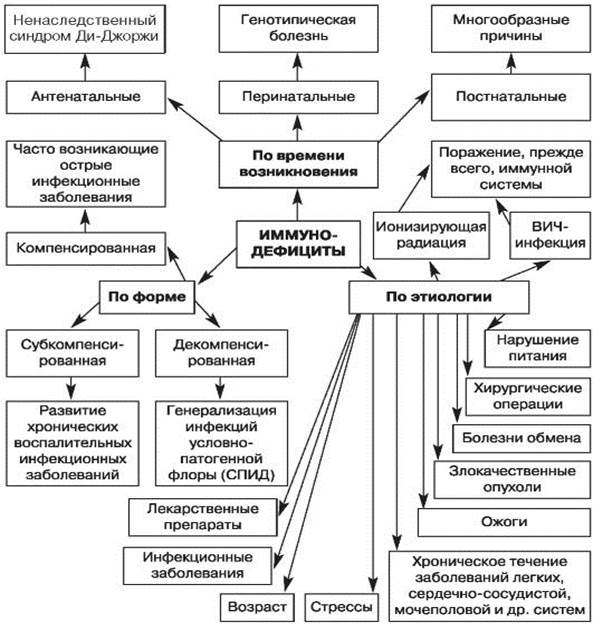
Рис. 1. Классификация вторичных иммунодефицитов по времени возникновения, этиологии, форме (по Белозерову Е.С. и др., 1992) [3]
Подводя итог в теоретической составляющей статьи – актуальности, необходимо обобщить следующее.
В педиатрии (17 лет 11 месяцев и 29 дней) в доминирующем большинстве речь идет об антенатальных и перинатальных иммунодефицитных болезнях, вторичных по отношению к анатомо-морфологическому субстрату иммунной системы – функциональных.
Таким образом, заключение врача-иммунолога должно быть сформулировано следующим образом. Антенатальная (или функциональная) иммунодефицитная болезнь, смешанного типа (или, при возможности, по отдельным звеньям, что мало вероятно), комбинированная индукция (инфекционная, гипоксическая и т.д.) с клиническими проявлениями основных синдромов – инфекционного, аллергического, аутоиммунного, неопластического и/или лимфопролиферативного.
Данные теоретические изыскания легли в основу целого цикла научно-исследовательских работ. Одно из таких исследований представлено в данной статье и посвящено исследованию иммуноиндуцирующей роли герпеса 4 типа - вируса Эпштейна-Барр у детей.
Цель: изучение особенностей клинических проявлений у детей с герпес-индуцированными формами иммунодефицитов (на примере 4 типа герпеса).
Все дети (100%) относились к часто и длительно болеющим, при этом 72 ребенка были неорганизованными (22,5%). У 78 (24,4%) детей были зарегистрированы признаки рецидивирующей герпетической инфекции с локализацией на губах, крыльях носа, слизистой оболочке полости рта. Ежегодно 92 ребенка (28,4%) переносили бактериальные инфекции в виде тонзиллитов, пневмоний, пиелонефритов, фурункулезов, гнойных конъюнктивитов, отитов, рино-синуситов. Признаки лимфоаденопатии (микролимфоаденопатии) регистрировались у 270 детей (84,4%). У 2 детей были диагностированы неопластические процессы (один ребенок умер в 2009 году). Одна девочка с лейкемоидной реакцией наблюдается у гематоонколога в течение 2 лет. Субфебрильные реакции более 12 месяцев были зарегистрированы у 39 детей (12,2%). Грубые неврологические нарушения (преимущественно двигательные) были зафиксированы у 43 детей (13,4%) (рис. 2).
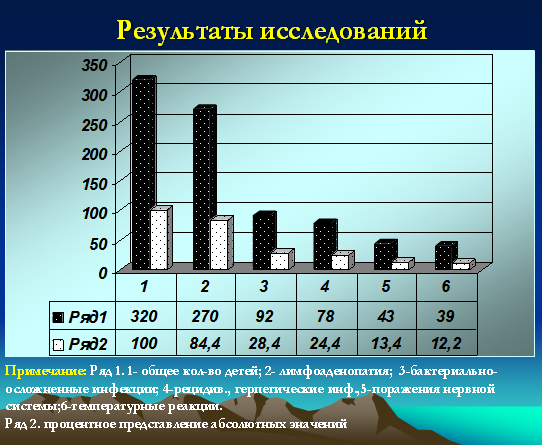
Рис. 2. Частота распределения клинических проявлений у детей с герпесиндуцированными иммунодефицитами
Иммунологические данные (в т.ч. данные лейкограммы), кроме количества лейкоцитов и лимфоцитов (абсолютное и относительное количество), носили неоднозначный характер. Классический супрессорный тип (в т.ч. и со снижением клеток цитолитической направленности) выявлялся у 108 детей (33,7%). Активация в системе клеток естественной цитотоксичности (CD16+) зафиксирована у 52 детей (16,2%). Увеличение В-клеточного пула было зарегистрировано у 38 детей (11,8%). Интересными, на наш взгляд, были полученные данные по CD95 маркеру, у 92 (28,7%) детей данный показатель был резко повышен и достигал значений 20-25%, у 30 (9,3%) детей указанный показатель не превышал 3% (рис. 3).
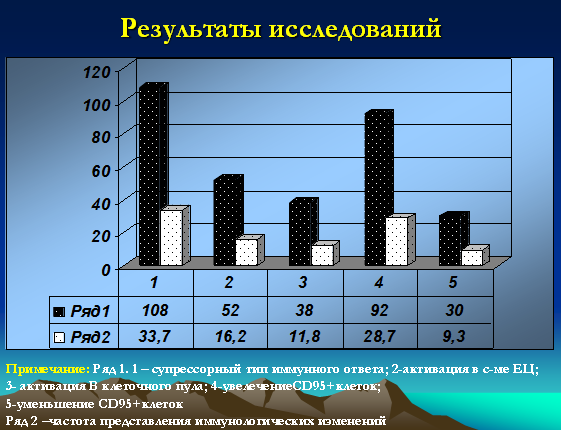
Рис. 3. Иммунологические особенности (типы распределения) у детей с герпесиндуцированными иммунодефицитами
ИФА, проведенный у детей, выявил 100% контаминацию вирусом ЭБ. Определялась следующая совокупность специфических антител:
- IgM к VCA (к капсидному антигену) – выявляются в крови в первые дни и недели болезни, максимально сохраняются до 3-4 недель;
- IgG к VCA (к капсидному антигену) – появляются в крови спустя 1-2 месяца от начала болезни, затем постепенно снижаются и сохраняются на пороговом (низком уровне) пожизненно. Повышение их титра характерно для обострения хронической ЭБВИ;
- IgM к EA (к раннему антигену) – появляются в крови в первую неделю заболевания, сохраняются в течение 2-3 месяцев и исчезают. Могут сохраняться в высоких титрах длительное время (более 3-4 месяцев), тревожно в плане формирования хронической формы ЭБВИ. Появление их при хронической инфекции служит индикатором реактивации;
- IgG к ЕA (к раннему антигену) – появляются к 3-4-й неделе заболевания, становятся максимальными на 4-6-й неделе болезни, исчезают через 3-6 месяцев. Появление высоких титров повторно указывает на активацию хронической инфекции;
- IgG к NA-1 или EBNA (к нуклеарному или ядерному антигену) – являются поздними, поскольку появляются в крови через 1-3 месяца после начала заболевания. При этом острофазные антитела выявлялись (IgM к VCA и IgM к EA) у 42 детей (13,1%), у 268 (83,7%) детей титры антител (IgG VCA + IgG к NA-1 или EBNA) значительно превышали нормативные и достигали значений более 160, у 10 (3,1%) детей диагностически значимых титров выявлено не было [9; 13] (рис. 4).
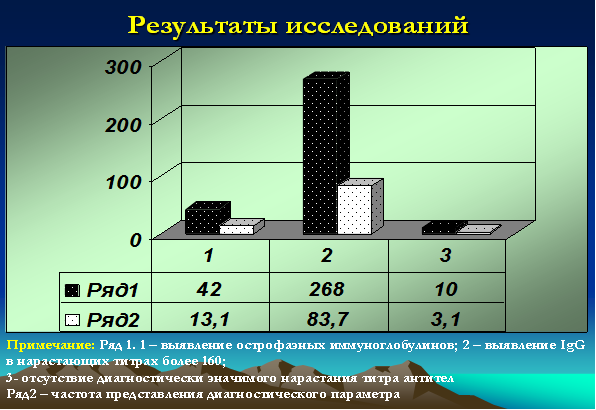
Рис. 4. Серологические исследования у детей с герпесиндуцированными иммунодефицитными болезнями
Клинические, иммунологические и этиологические сопоставления выявили следующие закономерности.
Отдельно хочется остановиться на методах ПЦР-диагностики. В литературе активно обсуждается вопрос об использовании ПЦР для исследований на инфекции семейства герпес в различных биологических субстратах. Здесь необходимо понимать, что данный метод, особенно при использовании его для исследования плазмы, имеет свои особенности – он всегда количественный! Определение качественное не имеет смысла, так как инфекция пожизненно персистирует в организме человека. Как у больных ЭБВИ, так и у носителей может быть положительная ПЦР. Поэтому для их дифференцировки проводится ПЦР-анализ с заданной чувствительностью: для носителей до 10 копий в пробе, а для активной инфекции – 100 копий в пробе. Специфичность данного метода хоть и достигает 100%, при этом не исключает ложноположительные результаты, т.к. ПЦР-анализ информативен только при размножении (репликации) вируса, то существует и определенный процент ложноотрицательных результатов с отсутствием репликации в момент исследования [5; 9].
В результате проведенного нами исследования, ПЦР крови всегда имела отрицательный результат, даже у детей с неопластическими процессами. Распределение ПЦР-положительных результатов у детей со слизистых оболочек (ротоглотка, нос) и мочи имело следующее цифровое распределение.
Положительные реакции с 3 биологических объектов имели 36 детей (11,25%), у 62 положительные ПЦР реакции были с зева и носа – 19,38%, у 43 детей диагностировали положительный результат только с зева (13.44%), и 71 ребенок имели положительные значения ПЦР со слизистой оболочки носа (22,19%). Положительные значения только в моче имели 51 ребенок (15,94%). Остальные дети (в количестве 57) имели отрицательный результат ПЦР-исследований с биологических сред.
Дети с неопластическими процессами, длительным субфебрилитетом, лейкемоидной реакцией, лимфоаденопатией имели признаки активации хронической инфекции, резкое увеличение CD95+ клеток, положительные маркеры наличия и обострения ВЭБ в ИФА и ПЦР-исследованиях.
Таким образом, все дети имели индуцированные формы функциональной иммунодефицитной болезни, доминирующей причиной которой являлся вирус ЭБ. Проведенные предварительные клинико-иммунологические исследования наглядно демонстрируют необходимость комплексного обследования детей с функциональными нарушениями в системе иммуногенеза с обязательной оценкой уровня инфекционной (вирусной) контаминации. Выявление основных причин трактуется необходимостью применения комплексных методов лечения, в т.ч. и с применением противовирусных препаратов.
Вирус Эпштейна — Барр (ВЭБ, EBV), он относится к герпесвирусам человека 4 типа. Это древний вирус, и он с нами и нашими предками, вероятно, несколько десятков миллионов лет. ВЭБ инфицирована большая часть людей на планете, и у большинства людей первая встреча с вирусом протекает бессимптомно, у некоторых — с однократным развитием симптомов инфекционного мононуклеоза. Однажды встретив ВЭБ — вы с ним навсегда. Эрадикация вируса на сегодня невозможна, да и не имеет никакого смысла.
Самая известная и распространенная форма заболевания, связанного с ВЭБ, — инфекционный мононуклеоз (ИМ), он развивается при первичном инфицировании. Вирус приобретают в детском возрасте, в развивающихся странах к 3-4 годам, в развитых странах процесс иногда затягивается до подросткового возраста, но все равно почти неизбежно наступает.
Латентная бессимптомная инфекция характерна практически всем, кто встретился с ВЭБ, и длится всю нашу жизнь. Вирус в латентной фазе находится в В-лимфоцитах и не размножается, а копирование генетического материала происходит вместе с делением лимфоцитов. Иногда случайным образом могут запускаться продуктивные циклы ВЭБ, и вот тогда бессимптомные носители инфекции и распространяют вирус далее.
ВЭБ имеет доказанную онкогенность. ВЭБ способен провоцировать слаборегулируемое деление клеток, что несет риски возникновения лимфопролиферативных заболеваний и эпителиальных опухолей.
Онкогенный потенциал ВЭБ может реализоваться, если клетки содержат генетические дефекты, не связанные с ВЭБ, но связанные с пролиферацией в присутствии вируса, также онкогенный потенциал может реализоваться при выраженном иммунодефиците: при ВИЧ-инфекции в стадии СПИД (чаще при уровне CD4-лимфоцитов менее 100 клеток в мкл), после трансплантации органов, при врожденных иммунодефицитах.
С ВЭБ связывают такие заболевания, как лимфома Беркитта, лимфома Ходжкина и неходжкинские лимфомы, назофарингеальная карцинома, волосатая лейкоплакия, ВИЧ-ассоциированные лимфомы ЦНС, посттрансплантационное лимфопролиферативное расстройство, Х-сцепленное лимфопролиферативное расстройство. В редких случаях ВЭБ может вызывать гепатиты, пневмонии, энцефалиты и т.д. за счет инфильтрации органов пораженными ВЭБ лимфоцитами.
Повышение anti-VCA IgM в плазме крови наблюдается при первичном инфицировании, а вот наличие anti-VCA IgG и anti-EBNA IgG говорит о давнем присутствии вируса в организме. В обычной работе терапевта определение антител (все классы) к ВЭБ имеет смысл почти исключительно в одной ситуации: дифдиагностика между ангиной и инфекционным мононуклеозом для принятия решения о целесообразности применения антибиотиков.
При заболеваниях, связанных с ВЭБ, к каковым относятся хроническая активная ВЭБ-инфекция и некоторые лимфопролиферативные заболевания, обязательно обнаруживаются клеточные инфильтраты из лимфоцитов, пораженных ВЭБ — увеличение лимфоузлов, селезенки, гепатит, пневмония и другие состояния - в зависимости от пораженного органа и клинической формы. Все клинические формы заболеваний, связанные с ВЭБ, так или иначе опосредованы лимфопролиферацией.
Противовирусные препараты не имеют смысла при латентной инфекции, когда поражения возникают из-за пролиферации пораженных лимфоцитов, а не из-за прямого действия вируса. В таких случаях применяют средства, направленные на снижение пролиферации клеток, а вот воздействовать на вирус в данном случае нет смысла, так как его репликация не происходит, а генетический материал вируса дублируется с делением клеток, которое запускается вирусным белком-промотором пролиферации LMP (latent membrane protein).
Фото: изображение ВЭБ, полученное при помощи электронного сканирующего микроскопа (Weisser, M., 2009).
- Arvin A, Campadelli-Fiume G, Mocarski E. Human Herpesviruses: Biology, Therapy, and Immunoprophylaxis. Cambridge University Press; 2007.

Вирус Эпштейна-Барр (далее — ВЭБ), официально — Human gammaherpesvirus 4, — один из 8 известных науке типов герпесвирусов и, с высокой вероятностью, самый распространённый вирус человека.
Например, в США у более 90 % взрослых и 50 % детей есть признаки инфицирования ВЭБ. Американские врачи считают, что оставшиеся 10 % взрослых просто не обследованы. В России медики определяют уровень инфицированности взрослого населения 97 %.
Особый случай — инфицирование при пересадке органов. В связи с распространением трансплантаций подобные инфекции встречаются всё чаще и вызывают нетипичные осложнения и заболевания после трансплантации.
Опасность вируса в том, что в активной форме он становится причиной инфекционного мононуклеоза, связан с возникновением лимфомы Беркитта, гемофагоцитарного лимфогистиоцитоза, лимфомы Ходжкина, рака желудка, рака носоглотки, лимфомы центральной нервной системы, синдрома Алисы в стране чудес (нарушение восприятия), острой мозжечковой атаксии (нарушение походки, движений).
По данным, полученным врачами Cincinnati Children’s Hospital Medical Center — Медицинского центра Цинцинатти (США), ВЭБ может послужить причиной развития рассеянного склероза, целиакии, системной красной волчанки, диабета I типа, ювенильного идиопатического артрита, ревматоидного артрита. Даже хроническая усталость человека связана напрямую с ним.
Показания к проведению анализа

Симптомы заражения при постепенном развитии:
температура повышается до субфебрильных показателей — 37,1—38,0 °C;
появляются катаральные симптомы — отёчность носа и носоглотки, заложенность, слизистая носоглотки становится красной, нёбные миндалины тоже краснеют;
лимфатические узлы — подчелюстные, на затылке, шее) отёчные, на ранней стадии — неболезненные или со слабыми болезненными ощущениями.
Симптомы заражения при остром начале болезни:
резкое повышение температуры до 38—39 °C;
лихорадка с ознобом и повышенным потоотделением;
боль в скелетных мышцах;
боль в горле при сглатывании;
У заражённых увеличиваются селезёнка, печень, появляется сыпь на 3—5 день. Иногда увеличенная селезёнка разрывается.
Однако единой, характерной симптоматики не существует — признаки заражения учёные объединили в "мононуклеозоподобный синдром". Потому при любых проявлениях необходимо сдать анализы на обнаружение вируса.
Анализы на вирус Эпштейна-Барр
Направление на анализы даёт терапевт, инфекционист, врач общей практики, педиатр. Исследование проводится на различном биоматериале — сыворотке крови, мазках и соскобах слизистой ротоглотки, урогенитального тракта, слюне, цереброспинальной жидкости, лейкоцитах периферической крови.
Для выявления инфекции чаще прочего проводят серологические тесты. Однако часто требуется комплексное тестирование, потому что серологические тесты в случаях переливания крови, иммунодефицита и некоторых других противоречат друг другу. Точную клиническую картину в сложных случаях даёт ПЦР-диагностика на ДНК ВЭБ.
Вирус определяется только лабораторными способами, причём в большинстве случаев требуется несколько тестов, чтобы исключить прочие инфекционные заболевания.
Общий анализ крови на вирус Эпштейна-Барр
Общий анализ крови не позволяет установить точно ВЭБ. Определение лейкоцитоза, лимфоцитоза, атипичных мононуклеаров свидетельствует лишь о наличии инфекционного заболевания, но не даёт его идентифицировать. Однако, если определено отсутствие лейкоцитоза, то можно с уверенностью говорить, что инфекционного мононуклеоза нет. Другими признаками против диагноза ВЭБ являются анемия и тромбоцитопения.

Если общий анализ крови вызывает подозрения на ВЭБ, проводят дополнительные исследования.
В биохимическом анализе при инфицировании ВЭБ наблюдают:
повышение АЛТ, или аланинаминотрансферазы, — фермента печени, почек, поджелудочной железы;
повышение АСТ, или аспартатаминотрансферазы, — фермент преимущественно клеток сердца и печени;
повышение ЩФ, или щелочной фосфатазы;
повышение билирубина — главного компонента желчи;
Изменение биохимических показателей печени характерны для 90 % инфицированных.
Гетерофильный тест, или реакция Пауля и Буннеля, основана на определении в сыворотке крови противобараньих агглютининов. Тест выявляет гетерофильные антитела, и при титре 1:224 ставится диагноз мононуклеоза.
Гетерофильный тест даёт положительный результат у 60 % инфицированных спустя 2 недели после обнаружения симптомов и у 90 % инфицированных спустя месяц после первых клинических проявлений. Потому точность его невелика, а на начальной стадии он не помогает определить ВЭБ, т. к. титр гетерофильных тел повышается и в ответе на другую вирусную инфекцию.
Чувствительность теста у детей составляет менее 70 %, а способность идентифицировать вирус — менее 20 %. С возрастом пациентов польза теста и его чувствительность/специфичность увеличиваются.
Жизнедеятельность ВЭБ в организме (завершённый и незавершённый литический (активный) цикл, латентная фаза) происходит на фоне выработки специфических антител к белкам вируса. Исследование антител позволяет определить и дифференцировать острую форму, перенесённую инфекцию и хроническую инфекцию вирусом.
На ранних стадиях (3—4 недели после заражения и до 3—4 месяцев после) определяются иммуноглобулины IgG к ранним антигенам EA — их считают маркерами острой стадии инфекции, хотя нередко они выявляются и при хроническом инфицировании.
Иммуноглобулины IgG к VCA — капсидному белку — определяются в момент проявления болезни и считаются маркерами острого стадии болезни. Они пропадают через несколько недель. Однако есть люди, у которых VCA-IgM не определяются, потому всегда необходимо комплексное тестирование.
Антиген EBNA IgG не определяется на начальной стадии заболевания, потому свидетельствует о перенесённой или хронической инфекции. Последняя отличается высоким титром антигена.
ПЦР-диагностика относится к высокочувствительным тестам при инфицировании ВЭБ. Для её проведения используют лейкоцитарную фракцию крови.
Если ДНК вируса выявляется в плазме крови, то ставится диагноз инфекции в активной форме. ДНК вируса выявляется даже в период латентной фазы у людей, признанных клинически здоровыми — 0,1–1 копий/106 клеток. Хроническая и острая стадия выявляются количественной ПЦР.
Если вирусная нагрузка высока, она может ассоциироваться с большим риском тяжёлых осложнений и требует антивирусной терапии. ДНК в ликворе говорит, что вирус активно размножается в нервной системе — эту ПЦР-диагностику ВЭБ проводят, когда выявляют этиологию поражения нервной системы.
ПЦР проводят при выявлении опухолей, тяжёлых осложнений. В этом случае ДНК вируса обнаруживают в лимфоузлах, слизистой кишечника, биоптатах печени. ПЦР необходимо и при заболеваниях, возникших после трансплантации органов.
Однако отрицательный результат ПЦР-диагностики не исключает репликации вируса в лимфоузлах, костном мозге, дерме, желудке и кишечнике. Потому ПЦР рекомендовано использовать всегда в сочетании с серологическими методами диагностики ВЭБ.
Профилактика и рекомендации
Не заразиться ВЭБ в современном мире почти невозможно. Для этого пришлось бы исключить всякие контакты с людьми, причём с рождения, никого не целовать, не вступать в сексуальные отношения.
Как ни парадоксально, но лучше, если заражение случится в детском возрасте, потому что дети легче переносят инфекцию (как, к примеру, и ветряную оспу, вызванную также герпесвирусом, только 3 типа), у них вырабатывается стойкий иммунитет.

Инфицирование в детстве характерно для стран с низким уровнем жизни, в подростковом и взрослом — с высоким уровнем жизни. Играет роль санитарная культура, общая культура людей. Но она же приводит и к более серьёзным последствиям инфекции, потому что иммунный ответ человека, живущего в благоприятных условиях, намного слабее.
Только иммунитет способен защитить нас от вируса Эпштейна-Барр. Попав в организм, он сохраняется в нас до конца жизни в латентной фазе. Снижение иммунитета, вызванное заболеваниями, образом жизни, ведёт к реактивации ВЭБ и непредсказуемым последствиям — учёным пока удалось только выявить ассоциированные с вирусом заболевания (о чём мы говорили вначале), но не установить закономерность их развития.
Инфекции против ВЭБ также не существует. Обезопасить себя можно хотя бы от повторного заражения, не целуясь, не пользуясь чужой посудой, едой, зубными щётками и другими личными вещами.
При появлении каких-либо симптомов заболевания следует обратиться к врачу или самостоятельно прийти в лабораторию, чтобы сдать анализы на выявление ВЭБ.
Если заражение обнаружено (острая фаза), то нужно отказаться от выхода на работу, посещения общественных мест, потому что вы становитесь распространителем инфекции, обеспечить себе покой, обильное питьё, хорошо питаться. При возникновении тяжёлых симптомов следует немедленно обратиться к врачу — будет назначено симптоматическое лечение, поддерживающая терапия.
Стоимость тестирование на вирус Эпштейна—Барр в АО "СЗДЦМ"
В АО "СЗДЦМ" вы сможете пройти все тесты на определение ВЭБ по низкой цене. Так как диагностика в большинстве случаев требует комплексного тестирования, исследования в медицинских центрах и лабораторных терминалах АО "СЗДЦМ" не станет финансово обременительным для вас — стоимость услуги в наших медучреждениях доступна для всех категорий населения.
Наши врачи-специалисты назначат вам только необходимые анализы, которые позволят поставить точный диагноз. Первое исследование и общий анализ крови можно сделать и без назначения врача, но последующие (если будут подозрения) мы рекомендуем делать только по назначению, чтобы не проводить бесполезных в вашем случае тестов.
Где сдать анализы на вирус Эпштейн—Барр
Сдать любые анализы на ВЭБ вы можете в наших медицинских центрах и лабораторных терминалах. Выбрать ближайшее к вам медучреждение можно по карте, таблице или выпадающему меню.
Рядом с названием медучреждения вы увидите точный адрес, часы работы, а по карте легко составить маршрут для посещения лаборатории на общественном транспорте или личном автомобиле.
Лаборатория АО "СЗЦДМ" предлагает услуги, обеспечивающие комплексное и преемственное лабораторное обследование пациента
Диагностика В медицинских центрах АО "СЗЦДМ" проводят качественные диагностические исследования всего организма
Лечение Наши медицинские центры ориентированы на обслуживание пациентов в амбулаторном режиме и объединены единым подходом к обследованию и лечению пациентов.
Реабилитация Реабилитация - это действия, направленные на всестороннюю помощь больному человеку или инвалиду для достижения им максимально возможной полноценности, в том числе и социальной или экономической.
Выезд на дом Внимание! Действует акция "Выезд на дом - 0 рублей"
Профосмотры АО "СЗЦДМ" проводит профилактические осмотры работников, которые включают в себя - комплексы лечебных и профилактических мероприятий, проводимых для выявления отклонений в состоянии здоровья, профилактики развития и распространения заболеваний.
Главная > Консультации > Детский врач > Существуют ли инфекции, способные спровоцировать рак? Онкогенные инфекции
В настоящее время доказано, что от 15 до 20% новообразований человека имеют вирусное происхождение.
Вирусами называют мельчайшие организмы, большую часть из которых нереально разглядеть, даже используя обыкновенный микроскоп. Они состоят из небольшого количества ДНК и РНК генов, которые находятся в белковой капсуле. Эти вирусы проникают в живые клетки, где впоследствии начинают размножаться. Бывают также вирусы вызывающие рак, которые могут помещать свою ДНК в клетки, в скором времени спровоцировав появление онкологических заболеваний. Характерной чертой онкогенных вирусов является то, что они могут стимулировать клетки размножаться с необычно высокой скоростью, что может привести к повреждению генетического материала в этих клетках. Дополнительные факторы, такие как курение или воздействие определенных канцерогенов, могут вызывать окончательное превращение нормальных клеток в раковые. Эти воздействия (дополнительные факторы), наряду с индивидуальными генетическими особенностями каждого человека, могут объяснить, почему у некоторых людей с онкогенными инфекциями развивается рак, а у других нет.
К онковирусам относятся инфекции, которые провоцируют появление раковых заболеваний, а также вирусы, которые способствуют развитию воспалительных процессов, носящих хронический характер.
По заключению экспертов Международного Агентства по Изучению Рака (МАИР) прямым канцерогенным действием на человека обладают следующие вирусы:
- вирусы гепатита В и С, вызывающие рак печени;
- определенные типы папилломавирусов человека, являющиеся причинным агентом рака шейки матки, некоторых опухолей ано-генитальной области и других локализаций;
- вирус Эпштейна-Барр, принимающий участие в возникновении целого ряда злокачественных новообразований;
- герпесвирус человека 8-го типа, играющий важную роль в возникновении саркомы Капоши, первичной выпотной лимфомы, болезни Кастлемана и некоторых других патологических состояний;
- вирус Т-клеточного лейкоза человека, являющийся этиологическим агентом Т-клеточного лейкоза взрослых, перHIVной выпотной лимфомы (Primary Effusion Lymphoma, PEL), а также тропического спастического парапареза (TSP) и ряда других неонкологических заболеваний;
- вирус иммунодефицита человека (ВИЧ), не обладающий трансформирующими генами, но создающего необходимые условия (иммунодефицит) для возникновения рака.
Все они включены в санитарные правила и нуждаются в кратких комментариях.
В настоящее время существует глобальная эпидемия вируса гепатита В (HBV): на планете инфицировано этим вирусом более 350 млн. человек. Каждый год от инфекции HВV умирает 2 млн. человек, из них более 300 тыс. от рака печени. Вирусом гепатита С в мире инфицировано более 170 млн. человек, и их число ежегодно увеличивается на 3–4 млн. По данным экспертов, вирус гепатита С ежегодно становится причиной смерти 250–350 тыс. человек от цирроза, печеночной недостаточности и гепатоцеллюлярной карциномы. Из общего числа случаев рака печени (гепатокарцином) более половины связано с инфицированием HBV, четверть — с инфицированием HCV и 22% случаев — с другими причинами.
Инфицированность населения HBV колеблется от низкой, не превышающей 2% в США и странах Западной Европы, до высокой в странах Африки и Юго-Восточной Азии, приближающейся к 10%. Россия по уровню инфицированности населения HBV занимает промежуточное положение. В окружающих Россию странах (Средняя Азия, Закавказье, Молдавия) инфицированность населения по данным ВОЗ достигает 8%.
Пути заражения вирусом гепатита В (HBV): перинатальный (от матери к плоду), парентеральный (главным образом с кровью или другими биологическим жидкостями больного человека, попадающими непосредственно в кровь инфицируемого, особенно при употреблении инъекционных наркотиков) и половым путем. Заразиться можно в местах, где собираются лица, употребляющие инъекционные наркотики, в салонах пирсинга и татуажа, парикмахерских (маникюр, педикюр — при совместном пользовании общими бритвами и маникюрными принадлежностями). Половой контакт с партнером носителем инфекции в 30% случаев заканчивается инфицированием партнера. Велика вероятность заразиться вирусом, если человек имеет много половых партнеров. У инфицированной HBV матери может родиться инфицированный ребенок. Заражение происходит при родах или нарушении целостности плаценты в ходе беременности. Вирус гепатита B обнаруживается в слюне, слезах, моче и кале инфицированных лиц. Риск заражения, хотя и незначительный, существует при попадании их на поврежденную кожу и слизистые оболочки другого человека. С пищей, при разговоре, т. е. контактно-бытовым путем гепатит В не передается.
Пути заражения вируса гепатита С (HCV): в основном такие же как при HBV. Половой путь передачи гепатита С мало актуален (не более 3–5%), однако значение его возрастает при наличии большого количества партнеров, случайных связей. От инфицированной матери плоду вирус гепатита С передается редко, не более, чем в 5% случаев и только в процессе родов при прохождении родовых путей. Не отмечена передача вируса с молоком матери и контактно-бытовым путем.
Профилактика. Исходя из вирусной природы указанных заболеваний, вакцинация является наиболее эффективным способом предотвращения распространения инфекции, возникновения острого и хронического гепатита, а, следовательно, и рака печени. В 1980 г. приготовлена вакцина против вируса гепатита В. Согласно рекомендациям, принятым в 1999 г. в США и практикуемым в России, вакцина рекомендована для лиц от 0 до 19 лет. В настоящее время во многих странах мира, включая Россию, введена обязательная вакцинация против гепатита В (HBV) среди новорожденных, детей раннего возраста, подростков и лиц из групп риска. С целью профилактики распространения HBV и рака печени проводится тестирование всех беременных и доноров крови на поверхностный антиген вируса (HbsAg) и антитела к нему (HBs).
Вирусы папилломы человека (HPV) принадлежат к группе Papillomavirus и являются вирусами, которые поражают клетки эпителия эктодермального происхождения (кожа, слизистые половых органов, ротовой полости).
В настоящее время известно более 100 типов HPV, которые могут вызывать бородавки на различных частях тела, но лишь немногие из них связывают с различными злокачественными новообразованиями. Некоторые штаммы вируса папилломы распространяются половым путем и вызывают остроконечные бородавки. Передаваемые половым путем вирусы папилломы связаны с развитием рака шейки матки, полового члена и анального прохода (последние встречаются не так часто). К группе высокого онкогенного риска относят наиболее распространенные в Европе и в России 16-й и 18-й типы вируса (HPV 16 и HPV 18), а также менее распространенные 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 типы, ответственные, соответственно, за возникновение 65–75% и 18–20% случаев рака шейки матки (РШМ). Раннее обнаружение и лечение может уменьшить риск рака шейки матки, поэтому врачи советуют женщинам с выявленными вирусами папиломы периодически проводить тест мазок Папаниколау. Вирус папилломы человека является довольно распространенными венерическим заболеваниям с несколькими миллионами новых случаев инфицирования, диагностируемых каждый год.
Пути заражения. Передача инфекции осуществляется половым путем, возможны перинатальный (от матери к плоду) и оральный пути заражения. Большинство лиц обоего пола инфицируется вирусом в первые годы половой жизни. В последние 20–30 лет уровень инфицированности существенно возрос. У 90% женщин HPV инфекция протекает без явных клинических проявлений и вирус исчезает самостоятельно через год после инфицирования под влиянием иммунной системы организма. В трети случаев вирусную ДНК можно выявить более чем через год и в 10% — более чем через два года. Инфекция данным вирусом очень распространена среди здоровых женщин. К 50-летнему возрасту ею переболевает 8 женщин из 10.
Факторами риска для развития рака шейки матки служат раннее начало половой жизни, частая смена партнеров, сопутствующие урогенитальные инфекции (например, хламидийная или герпетическая), снижение клеточного иммунитета, гормональные воздействия (аборт, беременность, прием гормональных контрацептивов и др.), курение, неправильное питание (дефицит фолиевой кислоты), а также индивидуальные генетические особенности.
Вирус Эпштейн-Барра широко известен как вирус, который вызывает инфекционный мононуклеоз. Вирусом Эпштейн-Барра инфицировано практически всё население планеты. В развивающихся странах почти у каждого ребенка к пятилетнему возрасту выявляются антитела к этому вирусу. В развитых странах инфицированность несколько меньше: в США антитела выявляются у 50% выпускников средних школ, к сорока годам антитела к этому вирусу появляются у 90% населения. 15–25% взрослых являются выделителями вируса.
Данный вирус передается через контакт с жидкостью полости рта и носа инфицированного человека. Дети редко имеют выраженные симптомы вируса Эпштейн-Барра, но даже если они есть, симптомы, как правило, являются такими же, как при широко распространенных вирусных инфекциях. Вирус Эпштейн-Барра после заражения остается в организме, главным образом в лимфоцитах, всю остальную части жизни человека. Он находится в состоянии покоя в течение большей части времени, иногда проявляя себя, но не причиняя никакого реального вреда. При ослаблении организма и снижении защитных сил иммунной системы — вирус может активироваться и вызывать более агрессивные воздействия. Вирус Эпштейн-Барра ассоциируется, в первую очередь с развитием лимфобластомы, болезни Ходжкина, лимфомы носоглотки и лимфомы Беркитта, редкой формой рака, возникающего в лимфатических узлах. Кроме лимфобластомы, следует назвать такие вызываемые вирусом доброкачественные и злокачественные новообразования, как волосатоклеточная лейкоплакия полости рта, рак носоглотки и др., возникающие на фоне иммунодефицита организма различного происхождения.
Пути заражения. Основной путь передачи вируса — воздушно-капельный, но наиболее часто передача вируса происходит при непосредственных контактах слизистой рта (поцелуях). Заражение возможно и через содержащие вирус пищевые продукты, а также бытовым путём через руки и предметы обихода, при переливании крови и других парентеральных вмешательствах. Зафиксирован также половой путь передачи.
Ко-факторы. Поскольку у большинства лиц, инфицированных EBV, какой-либо патологии не возникает, то для ее появления, включая злокачественные новообразования, очевидно, необходимо воздействие на организм дополнительных факторов. Среди известных следует назвать паразитарные инфекции типа малярии; массивную инфекцию EBV в. раннем детском возрасте; ослабление иммунной системы; хроническое недоедание, а также использование в пищу продуктов, обладающих коканцерогенным действием; влияние любых факторов, вызывающих хромосомные мутации. Таким образом, можно сделать вывод, что инфицирование EBV является важным, но недостаточным условием для возникновения ассоциированных с ним онкологических заболеваний, чтобы возникла опухоль, необходимо действие ряда дополнительных факторов.
Открытый в 1994 г. герпесвирус саркомы Капоши в семействе герпесвирусов обозначен под номером 8 (HHV-8). В настоящее время считается доказанной его этиологическая роль в возникновении довольно редко встречающихся заболеваний, а именно саркомы Капоши (СК), выпотной В-клеточной лимфомы полостей тела (PEL) и болезни Кастлемана.
Распространенность HHV-8. Инфицированность населения HHV-8 в различных географических регионах существенно отличается и варьирует от долей процента в США и большинстве стран Западной Европы до 8–10% в странах Средиземноморья (Греция, Италия). Самый высокий процент серопозитивных лиц обнаружен в странах Восточной, Центральной и Западной Африки — странах, эндемичных для СК, где уровень инфицированности населения этим вирусом достигал 50–70%. В России уровень инфицированности HHV-8 среди доноров крови находится в пределах 4%.
Пути заражения. Основной путь передачи HHV-8 — половой, но также со слюной (при поцелуе), и с кровью (редко).
Профилактика. Учитывая половой путь передачи вируса основной профилактической мерой является практика безопасного секса, лечение хронического уропростатита у больных с выявленным HHV-8 в эякуляте и/или секрете предстательной железы, применение противовирусных препаратов в группах риска (больные, нуждающиеся в трансплантации органов и ВИЧ-инфицированные).
Профилактическая анти-вирусная (противоопухолевая) вакцина не создана, над ее изготовлением ведется работа.
Вирус Т-клеточного лейкоза человека (HTLV-1) — это онкогенный ретровирус, являющийся этиологическим фактором Т-клеточного лейкоза/лимфомы взрослых, протекающей чрезвычайно агрессивно со средней продолжительностью жизни около 6 месяцев, и нейро-дегенеративного заболевания под названием HTLV-1-ассоциированная миелопатия или тропического спастического парапареза. В регионах с высокой инфицированностью данным вирусом диагностируются также ассоциированные с вирусом увеиты, артриты, базедова болезнь, инсулинзависимый диабет, синдром Цезаря и др.
Распространенность. Спорадические случаи HTLV-1 инфекции встречаются во многих странах мира, включая Россию. Эндемичными же для этой инфекции являются некоторые регионы Японии, Южной Америки, Африки и часть стран Карибского бассейна.
Пути заражения. Существуют 3 основных пути передачи инфекции от инфицированных лиц: а) с молоком матери; б) при половом контакте главным образом через сперму; и в) с переливаемой кровью при гемотрансфузиях.
Ко-факторы. У большинства лиц, инфицированных HTLV-1, какой-либо патологии не возникает. После заражения вирусом ATL регистрируют не более чем у 1–5% вирусоносителей даже в эндемических для этого заболевания регионах и после длительного латентного периода, длящегося порой десятилетиями. Факторами, способствующими развитию ATL, являются паразитарные инфекции типа эписторхоза, использование иммунодепрессантов любого происхождения, ВИЧ-инфекция и др.
Профилактика. Для профилактики инфекции рекомендованы: отмена кормления грудным молоком младенцев инфицированными матерями; предохраняемый секс и контроль на присутствие HTLV-1 донорской крови не только в регионах с высоким уровнем распространения HTLV-1 среди населения, но и в других, т. к. переливание инфицированной вирусом крови, может способствовать его распространению и появлению заболеваний, связанных с HTLV-1 там, где они сейчас отсутствуют.
Этот вирус был открыт в 1983 г. и его ассоциация с синдромом приобретенного иммунодефицита (СПИД) доказана в 1984 г. Как уже упоминалось ранее, ВИЧ не обладает трансформирующим геном (онкогеном). Инфицированные им клетки (главным образом СD4+ Т-клетки и макрофаги) не подвергаются усиленной пролиферации (делению), а разрушаются, вызывая у инфицированного лица нарастающую степень иммунодефицита, и создавая тем самым условия, необходимые для возникновения опухоли. Доказано, что у больных СПИД`ом примерно 50% новообразований ассоциировано с Эпштейн-Барр вирусом или герпес вирусом саркомы Капоши (HHV-8). Чаще всего у таких больных диагностируют саркому Капоши либо одну из разновидностей не-ходжкинских лимфом. Характеристика этих новообразований, механизмы канцерогенеза, а также методы профилактики и лечения даны в предыдущих разделах, их можно найти также в многочисленных отечественных и зарубежных публикациях.
Несмотря на различную организацию онкогенных вирусов человека, неодинаковый спектр их клеток-мишеней, они обладают рядом общих биологических свойств, а именно:
- вирусы лишь инициируют патологический процесс, усиливая пролиферацию (разрастание ткани организма путём размножения клеток делением) и генетическую нестабильность инфицированных ими клеток;
- у инфицированных онкогенными вирусами лиц возникновение опухоли, как правило, событие нечастое: один случай новообразования возникает среди сотен, иногда тысяч инфицированных;
- продолжительность латентного периода от инфицирования до возникновения опухоли составляет иногда десятилетия;
- у большинства инфицированных лиц возникновение опухоли не является обязательным, но они могут составить группу риска, с более высокой возможностью ее возникновения;
- для злокачественной трансформации инфицированных клеток в организме человека необходимы дополнительные факторы и условия, приводящие к возникновению опухоли.
Профилактика активации вирусов и развития рака
- отказ от курения;
- коррекция питания и образа жизни;
- сокращение воздействия канцерогенных веществ;
- повышение защитной функции организма;
- определение и терапия заболеваний, находящихся в предраковой стадии;
- наблюдение групп высокого риска появления онкологий;
- диагностика рака на ранних стадиях.
Можно ли заразиться раком от больного человека, либо от носителя вируса?
То, что окружающие в безопасности рядом с онкобольными людьми, уже неоднократно доказано и подтверждено проведенными опытами. В 19 веке французским хирургом был выделен экстракт рака молочной железы. Затем он ввел его себе, и еще нескольким людям, участвовавшим в опыте добровольно, этот экстракт под кожу. В месте, куда была проведена инъекция, начались острые воспалительные процессы, которые прошли спустя несколько дней. Опыт в скором времени был проведен еще раз и результаты оказались те же.
Современные ученые также проводили исследования, которые подтвердили, что заразиться раком от другого человека невозможно. Медицинские работники провели анализ 350 тысяч процедур переливания крови, проводимые в течение 35 лет. У трех процентов доноров был обнаружен рак, однако ни один из людей, которым переливали кровь онкобольных, не был заражен.
Еще один важный вывод после проведенных медицинских исследований — генетика на появление раковых образований влияет гораздо больше, чем вирусы и другие факторы. Это значит, что попавший в организм онковирус имеет в развитии рака практически нулевую значимость, тогда как сбой в генетическом коде — ключевую.
Выводы
Вирусы, вызывающие рак — очень опасны для жизни и здоровья человека. Их профилактика и своевременная диагностика поможет максимально снизить риск появления серьезных последствий. При появлении каких-либо признаков вирусной инфекции необходимо срочно обратиться к компетентному специалисту и сдать анализы, которые помогут их выявить и вовремя принять необходимые меры.
Читайте также:


