Дефицит иммунной системы при поражении вирусом спида
Рецептором для ВИЧ является дифференцировочный антиген CD4, а также неспецифические, не зависящие от наличия CD4 компоненты. Фиксация вируса с мембранным рецептором CD4 клетки хозяина блокирует основную функцию этих иммунокомпетентных клеток -- восприятие сигналов от антигенпрезентирующих клеток. Последующая за рецепцией репликация вируса ведет к гибели клеток, выпадению выполняемой ими функции и развитию иммунодефицита.
В организме человека имеется целый ряд иммунокомпетентных, соматических и ряд других клеток, имеющих рецепторы для ВИЧ (CD4+ лимфоциты, CD8+ лимфоциты, дендритные клетки, моноциты, эозинофилы, мегакариоциты, нейроны, микроглия, сперматозоиды).
Помимо основного рецептора для ВИЧ-1 -- CD4, имеется еще ряд корецепторов, в частности, хемокиновые рецепторы, необходимые для проникновения ВИЧ в клетку.
Проникнув в CD4+ клетки, ВИЧ сразу же начинает репликацию. Все регуляторы, активирующие СD4+клетки, обеспечивают увеличение репликации вируса. К подобным регуляторам относятся фактор некроза опухолей (ФНО), фактор, стимулирующий колонии гранулоцитов/макрофагов, интерлейкин-6 (ИЛ-6). К негативным регуляторам, тормозящим репликацию вируса, относятся интерферон (ИФ) и трансформирующий фактор роста.
Выделено два типа СР4+клеток: Т-хелперы-1 (Th1) и Т-хелперы-2 (Th2). У больных ВИЧ-инфекцией идет угнетение Th1, чем обеспечиваются и вирусная патология, и онкогенез.
Жизненный цикл ВИЧ после проникновения в организм имеет последовательный характер: связывание вириона с поверхностью клетки, слияние мембран вириона иклетки, проникновение вируса внутрь клетки, высвобождение нуклеотида и геномной РНК вируса, интеграция генома вируса в геном инфицированной клетки, латентная фаза, фаза активации транскрипции с ДНК провируса и последующая транскрипция белков вируса, наработка всех компонентов вируса с формированием новых вирионов и их высвобождением из клетки, влекущим за собой гибель клетки-мишени.
В патологический процесс вовлекаются в первую очередь и в большей степени CD4+ лимфоциты, моноциты крови, макрофаги тканей, дендритные клетки крови, лимфатических узлов, селезенки, кожи, альвеолярных и интерстициальных макрофагов легких, микроглия и другие клетки нервной системы, имеющие CD4-рецепторы. Так же поражаются В- и О-лимфоциты, ретикулярные клетки, эпителиальные клетки кишечника, клетки Лангерганса, причем последние инфицируются даже легче, чем CD4+ лимфоциты. Именно клеткам Лангерганса придается большое значение в распространении ВИЧ по организму, ибо в них вирус сохраняется длительное время, иногда годы.
Наличие CD4 рецептора на многих и не только иммунокомпетентных клетках, возможность поражать и клетки, не имеющие этого рецептора, определяют политропность ВИЧ и полиморфизм клинической картины.
Если на CD4+ лимфоциты вирус оказывает цитопатическое действие с лизисом клетки или слиянием в синцитий, то в моноцитах/макрофагах ВИЧ реплицируется с умеренной интенсивностью и не оказывают цитонекротического действия. Изучение динамики сывороточных монокинов подтверждает активное участие в патогенезе ВИЧ-инфекции моноцитов/макрофагов, основных продуцентов фактора некроза опухолей и интерлейкина-1B. С гиперпродукцией ФНО-а, ИЛ-1b и ИЛ-6 связывают развитие при ВИЧ-инфекции лихорадки, анемии, диареи, кахексии, патологических изменений на коже и слизистых при саркоме Капоши, церебральных симптомов. В то же время было установлено, что ВИЧ ингибирует продукцию ИЛ-2 и g -ИФ, синтезируемым Т-хелперами первого типа, и не ингибирует функцию Т-хелперов второго типа. Следовательно, играя важную роль в регуляции синтеза цитокинов, ВИЧ за счет переключения иммунного ответа с Т-хелперов первого типа на Т-хелперы второго типа, стимулирует гуморальное звено иммунитета.
После инфицирования клетки вирусом происходит соединение вирусной оболочки с мембраной клетки. Помимо того, вирусный белок обеспечивает слияние мембран соседних клеток между собой с образованием одной многоядерной клетки -- синцития. При этом слияние может быть как зараженных клеток между собой, так и зараженных с незараженными.
С момента интеграции генома вируса в геном клетки начинается стадия латентной инфекции. В этот период вирус находится в клетке в виде интегрированного в геном ДНК -- провируса.
В расшифровке патогенеза ВИЧ-инфекции многие вопросы решены, установлены основные этапы развития процесса в клетке после инфицирования ее вирусом. Выявлен ряд факторов, активирующих экспрессию генов ВИЧ. К ним относятся факторы, активирующие Т-лимфоциты: специфические антигены (например, вирусы группы Herpes), неспецифические антигены (например, митогены типа фитогемаглютинина), цитокины (например, фактор некроза опухолей, некоторые интерлейкины, гамма-интерферон), бактериальные иммуномодуляторы. К активаторам экспрессии ВИЧ относятся глюкокортикостероидные гормоны, ультрафиолетовое облучение, перекись водорода, свободные кислородные радикалы. Активирует инфекционный процесс беременность.
Исключительно важный этап патогенеза болезни -- сборка вирусных частиц и выход нового потомства вируса из инфицированной клетки. Отличительной чертой ВИЧ является взрывной характер процессов активации транскрипции, синтеза белков-предшественников, сборки вирионов и их почкования: за 5 минут одна лимфоцитарная клетка может образовать до 5000 вирусных частиц.
Вирусная экспрессия определяет клинику ранней фазы болезни. Пик экспрессии вируса в клетках лимфоидной ткани предшествует накоплению его в плазме. Появление вирусспецифических цитотоксических Т-лимфоцитов совпадает со временем окончания экспрессии вируса в лимфатических узлах. Образование нейтрализующих антител обеспечивает переход острой фазы болезни в хроническую.
Иммунопатогенетически ВИЧ-инфекция проявляется дефицитом Т- и В-звеньев иммунной системы, дефицитом комплемента, фагоцитов, снижением функции неспецифических факторов защиты. В результате идет формирование анергии с проявлениями аллергического, аутоаллергического и иммунокомплексного патологического процесса. Уже во II стадии ВИЧ-инфекция характеризуется снижением абсолютного числа лейкоцитов, повышением уровня естественных киллеров (NK-клетки), нарастанием реакции торможения миграции лимфоцитов. Изменения гуморального звена иммунитета проявляются нарастанием IgG+ В- лимфоцитов и 4-5-кратным ростом уровня сывороточных IgE. Выявляется диспропорция уровней подклассов иммуноглобулинов: IgG1 и IgG3 у больных увеличивается, а концентрация IgG2 и IgG4 существенно уменьшается. Несмотря на гипергаммаглобулинемию, увеличение количества циркулирующих в крови В-лимфоцитов, их функциональная активность на митогены остаются относительно сниженными, что позволяет В-систему иммунитета у ВИЧ-больных расценивать как супрессированную. Количество В-клеток в периферической крови больных в стадии СПИДа может быть снижено в три и более раз.
Взаимодействие ВИЧ-1 с мембраной CD4+ лимфоцитов определяет не только отрицательные реакции инфицированных клеток, но и приводит к программированной клеточной гибели -- апоптозу зрелых CD4+ лимфоцитов или CD34+ гемопоэтических клеток-предшественников даже при отсутствии их инфицирования вирусом.
Л.Монтанье (1996) считает, что в патогенезе СПИДа основное место принадлежит аутоиммунному процессу. В пользу этого говорят исследования характера иммунных реакций у больных: наличие аутоантител и аллоантител к лимфоцитам, формирование аллергических реакций цитотоксического типа, накопление циркулирующих иммунных комплексов, наличие комплементопосредованной цитотоксичности, активация антителозависимой клеточной цитотоксичности. В пользу наличия аутоиммунных процессов в патогенезе ВИЧ-инфекции говорят и клинические проявления болезни, в частности, часто сопутствующие болезни такие типичные аутоаллергические варианты патологии, как спондилоартропатии, системные ревматоидные синдромы.
Формирование иммунодефицита при ВИЧ-инфекции не ограничивается только поражением лимфоцитов с CD4-фенотипом. Так, нарушение синтеза белков НLA I ведет к ингибированию функции лимфоцитов с CD8-фенотипа, т.е. Т-супрессоров. Белок вируса оказывает супрессивное действие на продукцию Т-клетками ИЛ-2 и g - интерферона. А с продукцией ИЛ-2 и других цитокинов тесно связана функция цитотоксических Т-лимфоцитов, ответственных за противовирусную и противоопухолевую защиту организма. Все это патогенетически определяет характерную для ВИЧ-инфекции ассоциированную вирусную, бактериальную, грибковую и онкопатологию.
Наряду с поражением иммунной системы в патологический процесс вовлекается и кроветворная ткань. Для заболевания характерны лейкопения, анемия, тромбоцитопения.
Таким образом, поражение иммунной системы при ВИЧ-инфекции носит системный характер, проявляясь глубокой супрессией Т- и В-звеньев клеточного иммунитета. В ходе развития ВИЧ-инфекции происходят закономерные изменения гиперчувствительности немедленного и замедленного типа, гуморального иммунитета и факторов неспецифической защиты, функциональной активности лимфоцитов и моноцитов/макрофагов. Нарастает уровень сывороточных иммуноглобулинов, циркулирующих иммунных комплексов. Наряду с дефицитом CD4+ лимфоцитов в динамике болезни нарастает функциональная недостаточность CD8+ лимфоцитов, NK-клеток, нейтрофилов. Нарушение иммунного статуса клинически проявляется инфекционным, аллергическим, аутоиммунным и лимфопролиферативным синдромами иммунологической недостаточности, синдромами, свойственными болезни иммунных комплексов. Все это определяет в целом клинику ВИЧ-инфекции.
14 октября 2013
- 19771
- 15,7
- 2
- 4
Распространенность СПИДа в мире на 2009 год.

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Обратная транскрипция осуществляется вирусным белком обратной транскриптазой [31]. Обратная она потому, что обычно в клетке все наоборот — информация переносится с ДНК на РНК (а с РНК — в последовательность аминокислот белков). РНК по сравнению с ДНК очень нестабильна, и поэтому для ВИЧ характерна огромная скорость мутации — в десятки тысяч раз быстрее, чем для человека. Если скорость нейтральных мутаций для ДНК составляет у различных видов и для различных генов в среднем меньше 10 −9 замен на сайт в год, то скорость мутирования генетического материала РНК-вирусов — около 10 −3 замен на сайт в год (у гена env ВИЧ: 10 −2 –10 −3 замен на сайт в год [21]). Это одна из причин, почему иммунная система не может справиться с ВИЧ — он слишком быстро изменяется.
Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
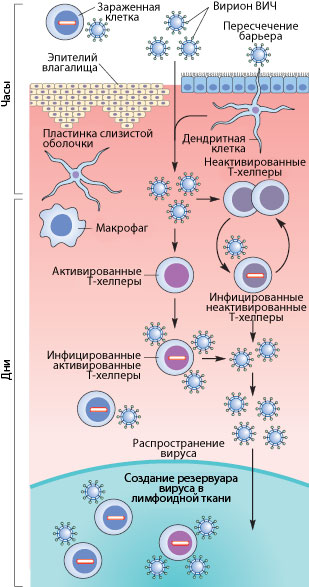
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
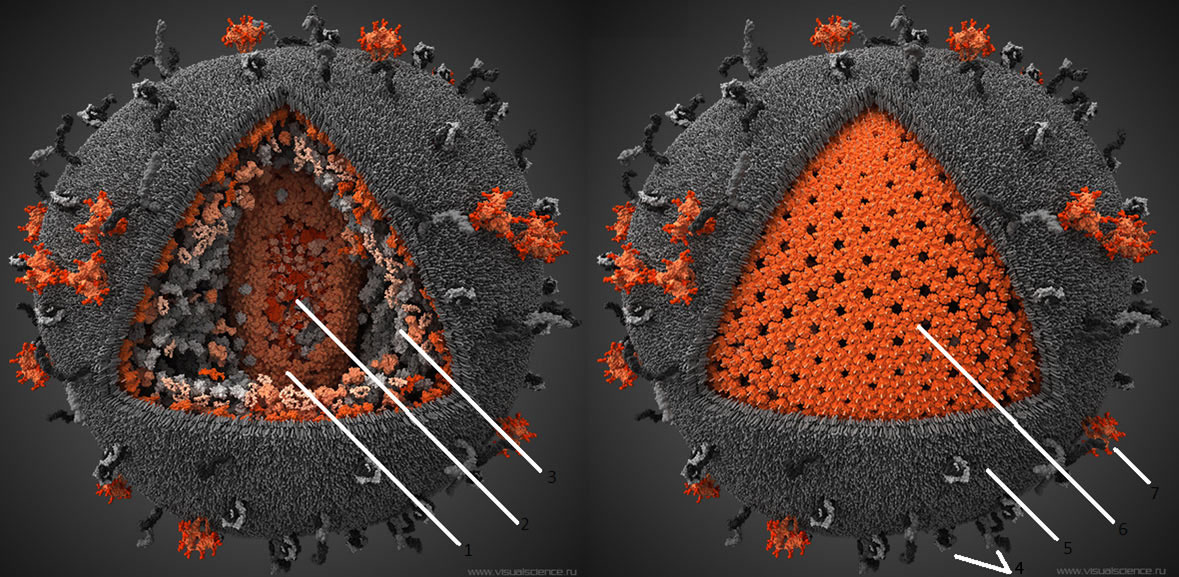
10000 нуклеотидов в каждой. Всего геном включает девять генов, которые в результате альтернативного сплайсинга кодируют 15 различных белков. 3 — Различные белки, захваченные вирусом из хозяйской клетки. 4 — Человеческие белки, обычно находящиеся на поверхности мембраны клеток. Захваченые в результате отпочковывания, они увеличивают вирулентность вируса. 5 — Внешняя оболочка ВИЧ, ведущая свое происхождение от цитоплазматической мембраны клетки, от которой когда-то отпочковался вирион. 6 — Матрикс, образованный тримерами белка р17. 7 — Тримерные комплексы белков gp120 и gp41, при помощи которых вирус проникает в клетку. На поверхности среднего вириона насчитывается около 20 таких тримеров. Чтобы увидеть рисунок в полном размере, нажмите на него.
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.
Синдром приобретенного иммунного дефицита (СПИД/AIDS — Acquired Immune Deficiency Syndrome) — патологическое состояние, при котором в результате поражения иммунной системы ослабляются защитные силы организма. Наиболее характерен для ВИЧ-инфекции — заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ).
Синдром приобретенного иммунодефицита (СПИД) — это термин, применяемый к самым последним стадиям ВИЧ-инфекции.
В отличие от некоторых других вирусов, человеческий организм не может полностью избавиться от ВИЧ. Это означает, если у человека был обнаружен ВИЧ, то он будет находится в организме в течение всей жизни.
5 июня 1981 года американский ученый из Центра по контролю над заболеваниями Майкл Готлиб впервые описал новое заболевание, протекающее с глубоким поражением иммунной системы. Тщательный анализ привел американских исследователей к выводу о наличии неизвестного ранее синдрома, получившего в 1982 году название Aquired Immune Deficience Syndrom (AIDS) — синдром приобретенного иммунодефицита (СПИД).
В 1983 году группой профессора Люка Монтанье в парижском институте Пастера из лимфатического узла больного СПИДом впервые был выделен вирус, вызывающий эту болезнь. 24 апреля 1984 года на пресс-конференции в Вашингтоне директор Института вирусологии человека Мэрилендского университета доктор Роберт Галло объявил о том, что он нашел истинную причину СПИДа. Ему удалось выделить вирус из периферической крови больных СПИДом. Эти два вируса оказались идентичными.
В 1987 году Всемирная организация здравоохранения приняла единое название — "вирус иммунодефицита человека" (ВИЧ, в английской аббревиатуре HIV).
Вирус иммунодефицита человека (ВИЧ) поражает иммунную систему и ослабляет системы контроля и защиты людей от инфекций и некоторых типов рака. Вирус разрушает и ослабляет функцию иммунных клеток, поэтому у инфицированных людей постепенно развивается иммунодефицит, который приводит к повышенной чувствительности к широкому ряду инфекций и болезней.
ВИЧ передается половым путем или через кровь — при многократном использовании общих игл или шприцев для внутривенных инъекций или же при переливании крови. Он может передаваться от матери ребенку в течение беременности, во время родов или при грудном вскармливании.
Заражение вирусом иммунодефицита может сопровождаться острым началом с повышением температуры, кожной сыпью и симптомами менингита.
При отсутствии лечения у большинства ВИЧ-инфицированных людей признаки болезни появляются в течение пяти-десяти лет, а иногда и раньше. После приобретения ВИЧ-инфекции до диагностирования СПИДа проходит обычно 10-15 лет.
Во время инкубационного периода СПИДа наблюдается увеличение лимфоузлов, что отражает активное размножение ВИЧ в тканях иммунной системы, активность которой постепенно подавляется. Для СПИДа характерны частые вторичные инфекции. Среди оппортунистических (сопутствующих) инфекций наиболее часто встречаются пневмоцистная пневмония, опоясывающий лишай, кандидоз полости рта и системные заболевания, вызываемые микобактериями. На ранних этапах поражения иммунной системы нередко развивается туберкулез. К другим проявлениям СПИДа относят некоторые виды кожных опухолей, в частности, саркому Капоши, опухоли иммунной системы (лимфомы), а также разнообразные расстройства нервной системы, включая слабоумие (деменцию).
Диагноз СПИДа устанавливается на основании клинической картины, эпидемиологического обследования и данных иммунологических методов диагностики. При эпидемиологическом обследовании выявляют принадлежность заболевшего к группам риска.
Лекарства от ВИЧ не существует, но при применении комплексной антиретровирусной терапии прогрессирование ВИЧ в организме можно замедлить почти до полной остановки.
Согласно данным Всемирной организации здравоохранения (ВОЗ), в середине 2015 года антиретровирусную терапию получали 15,8 миллиона человек во всем мире. До 2003 года высокая стоимость лекарств, слабая инфраструктура здравоохранения и нехватка финансовых средств препятствовали широкому использованию антиретровирусной терапии в странах с низким и средним уровнем дохода. В последние годы благодаря возросшей политической и финансовой поддержке доступ к лечению был значительно расширен.
По данным ВОЗ, в 2000-2015 годах уровень смертности, связанной со СПИДом, снизился на 24% — было спасено около 7,8 миллиона человеческих жизней.
Впервые в СССР выявил ВИЧ-инфицированных и больных СПИДом иностранцев профессор Вадим Покровский в 1985 году. В 1987 году в СССР официально объявили о регистрации первого случая СПИДа у гражданина страны.
В 2015 году, по сообщению министра здравоохранения РФ Вероники Скворцовой, в России от ВИЧ-инфекции умерли 12,5 тысячи человек.
По словам главы Минздрава РФ, риск вертикальной передачи вируса (от матери к ребенку) в 2015 году составил всего 2%, за последние несколько лет произошло пятикратное снижение числа ВИЧ-инфицированных детей, родившихся от ВИЧ-инфицированных матерей.
Материал подготовлен на основе информации РИА Новости и открытых источников
Зараженный человек остается источником инфекции пожизненно. ВИЧ-инфекция без лечения прогрессирует в течение 3-20 лет.
СПИД — это Синдром Приобретенного Иммунодефицита.
Синдром — потому что существует большое количество признаков, симптомов и осложнений, связанных с заболеванием.
Приобретенный — потому что заболевание не обусловлено генетической предрасположенностью, а приобретается специфическим образом.
Иммунодефицит — потому что при этом иммунная система подавляется и теряет способность сопротивляться различным инфекциям.
Таким образом, СПИД не является заболеванием в собственном смысле этого слова, а лишь создает условия для других инфекционных заболеваний.
В начале 80-х годов врачи начали сообщать о растущем числе случаев болезни, не поддающейся лечению и зачастую смертельной. Молодые люди внезапно умирали от таинственного заболевания, хотя до того чувствовали себя хорошо. Майкл Готтлейб, иммунолог из Калифорнийского Университета в Лос-Анджелесе, был первым ученым, опубликовавшим сообщение об этом заболевании.
| Что такое иммунная система? |
Иммунная система — это защитная система организма против болезнетворных микробов. Она очень сложна, но мы постараемся упростить ее для вас.
Клетки иммунной системы — лимфоциты и макрофаги Лимфоциты находятся в крови, макрофаги — в крови и во всех тканях организма.
Лимфоциты делятся на 2 группы: Т и Б.
Антитела — сложные белковые молекулы, вырабатываемые Б-лимфоцитами. Антитела связывают проникшие в кровь микробы.
Когда болезнетворные микробы проникают в организм, их захватывают макрофаги: Макрофаги разлагают микробы и передают информацию о ихо строении Т-лимфоцитам.
Количественное соотношение помощников и суппрессоров в норме составляет соотношение 2 к 1. Эти процессы происходят в нашем организме многие тысячи раз в течение жизни, и мы даже не замечаем их (когда они проходят успешно с самого начала и мы не заболеваем)!
Когда ВИЧ попадает в кровь, он проникает в клетки Т-помощников. Эти лимфоциты имеют специфический рецептор для белка оболочки вируса. Соединение вируса с клеткой подобно взаимодействию ключа с замком, где роль замка играет рецептор. В клетки, у которых нет такого рецептора, вирус не попадает.
Механизм размножения вируса примерно таков: ВИЧ встраивает свою генетическую информацию в синтезирующие белок структуры клетки, и они начинают производить вирусные белки вместо собственных.
| Источники и пути передачи ВИЧ-инфекции
Источником ВИЧ-инфекции является только человек. Инфицированный ВИЧ может предавать инфекцию на разных стадиях заболевания - практически с момента заражения и до гибели больного. Наиболее контагиозны (заразны) ВИЧ-инфицированные с высокой концентрацией вируса в кровивас. 1. Половым – заражение возможно при незащищенном сексуальном контакте в любой форме, сопровождающимся микро- или макроповреждениями и механическим втиранием инфекционного материала (проникновение вируса из семенной жидкости в кровь, из физиологических экскретов половых путей в кровь или из крови в кровь). Половой путь является основным путем передачи ВИЧ. В связи с тем, что концентрация вируса в семенной жидкостизначительно выше, чем в выделениях женских половых органов, риск передачи ВИЧ-инфекции от мужчины к женщине и от активного гомосексуального партнера к пассивному очень высок. Очаги прочих воспалительных заболеваний половых органов, приводящие к нарушению естественных барьеров (кожи и слизистых оболочек), значительно повышают риск передачи ВИЧ, так как являются входными воротами для вируса иммунодефицита.
Особенности развития заболевания Вопреки распространенным заблуждениям, ВИЧ-инфекция не принадлежит к каким-то уникальным болезням, а является инфекционным заболеванием, имеющим своеобразную и достаточно яркую клиническую картину, течение которого напоминает течение многих других давно и хорошо известных инфекционных заболеваний. Определенное своеобразие ВИЧ-инфекции придает лишь тропность (избирательная чувствительность) возбудителя к определенным клеткам организма, что и отличает одну инфекцию от другой. ВИЧ-инфекция характеризуется многолетним течением, клинически связанным с прогрессирующим снижением иммунитета, приводящим к развитию тяжелых форм вторичных заболеваний. Прогноз: средняя продолжительность жизни человека после инфицирования вирусом иммунодефицита человека 11-15 лет ( на фоне антиретровирусного лечения может быть значительно дольше до 20-30 лет).
Затем приблизительно в половине случаев возникает острая стадия ВИЧ-инфекции (острый ретровирусный синдром), которая характеризуется следующими симптомами: лихорадкой, общей интоксикацией, болями в мышцах и суставах, болями в горле, увеличением периферических лимфоузлов, сыпью, поносом, реже поражением центральной нервной системы по типу острого менингита. Продолжается острая стадия от нескольких дней до 2- 3 месяцев. Важно подчеркнуть, что в инкубационном периоде и в острой стадии ВИЧ-инфекции в крови еще нет антител к ВИЧ. В достаточных, для лабораторного определения, количествах антитела появляются в основном через 3 месяца от момента инфицирования, хотя активным источником инфицирования человек становится практически немедленно . Острая стадия ВИЧ-инфекции сменяется латентным периодом (период бессиптомного носительства), когда в течении многих лет (от 3 до 10) у ВИЧ-инфицированного человека уже есть незначительные нарушения иммунитета, но практически нет клинических проявлений заболевания. Человек в этот период трудоспособен, социально активен и в тоже время является источником инфекции для своих партнеров по сексу или совместному введению наркотиков. В дальнейшем происходит клиническая манифестация ВИЧ-инфекции, первым проявлением которой является увеличение периферических лимфоузлов. Затем заболевание переходит в стадию вторичных заболеваний. На этой стадии происходят первые серьезные нарушения здоровья. Иммунная система уже значительно повреждена и у инфицированного человека могут появляться ранее незнакомые ему болезни. Далее заболевание переходит в стадию преСПИДа и завершается стадией – стадией СПИДа. Эти периоды ВИЧ-инфекции характеризуются прогрессирующим уменьшением Т-лимфоцитов (клетки иммунной системы), к увеличенным лимфоузлам добавляются другие клинические синдромы – потеря массы тела, лихорадка, поносы, энцефалопатия (отставание психомоторного развития у детей, умственная деградация у взрослых). На фоне нарастающего иммунодефицита в различных сочетаниях и в различной последовательности присоединяются многочисленные бактериальные, вирусные, протозойные и грибковые инфекции. В стадии СПИДа эти инфекции протекают обычно крайне тяжело, приобретают генерализованный характер и плохо поддаются стандартной терапии. В этом периоде жизни пациент нуждается в посторонней помощи и уходе. | Последней стадией заболевания является терминальная стадия, которая характеризуется необратимым течением вторичных заболеваний. Даже адекватная специфическая терапия и лечение вторичных заболеваний оказывается неэффективным. В результате гибель больного наступает в течение нескольких месяцев.
Течение и длительность заболевания во многом зависят от типа вируса и индивидуальных особенностей организма человека восприимчивости к инфекционным болезням, состояния иммунитета, сопутствующих заболеваний, вредных привычек и т.п.).
Диагностика ВИЧ –инфекции осуществляется путем комплексной оценки: эпидемиологических данных (выявление факторов риска инфицирования); Эпидемиологические критерии – выявление факторов высокой степени риска инфицирования ВИЧ (переливание не тестированной крови, рождение ребенка от ВИЧ-инфицированной матери, половые контакты с ВИЧ-позитивным партнером; совместное употребление психоактивных веществ с ВИЧ-позитивным партнером). Возможности обследования на ВИЧ в Калужской области В соответсвии с в соответствии с ФЗ 38-83 от 30.03.95 и приказом 641от 28.08.09 Минздрава Калужской области каждый гражданин имеет право на доступное бесплатное консультирование и обследование на ВИЧ Отсутствие достоверных факторов риска заражения ВИЧ может ставить под сомнение данные лабораторных исследований. Клинические критерии диагностики ВИЧ-инфекции – клиническое обследование является обязательным этапом диагностики ВИЧ-инфекции. Без клинического обследования не возможно организовать правильное лечение пациента. Лабораторное подтверждение диагноза ВИЧ-инфекция – В настоящее время для лабораторной диагностики ВИЧ-инфекции используются различные методы обнаружения ВИЧ, антигенов и генного материалов ВИЧ, а также методы обнаружения антител к ВИЧ. Для первичного обследования на ВИЧ широко используется наиболее экономичный и достаточно информативный метод исследования, основанный на выявлении антител – иммуноферментный анализ (ИФА) с подтверждающим тестом (иммуноблотингом, ИБ). Для уточнения диагноза, с целью предотвращения ошибок, от одного пациента исследуется не менее 2-х проб крови! Решив пройти тест на ВИЧ, необходимо помнить: Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу. Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции
|


