Цирроз печени ассоциированный гепатитом с

Цирроз печени (ЦП), осложненный портальной гипертензией (ПГ), нередко развивается на фоне вирусного гепатита С (HCV). Он является одной из актуальных медико-социальных проблем современной гепатологии. Способность возбудителя оказывать прямое цитопатическое действие на гепатоциты, его репликация в моноцитах и макрофагах часто приводят к развитию первично-хронического течения гепатита, трансформации в цирроз и первичную гепатокарциному и является причиной развития стойкой иммунной недостаточности [13,16,20,21,22]. Длительная вирусная инфекция (гепатит С) приводит к истощению иммунных механизмов, в частности к дефициту и истощению функций Th1 лимфоцитов, ответственных за выработку интерлейкина-2 [4,18,20,21]. Отмеченная особенность наиболее важна при хронической и тяжело протекающей патологии, когда применение традиционных иммуномодуляторов или синтетических индукторов синтеза цитокинов бессмысленно из-за истощения компенсаторных возможностей иммунной системы при необходимости дальнейшей хирургической коррекции внутрипеченочной ПГ [2,5,6,7,11,14,15,19]. Также нельзя не учитывать у данной категории пациентов явлений эндотоксемии, ишемию кишечника с микробной транслокацией, фармакологический анамнез и инвазивные манипуляции – как последовательность событий в формировании системного воспалительного ответа [1,3,8,12].
Появление синдрома портальной гипертензии (ПГ) имеет чрезвычайно важное значение в течение заболевания. Являясь приспособительным явлением в начале заболевания, ПГ с прогрессированием процесса приобретает роль ведущего патогенетического клинического фактора [23].
Асцит, рефрактерный к медикаментозным мероприятиям, встречается примерно у 10 % больных с ЦП [9]. С момента появления асцита у пациентов летальность составляет 42–70 % в течение года [17].
В ряде исследований последнего десятилетия установлена роль и значение гипопротеинемии как одного из основных факторов неблагоприятного исхода хирургического лечения больных с синдромом портальной гипертензии [10].
Наличие свободной жидкости в животе на фоне цирроза печени нередко сопровождается ее инфицированием – спонтанным бактериальным перитонитом. За последние годы частота этого осложнения значительно возросла и достигла 12–21 % [24,25].
Целью работы является улучшение результатов лечения пациентов с вирус-ассоциированнымHCV циррозом печени путём ликвидации гипо- и диспротеинемии, а также необходимостью предотвращения инфекционных осложнений и опасности развития генерализованной инфекции с проведением опережающего лечения, а именно – раннего применения интерлейкина-2 человеческого рекомбинантного при дальнейшей хирургической коррекции внутрипеченочной портальной гипертензии одним из известных способов.
Материалы и методы. В клинике хирургии Ростовского государственного медицинского университета с 1997 года пролечен 341 пациент с портальной гипертензией. Внутрипеченочная форма ПГ была у 297 (87,1 %) больных и у 2 (0,6 %) пациентов носила смешанный характер (внутрипеченочный и надпеченочный).
Из 299 больных внутрипеченочной ПГ у 287 был выявлен цирроз печени (у 227 из них в анамнезе выявлен вирусный гепатит), у 6 пациентов выявлена альфа-1-антитрипсиновая недостаточность, у одного редко встречающаяся гепатоцеребральная дистрофия (болезнь Вильсона – Коновалова), приведшие к развитию фиброза печени, у ребенка 8 лет ПГ развилась, как осложнение врожденного фиброза печени. У одного пациента регенеративный узел печени вызвал ПГ. Трем пациентам был поставлен диагноз полинодулярной трансформации печени. У двоих из них ПГ носила смешанный характер за счет гипоплазии нижней полой вены в области впадения печеночных вен с деформацией и стенозом их устьев в одном случае и сдавления печеночных вен и нижней полой вены в другом.
Из 297 пациентов с внутрипеченочной ПГ было выполнено 79 операций спленоренального венозного шунтирования (СВШ) и 128 операций трансъюгулярного внутрипеченочного портосистемного шунтирования (ТВПШ). Помимо этого больным выполнялся лапароцентез с реинфузией концентрата асцитической жидкости (38).
Из 207 пациентов, которым выполнялась коррекция ПГ одним из вышеуказанных способов, у 79 (38,2 %) вирусный гепатит не был выявлен. У 9 (4,3 %) в анамнезе присутствовал вирусный гепатит А, у 26 (12,6 %) – вирусный гепатит В, у 75 (36,2 %) – вирусный гепатит С, различное сочетание двух или трех вирусных гепатитов было у 18 (8,7 %) больных. Подробная характеристика представлена на рис.1.
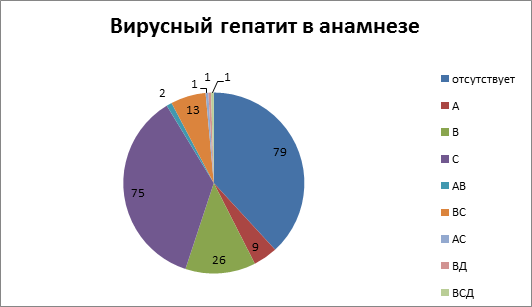
Рис.1. Этиология цирроза печени
Таким образом, вирус-ассоциированный цирроз печени присутствовал у 119 (67,5 %) больных, из них хронический вирусный гепатит С был выявлен у 89 (43,0 %) пациентов.
Сущность метода заключается в том, что внутривенно со скоростью перфузии 60 капель в минуту вводят 500 мл приготовленного концентрата асцитической жидкости с добавлением в него интерлейкина-2 человеческого рекомбинантного в дозе 500 МЕ, при необходимости оставшуюся часть концентрата вводят дробно по 500 мл интраоперационно и в первые сутки после хирургического лечения.
Результаты. 12 пациентам с вирус-ассоцированнымHCV циррозом печени и признаками иммунной недостаточности по клеточному типу с дефицитом CD3⁺- и CD4⁺-позитивных лимфоцитов, снижением содержания CD4⁺CD25⁺-лимфоцитов и NK-клеток, дисиммуноглобулинемией в предоперационном периоде была выполнена реинфузия концентрата асцитической жидкости по ранее заявленной методике.
Состав асцитической жидкости был исследован кроме данной группы еще у 26 больных с ЦП, всего у 38 пациентов. При биохимическом исследовании определялось содержание общего белка и белковых фракций, мочевины, креатинина и билирубина. Количество общего белка в асцитической жидкости составляло от 17,6 до 42,8 г/л (28,2±9,6 г/л). Низкое его содержание было у больных, которым ранее неоднократно выполнялся лапароцентез. Содержание альбумина в процентах составило 49,4±5,3, α-глобулина –14,1±2,4, β-глобулина – 13,4±1,9, γ-глобулина – 24,5±3,6, средние молекулы были в пределах 0,386±0,045 у.е.
В среднем показатели цитоза составляли 297±174 клеток в 1 мм3. Основную часть клеток при микроскопии осадка составляли лимфоциты (69 %), меньшую – сегментоядерные нейтрофилы (10 %), моноциты (2 %), макрофаги (2 %), мезотелиальные клетки (6 %), а также мононуклеары (11 %).
После ультрафильтрации объем асцитической жидкости уменьшался от 5 до 10 раз, содержание общего белка возрастало до 49,3±18,4 г/л. Фракция альбумина повышалась до 52,2±6,8 %, а количество γ-глобулина снижалось.
После выполнения реинфузии концентрата асцитической жидкости показатели общего белка плазмы крови составили 52,4±9,3 г/л до переливания и 58,8±8,4 г/л после, % содержание альбумина - 41,7±14,4 и 47,2±6,4 соответственно. Процент содержания гамма-глобулина – 32,6±7,5 до переливания и 28,4±5,4 после переливания. Коэффициент (отношение альбуминов к глобулинам) составил 0,62±0,04 и 1,1±0,03 соответственно.
После выполнения реинфузии перед операцией спленоренального венозного шунтирования (8) или трансъюгулярного внутрипеченочного портоситемного шунтирования (4) ни одному из 12 пациентов не понадобилось дополнительное введение альбумина, не было выявлено признаков гнойных осложнений, послеоперационные раны в 8 наблюдениях после СВШ зажили первичным натяжением, стабилизировались показатели биохимического анализа крови (табл.1).
Изменения показателей крови больных ЦП до и после лечения
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Ключевые слова: хронический гепатит С, цирроз печени, гепатоцеллюлярная карцинома.
Для цитирования: Макашова В.В., Омарова Х.Г., Хохлова О.Н., Лукашенко Т.Н. Хронический вирусный гепатит С с исходом в цирроз и гепатоцеллюлярную карциному (клиническое наблюдение). РМЖ. Медицинское обозрение. 2018;8(II):92-96.
Chronic hepatitis C virus with the outcome of cirrhosis and hepatocellular carcinoma (clinical observation)
V.V. Makashova 1,2 , H.G. Omarova 1 , O.N. Hohlova 1 , T.N. Lukashenko 3
1 Central Research Institute of Epidemiology, Moscow
2 Clinical Hospital for the Infectious Diseases, Moscow
3 Outpatient Clinic № 5, Moscow
The article presents a clinical case of a patient with a diagnosis of liver cirrhosis of Child-Pugh class B in the outcome of chronic hepatitis C, treated with interferon and ribavirin for 18 months. In the course of antiviral therapy, RNA of the hepatitis C virus became negative after 8 weeks and remained steadily negative for 2 years. Subsequently, on the background of stress, 3 months after the end of treatment, a relapse of chronic hepatitis C appeared with moderate biochemical and virological activity. 6 months after the relapse, a liver cancer was suspected during an ultrasound examination and histological confirmation was obtained. After a few months, hemorrhage from esophageal varicose veins dilatation (EVVD) occurred in the patient, and after another 1 month, there was repeated hemorrhage from EVVD. The patient was monitored and treated in the intensive care department. Ascites, bilateral pneumonia, fever, leukocytosis appeared. The patient’s condition progressively worsened and with increasing psychomotor agitation, progressive respiratory and cardiovascular insufficiency, biological death was recorded.
There was a divergence of diagnoses, category II. The cause of the fatal outcome was purulent intoxication, as a result of ulcers perforation of the esophagus, purulent mediastinitis with pleural empyema on the left.
Key words: chronic hepatitis C, cirrhosis, hepatocellular carcinoma.
For citation: Makashova V.V., Omarova H.G., Hohlova O.N., Lukashenko T.N. Chronic hepatitis C virus with the outcome of cirrhosis and hepatocellular carcinoma (clinical observation) // RMJ. Medical Review. 2018. № 8(II). P. 92–96.
Пациент Т., 1948 г. р., 22.01.2009 г. обратился в поликлинику к инфекционисту в связи с лейкопенией (до 3,2×10 9 /л), тромбоцитопенией (60–120×10 9 ). Со слов пациента, антитела к HCV впервые выявлены в 1998 г. Не обследовался, не лечился. Впервые обследовался в поликлинике ФСБ № 5 в 2009 г., выявлена РНК HCV+, 1в генотип, вирусная нагрузка — 1,3×10 6 коп/мл.
Жалобы на периодически возникающую слабость и утомляемость.
Перенесенные заболевания: 1972 г. — аппендэктомия, 1992 г. — острый вирусный гепатит А, 1995 г. — оперирован по поводу синдрома Меллори — Вейса. В это же время были гемотрансфузии. 1996 г. — грыжесечение, 1997 г. — повторное грыжесечение, 2004 г. — язвенная болезнь 12-перстной кишки, 2005 г. — правостороннее воспаление легких, хронический бронхит, 2007 г. — повторная пневмония, 2007 г. — сильное кровотечение при удалении зубов, гипертоническая болезнь, сахарный диабет 2-го типа.
Аллергоанамнез — не отягощен.
Наследственность: у отца — цирроз печени алкогольного генеза, у матери — инсульт, у брата — хронический вирусный гепатит В.
Вредные привычки: не курит, алкоголь употреблял часто, но немного (со слов), крепкие напитки (виски, коньяк).
Объективно при осмотре: сосудистые звездочки в области грудной клетки, умеренная пальмарная эритема, иктеричность склер. Печень пальпаторно и перкуторно увеличена — выступает на 4–5 см ниже реберной дуги, селезенка не пальпируется.
Рост — 173 см, вес — 80 кг.
Динамика основных показателей общего и биохимического анализов крови, данные ПЦР-диагностики представлены в таблице 1.
Состояние, при котором в результате генерализованного повреждения паренхимы печени развивается фиброз и замена нормальной архитектоники органа на структурально аномальные регенерационные узелки → уменьшается количество функционирующей паренхимы → развиваются нарушения функции печени и структуры сосудистой системы, что приводит к портальной гипертензии (повышение давления в портальной вене >12 мм рт. ст.; в норме ≤10 мм рт. ст.). Портальная гипертензия приводит к развитию порто-системного коллатерального кровообращения (в районе пищевода, ануса и передней брюшной стенки), спленомегалии и гиперспленизму, асциту и портальной гастропатии. Цирроз составляет конечную стадию многих хронических заболеваний печени.
Причины: алкогольная болезнь печени, вирусный гепатит В, D или C, аутоиммунный гепатит, метаболические заболевания (гемохроматоз, болезнь Вильсона-Коновалова, дефицит α 1 -антитрипсина, муковисцидоз, поздняя кожная порфирия, галактоземия, врожденная тирозинемия, гликогенозы [тип III и IV], врожденная геморрагическая телеангиэктазия, гипервитаминоз А, абеталипопротеинемия, НАСГ), болезни желчных путей (непроходимость внепеченочных желчных путей, непроходимость внутрипеченочных желчных путей, первичный холангит, первичный склерозирующий холангит), нарушения венозного оттока (веноокклюзионная болезнь печени, синдром Бадда-Киари, правожелудочковая сердечная недостаточность), ЛС (метотрексат, метилдопа, амиодарон), токсины, обходные кишечные анастомозы (при лечении ожирения), криптогенный цирроз (причина неизвестна).
КЛИНИЧЕСКАЯ КАРТИНА И ЕСТЕСТВЕННОЕ ТЕЧЕНИЕ наверх
Клинические симптомы зависят от длительности заболевания, количества функционирующей печеночной паренхимы, нарушений портального кровообращения и назначенного лечения. У 30–40 % больных цирроз печени протекает полностью бессимптомно и диагностируется случайно. Цирроз без симптомов нарушения метаболической функции и осложнений портальной гипертензии называется компенсированным.
3. Нарушение функции пищеварительной системы: метеоризм, тошнота и рвота, сглаживание языка, отек слюнных желез (у некоторых больных), болевые ощущения в правом подреберье, спленомегалия (≈60 % больных), гепатомегалия с ощутимой узелковой поверхностью (только у некоторых больных; печень в типичных случаях уменьшена и глубоко спрятана под реберной дугой), асцит, грыжи передней брюшной стенки (чаще всего, пупочная грыжа).
4. Нарушение функции репродуктивной системы: гипогонадизм (снижение либидо, нарушения менструального цикла и бесплодие, у мужчин — атрофия яичек) и феминизация (гинекомастия, сосудистые паучки, пальмарная эритема, изменение характера оволосения).
5. Типичное течение: цирроз печени является прогрессирующим заболеванием и со временем развиваются лабораторные и клинические симптомы декомпенсации. Классификация Чайлд- Пью степени печеночной недостаточности при циррозе печени →табл. 7.12-1. Прогрессирование заболевания от раннего этапа, который можно обнаружить исключительно при гистологическом исследовании, до критической печеночной недостаточности имеет разную продолжительность и зависит от этиологии и применяемого лечения. С момента появления первых симптомов декомпенсации до 5 лет доживают 45 % больных, а до 10 лет —10–20 %.