Битва вирусов и клеток
| Доска и фигуры | ||||||||||||||||||
| Цель игры |
| Игрок побеждает в игре, если его противник остается без возможных ходов. |
| Процесс игры | |||||||||||||||
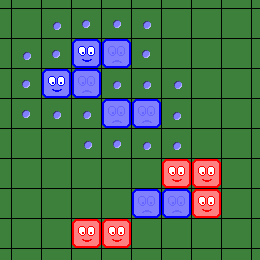 | 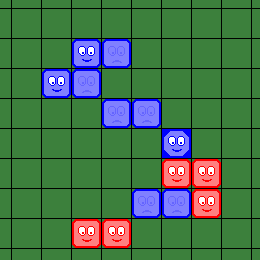 |
| На этой иллюстрации все "доступные" клетки помечены голубыми точками. Обратите внимание на то, что клетки вокруг двух синих "зомби" внизу доски не являются "доступными", потому что от них нет цепочки к "живым" синим "вирусам". | Синий игрок делает 1-ый "шаг", помещая свой вирус в одну из "доступных" клеток. |
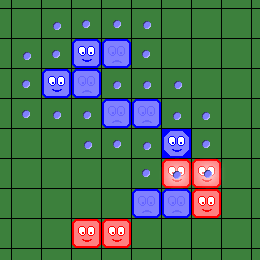 | 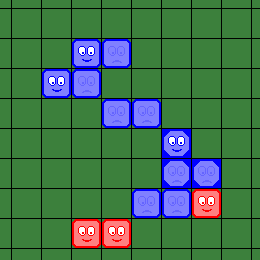 |
| Новый "вирус" добавляет 5 новых "доступных" клеток. Теперь два красных "вируса" могут быть "зомбированы". | Синий игрок делает 2-й и 3-й "шаги", "зомбируя" два красных "вируса". |
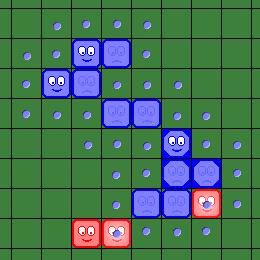 | 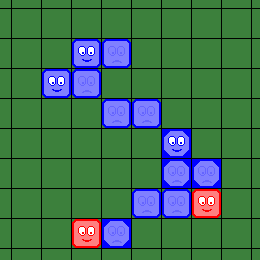 |
| "Зомбирование" двух красных "вирусов" позволяет "добраться" до еще одного красного "вируса" внизу доски. | Синий игрок делает 4-й "шаг", "зомбируя" один красный "вирус" внизу доски. |
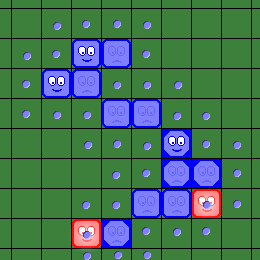 | 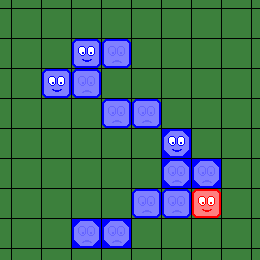 |
| Теперь и второй красный "вирус" внизу доски является "доступным". | Синий игрок завершает свой ход 5-ым шагом, "зомбируя" второй красный "вирус" внизу доски. |
В начале игры доска является пустой и потому на ней нет "доступных" клеток. Поэтому Синий игрок может разместить свой самый первый "вирус" в любую клетку на левом крае доски, а Красный игрок - в любую клетку на правом крае доски.
Игрок обязан сделать все 5 "шагов" каждый ход. Если игрок не может сделать все 5 "шагов", то он проигрывает партию.
Коронавирус заразил множество людей. Наверное, вы уже задавались вопросом, а что же вообще такое эти вирусы?
Если из носа у вас течет, в этом, как правило, виноват обычный простудный вирус. К счастью, у нас имеется иммунитет, способный справиться с простудой, так что она быстро проходит.
Другие вирусы победить сложнее.
Существуют лекарства против вирусов, но они не всегда эффективны. Поэтому если вирус проник в клетки организма, задача иммунной системы — очистить их.
Между бактериями и вирусами — большая разница
И бактерии, и вирусы могут стать причиной болезни человека. Но при этом они очень разные.
Внутри бактериальной клетки есть все, что требуется для жизни. Бактерия способна питаться, размножаться и избавляться от ненужных ей веществ. А вот вирус этого не может. Он выживает только за счет других, просто-напросто заставляя чужие клетки работать на себя.
Вирус проникает в клетку. А затем начинает пользоваться ею, производя множество своих копий. Некоторые вирусы копируют себя в таких количествах, что клетка в итоге просто лопается и погибает. Из нее высвобождаются миллионы новых вирусов, готовых атаковать следующую клетку.
Коробка с инструкцией внутри
Клетка — очень сложная система. Вирус же, напротив, относительно примитивен. На самом деле он даже не выполняет все требования, сформулированные учеными, чтобы дать определение живого существа.
Вирусы ничего не поглощают и не выделяют. Все эти заботы они перекладывают на других.
Представьте себе вирус в виде маленькой коробочки. Внутри лежат его гены — своего рода инструкция, в которой описывается, как вирус работает.
Хорошие вирусы
Мы постоянно носим в себе множество вирусов. Они присутствуют повсюду. Но, к счастью, далеко не все вирусы опасны. Некоторые из них даже участвуют в очень важных процессах в природе.
Например, в чайной ложке воды — несколько миллионов вирусов! В море они убивают бактерии, обеспечивая питанием прочие организмы.
Большинство вирусов не вредят людям, ведь они атакуют лишь определенный тип клеток.
Некоторые вирусы нападают только на свиней, другие вызывают заболевания у растений. Третьи предпочитают бактерии. На земле существуют вирусы практически для всего живого.
Могут изменяться
Нынешний коронавирус изначально был вирусом животных. Вероятно, его носителями были летучие мыши.
Как вышло, что он перекинулся на людей?
В процессе создания копий вируса периодически случаются ошибки. Копия получается не совсем точной. Это называется мутацией.
Но изредка вирусы мутируют так, что, вместо того чтобы заражать животных, начинают атаковать клетки человека. Если в организм человека попадает такой вирус, это может стать началом нового опасного заболевания.
Нужен ключ

Клетка стала фабрикой по производству вируса
Клетка вырабатывает все, что нужно вирусу. Она становится вирусной фабрикой.
Готовые вирусы затем могут покинуть клетку и отправиться в путешествие по организму. Либо клетка настолько переполняется вирусами, что лопается и погибает. И тогда множество новых вирусов вырываются на волю и атакуют новые жертвы.
Вот почему человек болеет
В организме поднимается тревога. Иммунитет выпускает своих агентов, чтобы они арестовали непрошеных гостей. В этот момент человек чувствует себя слабым и больным.
Вирусы гриппа и коронавирус атакуют и повреждают клетки легких.
У заболевших коронавирусом поднимается температура и начинается кашель. Когда мы болеем гриппом, мы тоже страдаем от насморка и кашля. Так организм реагирует на инфекцию и защищается от нее.
Коронавирус распространяется по воздуху в маленьких капельках жидкости, при кашле вылетающих изо рта человека. Вдохнуть эти капельки может кто угодно. Либо кто-то может прикоснуться к месту, где они осели, а затем дотронуться до рта. Таким образом вирус распространяется.
Лекарства и вакцины могут помочь
Поскольку вирус на самом деле не совсем живое существо, очень трудно найти против него эффективное лекарство, которое при этом не навредило бы клеткам.
От некоторых вирусов защищают вакцины. Когда мы прививаемся, наш иммунитет учится распознавать вирус. В таком случае он нападает на вирус настолько быстро, что тот просто не успевает наплодить множество копий.
Сейчас ученые одновременно разрабатывают и лекарства, и вакцины против коронавируса.
От некоторых вирусов избавиться нельзя
Такое случается, например, когда иммунная система не в состоянии отследить вирус. К подобному типу относится вирус герпеса.

О мире вирусов известно многое, но еще больше ученым только предстоит узнать.
Гигантские вирусы
Вирусы — мельчайшие и простейшие микроорганизмы из всех существующих на Земле.
Если представить, что клетка — это авианосец, то бактерия по сравнению с ней покажется обычной весельной лодкой. А вирус — бутылочной пробкой, качающейся на волнах поблизости.
Но на самом деле есть и вирусы побольше. Их обнаружили всего несколько лет назад. Самые большие вирусы даже крупнее, чем простые бактерии. У них гораздо больше генов, чем у остальных вирусов, и большая часть их генетического материала совершенно не изучена.
Ученые задаются вопросом, откуда взялись гигантские вирусы. Может, прежде чем стать паразитами, они относились к отдельному виду живых организмов, обитавших на планете давным-давно?
К счастью, нам не стоит особенно бояться этих гигантских вирусов, как свидетельствуют проведенные исследования. Похоже, они предпочитают жить за счет амёб — одноклеточных организмов.
Материалы ИноСМИ содержат оценки исключительно зарубежных СМИ и не отражают позицию редакции ИноСМИ.
![]()
![]()
![]()
![]()
![]()

![]()
![]()
![]()



![]()

![]()

![]()
- Популярное
- Обсуждаемое
При полном или частичном использовании материалов ссылка на ИноСМИ.Ru обязательна (в интернете — гиперссылка).


Произошла ошибка. Пожалуйста, повторите попытку позже.
Факт регистрации пользователя на сайтах РИА Новости обозначает его согласие с данными правилами.
Пользователь обязуется своими действиями не нарушать действующее законодательство Российской Федерации.
Пользователь обязуется высказываться уважительно по отношению к другим участникам дискуссии, читателям и лицам, фигурирующим в материалах.
Публикуются комментарии только на русском языке.
Комментарии пользователей размещаются без предварительного редактирования.
Комментарий пользователя может быть подвергнут редактированию или заблокирован в процессе размещения, если он:
В случае трехкратного нарушения правил комментирования пользователи будут переводиться в группу предварительного редактирования сроком на одну неделю.
При многократном нарушении правил комментирования возможность пользователя оставлять комментарии может быть заблокирована.
Пожалуйста, пишите грамотно – комментарии, в которых проявляется неуважение к русскому языку, намеренное пренебрежение его правилами и нормами, могут блокироваться вне зависимости от содержания.
Бактериофаги – это вирусы, которые поражают только бактерий. В ходе инфекции они влияют на все процессы жизнедеятельности бактериальной клетки, фактически превращая ее в фабрику по производству вирусного потомства. В конце концов клетка разрушается, а вновь образованные вирусные частицы выходят наружу и могут заражать новые бактерии.
Несмотря на огромное число и разнообразие природных фагов, встречаемся мы с ними редко. Однако бывают ситуации, когда деятельность этих вирусов не остается незамеченной. Например, на предприятиях, где производят сыры, йогурты и другие молочно-кислые продукты, часто приходится сталкиваться с вирусной атакой на бактерии, сбраживающие молоко. В большинстве таких случаев фаговая инфекция распространяется молниеносно, и полезные бактерии гибнут, что приводит к значительным экономическим потерям (Neve et al., 1994).
Именно благодаря прикладным исследованиям в интересах молочной промышленности, направленным на получение устойчивых к бактериофагам штаммов молочно-кислых бактерий, был открыт ряд механизмов, с помощью которых бактерии избегают инфекции. Параллельно были изучены способы, с помощью которых вирусы, в свою очередь, преодолевают бактериальные системы защиты (Moineau et al., 1993).
Кто защищен – тот вооружен
На сегодня известно пять основных, весьма хитроумных механизмов защиты, которые бактерии выработали в непрестанной борьбе с вирусами: изменение рецептора на поверхности клетки; исключение суперинфекции; системы абортивной инфекции; системы рестрикции-модификации и, наконец, системы CRISPR-Cas.
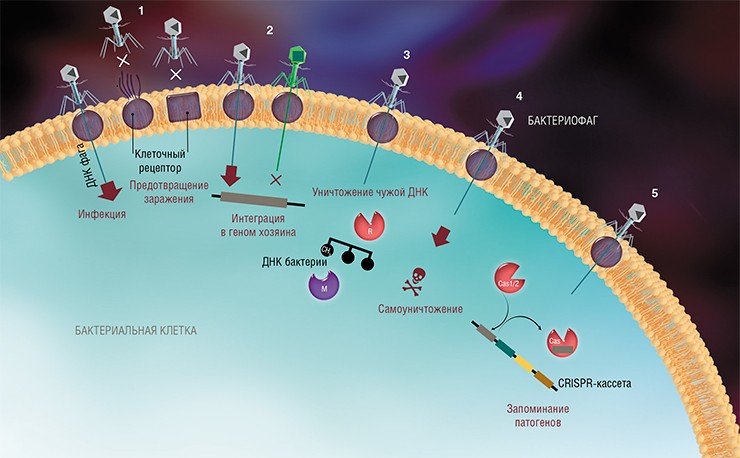
К средствам противовирусной защиты бактерий относятся и системы рестрикции-модификации, в которые входят гены, кодирующие два белка-фермента – рестриктазу и метилазу. Рестриктаза узнает определенные последовательности ДНК длиной 4—6 нуклеотидов и вносит в них двуцепочечные разрывы. Метилаза, напротив, ковалентно модифицирует эти последовательности, добавляя к отдельным нуклеотидным основаниям метильные группы, что предотвращает их узнавание рестриктазой.
Врага нужно знать в лицо
Системы CRISPR-Cas являются уникальным примером адаптивного иммунитета бактерий. При проникновении в клетку ДНК фага специальные белки Cas встраивают фрагменты вирусной ДНК длиной 25—40 нуклеотидов в определенный участок генома бактерии (Barrangou et al., 2007). Такие фрагменты называются спейсерами (от англ. spacer – промежуток), участок, где происходит встраивание, – CRISPR-кассета (от англ. Clustered Regularly Interspaced Short Palindromic Repeats), а сам процесс приобретения спейсеров – адаптацией.
Чтобы использовать спейсеры в борьбе с фаговой инфекцией, в клетке должен происходить еще один процесс, управляемый белками Cas, названный интерференцией. Суть его в том, что в ходе транскрипции CRISPR-кассеты образуется длинная молекула РНК, которая разрезается белками Cas на короткие фрагменты – защитные криспрРНК (крРНК), каждая из которых содержит один спейсер. Белки Cas вместе с молекулой крРНК образуют эффекторный комплекс, который сканирует всю ДНК клетки на наличие последовательностей, идентичных спейсеру (протоспейсеров). Найденные протоспейсеры расщепляются белками Cas (Westra et al., 2012; Jinek et al., 2012).
Системы CRISPR-Cas обнаружены у большинства прокариот – бактерий и архей. Хотя общий принцип действия всех известных систем CRISPR-Cas одинаков, механизмы их работы могут существенно отличаться в деталях. Наибольшие различия проявляются в строении и функционировании эффекторного комплекса, в связи с чем системы CRISPR-Cas делят на несколько типов. На сегодняшний день описаны шесть типов таких неродственных друг другу систем (Makarova et al., 2015; Shmakov et al., 2015).
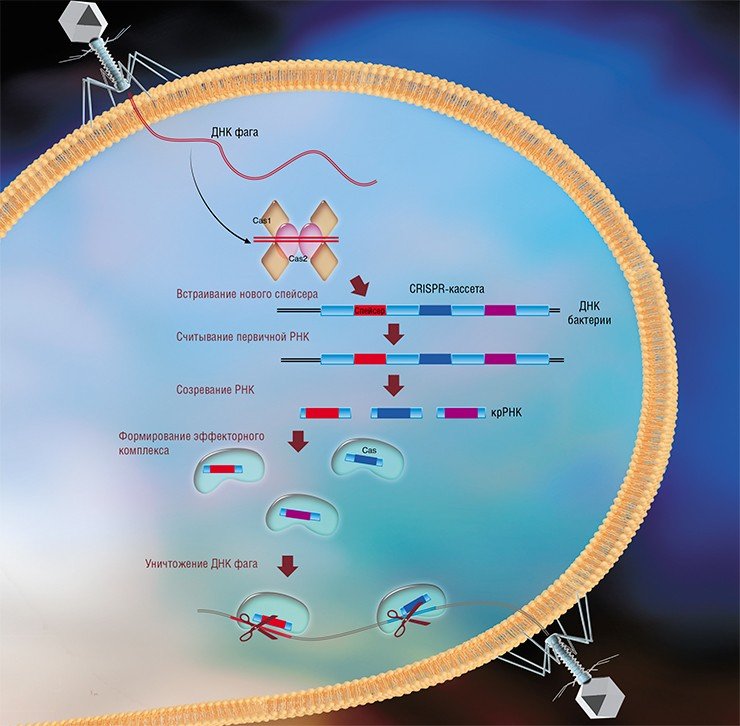
Наиболее изученной является система CRISPR-Cas I типа, которой обладает излюбленный объект молекулярно-биологических исследований – бактерия кишечная палочка (Esсherichia coli). Эффекторный комплекс в этой системе состоит из нескольких небольших белков Cas, каждый из которых отвечает за разные функции: разрезание длинной некодирующей CRISPR РНК, связывание коротких крРНК, поиск, а затем разрезание ДНК-мишени.
Гонка вооружений
Бактериофаги, как факторы среды, вызывают направленные изменения в геноме бактерий, которые наследуются и дают бактериям явное преимущество, спасая от повторных инфекций. Поэтому системы CRISPR-Cas можно считать примером ламарковской эволюции, при которой происходит наследование благоприобретенных признаков (Koonin et al., 2009)
Некоторые бактериофаги реагируют на наличие в бактериальной клетке систем CRISPR-Cas выработкой особых анти CRISPR-белков, способных связываться с белками Cas и блокировать их функции (Bondy-Denomy et al., 2015). Еще одно ухищрение — обмен участков генома вируса, на которые нацелена система CRISPR-Cas, на участки геномов родственных вирусов, отличающихся по составу нуклеотидной последовательности (Paez-Espino et al., 2015).
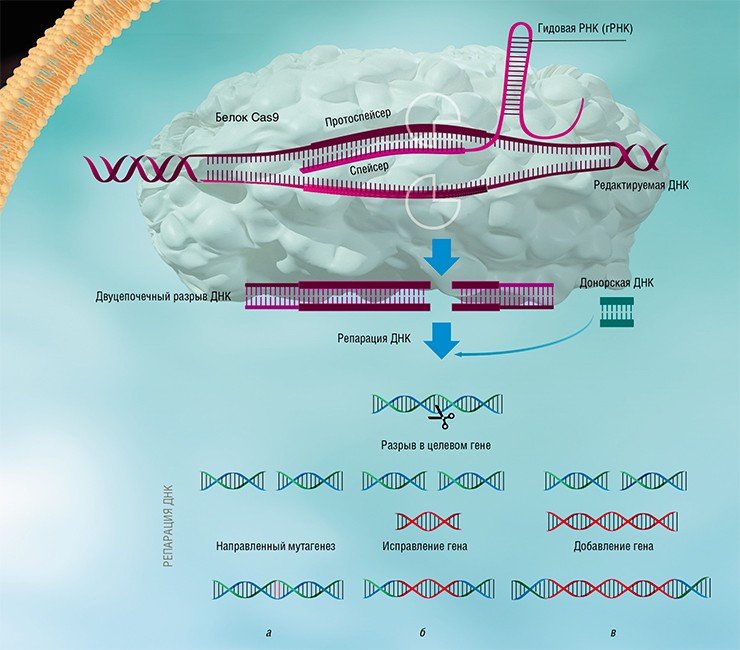
Благодаря постоянному совершенствованию биоинформатических алгоритмов поиска, а также включению в анализ все большего количества прокариотических геномов, открытие новых типов CRISPR-Cas систем является делом недалекого будущего. Предстоит также выяснить и детальные механизмы работы многих недавно открытых систем. Так, в статье, опубликованной в 2016 г. в журнале Science и посвященной анализу системы CRISPR-Cas VI типа, описан белок С2с2, образующий эффекторный комплекс с крРНК, который нацелен на деградацию не ДНК, а РНК (Abudayyeh et al., 2016). В будущем такое необычное свойство может быть использовано в медицине для регулирования активности генов путем изменения количества кодируемых ими РНК.
Изучение стратегий борьбы бактерий с бактериофагами, несмотря на свою кажущуюся фундаментальность и отвлеченность от задач практической медицины, принесло неоценимую пользу человечеству. Примерами этого могут служить методы молекулярного клонирования и редактирования геномов – направленного внесения или удаления мутаций и изменения уровня транскрипции определенных генов.
Благодаря быстрому развитию методов молекулярной биологии всего лишь через несколько лет после открытия механизма действия систем CRISPR-Cas была создана работающая технология геномного редактирования, способная бороться с болезнями, ранее считавшимися неизлечимыми. Доступность и простота этой технологии позволяют рассматривать ее как основу для медицины, ветеринарии, сельского хозяйства и биотехнологий будущего, которые будут базироваться на направленных и безопасных генных модификациях.
Нет никаких сомнений, что дальнейшее изучение взаимодействия бактерий и их вирусов может открыть перед нами такие возможности, о которых мы сейчас даже не подозреваем.
Abudayyeh O. O., Gootenberg J. S., Konermann S. et al. C 2c2 is a single-component programmable RNA-guided RNA-targeting CRISPR effector // Science. 2016. V. 353: aaf5573.
Barrangou R., Fremaux C., Deveau H. et al. CRISPR provides acquired resistance against viruses in prokaryotes // Science. 2007. V. 315. P. 1709–1712.
Bikard D., Marraffini L. A. Innate and adaptive immunity in bacteria: mechanisms of programmed genetic variation to fight bacteriophages // Curr. Opin. Immunol. 2012. V. 1 P. 15–20.
Bondy-Denomy J., Garcia B., Strum S. et al. Multiple mechanisms for CRISPR-Cas inhibition by anti-CRISPR proteins // Nature. 2015. V. 526. P. 136–139.
Calendar R., Abedon S. T. The Bacteriophages // 2nd Ed., Oxford University Press. 2006.
Datsenko K. A., Pougach K., Tikhonov A. et al. Molecular memory of prior infections activates the CRISPR/Cas adaptive bacterial immunity system // Nat. Commun. 2012. V. 3. P. 945
Jiang W., Marraffini L. A. CRISPR-Cas: New Tools for Genetic Manipulations from Bacterial Immunity Systems // Annu. Rev. Microbiol. 2015. V. 69. P. 209–28.
Jinek M., Chylinski K., Fonfara I., et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity // Science. 2012. V. 337. P. 816–821.
Koonin E. V., Wolf Y. I. Is evolution Darwinian or/and Lamarckian? // Biol. Direct. 2009. V. 4. P. 42.
Lopez-Pascua L., Buckling A. Increasing productivity accelerates host-parasite coevolution // J. Evol. Biol. 2008. V. 3. P. 853–860.
Makarova K. S., Wolf Y. I., et al. An updated evolutionary classification of CRISPR-Cas systems // Nat. Rev. Microbiol. 2015. V. 11. P. 722–736.
Moineau, S., Pandian S., Klaenhammer T. R. Restriction/modification systems and restriction endonucleases are more effective on lactococcal bacteriophages that have emerged recently in the dairy industry // Appl. Envir. Microbiol. 1993. V. 59. P. 197–202.
Neve H., Kemper U., et al. Monitoring and characterization of lactococcal bacteriophage in a dairy plant // Kiel. Milckwirtsch. Forschungsber. 1994. V. 46. P. 167–178.
Nuñez J. K., Harrington L. B., et al. Foreign DNA capture during CRISPR-Cas adaptive immunity // Nature. 2015a. V. 527. P. 535–538.
Nuñez J. K., Kranzusch P. J., et al. Cas1-Cas2 complex formation mediates spacer acquisition during CRISPR-Cas adaptive immunity // Nat. Struct. Mol. Biol. 2014. V. 21. P. 528–534.
Nuñez J. K., Lee A. S., Engelman A., Doudna J. A. Integrase-mediated spacer acquisition during CRISPR-Cas adaptive immunity // Nature. 2015b. V. 519. P. 193–198.
Paez-Espino D., Sharon I., et al. CRISPR Immunity Drives Rapid Phage Genome Evolution in Streptococcus thermophilus // MBio. 2015. V. 6: e00262–15.
Shmakov S., Abudayyeh O. O., Makarova K. S., et al. Discovery and Functional Characterization of Diverse Class 2 CRISPR-Cas Systems. // Mol. Cell. 2015. V. 60. P. 385–397
Tan D., Svenningsen S. L., Middelboe M. Quorum sensing determines the choice of antiphage defense strategy in Vibrio anguillarum. // mBio 2015. V. 6: e00627–15.
Westra E. R., van Erp P. B., Künne T., et al. CRISPR immunity relies on the consecutive binding and degradation of negatively supercoiled invader DNA by Cascade and Cas3 // Mol. Cell. 2012. V. 46. P. 595–605.
Работа поддержана грантом РФФИ (№ 16-34-01176)


Как уберечь от них себя и детей, в интервью "РГ" рассказал профессор кафедры клинической фармакологии лечебного факультета РНИМУ им. Н.И. Пирогова, доктор медицинских наук Андрей Спасский.
Андрей Александрович, есть ли способы избежать заражения в сезон острых респираторных инфекций?
Андрей Спасский: В начале эпидемии поможет обычная медицинская маска. Конечно, полностью она не защитит, но уменьшит число патогенных вирусов и микробов, попадающих в органы дыхания. Следует избегать переохлаждений, которые ведут к сбою иммунной системы, а это влияет на развитие патогенных микроорганизмов.


Важны здоровая пища, обогащенная витаминами и минералами, а также частое проветривание. Если есть возможность, то помещения следует кварцевать - это тоже снижает число микробов внутри. Необходимо соблюдать правила личной гигиены и как можно чаще мыть руки. Употребление "природных антибиотиков" - чеснока и лука - тоже значительно снижает риск заболеть. И нельзя забывать закалять организм и стремиться к активному образу жизни, который ускоряет метаболизм и запускает усиливающие иммунитет механизмы.
Многие люди переносят болезнь на ногах или считают себя нездоровыми всего 3-4 дня. Это правильно?
Андрей Спасский: Этого времени организму обычно достаточно, чтобы начать бороться с вирусом. Его концентрация и количество продуктов распада клеток в крови падает, самочувствие улучшается. Но о выздоровлении речи пока не идет. Вирус поражает эпителий дыхательных путей и нарушает его барьерную функцию, что ведет к активации бактерий и осложнениям. На мой взгляд, на восстановление эпителиального слоя требуется, как минимум, две недели. Это же время требуется для выработки антител, чтобы иммунная система окончательно убила вирус.
Ранний переход к активной деятельности, а особенно преждевременный выход на работу, крайне нежелателен. Постинфекционная астения (слабость) не позволит полноценно трудиться, особенно тем, кто, например, водит машину или управляет самолетом. А незаконченное выздоровление может привести к рецидивам и осложнениям.
Какие осложнения тогда возможны?
Андрей Спасский: На поврежденной вирусом слизистой оболочке на фоне слабого иммунитета часто активируются болезнетворные бактерии из нашего же организма. Прежде всего пневмококки. Такие осложнения называются вторичными - это бронхит, пневмония, отит, синусит. Возникают и специфические осложнения, прямо связанные с деятельностью вирусных частиц. Это повышение внутричерепного давления, когда развиваются симптомы менингизма. Далее может возникнуть острая дыхательная недостаточность и даже развиться инфекционно-токсический шок. Хотя ОРВИ обычно проходит без последствий, у взрослых с хроническими заболеваниями, особенно при гриппе, возможны тяжелые осложнения. И тогда для спасения пациента требуется госпитализация и серьезная терапия.
Все напуганы коронавирусом, но осложнений от сезонного гриппа и смертность от них не меньше. Как распознать осложнение?


Андрей Спасский: Если на третий-пятый день после острой фазы болезни возникла и держится несколько дней температура 38 градусов и выше, а жаропонижающие не действуют, нужно срочно обращаться к врачу. Усиливающийся кашель, одышка, боль в горле, насморк в этой ситуации предвещают серьезные осложнения. Тут уже нельзя заниматься самолечением. Только врач сумеет поставить диагноз и назначить нужную терапию. Позднее обращение за его помощью грозит развитием таких тяжелых осложнений, как инфекционно-токсический шок и пневмония, которые могут закончиться и летальным исходом.
Какие схемы лечения ОРВИ и гриппа сегодня считаются наиболее эффективными?
Андрей Спасский: Для лечения гриппа существуют препараты, действующие исключительно на вирус. Но поставить диагноз "грипп" сложно: кроме клинической картины нужно лабораторное подтверждение наличия вируса гриппа. В структуре всех циркулирующих вирусов на грипп приходится 20-30 процентов, а остальное, как правило, это риновирусы или аденовирусы, которых насчитывается более 200. От них специфических препаратов нет. Поэтому врачи сегодня используют хорошие противовирусные препараты широкого спектра действия, работающие прежде всего через интерфероновое звено иммунитета. Интерфероны - это регуляторные молекулы, которые посылают в клетки сигнал о выработке специальных белков, способных остановить размножение вируса.
Интерфероны также стимулируют работу специальных рецепторов на поверхности пораженных клеток, по которым иммунитет определяет, что клетка заражена и ее нужно уничтожить. С помощью препаратов можно либо повысить концентрацию интерферонов, стимулируя выработку собственных, либо привнести их извне, либо настроить работу имеющихся у человека интерферонов так, что их уровня будет достаточно для реального отпора вирусу. Так работает, например, Эргоферон. Эргоферон и подобные ему препараты не вызывают истощения иммунной системы, поэтому и восстановление после инфекции пройдет быстрее, и риск вторичных осложнений уменьшается.
Чем можно помочь своему иммунитету?


Андрей Спасский: В первую очередь нужно устранить факторы, его снижающие: постараться исключить простудные и инфекционные заболевания. Это замкнутый круг - чем чаще человек простужается, тем больше страдает иммунитет, а чем хуже иммунный ответ организма, тем чаще человек "цепляет" инфекции. При сезонном гипоавитаминозе и дефиците солнца растет выработка гормонов стресса адреналина и кортизола, а также нейромедиатора ацетилхолина, который называют гормоном слабости. Они делают уязвимее иммунную систему. Особенно это касается людей, сидящих на жестких диетах, а также тех, кто злоупотребляет алкоголем и сигаретами. Иммунитет также ослабляет неграмотное применение антибиотиков. Вилочковая железа и селезенка, которые производят защитные тела, должны быть защищены от вредных веществ такими окислителями, как витамины А и Е. Провитамин А содержится в моркови, шпинате, ягодах шиповника и т.д. Витамина Е много в растительных маслах - ВОЗ рекомендует съедать две столовые ложки оливкового масла в день. В рационе должны быть цитрусовые и яблоки, содержащие витамин C и железо. Также важны цинк и селен: первого много в неочищенном зерне и пивных дрожжах, второго - в зерновом хлебе, говядине, телятине, индейке, чесноке. И, конечно, важен активный образ жизни. 30-40 минут ходьбы в день организму хватает, чтобы активизировать сердечно-сосудистую и иммунную системы.
Читайте также:
- Вирус зика какие страны не посещать
- Эффективные противовирусные препараты при пневмонии
- Как опасаться от гепатита с
- Ротавирус боль в мышцах
- Может ли вирус упасть на землю
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции

