Бактериофаги это вирусы или прокариоты
Разделы: Биология
Класс: 10
Тип урока: изучение и первичное закрепление новых знаний.
| Этапы работы | Содержание этапа | ||||||
| 1. Организационный момент. | |||||||
| 2. Опрос учащихся по заданному на дом материалу (актуализация опорных знаний).
Цель для учащихся: – вспомнить строение ядра и его функции; строение прокариот и эукариот. Цели и задачи для учителя: – воспроизвести необходимые для овладения новым материалом знания учащихся о клеточных формах жизни; – оценить уровень подготовленности учащихся, скорректировать их знания, проверить готовность к восприятию новой информации. Методы организации работы: индивидуальный опрос, фронтальный опрос, опрос по карточкам. Форма организации работы: фронтальная Критерии достижения целей и задач данного этапа урока: успешные ответы учащихся, понимание ими связи вопросов с темой урока. При затруднении в ответах учитель оказывает помощь, задает наводящие вопросы. Методы мотивирования учебной активности учащихся: использование поощрительных слов за хорошие ответы. | Подавляющее большинство ныне живущих организмов состоит из клеток. Лишь немногие примитивнейшие организмы – вирусы и фаги – не имеют клеточного строения. Поэтому важнейшему признаку все живое делится на две империи.
1.Какие? (доклеточные и клеточные). 2. Какие надцарства объединяют клеточные? Почему их так назвали? (безъядерные – прокариоты и ядерные – эукариоты). 3. Покажите связь ядра с его функцией в клетке. 4. Имеются ли принципиальные различия между прокариотами и эукариотами? 5. Опрос по карточкам: Дайте сравнительную характеристику клеткам эукариот.
| ||||||
| 3. Объяснение нового учебного материала.
Цель для учащихся: – изучить строение вирусов, этапы проникновения вирусов в клетку-хозяина; – сравнить строение вирусов с живыми организмами. Цели и задачи для учителя: – познакомить учащихся со строением вирусов и фагов, этапами их проникновения в клетку; – осмысление новых знаний при сравнении доклеточных и клеточных организмов; – развивать у учащихся умения сравнивать, анализировать, находить главное; – работая с рисунками научить путям достижения поставленных целей; – при коллективном выполнении заданий, создать атмосферу сотрудничества и заинтересованности, наличие обратной связи с учащимися, развитие у них коммуникативных способностей. Основные положения нового материала: 1. История открытия вирусов. 2. Строение вирусов и бактериофагов. 3. Пути проникновения вирусов в клетку. 4. Гипотезы возникновения вирусов. Методы организации работы: использование проблемных вопросов, рассказ учителя с элементами беседы, работа с тетрадью, использование технических средств обучения. Форма организации работы: фронтальная, индивидуальная, работа в парах, коллективная (эвристическая беседа). Критерии достижения целей и задач данного этапа урока: – могут рассказать о строении вирусов, сравнивать их с клеточными организмами; – умеют найти из предложенного материала нужную информацию, вычленить главное. Критерии определения уровня внимания и интереса учащихся к излагаемому материалу: – активность в ответах на вопросы; – наличие уточняющих вопросов в сложных местах. Методы мотивирования учебной активности учащихся: использование поощрительных слов. | 1. Учитель: Я зашла в аптеку, узнать, какие есть медицинские препараты против инфекций, вызывающих различные заболевания. Лекарств, предупреждающих и лечащих бактериальные заболевания очень много. И совсем немного препаратов мне предложили в аптеке для профилактики вирусных заболеваний.
Беседа: 1. Почему же так мало противовирусных препаратов? 2. Что для этого надо знать, чтобы противостоять вирусам? 3. Представьте себя в роли тех людей, которые должны защитить человечество от вирусов. Какие знания о вирусах вам необходимы, чтобы выполнить эту важную миссию? 4. Какие цели и задачи мы должны решить на уроке? Учитель называет тему урока, ученики записывают в тетради. (слайды 1, 2) Учитель: Об истории открытия вирусов нам расскажет ученица А. Учитель: А я расскажу о гипотезах возникновения вирусов. (слайды 3-6) 3. Учитель: Чтобы узнать, как устроен вирус, на него необходимо посмотреть. Как вы думаете, почему я не предлагаю вам для этого световой микроскоп? (Ответы учащихся) Комментарий учителя: Действительно, увидеть вирусы можно только с помощью электронного микроскопа. Сегодня науке известно около полутора тысяч вирусов. Но они настолько малы, что, по словам одного из ученых, коллекция, собранная из всех известных вирусов, “поместилась бы в коробочке размером с маковое зернышко”! Давайте, для того чтобы узнать, как устроены вирусы, отправимся с вами в виртуальную вирусную лабораторию. В ваших лабораториях есть образцы некоторых вирусов. Рассмотрите их. Ответьте на вопросы, которые есть в информационных листах. Вирусологи имеют дело с опасными инфекциями. Их работа требует исключительной аккуратности и оперативности. Поэтому, чтобы рассмотреть, как устроены вирусы, вам дается 5 минут. (Работа учащихся в парах). Строение вируса. (слайды 7, 8) В клетке хозяина вирус находится в виде молекул нуклеиновой кислоты. В свободноживущем состоянии в форме вириона. Вирион это генетические элементы, одетые в защитную белковую оболочку способные переходить из одной клетки в другую Вирионы представляют собой симметричные тела, состоящие из повторяющихся элементов. В сердцевине каждого вириона находится генетический материал, представленный молекулами ДНК или РНК. (У всех организмов каждая клетка содержит и ДНК и РНК). И ДНК и РНК могут быть как двух цепочные, так и одно цепочные, линейные или кольцевые. Генетический материал вируса (геном) окружен капсидом – белковой оболочкой, защищающей его как от действия нуклеаз – ферментов, разрушающих нуклеиновые кислоты, так и от воздействия ультрафиолетового излучения. Капсиды состоят из многократно повторяющихся полипептидных цепей одного или нескольких типов белков. Оболочка часто построена из повторяющихся субъединиц – капсомеров. Капсомеры образуют структуры с высокой степенью симметрии. Сложноорганизованные вирусы имеют дополнительную белковую или липопротеиновую оболочку, которая иногда может содержать и углеводы, например, у возбудителей гриппа и герпеса. Учитель: Так просто не устроен ни один живой организм. 1. Какой вывод по этой части работы можно сделать? Сходство с живыми организмами: а) Способны воспроизводить себе подобные формы. 3. Чем отличаются вирусы по строению от клеток растений, животных, грибов и бактерий? Ученики записывают в тетради вывод: 4. Почему же вирусы выделяют в особое царство живой природы? (Предполагаемый ответ: они, как никакие другие живые организмы, сочетают в себе признаки живых систем и неживой материи, поэтому их выделяют в особое царство живой природы). В отличие от всех организмов у вирусов отсутствует собственная система биосинтеза белка, что побуждает их вести паразитический образ жизни. В целом жизненный цикл вируса имеет две фазы: – внеклеточную или покоящуюся (вирусные частицы или вирионы) Процесс размножения вирусов особенный в органическом мире, он характеризуется огромной скоростью. Этапы проникновения вируса в клетку и его размножение. Только внедряясь в чужую клетку, вирус может воспроизводить себе подобные формы. Для этого он использует органоиды и ферменты клетки-хозяина, т.к. своих органоидов и ферментов у него нет. Как же это происходит? 1) Вирус осаждается на поверхности мембраны клетки. После этого клетка либо погибает, либо продолжает существовать и производить новые поколения вирусных частиц. – Подумайте, пожалуйста, и ответьте на вопрос: – Противоречит ли существование вирусов одному из главных положений клеточной теории о том, что все живые организмы состоят из клеток? Почему? (Предполагаемый ответ: Не противоречит, а подтверждает, так как свойства живых организмов вирусы могут проявлять только внутри других живых клеток). 4. Строение бактериофага: Особой группой вирусов являются бактериофаги, или просто фаги, которые заражают бактериальные клетки. Их строение: 1) капсидная головка с нуклеиновой кислотой (ДНК или РНК); Посмотрите, как размножается Уже через 10 мин после заражения в бактерии формируются новые фаги, а через полчаса бактериальная клетка разрушается, и из нее выходят около 200 заново сформированных вирусов – фагов, способных заражать другие бактериальные клетки. Некоторые фаги используются человеком для борьбы с болезнетворными бактериями, например с бактериями, вызывающими холеру, дизентерию, брюшной тиф. И сегодня, я не могу не сказать еще об одном вирусе, который известен человечеству уже более 20 лет. Но ученые до сих пор не нашли лекарства против этого вируса. Что это за вирус? (Предполагаемый ответ: ВИЧ – Вирус иммунодефицита человека). О вирусе СПИДа расскажет ученик Б. 1. Вирусы являются возбудителями многих опасных болезней человека, животных и растений. (Дополнительная информация: Попытки использовать вирусы на пользу человечеству довольно немногочисленны. Так, в середине XX века вирус кроличьего миксоматоза использовали в Австралии, чтобы уменьшить поголовье этих чрезвычайно расплодившихся животных. Благодаря успехам генетики в будущем, возможно, искусственные вирусы смогут уничтожать больные клетки, не затрагивая при этом здоровые, или излечивать их, добавляя необходимый ген). | ||||||
| 4. Закрепление учебного материала:
– первичное закрепление материала; Цели для учащихся: – подкрепить свои знания о строении вирусов; Цели и задачи для учителя: – осмыслить, систематизировать, обобщить и закрепить новые знания и умения; Метод организации работы: Форма организации работы: Критерии, позволяющие определить степень усвоения нового материала: хорошие оценки за работу. Возможные пути и методы реагирования на ситуации, когда часть учащихся не усвоила новый материал: – учитель исправляет и корректирует ответы учеников; – в случае выявления ошибок, проводится коррекция знаний на следующем уроке. | Для того чтобы подвести итог нашей работы, я предлагаю составить рассказ о вирусах с использованием слов выписанных на доске. По цепочке составляем по одному предложению, но чтобы получился логически завешенный текст.
ВИРУСНЫЕ ЗАБОЛЕВАНИЯ. (слайд 14) – Вирусы — неклеточная форма жизни. – Вирусы являются облигатными паразитами — они не способны размножаться вне клетки – Вирусы имеют специфический механизм взаимодействия с клетками. – Вирусы внутриклеточные паразиты бактерий, растений, животных. – Вирусы — возбудители опасных заболеваний человека. – Обнаружен также вирус, поражающий другие вирусы. Давайте вернемся к задачам нашего урока. Удалось ли их решить в процессе совместной деятельности? Рефлексия. (слайд 16) Давайте вернемся к задачам нашего урока. Удалось ли их решить в процессе совместной деятельности? Рефлексия. (слайд 16) | ||||||
| 5. Задание на дом.
Цели для учащихся: – используя текст параграфа и записи в тетради выучить строение и значение вирусов, уметь отвечать на вопросы; – выполнить творческие задания. Цели и задачи для учителя: – объяснить особенности выполнения домашнего задания; – мотивировать выполнение учащимися дополнительных заданий хорошими оценками. Критерии успешного выполнения творческих заданий: Запишите домашнее задание: 1. Параграф 59, записи в тетради. – Провести мини-исследование по вопросу: почему то, что поражает компьютерные программы, тоже назвали вирусом? Урок окончен. До скорой встречи! | |||||||
При подготовке к уроку были использованы:
- Ресурсы интернет.
- Биологический энциклопедический словарь.
- Общая биология: Учеб. для 10-11 кл. Д.К.Беляев, 2010г.
- Общая биология: Учеб. Для 10-11 кл. А.О.Рувинский, 2009г.
- Материалы учителей биологии В.И.Аржановой, О.В.Рындиной, Н.Б.Кузнецова.

Формы жизни
Выделяют две основные формы жизни: клеточные и неклеточные. Подавляющее большинство организмов относится к клеточным формам жизни, к неклеточным – только вирусы.
Клеточные формы делятся на прокариот (доядерные) и эукариот (собственно ядерные). Прокариоты не имеют оформленного ядра, у эукариот ядро четко выражено. К прокариотам относятся бактерии и сине-зеленые водоросли, к эукариотам — растения, животные и грибы.
Вирусы
Вирусы (от лат. virus — яд) не проявляют признаков жизни вне других организмов и являются внутриклеточными облигатными паразитами. Они поражают любые организмы. Вирусы — это самые мелкие организмы Земли: их молекулы видны только под электронным микроскопом. Вирусы бактерий имеют специальное название: бактериофаги или просто фаги. Изучением вирусов занимается вирусология.
Вирусы были открыты в XIX в. Д. И. Ивановским: он обнаружил и описал вирус табачной мозаики. Этот вирус поражает табак, вызывая разрушение хлорофилла, из-за чего некоторые участки органов становятся более светлыми по сравнению со здоровыми. Внешне такой орган (чаще всего лист) действительно напоминает мозаику: темные участки чередуются со светлыми.
Вирус — это генетический элемент, покрытый защитной белковой оболочкой. Отдельные вирусные частицы (вирионы) представляют собой симметричные тела, состоящие из повторяющихся элементов .
В центре вируса находится генетический материал — ДНК (ДНК-содержащие вирусы) или РНК (РНК-содержащие вирусы). ДНК может быть двухцепочечной или одноцепочечной, кольцевой или линейной; РНК — одно- или двухцепочечной. Генетический материал вируса окружен капсидом — белковой оболочкой, выполняющей защитную функцию. Эта оболочка состоит из многократно повторяющихся полипептидных цепочек одного или нескольких белков. Снаружи от белковой оболочки может образовываться еще одна оболочка — внешняя.
Цикл вирусов. Сначала вирус прикрепляется к клетке хозяина, затем его генетический материал проникает внутрь клетки хозяина. Если вирус содержит ДНК, то она встраивается в ДНК клетки хозяина. Далее происходит образование и-РНК вируса, синтез его белков и образование новых вирусных частиц, т. е. клетка хозяина начинает работать на вирус.
РНК-содержащие вирусы ведут себя немного по-другому. Если РНК вируса состоит из двух цепей, то на одной из них синтезируется и-РНК, затем происходит синтез белков вируса и т.д.
У ретровирусов, также относящихся к РНК-содержащим (например, вирус иммунодефицита человека – ВИЧ), с помощью фермента обратной транскриптазы на РНК синтезируется сначала одна цепь ДНК, а затем и вторая. После этого ДНК вируса встраивается в ДНК клетки хозяина.
Весь цикл может занимать несколько минут.
Вирусы вызывают различные заболевания человека: грипп, СПИД, гепатит, полиомиелит, оспу, корь, бешенство (водобоязнь), герпес, геморрагическую лихорадку.
Прокариоты
К прокариотам относятся бактерии и цианобактерии, которые объединяются в царство Дробянки. У них отсутствует оформленное ядро и мембранные органоиды, генетический материал представлен нуклеоидом (молекулой хромосомной ДНК, замкнутой в кольцо) и плазмидами (небольшими внехромосомными ДНК). Характерны мелкие рибосомы (70S), расположенные в цитоплазме, и мезосомы (впячивание мембраны внутрь клетки), выполняющие функции митохондрий.
| Признак | Прокариоты | Эукариоты |
| Клеточная стенка | У бактерий – из муреина, у цианобактерий — из целлюлозы | У животных нет, у грибов из хитина, у растений из целлюлозы |
| Ядро и генетический материал | Ядра нет; кольцевая ДНК в цитоплазме, хромосом нет. Гистонов нет | Ядро есть; двуцепочечная ДНК находится в ядре, соединена с белками-гистонами и образует хромосомы |
| Мембранные органоиды | Нет | Есть |
| Рибосомы | Мелкие, находятся в цитоплазме, 70S | Крупные, большинство располо-жено на эндоплазматической сети, 80S |
| Деление клеток | Деление пополам. Митоз не характерен | Митоз и мейоз |
| Диссимиляция | Анаэробная и аэробная | Преобладает аэробная |
| Фотосинтез | У некоторых бактерий и цианобактерий | Только у растений |
| Хемосинтез | Некоторые бактерии | Не возможен |
| Азотфиксация | Некоторые бактерии | Не возможна |
Бактерии
Бактерии — микроскопические одноклеточные организмы. Они широко распространены в природе и занимают все среды жизни (почвенную, наземно-воздушную, водную; также обитают внутри живых организмов).
Снаружи клетка бактерий покрыта клеточной стенкой, в состав которой входит муреин. Многие бактерии способны формировать дополнительную внешнюю капсулу, защищающую их внутри организма хозяина от его иммунной системы. Под оболочкой находится плазматическая мембрана, а внутри клетки — цитоплазма с включениями, рибосомами и генетическим материалом (кольцевая ДНК). Многие бактерии имеют жгутики, обеспечивающие их подвижность.
Размножение бактерий происходит делением на две клетки: сначала делится нуклеоид, затем — цитоплазма. При благоприятных условиях одно деление происходит каждые 15-20 мин. При возникновении неблагоприятных условий бактерии способны образовывать споры. У спор очень плотная внешняя оболочка, способная переносить различные внешние воздействия и сохранять жизнеспособность в течение десятков и сотен лет. При наступлении благоприятных условий спора прорастает и образует бактериальную клетку.
Сине-зеленые водоросли (цианобактерии)
Обитают в водной среде и на почве. Различают одноклеточные и колониальные формы. Многие из них в цитоплазме содержат вакуоли, которые поддерживают плавучесть клетки.
Цианобактерии являются автотрофами и содержат хлорофилл. При фотосинтезе выделяют кислород в атмосферу. Размножение осуществляется делением. Способны образовывать споры для пережидания неблагоприятных условий.
Прошло сто лет с того времени, как английский микробиолог Ф. Туорт отметил прозрачные стекловидные пятна в колониях микрококков, где погибли бактериальные клетки. После открытия бактериофагов их исследования долгое время имели феноменологический характер из-за недостаточного развития экспериментальных методов. Ученые не имели возможности детально изучить особенности противобактериального воздействия бактериофагов, так как последние нельзя увидеть не только невооруженным глазом, но и с помощью светового микроскопа. Изучение вирусов, в том числе вирусов бактерий, вышло на принципиально новый уровень лишь с созданием и внедрением в научную практику электронного микроскопа
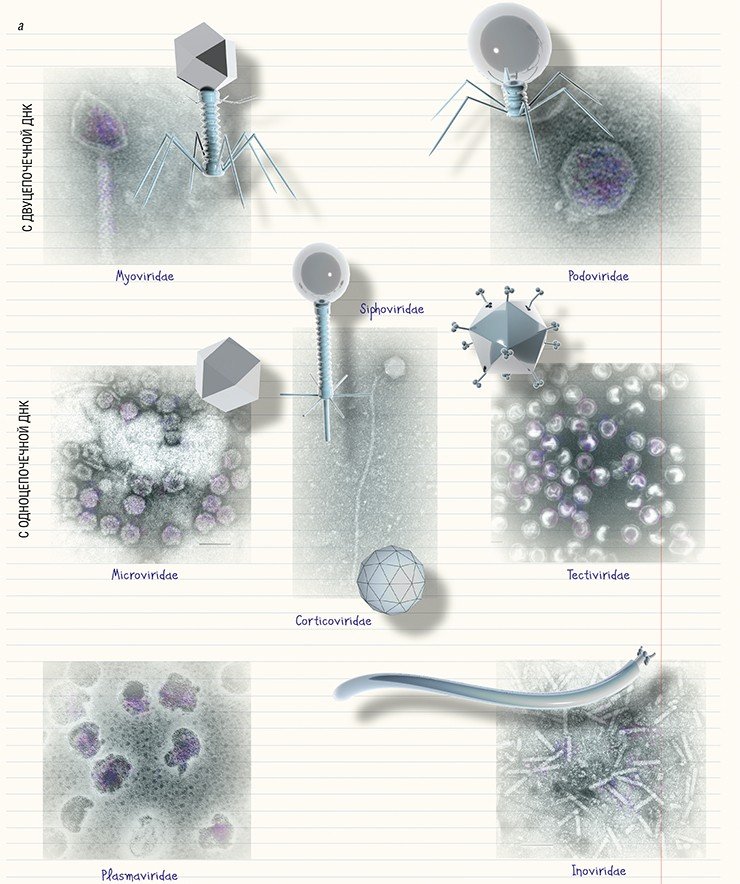
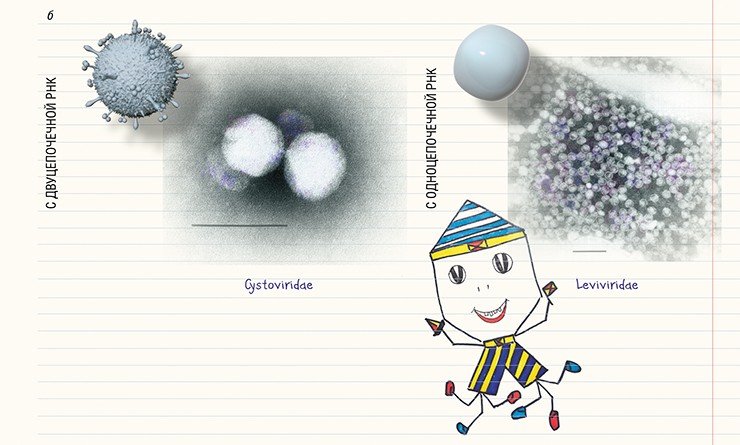
С появлением электронной микроскопии стало понятно, что бактериофаги являются даже не микро- а наноорганизмами, так как их размеры не превышают 100 нм. Также оказалось, что по своему строению они отличаются колоссальным разнообразием. Соответственно, возник вопрос об их номенклатуре. В основу первой классификации, которая была предложена еще в 1943 г., легли особенности строения фагов, установленные с помощью электронной микроскопии. Один из ее основоположников, Э. Руска, в своей общей схеме классификации вирусов выделил бактериофаги отдельно, разделив их на три типа по морфологическим характеристикам (Ackermann, 2009).
В основу современной систематики бактериофагов, созданной в 1967 г., легла классификация, включавшая шесть морфотипов. Но по мере открытия новых бактериофагов в нее включались новые семейства, роды и виды. С развитием методов молекулярной биологии появились дополнительные критерии классификации, учитывающие тип нуклеиновой кислоты и (или) композицию белков в составе фага.
Применение в исследованиях бактериофагов современных молекулярных методов, позволило выявить множество особенностей этих интересных организмов. Сами бактериофаги в свою очередь оказались для молекулярных биологов очень полезным методологическим инструментом (Brussow, 2013).
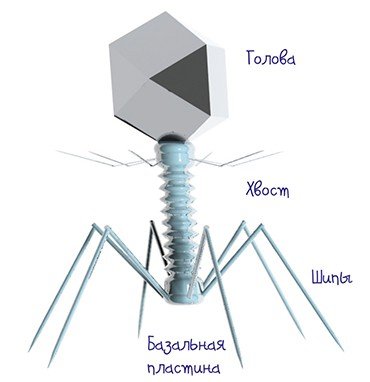
Была бы голова, а хвост будет
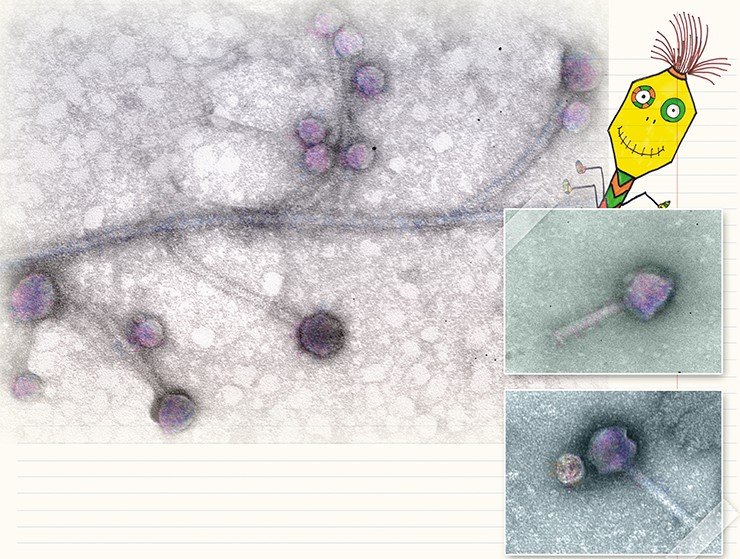
Чтобы узнать вид бактериофага, нужно определить его ультраструктурные характеристики, для чего используют метод негативного контрастирования. Образцом может служить любая суспензия, содержащая фаги: вода из природного источника, смывы с кишечника животных или суспензия бактериальных клеток после инкубации с бактериофагом в условиях лаборатории. На каплю подготовленной суспензии помещают специальную медную сетку, покрытую тонкой полимерной пленкой, на которую и сорбируются бактериофаги. Затем сетку обрабатывают контрастирующим веществом (обычно уранилацетатом или фосфорно-вольфрамовой кислотой), которое окружает частицы бактериофага и создает темный фон, на котором бактериофаги, имеющие низкую электронную плотность, становятся видны в электронном микроскопе.
Охота на бактерию
Сочетание методов негативного контрастирования и ультратонких срезов* позволяет проследить все этапы воспроизводства бактериофагов, включая сорбцию частиц фага на поверхности бактериальных клеток, их проникновение в клетки и копирование. К сожалению, эта область исследований разработана существенно хуже, чем визуализация и идентификация бактериофагов методом негативного контрастирования. Между тем ультраструктурные характеристики каждого из этапов жизненного цикла бактериофагов могут быть полезны для адекватной оценки эффективности разрабатываемых методов фаговой терапии.
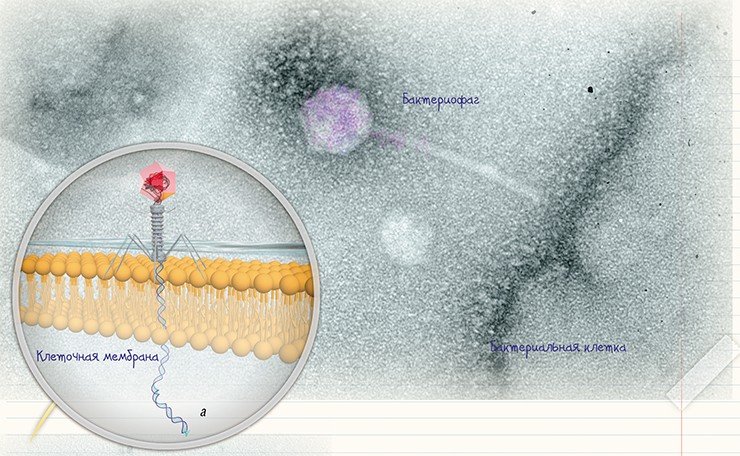
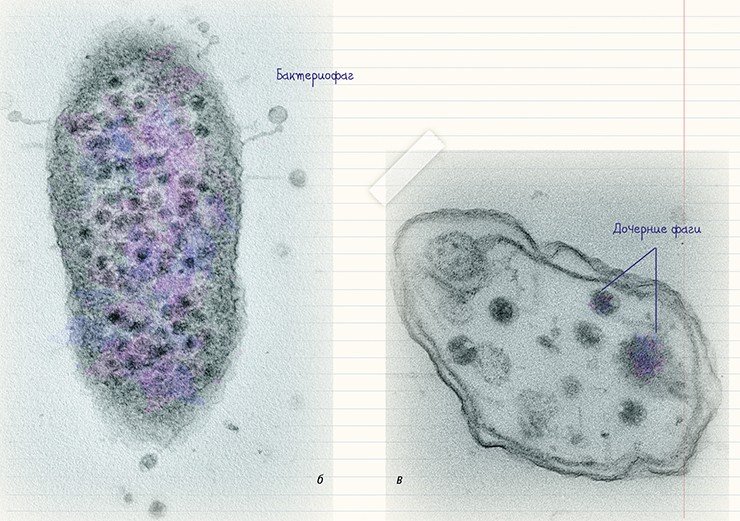
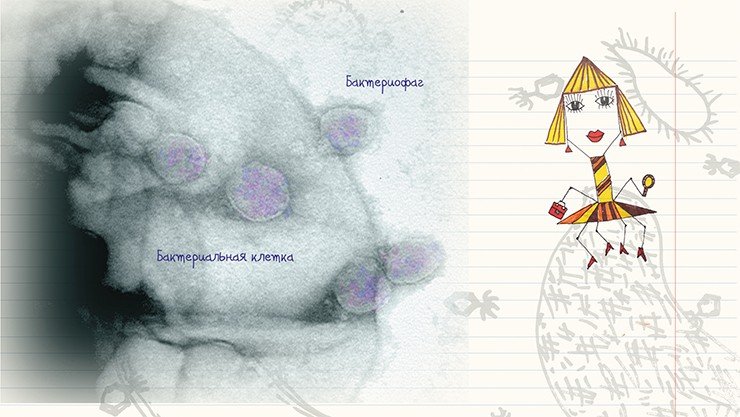
* При методе ультратонких срезов клетки заливают в особую смолу, и из получившихся твердых блоков готовят срезы толщиной 60—80 нм на ультрамикротоме с помощью стеклянного или алмазного ножа
Ackermann H. W., Prangishvili D. Prokaryote viruses studied by electron microscopy. 2012. N. 157. P. 1843—1849.
Ackermann H. W., Tiekotter K. L., Murphy’s law – if anything can go wrong, it will // Bacteriophage. 2012. N. 2:2. P. 122—129.
Bacteriophages methods and protocols / Ed. A. M. Kropinski, R. J. Clokie. Humana Press, 2009. V. 1.
Duckworth D. H. Who discovered bacteriophage? // Bacteriological reviews. 1976. V. 40. N. 4. P. 793—802.
Introduction: a short history of virology // Viruses and man: a history of interactions / Ed. M. W. Taylor. Springer, 2014. P. 1—21.
Krylov V. N. Phage therapy in therms of Bacteriophage genetics: hopes, prospects, safety, limitation // Rus. J. of genetics. 2001. V. 37. N. 7. P. 869—887.
Matsuzaki S., Rashel M., Uchiyama J., et al. Bacteriophage therapy: a revitalized therapy against bacterial infectious deseases // J. Infect. Chemother. 2005. N. 11. P. 211—219.
В публикации использованы фото авторов и рисунки Жени Власова
Бактериофаги – это вирусы, которые поражают только бактерий. В ходе инфекции они влияют на все процессы жизнедеятельности бактериальной клетки, фактически превращая ее в фабрику по производству вирусного потомства. В конце концов клетка разрушается, а вновь образованные вирусные частицы выходят наружу и могут заражать новые бактерии.
Несмотря на огромное число и разнообразие природных фагов, встречаемся мы с ними редко. Однако бывают ситуации, когда деятельность этих вирусов не остается незамеченной. Например, на предприятиях, где производят сыры, йогурты и другие молочно-кислые продукты, часто приходится сталкиваться с вирусной атакой на бактерии, сбраживающие молоко. В большинстве таких случаев фаговая инфекция распространяется молниеносно, и полезные бактерии гибнут, что приводит к значительным экономическим потерям (Neve et al., 1994).
Именно благодаря прикладным исследованиям в интересах молочной промышленности, направленным на получение устойчивых к бактериофагам штаммов молочно-кислых бактерий, был открыт ряд механизмов, с помощью которых бактерии избегают инфекции. Параллельно были изучены способы, с помощью которых вирусы, в свою очередь, преодолевают бактериальные системы защиты (Moineau et al., 1993).
Кто защищен – тот вооружен
На сегодня известно пять основных, весьма хитроумных механизмов защиты, которые бактерии выработали в непрестанной борьбе с вирусами: изменение рецептора на поверхности клетки; исключение суперинфекции; системы абортивной инфекции; системы рестрикции-модификации и, наконец, системы CRISPR-Cas.
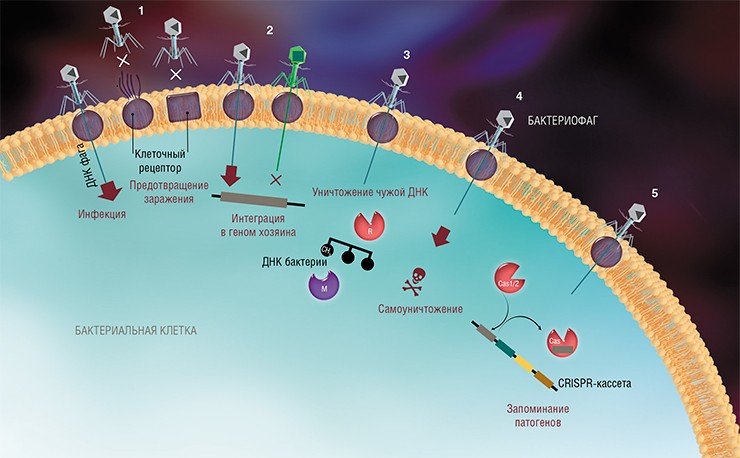
К средствам противовирусной защиты бактерий относятся и системы рестрикции-модификации, в которые входят гены, кодирующие два белка-фермента – рестриктазу и метилазу. Рестриктаза узнает определенные последовательности ДНК длиной 4—6 нуклеотидов и вносит в них двуцепочечные разрывы. Метилаза, напротив, ковалентно модифицирует эти последовательности, добавляя к отдельным нуклеотидным основаниям метильные группы, что предотвращает их узнавание рестриктазой.
Врага нужно знать в лицо
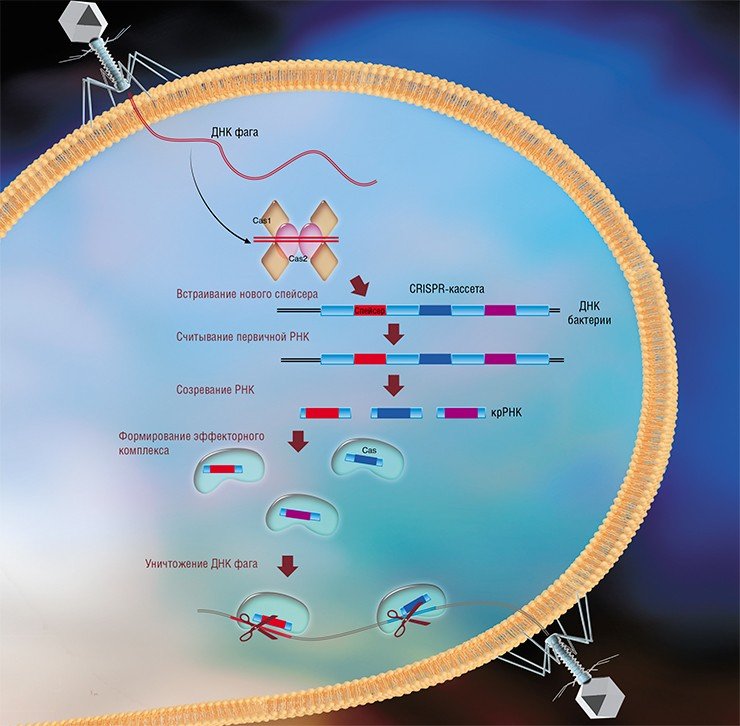
Системы CRISPR-Cas являются уникальным примером адаптивного иммунитета бактерий. При проникновении в клетку ДНК фага специальные белки Cas встраивают фрагменты вирусной ДНК длиной 25—40 нуклеотидов в определенный участок генома бактерии (Barrangou et al., 2007). Такие фрагменты называются спейсерами (от англ. spacer – промежуток), участок, где происходит встраивание, – CRISPR-кассета (от англ. Clustered Regularly Interspaced Short Palindromic Repeats), а сам процесс приобретения спейсеров – адаптацией.
Чтобы использовать спейсеры в борьбе с фаговой инфекцией, в клетке должен происходить еще один процесс, управляемый белками Cas, названный интерференцией. Суть его в том, что в ходе транскрипции CRISPR-кассеты образуется длинная молекула РНК, которая разрезается белками Cas на короткие фрагменты – защитные криспрРНК (крРНК), каждая из которых содержит один спейсер. Белки Cas вместе с молекулой крРНК образуют эффекторный комплекс, который сканирует всю ДНК клетки на наличие последовательностей, идентичных спейсеру (протоспейсеров). Найденные протоспейсеры расщепляются белками Cas (Westra et al., 2012; Jinek et al., 2012).
Системы CRISPR-Cas обнаружены у большинства прокариот – бактерий и архей. Хотя общий принцип действия всех известных систем CRISPR-Cas одинаков, механизмы их работы могут существенно отличаться в деталях. Наибольшие различия проявляются в строении и функционировании эффекторного комплекса, в связи с чем системы CRISPR-Cas делят на несколько типов. На сегодняшний день описаны шесть типов таких неродственных друг другу систем (Makarova et al., 2015; Shmakov et al., 2015).
Наиболее изученной является система CRISPR-Cas I типа, которой обладает излюбленный объект молекулярно-биологических исследований – бактерия кишечная палочка (Esсherichia coli). Эффекторный комплекс в этой системе состоит из нескольких небольших белков Cas, каждый из которых отвечает за разные функции: разрезание длинной некодирующей CRISPR РНК, связывание коротких крРНК, поиск, а затем разрезание ДНК-мишени.
Гонка вооружений
Бактериофаги, как факторы среды, вызывают направленные изменения в геноме бактерий, которые наследуются и дают бактериям явное преимущество, спасая от повторных инфекций. Поэтому системы CRISPR-Cas можно считать примером ламарковской эволюции, при которой происходит наследование благоприобретенных признаков (Koonin et al., 2009)
Некоторые бактериофаги реагируют на наличие в бактериальной клетке систем CRISPR-Cas выработкой особых анти CRISPR-белков, способных связываться с белками Cas и блокировать их функции (Bondy-Denomy et al., 2015). Еще одно ухищрение — обмен участков генома вируса, на которые нацелена система CRISPR-Cas, на участки геномов родственных вирусов, отличающихся по составу нуклеотидной последовательности (Paez-Espino et al., 2015).
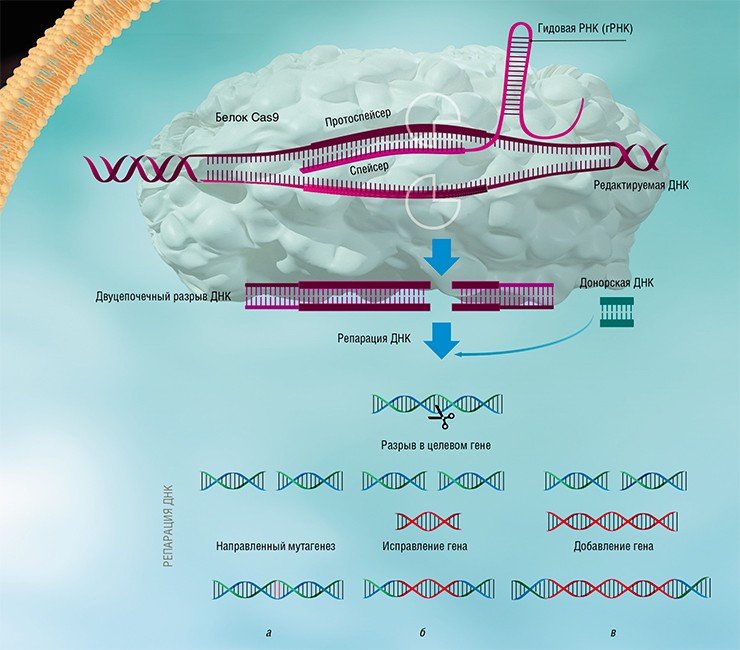
Благодаря постоянному совершенствованию биоинформатических алгоритмов поиска, а также включению в анализ все большего количества прокариотических геномов, открытие новых типов CRISPR-Cas систем является делом недалекого будущего. Предстоит также выяснить и детальные механизмы работы многих недавно открытых систем. Так, в статье, опубликованной в 2016 г. в журнале Science и посвященной анализу системы CRISPR-Cas VI типа, описан белок С2с2, образующий эффекторный комплекс с крРНК, который нацелен на деградацию не ДНК, а РНК (Abudayyeh et al., 2016). В будущем такое необычное свойство может быть использовано в медицине для регулирования активности генов путем изменения количества кодируемых ими РНК.
Изучение стратегий борьбы бактерий с бактериофагами, несмотря на свою кажущуюся фундаментальность и отвлеченность от задач практической медицины, принесло неоценимую пользу человечеству. Примерами этого могут служить методы молекулярного клонирования и редактирования геномов – направленного внесения или удаления мутаций и изменения уровня транскрипции определенных генов.
Благодаря быстрому развитию методов молекулярной биологии всего лишь через несколько лет после открытия механизма действия систем CRISPR-Cas была создана работающая технология геномного редактирования, способная бороться с болезнями, ранее считавшимися неизлечимыми. Доступность и простота этой технологии позволяют рассматривать ее как основу для медицины, ветеринарии, сельского хозяйства и биотехнологий будущего, которые будут базироваться на направленных и безопасных генных модификациях.
Нет никаких сомнений, что дальнейшее изучение взаимодействия бактерий и их вирусов может открыть перед нами такие возможности, о которых мы сейчас даже не подозреваем.
Abudayyeh O. O., Gootenberg J. S., Konermann S. et al. C 2c2 is a single-component programmable RNA-guided RNA-targeting CRISPR effector // Science. 2016. V. 353: aaf5573.
Barrangou R., Fremaux C., Deveau H. et al. CRISPR provides acquired resistance against viruses in prokaryotes // Science. 2007. V. 315. P. 1709–1712.
Bikard D., Marraffini L. A. Innate and adaptive immunity in bacteria: mechanisms of programmed genetic variation to fight bacteriophages // Curr. Opin. Immunol. 2012. V. 1 P. 15–20.
Bondy-Denomy J., Garcia B., Strum S. et al. Multiple mechanisms for CRISPR-Cas inhibition by anti-CRISPR proteins // Nature. 2015. V. 526. P. 136–139.
Calendar R., Abedon S. T. The Bacteriophages // 2nd Ed., Oxford University Press. 2006.
Datsenko K. A., Pougach K., Tikhonov A. et al. Molecular memory of prior infections activates the CRISPR/Cas adaptive bacterial immunity system // Nat. Commun. 2012. V. 3. P. 945
Jiang W., Marraffini L. A. CRISPR-Cas: New Tools for Genetic Manipulations from Bacterial Immunity Systems // Annu. Rev. Microbiol. 2015. V. 69. P. 209–28.
Jinek M., Chylinski K., Fonfara I., et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity // Science. 2012. V. 337. P. 816–821.
Koonin E. V., Wolf Y. I. Is evolution Darwinian or/and Lamarckian? // Biol. Direct. 2009. V. 4. P. 42.
Lopez-Pascua L., Buckling A. Increasing productivity accelerates host-parasite coevolution // J. Evol. Biol. 2008. V. 3. P. 853–860.
Makarova K. S., Wolf Y. I., et al. An updated evolutionary classification of CRISPR-Cas systems // Nat. Rev. Microbiol. 2015. V. 11. P. 722–736.
Moineau, S., Pandian S., Klaenhammer T. R. Restriction/modification systems and restriction endonucleases are more effective on lactococcal bacteriophages that have emerged recently in the dairy industry // Appl. Envir. Microbiol. 1993. V. 59. P. 197–202.
Neve H., Kemper U., et al. Monitoring and characterization of lactococcal bacteriophage in a dairy plant // Kiel. Milckwirtsch. Forschungsber. 1994. V. 46. P. 167–178.
Nuñez J. K., Harrington L. B., et al. Foreign DNA capture during CRISPR-Cas adaptive immunity // Nature. 2015a. V. 527. P. 535–538.
Nuñez J. K., Kranzusch P. J., et al. Cas1-Cas2 complex formation mediates spacer acquisition during CRISPR-Cas adaptive immunity // Nat. Struct. Mol. Biol. 2014. V. 21. P. 528–534.
Nuñez J. K., Lee A. S., Engelman A., Doudna J. A. Integrase-mediated spacer acquisition during CRISPR-Cas adaptive immunity // Nature. 2015b. V. 519. P. 193–198.
Paez-Espino D., Sharon I., et al. CRISPR Immunity Drives Rapid Phage Genome Evolution in Streptococcus thermophilus // MBio. 2015. V. 6: e00262–15.
Shmakov S., Abudayyeh O. O., Makarova K. S., et al. Discovery and Functional Characterization of Diverse Class 2 CRISPR-Cas Systems. // Mol. Cell. 2015. V. 60. P. 385–397
Tan D., Svenningsen S. L., Middelboe M. Quorum sensing determines the choice of antiphage defense strategy in Vibrio anguillarum. // mBio 2015. V. 6: e00627–15.
Westra E. R., van Erp P. B., Künne T., et al. CRISPR immunity relies on the consecutive binding and degradation of negatively supercoiled invader DNA by Cascade and Cas3 // Mol. Cell. 2012. V. 46. P. 595–605.
Работа поддержана грантом РФФИ (№ 16-34-01176)
Читайте также:


