Анализ на эффективность противовирусной терапии

Статья написана гастроэнтерологом нашего центра Уховой Марией Владимировной.
Хронический гепатит С – это заболевание печени, вызванное особым вирусом, который разрушает клетки печени и при длительном течении может приводить к развитию цирроза и рака печени. Поэтому при выявлении вирусного гепатита С рекомендуем как можно раньше начать противовирусное лечение.
На старте лечения хронического гепатита С необходимо пройти предварительную диагностику с осмотром врача для выявления сопутствующих заболеваний и при необходимости провести подготовительное лечение. Подготовительная терапия необходима пациентам, имеющим фоновые заболевания, для успешного прохождения противовирусной терапии и профилактики осложнений.
При наличии хронических заболеваний, в первую очередь, сердца, легких, щитовидной железы, обязательно сообщите лечащему врачу, какие лекарства вы принимаете.
На этапе предварительной диагностики сдают анализы крови, которые оценивают характеристики вируса, активность воспаления в печени и риски влияния сопутствующих заболеваний на процесс лечения, а также помогают исключить другие причины повреждения печени.
Перечень необходимых анализов
1. Общий анализ крови – используется для общей оценки изменений, происходящих в организме. Важными показателями являются уровень гемоглобина и гематокрита, количество лейкоцитов и тромбоцитов, СОЭ.
2. Количественная ПЦР HCV – один из самых важных критериев, который позволяет оценить концентрацию вирусной РНК (вирусную нагрузку) в крови. Вирусная нагрузка показывает степень инфицирования и количество вирусов в крови.
3. Генотип вируса гепатита С – второй важнейший анализ, именно он помогает косвенно определить шансы на успешное лечение, подобрать необходимые дозы препаратов и длительность терапии.
4. аntiHBcor – наиболее чувствительный маркер хронического гепатита B. Иногда люди, страдающие гепатитом С, могут одновременно иметь и гепатит B. Лечение в таком случае будет значительно отличаться, так как некоторые новые противовирусные препараты вызывают опасные побочные эффекты у пациентов, инфицированных сразу двумя вирусами гепатита С и В.
Лечение в таком случае будет значительно отличаться- некоторые новые противовирусные препараты вызывают опасные побочные эффекты у пациентов, инфицированных сразу двумя вирусами.
5. АЛТ (аланинаминотрансфераза) – фермент из группы аминотрансфераз. Показывает активность воспаления печени при хроническом гепатите.
6. АСТ (аспартатаминотрансфераза) - фермент из группы аминотрансфераз. Показывает активность воспаления печени при хроническом гепатите.
7. ГГТП (гамма-глутамилтрансфераза) – это наиболее чувствительный лабораторный показатель не только при заболеваниях печени, но и желчных путей и поджелудочной железы.
9. Билирубин – уровень билирубина в сыворотке крови отражает способность печени к метаболизму лекарственных средств. Повышение уровня билирубина при вирусном гепатите С также отражает степень повреждения и гибели клеток печени в результате воспаления.
9. АФП (альфа-фетопротеин) – первичный маркер рака печени, для оценки рисков онкологического заболевания, так как наличие гепатита С повышает риск развития рака печени.
Кроме анализов крови необходимо пройти УЗИ печени с эластографией для оценки стадии фиброза печени. Без определения стадии фиброза начинать лечение гепатита С не рекомендуется, так как фиброз определяет выбор противовирусного препарата и длительность противовирусной терапии.
Запись на эластографию печени сдвиговой волной – самую новую и эффективную неинвазивную диагностику печени для оценки стадии фиброза, по тел. 426-33-88.
Перечень обследований в некоторых случаях может быть расширен. Например, при наличии хронических заболеваний могут потребоваться дополнительные анализы и исследования, их определяет врач во время приема.
В процессе лечения проводятся промежуточные обследования для оценки эффективности противовирусной терапии (анализы крови, мочи). Кроме того, на каждом этапе лечения необходимо сопровождение врача-куратора с опытом проведения противовирусной терапии новыми препаратами для выявления побочных эффектов и корректировки противовирусной терапии при необходимости.
Комплексное обследование, включающее определение уровня вирусной нагрузки и наличия и выраженности антительного ответа, рекомендуется пациентам с вирусным гепатитом С для контроля эффективности терапии.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исключить из рациона жирную пищу в течение 24 часов до исследования.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
В настоящее время для лечения хронического гепатита С (ХГС) применяются схемы терапии с использованием препаратов прямого противовирусного действия (ПППД).
Мониторинг противовирусной терапии (ПВТ) хронического гепатита С (ХГС) с использованием ПППД должен проводиться в соответствии с существующими рекомендациями по лечению ХГС. Российские рекомендации по диагностике и лечению взрослых больных гепатитом С, опубликованные в 2013 г., содержат рекомендации по проведению стандартной терапии и терапии с использованием NS3-ингибиторов протеазы первой волны – боцепревира и телапревира и, соответственно, не могут быть использованы для ведения противовирусной терапии ХГС другими ПППД, в т.ч. при безинтерфероновой терапии.
В настоящее время при проведении лечения ХГС с помощью ПППД необходимо руководствоваться рекомендациями двух ведущих мировых гепатологических организаций - Европейской ассоциации по изучению печени (EASL), опубликованных 2015 году, и/или Американской ассоциации по изучению заболеваний печени (AASLD) 2016 года. В соответствии с этими рекомендациями мониторинг противовирусной терапии необходимо проводить с использованием ультрачувствительных качественных тестов по выявлению РНК HCV и/или ультрачувствительных количественных тестов, позволяющих определить концентрацию РНК HCV в процессе проведения лечения и после его окончания. Значения аналитической чувствительности этих тестов отличаются в рекомендациях по лечению ХГС, разработанных различными гепатологическими ассоциациями - в российских рекомендациях 2013 года при проведении терапии с использованием ПППД рекомендованная чувствительность качественного исследования - 10 МЕ/мл, в рекомендациях EASL - 15 МЕ/мл и выше, в рекомендациях AASLD - 25 МЕ/мл и выше.
AASLD рекомендует следующую схему контроля эффективности противовирусной терапии с использованием ПППД – определение концентрации РНК HCV на 4 неделе терапии и 12 неделе после ее окончания. Дополнительное аналогичное тестирование желательно (но необязательно) провести непосредственно после окончания терапии (ответ по окончании терапии) и через 24 недели после завершения лечения. Устойчивый вирусологический ответ - УВО определяется у всех пациентов, завершивших терапию. Лечение не следует прерывать, без проведения мониторинговых исследований. В случае выявления РНК HCV на 4 неделе терапии, не прерывая терапию, следует провести дополнительное тестирование через 2 недели (на 6-й недели терапии), при возрастании вирусной нагрузки более чем в 10 раз, по сравнению с предыдущим тестированием, рекомендуется завершить лечение. Во остальных случаях лечение должно быть продолжено.
Для оценки эффективности проведенной терапии определение уровня РНК HCV проводится на 12 или 24 неделе после завершения терапии, вне зависимости от результатов оценки ответа по окончании терапии, в том числе у пациентов с выявленной в конце терапии РНК HCV.
Согласно рекомендациям EASL, мониторинг эффективности терапии должен проводиться с использованием одних и тех же тест-систем, желательно в одной и той же лаборатории - для обеспечения объективности при сопоставлении результатов исследования.
Исследование одномоментно позволяет оценить эффективность терапии по двум основным показателям: элиминации вируса из организма и напряженности специфического иммунитета.
Когда назначается исследование?
- При подтвержденном вирусном гепатите С, независимо от формы инфекционного процесса, для контроля эффективности противовирусной терапии (ПВТ).
Что означают результаты?
Для каждого показателя, входящего в состав комплекса:
- Длительность ПВТ и периодичность количественного определения РНК зависит от генотипа вируса и степени повреждения печени.
- Эффективность лечения оценивается по уровню РНК в динамике (до, во время (4 и 12 неделя) и через 24 недели после курса ПВТ).
- Подтверждение вирусемии: РНК HCV может быть обнаружена в концентрации, находящейся за нижней границей линейного диапазона концентраций (7,5×10 2 – 1,0×10 8 копий/мл образца).
Эффективная терапия - вирусная нагрузка крови снижается на 2 порядка в первые 4-12 недель лечения и не обнаруживается после окончания курса.
Неэффективная терапия - отсутствие снижения виремии через 12 недель ПВТ.
(200 копий/мл = 400 МЕ/мл)
Не обнаружено или значение ниже предела чувствительности метода
Концентрация ниже линейного диапазона
Низкая виремия (наиболее благоприятный прогноз течения заболевания и эффективности терапии)
> 1,0х10 8 копий/мл
Выше линейного диапазона концентрации
В первые 2 недели болезни в сыворотке крови у инфицированных вирусным гепатитом С появляются антитела класса IgM (и сохраняются около 2 месяцев), в период ранней реконвалесценции в крови определяются антитела классов IgM и IgG, а в период поздней реконвалесценции - только IgG. Определение суммарных антител к различным антигенам вируса гепатита С является стандартом диагностики данного заболевания и используется в качестве скринингового метода.
Выработка антител к ВГС
IgM – начинают вырабатываться спустя 2 недели после развития клинической картины острого ВГС или обострения ХГС и обычно исчезают спустя 4-6 месяцев.
IgG – начинают определяться в период ранней реконвалесценции (11-12 неделя болезни), сохраняются весь период реконвалесценции.
Актуальность. Проблема этиотропного лечения хронического вирусного гепатита С (ХВГС), несмотря на большое количество исследований, по-прежнему остается актуальной и до конца не решена.
Эффективность лечения по данным разных исследователей не превышает 46-51% у больных ХВГС с 1-м генотипом и 70-80% у больных ХВГС с не 1-м генотипом 3. Так же ограничивают их применение высокая стоимость препаратов и большое количество побочных эффектов от проводимой терапии. Целью проведения этиотропной терапии ХВГС является подавление вирусной репликации, эрадикация вируса из организма и, соответственно, прекращение инфекционного процесса. Даже отсутствие вирусологического эффекта при специфической терапии приводит к замедлению прогрессирования заболевания, стабилизации или регрессии патологических изменений в печени, предупреждению формирования цирроза печени и первичной гепатоцеллюлярной карциномы, а также повышению качества жизни.
Оценку эффективности специфического лечения осуществляют на основании нескольких критериев: вирусологического (исчезновение рибонуклеиновой кислоты (РНК) вируса из сыворотки крови), биохимического (стойкая нормализация уровня ферментов печени) и морфологического (уменьшение индекса гистологической активности и стадии фиброза).
В целом около 5% больных [1,5] вынуждены отказаться от специфического противовирусного лечения в начале курса из-за многочисленных побочных эффектов, а 20% не доводят его до конца.
Побочные эффекты интерферона (ИФН) и рибавирина иногда вынуждают временно или постоянно снижать их дозы или отменять препараты. Некоторыми исследователями [5] показано, что для достижения устойчивого вирусологического ответа (УВО) необходимо получение не менее 2/3 дозы ИФН и рибавирина, поэтому эффективность комбинированной противовирусной терапии (КПВТ) напрямую зависит от наличия побочных эффектов и возможностью их коррекции.
Некоторые побочные эффекты не требуют медикаментозной терапии, так как носят легкий или среднетяжелый характер, другие - тяжелый и угрожающий жизни характер, при этом необходима специфическая коррекция. Как правило, после окончания терапии большинство побочных эффектов полностью исчезает без применения симптоматической терапии.
Проблема побочных эффектов на фоне проводимой КПВТ остается до конца не изученной, несмотря на проведенные многочисленные исследования.
Основными побочными явлениями, описанными в литературе, являются: гематологические изменения; гриппоподобный, диспепсический, неврологический и астеновегетативный синдромы; аутоиммунные поражения; снижение массы тела; выпадение волос; огрубение кожи; аллергические реакции различной степени выраженности; местная реакция в области введения интерферонов.
Таким образом, проблема побочного действия комбинированного противовирусного лечения ХВГС, его влияние на достижение УВО является актуальной в настоящее время.
Целью данного исследования было изучение побочных явлений КПВТ в зависимости от схемы лечения, сопутствующих заболеваний, влияние на достижение УВО. Для достижения поставленной цели были сформулированы следующие задачи: оценить переносимость КПВТ пациентами с различными схемами терапии, выявить частоту побочных эффектов КПВТ и взаимосвязь их с достижением УВО.
Материалы и методы. В исследование были включены 50 пациентов с установленным диагнозом ХВГС, которые получали КПВТ. Диагноз был подтвержден согласно общепринятым методикам.
Из исследования исключались пациенты с микст-инфекцией (вирусный гепатит В, ВИЧ-инфекция) а так же наличием сопутствующей патологии печени (первичный билиарный цирроз, болезнь Вильсона-Коновалова, синдром Бадда-Киари, гемохроматоз, аутоиммунный гепатит, дефицит альфа-1 антитрипсина) и предшествующего специфического противовирусного лечения по поводу ХВГС, больные с наличием любого из общепринятых противопоказаний для проведения КПВТ.
Продолжительность лечения составила 48 недель для пациентов, инфицированных генотипом 1в вирусного гепатита С или при наличии у больного цирроза печени; 24 недели для пациентов, инфицированных генотипом 2 и 3а. Согласно рекомендациям по ведению пациентов с ХВГС, КПВП включала комбинацию стандартного (Интрон или Альтевир 3 млн МЕ 3 раза в неделю) или пегилированного (ПегИнтрон 120 мкг или Пегасис 180 мкг в неделю) ИФН и рибавирина в дозировке 800-1200 мг в зависимости от массы тела.
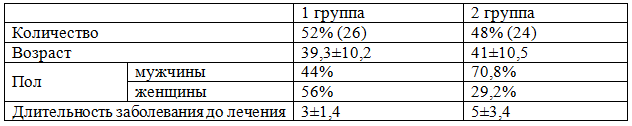
Устойчивый вирусологический ответ (УВО) определялся как отсутствие РНК вируса в сыворотке крови спустя 24 недели после окончания КПВТ. Больные находились под наблюдение в течение терапии на базе Воронежской областной клинической инфекционной больницы и поликлиник Воронежа. Все пациенты были разделены на 2 группы: получающие в составе КПВТ стандартные ИФН – 52,0% (26 человек) или пегилированные ИФН – 48,0% (24 человек). Пациенты были сопоставимы по возрасту и полу: средний возраст составил 40,3 ±10,4, количество мужчин - 57,1%, женщин 42,9%. Распределение по группам показано в табл. 1.
Таблица 1. Характеристика пациентов в исследуемых группах
При анализе полученных результатов использовались описательные методы математической статистики с применением пакета программ Microsoft Excel 2010. Достоверность различий оценивалась методами непараметрической статистики, статистически значимыми считались различия результатов при р≤0,05.
Результаты. При анализе эпидемиологических данных выяснено, что в большинстве случаев (34% случаев) ХВГС выявлен случайно, без клинических проявлений. Одинаковое количество пациентов (по 8 человек - 19,2%) обследовались по поводу диспепсических жалоб и длительного повышения печеночных ферментов. У 30 % пациентов в анамнезе отмечались неоднократные операции или переливание крови; употребление внутривенных наркотиков - у 16% человек. Длительность заболевания до начала противовирусной терапии составила в 1 группе 3±1,4 лет, во 2 группе 5±3,4лет. Степень фиброза по Metavir в среднем составил в 1 группе 1±0,85 балла, во второй группе выше - 1,9±1,5 баллов.
Соотношение генотипов вируса гепатита С, определенных до начала КПВТ, показано в табл. 2.
Таблица 2. Соотношение генотипов вирусного гепатита С
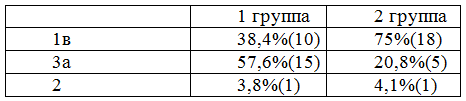
Среди всех пациентов УВО определялся в большинстве случаев - 80,0%, при применении обоих видов терапии, но при этом достоверных различий между группами по этому признаку не выявлено. Эффективность терапии в 1 группе составила 75,1%, во 2 группе - 78,2%. Отсутствие вирусологического ответа в половине случаев связано с отменой препаратов из-за развития выраженных побочных эффектов (прогрессирование неврологической симптоматики с развитием энцефалопатии в 1 группе, длительная некупируемая лихорадка во 2 группе).
Частота побочных эффектов в общей выборке была достаточно высокой - 72,3% среди всех пациентов, при этом в 1 и 2 группе нежелательные явления встречались с одинаковой частотой (69,1% и 73% соответственно).
На протяжении всей терапии у большинства пациентов встречался астеновегетативный синдром в виде выраженной слабости, усталости, нарушения сна, при этом значительно чаще эти проявления отмечали пациенты 2 группы - принимающие пегилированные ИФН (30,7%), что в 2,1 раза чаще, чем во 1 группе (66,6%). Снижение настроения, появление раздражительности, неконтролируемой агрессии при опросе отмечали 23,0% пациентов 1 группы и 25,0% пациентов 2 группы. Данные жалобы чаще встречались на 24±2 неделе терапии. Описанная в литературе депрессия, индуцированная КПВТ, среди данной выборки не встречалась. Для выявления депрессии у всех пациентов применялся опросник Цунга в начале и при завершении КПВТ.
Гриппоподобный синдром, проявляющийся лихорадкой до 38±0,85?С, миалгией, артралгией, выявлен достоверно чаще в у пациентов 1 группы (38,4%), чем у 2 группы (30,1%). Длительность лихорадки составляла в среднем 14±2 недель, первый подъем температуры всегда сопровождал начало КПВТ. Лихорадка купировалась применением препаратов НПВС в стандартных дозировках.
Жалобы со стороны желудочно-кишечного тракта в виде снижения аппетита, тошноты, периодической диареи, боли, вздутия в животе отмечались у 34,6% пациентов 1 группы, что в 2,08 раза чаще, чем во 2 группе (16,6%) .Желтуха на фоне КПВТ встречалась у 2 человек в каждой группе (по 8,3% и 7,6% соответственно).
Снижение веса в среднем на 10,5±5,1 кг, регистрируемое к концу КПВТ, встречалась в 2,3 раза чаще у пациентов 1 группы (19,2%) чем у пациентов среди пациентов 2 группы (8,3%).
Выпадение волос, жалобы на сухость кожи, зуд кожи регистрировались редко: в 1 группе у 2 человек (7,6%среди группы), во 2 группе чаще - у 3 человек(12,5%).
Обострение имеющихся сопутствующих соматических заболеваний встречались в обеих группах приблизительно с одинаковой частотой (30,1% и 27,6% соответственно). Чаще всего встречались обострения хронического панкреатита, язвенной болезни желудка, сахарного диабета.
Частота манифестации впервые выявленных соматических заболеваний на фоне проведения КПВТ имеет прямую корреляционную связь с используемыми препаратами, то есть значительно чаще выявляется при применении ИФН короткого действия, чем пролонгированных форм. При этом в 1 группе на фоне КПВТ манифестировали псориаз (7,6%), аутоиммунный тиреодит (15,3%). А во 2 группе выявлялись гипотиреоз и сахарный диабет (по 4,1% пациентов).
Гематологические осложнения встречались в обеих группах. Анемия, регистрируемая в виде снижения гемоглобина ниже 110г/л, встречалась чаще всего в середине терапии (24±3недели КПВТ). Во второй группе анемия выявлена достоверно чаще – в 2,4раза чаще (38,4%случаев), чем в 1 группе (16% случаев). Эритропоэтин для коррекции анемии применялся в 4 случаях (8%), у остальных коррекции анемии не требовалось.
Среди пациентов обеих групп при наличии анемии УВО встречается в 49,7% случаев, при отсутствии анемии достоверно реже (в 1,35 раз) - у 36,6% пациентов. Таким образом, наличие анемии, в сочетании с другими факторами можно считать предиктором эффективности КПВТ.
Напротив, частота тромбоцитопении на фоне КПВТ коррелировала с отсутствием УВО. Пациенты со снижением уровня тромбоцитов в 1,8 раз реже достигали УВО. Среди всех пациентов тромбоцитопения встречалась только у 8,0% пациентов, что реже, чем по литературным данным. В обеих группах частота данного побочного действия была одинаковой.
Выводы
1. Эффективность терапии с применением препаратов пегилированных или стандартных интерферонов оказалась сходной.
2. Гематологические нежелательные эффекты выявлены достоверно чаще при использовании пегилированных ИФН в составе противовирусной терапии.
3. Гриппоподобный на фоне КПВТ встречались достоверно чаще у пациентов, получающих стандартные ИФН.
4. Астеновегетативный синдром зарегистрирован чаще у пациентов на фоне терапии пегилированными ИФН.
5. Выявлена зависимость между достижением устойчивого вирусологического ответа и величиной снижения уровня гемоглобина.
Список использованных источников:
1. Беляева Н.М., Турьянов М.Х., Рабинович Э.З. Комбинированная терапия гепатита С рибавирином и альфа-интерфероном: Пособие для врачей. - М.: РМАПО. – 2002.
2. Громова Н.И. и Богомолов Б.П. Клиническая эффективность этиотропной терапии хронического вирусного гепатита С// Клин. мед. - 2003.-№1. - С.48.
3. Ивашкин В.Т. Комбинированное лечение хронического гепатита В// Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 1998. №5. С. 57-60.
4. Ferenci P., Fried M., Shiffman M. et al. Predicting sustained virological responses in chronic hepatitis C patients treated with peginterferon alfa-2a// J. Hepatol. – 2005. – Vol. 43. – P. 425–433.
5. Fried M.W. Side effects of therapy of hepatitis C and their management. Hepatology. 2002. - P.237-244
6. Князькина О.В., Каган Ю.Д., Скачков М.В. Микробиоценоз кишечника у больных хроническим вирусным гепатитом С и его лечение// Врач-аспирант, №3.4(52), 2012. – С.579-586.
7. Пирогова И.Ю., Пышкин С.А. Неинвазивная диагностика стадии фиброза у пациентов с хроническими гепатитами В и С// Врач-аспирант, №2(45), 2011. – С. 21-27.
8. Попов С.С., Попов С.Ф. Динамика биохимических показателей гепато-билиарной системы рабочих основных цехов металлургического завода, инфицированных вирусами гемоконтактных гепатитов В и С// Врач-аспирант, №6(55), 2012. – С.55-61.
9. Рихсиева Г.М. Особенности клинико-иммунологических показателей детей, больных острыми вирусными гепатитами А и В, родившихся от матерей, злоупотребляющих алкоголем// Врач-аспирант, №4.4(47), 2011. – С. 675-681.
10. Рюмин А.М., Корочкина О.В., Соболевская О.Л. Закономерности естественного течения хронического гепатита В// Врач-аспирант, №4.1(53), 2012. – С. 214-223.

Автореферат диссертации по медицине на тему Оптимизация прогноза эффективности противовирусной терапии хронического гепатита C
На правах рукописи
ФРЕЗЕ Елена Борнсовна
ОПТИМИЗАЦИЯ ПРОГНОЗА ЭФФЕКТИВНОСТИ ПРОТИВОВИРУСНОЙ ТЕРАПИИ ХРОНИЧЕСКОГО ГЕПАТИТА С
14.01.04 - внутренние болезни
диссертации на соискание ученой степени кандидата медицинских наук
доктор медицинских наук Лисовская Татьяна Валентиновна
Автореферат разослан « 2012 г.
диссертационного совета Гришина Ирина Федоровна
доктор медицинских наук профессор
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Проблема эффективности противовирусной терапии (ПВТ) хронического вирусного гепатита С (ХВГ С) остается актуальной до настоящего времени (Бурневич Э.З. и соавт., 2007; Marcellin Р., 2008; Petta S. et al., 2011; Chevaliez S. et al., 2011). Это связано, прежде всего, с отсутствием желаемых результатов при использовании в комбинированной ПВТ стандартных (короткодействующих) интерферонов-альфа (ИФН-а), которые до сих пор широко применяются в ряде стран, в том числе и в России.
Причиной недостаточной прогностической значимости рутинных предикторов эффективности ПВТ, очевидно, является отсутствие их использования для прогноза результатов ПВТ в совокупности и игнорирование некоторых дополнительных параметров, влияющих на исход терапии.
Максимально раннее выявление лиц с отсутствием ответа и прекращение ПВТ у больных с низкой вероятностью ее успеха, способствовало бы значительному снижению материальных затрат на продолжающееся дорогостоящее лечение и риска возможных серьезных побочных эффектов, включая тяжелые лекарственные реакции на лечение.
Вышеизложенное обусловливает актуальность разработки многофакторной прогностической модели исходов ПВТ короткодействующими ИФН-а и
рибавирином, включающей совокупность наиболее информативных рутинных параметров, а также дополнительные предикторы, влияющие на достижение устойчивого вирусологического ответа (УВО). Оптимизация отбора больных с учетом данных интегрального анализа предикторов эффективности ПВТ является практически важным условием индивидуализации противовирусной терапии ХВГ С и, в конечном счете, повышения ее эффективности.
Цель настоящей работы
Повышение эффективности лечения хронического гепатита С на основе оптимизации отбора больных для противовирусной терапии с использованием интегральной прогностической модели.
1. Провести ретроспективный анализ результатов ПВТ у больных ХВГ С в зависимости от базовых предикторов ее эффективности.
2. Определить наиболее информативные предикторы исходов ПВТ у больных ХВГ С.
3. Разработать с использованием модуля многомерных адаптивных сплайнов (МАР-сплайнов) прогностическую модель результатов ПВТ, включающую не только базовые параметры, но и динамические (в процессе ее проведения).
4. Определить алгоритм применения интегральной прогностической модели и оценить ее эффективность при проведении ПВТ у больных ХВГ С.
5. Провести анализ экономического эффекта от снижения прямых затрат на лекарственное обеспечение больных, отбор которых на ПВТ осуществлялся на основе интегральной прогностической модели.
Уточнена информативность предикторов достижения УВО при проведении ПВТ короткодействующими ИФН-а и рибавирином. Выявлены наибо-
Предложена интегральная прогностическая модель исходов ПВТ короткодействующими ИФН-а и рибавирином, включающая наиболее информативные критерии; доказана эффективность ее использования при отборе больных на ПВТ и в процессе лечения.
Разработан алгоритм применения интегральной прогностической модели при лечении короткодействующими ИФН-а и рибавирином.
Оптимизирован отбор больных на ПВТ с использованием разработанной интегральной прогностической модели, позволяющей определить пациентов, наиболее приверженных к ПВТ короткодействующими ИФН-а, с учетом их индивидуальных параметров.
Определена целесообразность коррекции курса ПВТ (прекращение терапии короткодействующими ИФН-а с возможным переводом на лечение пеги-лированными ИФН-а) с учетом показателей АЛТ и быстрого вирусологического ответа (БВО) к концу 4-й недели лечения, что способствует снижению риска развития побочных эффектов и уменьшению затрат на заранее неэффективное лечение.
Разработан и внедрен в клиническую практику алгоритм действий врача по отбору больных на ПВТ с применением короткодействующих ИФН-а и ее коррекции.
Оптимизация отбора больных на ПВТ, мониторинг лабораторных и вирусологических параметров и коррекция курса терапии после 4-й недели ее проведения позволили добиться увеличения эффективности ПВТ ХВГ С на 23,5%.
Положения, выносимые на защиту:
1. Использование отдельных рутинных предикторов для прогноза результатов ПВТ с применением короткодействующих ИФН-а не является целесообразным в виду их малой информативности.
2. Для повышения качества прогноза результатов комбинированной ПВТ с применением короткодействующих ИФН-а целесообразно использовать интегральную прогностическую модель, включающую наиболее информативные предикторы.
3. Оптимизация отбора больных ХВГ С на лечение короткодействующими ИФН-а и рибавирином с использованием интегральной прогностической модели увеличивает число пациентов, достигших УВО.
4. Отбор больных на ПВТ короткодействующими ИФН-а с учетом интегральных прогностических коэффициентов (К1УВО, К2УВо) позволяет снизить прямые затраты на лекарственное обеспечение данной схемы ПВТ.
Внедрение результатов исследования
Объем и структура диссертации
Работа иллюстрирована 38 рисунками, 19 таблицами, 3 клиническими примерами.
Работа выполнена на клинической базе кафедры внутренних болезней, клинической фармакологии, эндокринологии (зав. кафедрой доктор медицинских наук, профессор О.Г. Смоленская) ГБОУ ВПО УГМА Минздравсоцразви-тия России (ректор доктор медицинских наук, профессор С.М. Кутепов). Лабораторные и инструментальные методы диагностики проведены на базе МАУ Городская клиническая больница №40 г. Екатеринбурга (главный врач А. И. Прудков); фиброэластография печени - на базе Свердловского областного центра по профилактике и лечению ВИЧ-инфекции (главный врач A.C. Подымова). Протокол исследования одобрен локальным комитетом по этике МАУ ГКБ №40(17.12.2009).
Исследование выполнено в два этапа. На первом этапе работы был проведен ретроспективный анализ историй болезни 111-ти пациентов с ХВГ С, получавших противовирусную терапию с использованием короткодействующих ИФН-а и рибавирина в стандартных терапевтических дозировках. Были сформированы две группы больных в зависимости от достижения УВО: пациенты, достигшие УВО, п=63; и пациенты, не достигшие УВО, п=48.
По итогам ретроспективного этапа исследования была разработана интегральная прогностическая модель, включающая наиболее информативные предикторы достижения УВО.
На втором этапе работы в проспективном исследовании проведен анализ эффективности ПВТ у 77-ми пациентов с ХВГ С. При рандомизации с исполь-
Материал и методы исследования
Учитывая, что группы сравнения ретроспективного этапа исследования были рандомизированы исключительно по достижению УВО, основные клини-ко-лабораторные и вирусологические параметры пациентов этих групп (пол, возраст, индекс массы тела (ИМТ), генотип НСУ, вирусная нагрузка (ВН), стадия фиброза (СФ), уровень АЛТ до начала лечения, базовый уровень ферритина сыворотки крови, БВО, уровень АЛТ к концу 4-й недели лечения) - оценивались с точки зрения их влияния на исход ПВТ.
Возраст 77-ми больных двух групп сравнения проспективного этапа исследования составил 30,0 (28,0-33,0) лет (41 или 53,2% - мужчин и 36 или 46,8% - женщин). Группы достоверно не отличались между собой по возрасту и полу, а также по основным клинико-лабораторным параметрам, учитываемым при назначении ПВТ: уровню исходной АЛТ, ВН, вариантов генотипа вируса и СФ (р= от 0,06 до 0,91). Характеристика пациентов групп проспективного этапа исследования представлена в таблице 1.
Характеристика пациентов проспективного этапа исследования
Признаки Первая группа сравнения, п=39 Вторая (основная) группа сравнения, п=38 Достоверность различий, р
Возраст М (25-75), лет 32,0 (30,0-33.0) 29.0 (27,0-32,0) 0.06
Мужчины, п (%) 21 (53,8) 20 (52.6) 1,0
Женщины, п (%) 18 (46.2) 18 (47.4) 1,0
ИМТ, М (25-75), кг/м' 23,0 (20,5-24,5) 23.0 (20.5-27,8) 0.88
Уровень исходной АЛТ М (25-75), МЕ/мл 106,0 (88,0-221,0) 105,0 (59,0-158,0) 0,53
Уровень исходной ВН М (25-75). коп/мл 1,54x103 (1,0хЮ5-2.4ХЮ5) 1,0x10' (1,0х105-2,97х106) 0,59
Распределение по стадиям фиброза, п (%) Р0 Р1 Р2 РЗ 3(7,7) 18(46,2) 10(25,6) 8(20,5) 2(5,3) . 21(55,2) 8(21,1) 7(18.4) 0,91
Критериями включения пациентов в исследование являлись: диагноз ХВГ С, подтвержденный методом иммуноферментного анализа (ИФА) и количественной ПЦР; получение информированного согласия на участие в исследовании; возраст от 18 до 50 лет; выполнение протокола противовирусной терапии (правило 80/80/80).
К критериям исключения относились: наличие цирроза печени (F4-6 баллов по МЕТА VIR); хронический гепатит другой этиологии; микст-вирусная инфекция; ранее проведенная ПВТ в анамнезе; выраженные анемии, нейтро- и тромбоцитопении (Hb 0,6 отмечался у 6-ти чел. (16,7%); К1УВО от
0,4 до 0,6 - у 28 чел. (77,8%). Данным больным была назначена комбинированная ПВТ, включающая короткодействующий ИФН-а2 и рибавирин. Два (5,5%) пациента с заведомо плохим прогнозом ПВТ (К1УВО=0,32 и 0,19 соответственно) были исключены из протокола лечения в связи с предложенным переводом на комбинированную ПВТ с Пег-ИФН-а. Двум пациентам из основной группы ПВТ была прекращена из-за нежелательных явлений, проявившихся на 1-м месяце лечения, и они были исключены из протокола исследования.
Всем пациентам второй группы в конце 4-й недели ПВТ рассчитывался интегральный коэффициент К2УВ0, в формулу которого вошли 3 параметра: показатель базового коэффициента К,, факт наличия или отсутствия БВО и уровень АЛТ на 4-й неделе лечения.
У 3-х (8,3%) пациентов значения К2УВо были 0,5 и продолжили ПВТ. Следует подчеркнуть при этом, у 6-ти из них изначально был благоприятный прогноз (К(УВ0 >0,6), и всем этим пациентам был подтвержден благоприятный прогноз достижения УВО при расчете К2УВ0. У 25-ти же чел., продолживших ПВТ после 4-й недели, значения К1УВ0 трактовались как сомнительные (от 0,4 до 0,6), что подтверждает особую значимость анализа лабораторных и вирусологических параметров на 4-й неделе ПВТ и расчета динамического коэффициента К2УВо для данной категории больных.
Устойчивый ответ на лечение во второй группе сравнения был отмечен у 29 из 36-ти, получивших курс ПВТ пациентов, то есть эффективность лечения составила 80,6% и была на 23,5% выше таковой в первой группе сравнения, р=0,04 (рис. 3). При этом, эффективность ПВТ для пациентов даже с первым
100% 90% 80% 70%-60%-50%-40% 30% 20%-10%-0%
конец 4-й нед., р=0,02
конец 12-й нед., р=0,43
окончание ПВТ р=0.12
24 нед. после ПВТ, р=0,04
□ первая (контрольная)группа □ вторая(основная)группа
Рис. 3. Сравнительный анализ эффективности ПВТ (по данным вирусологического мониторинга) у больных ХВГ С, % (р - достоверность различий между группами)
Пациенты, не ответившие на ПВТ (7 чел. или 19,4%), были представлены двумя больными с исходно неблагоприятным прогнозом (К1УВО 0,5, продолжившими курс лечения, но не достигшими УВО.
Интегральная прогностическая модель эффективности ПВТ имела значительную чувствительность - 100%, и специфичность - 71,4%. Диагностическая эффективность прогностической модели составила 85,7%.
Оптимизация отбора больных на ПВТ ХВГ С позволила значительно снизить прямые финансовые потери на лекарственное обеспечение в основной группе проспективного исследования - на 2093=80 рублей на одного человека ежемесячно. Учитывая, что курсовая длительность лечения пациентов с первым
первый генотип "не первый" генотип
ЕЗ первая группа И вторая (основная) группа
Рис. 4. Курсовая стоимость лечения одного пациента с учетом вирусного генотипа
Проведенное рандомизированное проспективное контролируемое открытое исследование свидетельствует о достоверной эффективности интегральной прогностической модели при отборе больных на ПВТ стандартным ИФН-а и рибавирином по сравнению с рутинными предикторами. Это подтверждается значительно более высоким процентом достижения УВО в группе пациентов, для которых были рассчитаны К,у.во и К2УВо, а также экономическим эффектом от снижения прямых затрат на лекарственные препараты данной схемы ПВТ.
Читайте также:


