Что обуславливает устойчивость микобактерий туберкулеза

Республика Саха (Якутия) представляет собой крупный субъект Российской Федерации и занимает 1/5 ее территории. Большей частью она лежит в зоне многолетней мерзлоты, что накладывает своеобразный отпечаток на всю природу Якутии и, следовательно, на технологии ведения животноводческой отрасли. Несмотря на экстремальные природно-климатические условия, сельское хозяйство Республики Саха (Якутия) специализируется главным образом на производстве продуктов животноводства. Скотоводство - ведущая отрасль сельского хозяйства республики. Однако негативное влияние многих экологических факторов на развитие животноводства создает благоприятные условия для возникновения инфекционных болезней, в том числе туберкулеза крупного рогатого скота. В настоящее время Республика Саха (Якутия) оздоровлена от этой инфекции, однако имеет место повторное возникновение заболевания в благополучных хозяйствах. При туберкулезе основным источником инфекции являются больные животные, выделяющие возбудителя во внешнюю среду. Среди факторов сохранения и передачи возбудителя туберкулеза животным почва и навоз занимают ведущее место.
Все почвы Якутии относятся к мерзлотным, изучение выживаемости возбудителя туберкулеза бычьего и птичьего видов проводили на почвах, типичных для животноводческих районов Якутии по содержанию микроэлементов, гумуса, степени засоленности и глубины сезонного протаивания. Опыты проводили в течение 6 лет в условиях, максимально приближенными к естественным. Выживаемость возбудителя туберкулеза изучали на поверхности почвы, глубине 5, 10 и 20 см. Нашими исследованиями установлено, что возбудитель туберкулеза в мерзлотных почвах проявляет значительную устойчивость к воздействию неблагоприятных факторов. Так, подвергаясь многократному замерзанию и оттаиванию, он сохраняет жизнеспособность на поверхности почвы 12 мес, глубине 5 см - 27 мес и глубине 10-20 см - 60 мес. Микобактерии туберкулеза проникают с инфицированной поверхности почвы под влиянием осадков и биологических процессов в нижележащие слои и механически выносятся произрастающими растениями. Миграция микобактерий с поверхностных слоев почвы в глубьлежащие носит сезонный характер, что связано со спецификой солевого режима мерзлотных почв.
Нами изучена выживаемость возбудителя туберкулеза в навозе при технологии складирования, осуществляемой в хозяйствах республики. В Якутии распространен бесподстилочный метод содержания животных. При такой технологии содержания животных навоз, имеет высокое содержание влаги. Типовые навозохранилища отсутствуют и навоз используется в качестве удобрений без обеззараживания и переработки, так как из-за природно-климатических условий биотермический метод обеззараживания навоза не приемлем.
Результаты исследований показали, что в условиях Якутии возбудитель туберкулеза бычьего вида сохраняет жизнеспособность в навозе 48 мес, а птичьего -24 мес. В течение длительного выживания в почве и навозе возбудитель туберкулеза изменяет свои культуральные и морфологические свойства.
Полученные данные показывают, что сроки сохранения жизнеспособности и патогенных свойств возбудителя туберкулеза на объектах внешней среды (почва и навоз) в экстремальных условиях Якутии значительно дольше, чем в других регионах России, и этому способствует специфика ведения животноводства и природно-климатические условия. При загрязнении почвы возбудителем туберкулеза не исключается возможность распространения его в окружающей среде.
В этой связи обеззараживание почвы и навоза в отношении патогенных для животных бактерий, в том числе возбудителя туберкулеза, является актуальной. Трудность разрешения этой проблемы обусловливается чрезвычайной устойчивостью микобактерий туберкулеза к физическим и химическим факторам, разным климатическим и почвенным условиям, что ограничивает выбор дезинфицирующих свойств. При обеззараживании глубоких слоев почвы нецелесообразно применять растворы дезинфицирующих средств, так как это практически трудно выполнимо и при этом расходуется большее количество дезинфектантов. Мы изучили природные цеолиты в качестве пролонгатора действия активного вещества сухой хлорной извести. Было показано, что природные цеолиты - хонгурин (месторождение Якутского Хонгуруу) при включении их в сухую хлорную известь повышают бактерицидную активность ее по отношению к патогенным возбудителям туберкулеза в два раза. Полученные результаты дали возможность применить природные цеолиты в смеси с сухой хлорной известью для дезинфекции почвы при туберкулезе крупного рогатого скота.
Таким образом, метод биологического обеззараживания навоза является экологически безопасным и естественным в условиях экстремального климата Якутии.
Патогенные микобактерии - Ф. К. Черкес
Глава 33. Возбудители туберкулеза
Представители семейства микобактерий Mycobacteriaceae имеют вид тонких, иногда ветвистых палочек, чем напоминают гриб. Медленный рост на питательных средах также сближает их с грибами. Эти особенности объясняют название семейства, рода - Mycobacterium.
Микобактерий кислото-щелоче- и спиртоустойчивы, что обусловливается наличием в оболочках их клеток жировосковых веществ.
Род микобактерий включает патогенных и непатогенных представителей. Патогенными для человека являются возбудители туберкулеза и возбудитель лепры.
Туберкулез широко распространен среди животных, птиц, грызунов.
Существуют несколько видов туберкулезных палочек:
1. Человеческий - Mycobacterium tuberculosis
2. Бычий - Mycobacterium bovis
3. Птичий - Mycobacterium avium
4. Мышиный - Mycobacterium murium
5. Встречаются микобактерий, вызывающие заболевания у холоднокровных. К ним относится особая группа атипичных микобактерий.
В настоящее время атипичные микобактерий приобретают особое значение. Их делят по ряду признаков на 4 группы: I, II, III, IV (по Раньону). Они отличаются от микобактерий туберкулеза меньшей требовательностью к питательным средам. Между собой они различаются по отношению к питательным средам, скорости роста, по способности образовывать пигмент, а также по каталазной и пероксидазной активности. Вызывают заболевания у человека представители групп I и III.
Морфология. Возбудители туберкулеза были открыты р. Кохом в 1882 г. Это тонкие палочки величиной 1,5-4 × 0,3-0,5 мкм. Они очень полиморфны: встречаются прямые, изогнутые, колбовидные. Как результат изменчивости бактерий, имеются кислотоподатливые формы и очень мелкие, так называемые зерна Муха. Разнообразие форм нередко зависит от состава среды, воздействия на них антибиотиков и химиотерапевтических средств. Бактерии туберкулеза неподвижны, не имеют спор и капсул. Грамоположительны, однако они плохо воспринимают анилиновые краски. Хорошо окрашиваются в красный цвет по методу Циля- Нильсена (см. рис. 4), где используются концентрированные краски и протравливание.
Культивирование. Возбудители туберкулеза - аэробы. Растут при температуре 37-38° С и рН среды 5,8-7,0, Отличительными культуральными особенностями туберкулезной палочки являются медленный рост и требовательность к питательным средам. Первично они растут только на специальных средах: среде Петраньяни, Петрова, Левенштейна - Йенсена. Их можно выращивать на глицериновом бульоне, глицериновом агаре, глицериновом картофеле. Глицерин стимулирует рост микобактерий. М. bovis не нуждаются в глицерине. Наибольшее распространение получила среда Левенштейна - Йенсена, которая рекомендована ВОЗ в качестве стандартной среды для выращивания туберкулезных палочек. В настоящее время пользуются также средой Финна II, которая отличается от среды Левенштейна - Йенсена тем, что вместо аспарагина в ней используется глутамин натрия. На этой среде микобактерий туберкулезарастут несколько быстрее, чем на среде Левенштейна - Йенсена, и процент выделения культур выше. Туберкулезные палочки можно культивировать и на синтетических средах, например среде Сотона.
Микобактерий туберкулеза встречаются в R- и S-форме. Более вирулентной является R-форма (М. bovis чаще встречается в R-форме). На плотных питательных средах возбудители туберкулеза образуют сухие морщинистые колонии кремового цвета с чуть приподнятым Центром и изрезанными краями (см. рис. 26). В жидких питательных средах микобактерий туберкулеза вырастают на 10-15-й день в виде пленки, которая постепенно утолщается, становится грубой, морщинистой, ломкой и в силу тяжести иногда падает на дно. Бульон под пленкой остается прозрачным.
Ферментативные свойства. Возбудители туберкулеза биохимически мало активны. У них обнаружен протеолитический фермент, который в определенных условиях (кислая и щелочная среда) расщепляет белок. Они расщепляют также некоторые углеводы, образуют уреазу. Но свойства эти непостоянны. Поэтому изучение ферментов не имеет диагностического значения.
Токсинообразование. Возбудители туберкулеза образуют эндотоксин - это белковое вещество впервые выделил Р. Кох (1890) и назвал его туберкулином. "Старый" туберкулин - это культуральная жидкость, полученная при росте культуры в глицериновом бульоне и выпаренная при 70° С до 1 /10 своего первоначального объема. "Новый" туберкулин - очищенный белковый дериват туберкулина.
Туберкулин обладает свойствами аллергена. Он не оказывает токсического действия на здоровый организм. Его действие проявляется только в зараженном организме. Поэтому введение туберкулина используют с диагностической целью, в постановках аллергических проб (Пирке или Манту). Для этой цели туберкулин готовят из бычьего типа микобактерий туберкулеза.
Вирулентные штаммы возбудителей туберкулеза содержат особый липид корд-фактор, который способствует склеиванию микобактерий и росту их в виде кос и тяжей.
Антигенная структура. Микобактерий туберкулеза содержат антиген, в который входят белковые, липоидные и полисахаридные факторы. Этот антиген вызывает в организме выработку антител (агглютининов, преципитинов, комплементсвязывающих веществ и др.). Однако эти антитела обнаруживаются в малых концентрациях, поэтому практически с целью диагностики мало используются.
Устойчивость к факторам окружающей среды. Микобактерий туберкулеза самые устойчивые из неспороносных форм бактерий (устойчивость обусловливается наличием в их оболочке липидов). Температуру 100° С они переносят в течение 5 мин. УФ-лучи вызывают их гибель только через несколько часов.
В высохшей мокроте они живут до 10 мес. При низких температурах микобактерий туберкулеза длительно сохраняются.
Дезинфицирующие растворы: сулема (1:1000), карболовая кислота (5%) губят их только через сутки. Наиболее чувствительны они к хлорамину и хлорной извести.
Восприимчивость животных. К М. tuberculosis человек очень чувствителен, животные и птицы малочувствительны. Из экспериментальных животных к нему высокочувствительны морские свинки, у которых инфекция протекает генерализованно и заканчивается обычно гибелью животного.
К M. bovis чувствительны крупный и мелкий домашний скот и домашние животные (человек малочувствителен, но дети могут заражаться при использовании молока больных животных).
Из экспериментальных животных наиболее чувствительны кролики, у которых инфекция протекает генерализованно. М. avium вызывает заболевание у птиц: кур, голубей, фазанов и т. д. Однако могут болеть и некоторые животные (человек редко заражается).
Из экспериментальных животных чувствительны кролики. Инфекция протекает у них остро.
Мышиный вид патогенен главным образом для полевок. У кроликов и морских свинок заболевание протекает в хронической форме.
Источники инфекции. Человек. Реже животные.
Пути передачи. Наиболее частые пути передачи - воздушно-капельный и воздушно-пылевой; реже пищевой. Возможно внутриутробное инфицирование через плаценту.
Заболевания у человека и патогенез. Заболевание туберкулезом характеризуется многообразием клинических форм. Различают легочную (наиболее часто встречающуюся) и внелегочные формы: туберкулез желудка и кишечника, почек, мозговых оболочек, костей и других органов.
Каждая из этих форм может закончиться генерализацией процесса. При воздушно-капельном и воздушно-пылевом заражении первичный очаг возникает в легком. В пораженном органе образуется бугорок - tubercul. Бугорок представляет собой скопление лейкоцитов и гигантских клеток, внутри которых находятся микобактерий туберкулеза. При хорошей сопротивляемости организма соединительная ткань окружает бугорок, он обызвествляется и бактерии, оставаясь жизнеспособными, не выходят за пределы бугорка. Таков "очаг Гона" - обызвествленный, небольшой очаг на месте первичного внедрения туберкулезной палочки (закрытый процесс).
При закрытом процессе палочки туберкулеза не выделяются с мокротой, мочой и др.
Таким образом, даже при доброкачественном течении процесса организм не освобождается от возбудителей туберкулеза. Считают, что 80% людей инфицированы туберкулезными бактериями. Однако клинически они здоровы. Когда организм попадает в неблагоприятные условия, защитные функции его снижаются, бугорок подвергается некрозу, бактерии высвобождаются и вовлекают в процесс новые участки, наступает обострение, образуются каверны - открытый процесс. Иногда может быть генерализация процесса, которая приводит организм к гибели. Чаще туберкулез протекает в хронической форме (закрытый процесс). Большое значение при обострении имеют условия труда и быта.
Иммунитет. Человек обладает определенной резистентностью, т. е. при заражении не всегда возникает заболевание, а образуется инфекционный (нестерильный) иммунитет, который обусловливается комплексом защитных факторов: гуморальных, клеточных, а также резистентностью органов и тканей.
Профилактика. Ранняя диагностика, изоляция и т. д. Для специфической профилактики используется живая вакцина БЦЖ (BCG), полученная французскими учеными Кальметтом и Гереном. Эту вакцину вводят новорожденным однократно, внутрикожно в наружную поверхность плеча. Ревакцинацию проводят через 7-12 лет, а затем через каждые 5-6 лет до 30 лет.
Лечение. Антибактериальные препараты: стрептомицин, рифампицин, ПАСК, фтивазид и др.
1. Кем и когда был открыт возбудитель туберкулеза?
2. На какие типы делится туберкулезная палочка? Какой тип патогенен для человека?
3. Что обусловливает устойчивость микобактерий туберкулеза?
4. Каким методом окрашивают мазки для обнаружения туберкулезных микобактерий?
5. На какие формы диссоциируют микобактерий туберкулеза и какая форма является патогенной?
Цель исследования: выявление возбудителя.
1. Мокрота (туберкулез легких и бронхов).
2. Экссудат из плевральной полости (туберкулез легких, плевры).
3. Асцитическая жидкость и кал (кишечная форма туберкулеза).
4. Моча (туберкулез почек).
5. Спинномозговая жидкость (туберкулезный менингит).
6. Кровь (генерализация процесса).

Способы сбора материала
Примечание. Баночки для сбора материала должны быть с завинчивающимися пробками. Посуду для сбора материала стерилизуют в автоклаве при 120° С в течение 20 мин или кипячением в течение 1 ч.

Ход исследования
1. На каких питательных средах выращивают микобактерии туберкулеза и какова длительность их роста?
2. Чем и для чего обрабатывают мокроту до посева ее на питательные среды?
3. Опишите рост туберкулезной палочки на плотной и жидкой питательных средах.
4. Какое животное является наиболее чувствительным к человеческому типу туберкулезной палочки?
Среда Левенштейна - Йенсена: солевой раствор; однозамещенный фосфат калия - 2,4 г; магния сульфат - 0,24 г; магния цитрат 10,6 г; аспарагин - 3,6 г; глицерин - 12 мл; картофельная мука - 5 г; вода дистиллированная - 600 мл.
Реактивы растворяют в указанной последовательности при слабом подогреве и стерилизуют 2 ч текучим паром. Солевая основа может быть приготовлена с запасом на 3-4 нед.
Яичная масса. 24-27 (в зависимости от величины) свежих диетических яиц моют проточной теплой водой, щеткой с мылом, погружают на 30 мин в 70% спирт, затем над спиртовкой в боксе разбивают стерильным пинцетом в колбу с бусами, хорошо размешивают и к 1 л яичной массы добавляют 600 мл солевого раствора. Смесь фильтруют через марлевый фильтр, добавляют 20 мл стерильного 2% раствора малахитового зеленого и разливают в пробирки по 5 мл. Свертывание производят при 85° С в течение 45 мин.
Среда Финна II. Солевая основа: магния сульфат - 0,5 г; натрия цитрат - 1 г; квасцы железоаммиачные - 0,05 г; калия фосфат однозамещенный - 20 г; аммония цитрат однозамещенный - 20 г; натрия глутамат однозамещенный - 5 г; глицерин - 20 мл; вода дистиллированная - до 1 л.
Ингредиенты растворяют в указанном порядке в теплой дистиллированной воде. Устанавливают рН 6,3-6,5. Стерилизуют при 1 атм 20 мин.
Яичная среда. 12 яиц моют щеткой с мылом, обрабатывают спиртом. Разбивают стерильным пинцетом и выливают в стерильную колбу с бусами, которую после добавления каждого яйца встряхивают до образования однородной массы. Добавляют 10 мл 20% водного раствора малахитового зеленого и 300 мл солевого раствора. Фильтруют через марлевый фильтр и свертывают при температуре 85° С в течение 30 мин.
Синтетическая среда Сотона. К 200 мл дистиллированной воды добавляют 4 г аспарагина, 0,5 г цитрата железа, 2 г лимонной кислоты, 0,5 г сульфата магния, 0,5 г основного фосфата калия, 60 г глицерина, 800 мл дистиллированной воды.
Клинический ординатор 1-ого года обучения
Абасов Тарлан Мамед Рагим оглы
Лекарственная резистентность МБТ……………………………………. 3
Механизм и динамика формирования лекарственной устойчивости… 4
Методы диагностики лекарственной устойчивости…………………… 8
Профилактика развития лекарственной устойчивости……………….. 22
Лекарственная резистентность МБТ.
Появление множественной лекарственной устойчивости микобактерий туберкулеза стало серьезной угрозой эффективности противотуберкулезных программ во многих странах мира. В Российской Федерации распространение микобактерий, устойчивых к основным противотуберкулезным препаратам, является одной из главных проблем фтизиатрической службы. В 2007 г в Российской Федерации у 13% больных с вновь выявленным туберкулезом до лечения была диагностирована множественная лекарственная устойчивость микобактерий. Приобретенная множественная лекарственная устойчивость в ряде регионов страны достигает 50-60% среди повторных случаев лечения туберкулеза. Излечение больных туберкулезом является главным компонентом национальной противотуберкулезной программы. Больной, который излечивается от туберкулеза, обрывает цепочку передачи инфекции. В тех случаях, когда пациенты не получают необходимого лечения и продолжают выделять микобактерий туберкулеза, происходит распространение инфекции в обществе в течение нескольких лет. У большинства больных туберкулезом можно достигнуть излечения, несмотря на наличие лекарственной устойчивости микобактерий туберкулеза (МБТ), сопутствующих заболеваний и развития побочных эффектов от приема лекарственных средств. Своевременно диагностированные больные с МБТ, чувствительными к основным противотуберкулезным препаратам, получают лечение в течение не менее 6 месяцев и практически всегда излечиваются от туберкулеза. Наиболее сложная ситуация возникает, когда у МБТ определяется устойчивость к основным противотуберкулезным препаратам. Больные с множественной лекарственной устойчивостью (МЛУ) микобактерий туберкулеза - те, у которых диагностирована устойчивость МБТ к действию изониазида и рифампицина одновременно, с наличием или без наличия устойчивости к любым другим противотуберкулезным препаратам. Организация диагностики и лечения больных с множественной лекарственной устойчивостью МБТ требует значительных финансовых затрат в лабораторной диагностике, организации специализированного отделения для лечения данной категории больных, покупке противотуберкулезных препаратов второго ряда и лекарственных средств, для купирования побочных эффектов. Больные туберкулезом, выделяющие лекарственно-устойчивые штаммы МБТ, длительное время остаются бактериовыделителями и могут заражать окружающих лекарственно-резистентными возбудителями. Чем больше число больных, выделяющих лекарственно-устойчивые МБТ, тем выше риск распространения инфекции среди здоровых лиц и появления новых случаев заболевания туберкулезом с первичной лекарственной устойчивостью. По определению экспертов ВОЗ, лекарственно-устойчивый туберкулез – это случай туберкулеза легких с выделением МБТ, устойчивых к одному и более противотуберкулезным препаратам. В последние годы в связи с ухудшением эпидемической ситуации существенно увеличилось число больных, выделяющих МБТ, устойчивые к основным противотуберкулезным препаратам. По данным ЦНИИ туберкулеза РАМН в 2008г. у 50% впервые выявленных и ранее не леченных противотуберкулезными препаратами больных в мокроте определялись лекарственно-устойчивые МБТ, из них у 27,7% имелась устойчивость к 2 основным противотуберкулезным препаратам – изониазиду и рифампицину. При хроническом фиброзно-кавернозном туберкулезе частота выявления лекарственно-устойчивых МБТ возрастает до 95,5%. Феномен лекарственной устойчивости МБТ имеет важное клиническое значение. Существует тесная взаимосвязь количественных изменений микобактериальной популяции и изменения ряда биологических свойств МБТ, одним из которых является лекарственная устойчивость. В активно размножающейся бактериальной популяции всегда имеется некоторое количество лекарственно-устойчивых мутантов, которые практического значения не имеют, но по мере сокращения бактериальной популяции под влиянием химиотерапии изменяется соотношение между количеством лекарственно-чувствительных и устойчивых МБТ. В этих условиях происходит размножение главным образом устойчивых МБТ, эта часть бактериальной популяции увеличивается. В клинической практике необходимо исследовать лекарственную чувствительность МБТ и результаты этого исследования сопоставлять с динамикой туберкулезного процесса в легких.
Механизм и динамика формирования лекарственной устойчивости .
Развитие лекарственной устойчивости у МБТ является результатом случайных генетических мутаций. В любой достаточно большой популяции МБТ существуют возникшие естественным путем микобактерии-мутанты. Подвижного фактора устойчивости, подобного плазмидам грамотрицательных палочек, в данном случае нет. Мутации не связаны между собой и происходят с низкой, но предсказуемой частотой в пределах 1-2 делений на 106- 108 МБТ. В Таблице 1 показаны коэффициенты и распространенность мутаций, обусловливающих устойчивость к четырем противотуберкулезным препаратам первого ряда.
Таблица 1. Коэффициенты и распространенность мутаций
Изобретение относится к медицине, а именно к фтизиатрии, и может быть использовано для прогнозирования риска развития приобретенной лекарственной устойчивости микобактерий туберкулеза (МБТ) к фторхинолонам (ФХ) в ходе лечения больных туберкулезом с множественной лекарственной устойчивостью возбудителя (МЛУ-ТБ).
Лечение МЛУ-ТБ является одной из основных проблем общественного здравоохранения в мире [1]. Ресурс этиотропной терапии МЛУ-ТБ ограничен 6-7 резервными противотуберкулезными препаратами (ПТП), которые необходимо применять комбинировано 3. Среди них наибольшей клинической эффективностью обладают препараты группы фторхинолонов, благодаря высокой антимикобактериальной активности и относительно низкой токсичности [3; 5; 6]. Формирование приобретенной устойчивости микобактерий туберкулеза к фторхинолонам приводит к увеличению случаев неблагоприятных исходов лечения, в том числе летальных, формированию хронических форм МЛУ-ТБ, в том числе с бактериовыделением, дальнейшей амплификации лекарственной устойчивости МБТ, что приводит к распространению ТБ с множественной и широкой лекарственной устойчивостью возбудителя [7; 8]. Прогнозирование риска формирования фторхинолон-устойчивости МБТ в ходе лечения больных МЛУ-ТБ или при отсутствии лабораторных данных может помочь врачу-фтизиатру в выборе тактики и организационных форм лечения для ее предупреждения.
Известен способ прогнозирования риска развития лекарственно-устойчивого туберкулеза [9], заключающийся в следующем. В первые 3-5 дней после поступления больного в стационар в качестве факторов риска при балльной оценке определяют: бактериовыделение, клиническую форму туберкулеза, распространенность туберкулезного процесса в легких, категорию, контакт с больным туберкулезом, злоупотребление алкоголем, социальный статус пациента, пол, возраст, табакокурение, давность флюорографического обследования, тип структуропостроения фракций сыворотки крови, совокупность патологических маркеров некробиоза во фракциях сыворотки крови. Подсчитывают сумму баллов, и при сумме баллов 1-7 вероятность развития лекарственно-устойчивого ТБ оценивается как низкая, 8-12 - умеренная, 13-19 - высокая. Недостатками способа являются использование как прогностических факторов, лишь опосредованно связанных с формированием лекарственной устойчивости МБТ, балльные градации вероятности являются эмпирическими, что обусловливает невысокую точность и информативность прогноза.
Известен способ прогнозирования [10], представляющий собой экспресс-диагностические таблицы, в которые включены основные взаимосвязанные клинического и социального характера, опосредовано указывающие на вероятность развития лекарственно-устойчивого туберкулеза легких, основанный на методе неоднородной последовательной статистической процедуры распознавания (последовательный анализ Вальда) и заключающийся в последовательном вычислении значений диагностического коэффициента и показателя информативности для категорий включенных прогностических признаков и последующем сравнении полученных значений с контрольными таблицами. Недостатком метода является необходимость сложных математических вычислений данных показателей, что делает его неудобным для применения в повседневной врачебной практике.
Основным свойством вышеописанных способов является то, что разработаны они по результатам статистической и математической обработки данных, полученных в исследованиях факторов риска лекарственной устойчивости МБТ к ПТП 1 ряда, и не имеют оснований быть использованными для прогнозирования лекарственной устойчивости МБТ к резервным ПТП в условиях лечения уже имеющейся МЛУ МБТ.
Наиболее близким аналогом предлагаемому способу является способ прогнозирования, описанный в работе Д.А. Чичеватова, в котором для построения прогностической модели используют методы бинарной логистической регрессии и категориальной регрессии (регрессии с оптимальным шкалированием) [11]. Но данный способ не относится к области фтизиатрии. Кроме того, отбор предикторов в данную модель осуществлен по результатам анализа таблиц сопряженности и рангового критерия Kruskal-Wallis при сравнении двух выборок, различающихся по значению бинарной зависимой переменной.
Нами предлагается отбор предикторов по результатам вероятностной оценки связи потенциальных предикторов с зависимой переменной (формирование приобретенной фторхинолон-резистентности МБТ) путем вычисления показателя отношения шансов в однофакторном анализе и по результатам многофакторного анализа методом бинарной логистической регрессии, что позволяет получить приемлемую точность прогноза и приемлемое качество предлагаемой прогностической модели в целом (коэффициент детерминации R 2 =0,325). Другим отличительным признаком предлагаемого способа прогнозирования является то, что для оценки риска имеется возможность как вычисления точного значения вероятности формирования приобретенной фторхинолон-устойчивости МБТ, так и ее интервальная оценка. Таким образом, разработка способа прогнозирования приобретенной лекарственной устойчивости микобактерий туберкулеза к препаратам группы фторхинолонов у больных МЛУ-ТБ представляет собой новое техническое решение. Предлагаемый способ прогнозирования может применяться в рутинной клинической практике врача-фтизиатра, отличается приемлемой долей корректно предсказанных значений - 83,4%, простотой в использовании, быстрым получением результата без использования вычислительной техники.
Предлагаемый способ прогнозирования представляет собой балльную шкалу оценки риска и разработан на основе выявления факторов риска формирования приобретенной фторхинолон-устойчивости МБТ в ходе лечения больных МЛУ-ТБ при ретроспективном анализе двух групп пациентов: 1 группа (основная, 115 человек) - пациенты, у которых в процессе лечения сформировалась устойчивость МБТ к фторхинолонам, 2 группа (сравнения, 348 человек) - пациенты, у которых формирование приобретенной фторхинолон-устойчивости МБТ не наступило. В качестве факторов риска рассматривали клинические, микробиологические, социально-демографические параметры пациентов и факторы, связанные с лечением. Для их количественной оценки проведены:
1) однофакторный анализ путем расчета статистического показателя отношения шансов (OR-odds ratio) и его 95% доверительного интервала соответственно по формулам:
OR=(a×d)/(b×c), где a - число лиц с наличием, b - отсутствием фактора риска среди пациентов с приобретенной фторхинолон-устойчивостью МБТ, c и d - число лиц соответственно с наличием и отсутствием фактора риска среди пациентов без приобретенной фторхинолон-резистентности МБТ;
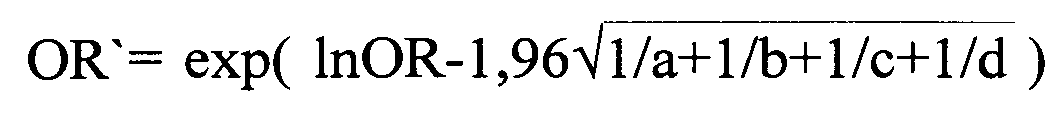
- нижняя граница доверительного интервала;

- верхняя граница доверительного интервала.
При OR>1 каждый из рассмотренных факторов оценивался как фактор повышенного риска, при OR ® SPSS ® Statistics ver. 20.0.
В результате анализа были выявлены факторы со статистической значимостью, связанные с риском формирования приобретенной устойчивости МБТ к фторхинолонам, представленные в таблице 1.
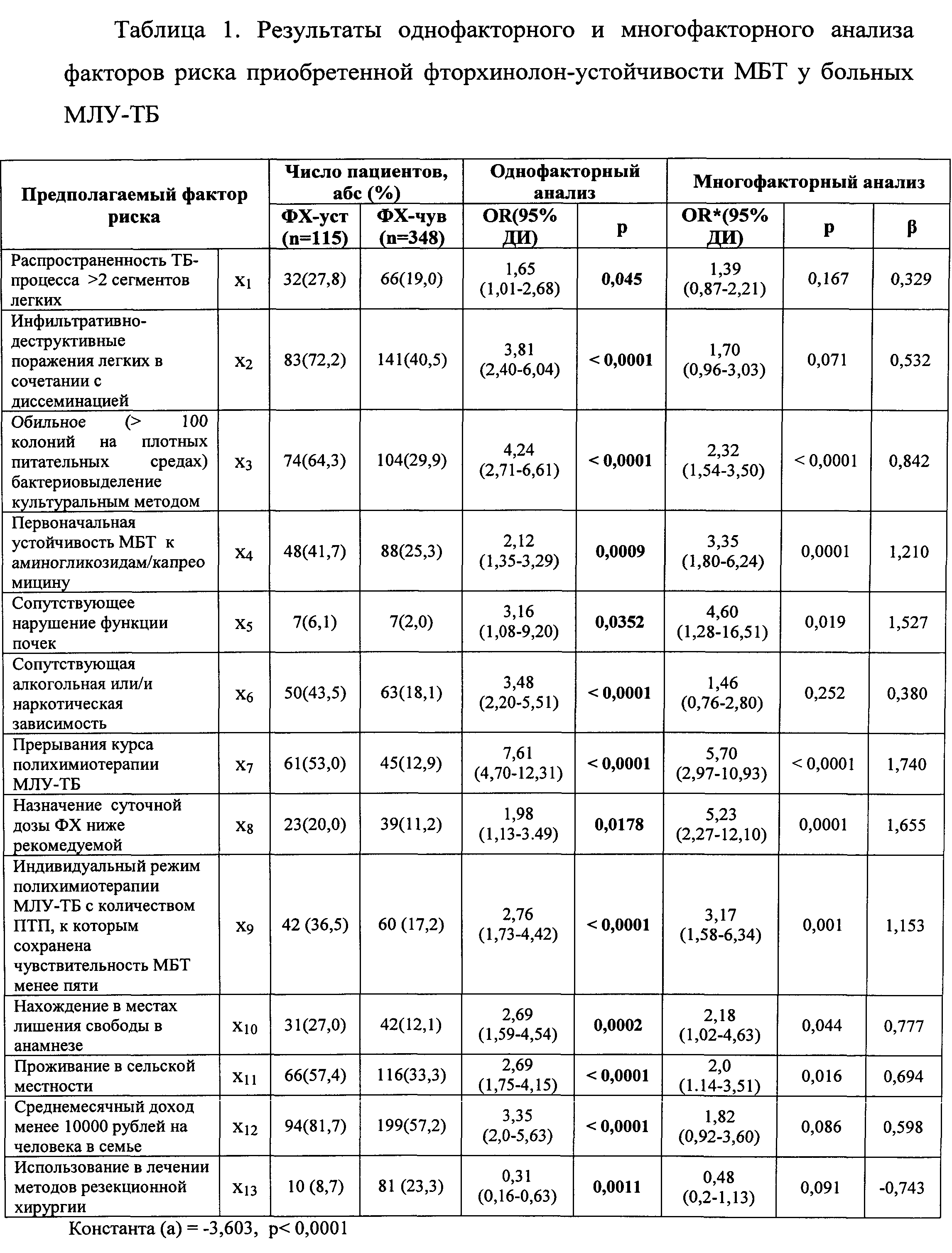
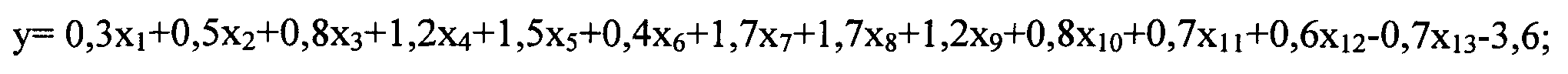
Параметры регрессионной модели: χ 2 =193,83, р 2 =5,66, р=0,685;
- общий процент корректно предсказанных - 85,1.
Далее для создания балльной шкалы были отобраны предикторы, связь которых с приобретенной фторхинолон-устойчивостью МБТ имела статистическую значимость p 2 =0,325, F=24,2, p 2 =134,9, р 2 =8,9, р=0,351;
- общий процент корректно предсказанных - 83,4.
Вероятность приобретенной фторхинолон-устойчивости МБТ рассчитывают по формуле:
е - основание натурального логарифма, константа, равная 2,718…,
x - абсолютное значение суммарного балла.
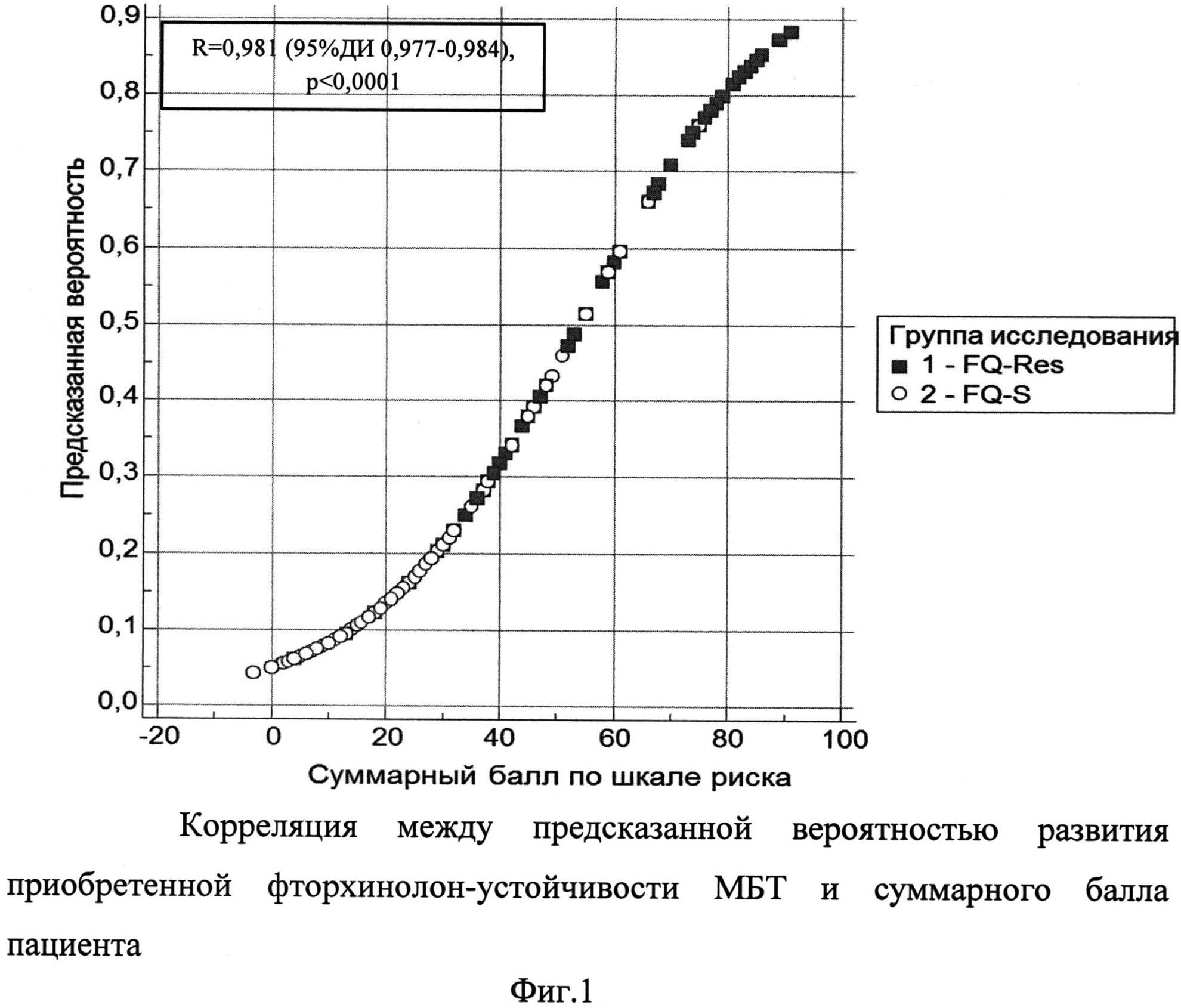
Зависимость значений рассчитанной вероятности и суммарного балла для пациентов групп сравнения представлена на фиг. 1.
Высокий коэффициент корреляции между значениями суммарного балла и вероятности вторичной ФХ-резистентности МБТ позволяют использовать данную шкалу для оценки степени риска. В пользу этого также свидетельствует высокозначимое различие значения среднего суммарного балла в группах сравнения: в первой - 20,03(95% ДИ 18,04-22,0); во второй - 51,0 (95% ДИ 46,2-55,8), Mann-Whitney U-test=33155,5 p 0,2-0,5), при 50-70 баллах - высокая (р>0,5-0,7), при >70 баллов - очень высокая (р>0,7-0,9), либо путем вычисления точного значения вероятности по формуле:p=1/1+e, гдее - основание натурального логарифма, константа, равная 2,718…,х - абсолютное значение суммарного балла.
Читайте также:


