| Комментарии: 1 |
В середине 40-х годов группа молодых американских учёных, интересовавшихся природой гена, решила сконцентрировать усилия на работе с кишечной палочкой и её фагами. И тогда оказалось, что генетика у бактерий есть, да ещё какая! Перед исследователями открылось великое разнообразие природных генетических процессов, которые потом обнаружили и у более сложно устроенных эукариот. Короче говоря, практически всю молекулярную генетику сделали на кишечной палочке и её фагах. Подробнее об этом не стоит, ибо, как сказал Козьма Прутков, никто не обнимет необъятного. Желающие могут раскрыть любой учебник молекулярной генетики: почти на каждой странице кишечная палочка будет помянута в связи с каким-нибудь экспериментом. А мы поговорим о самой бактерии.
![]()
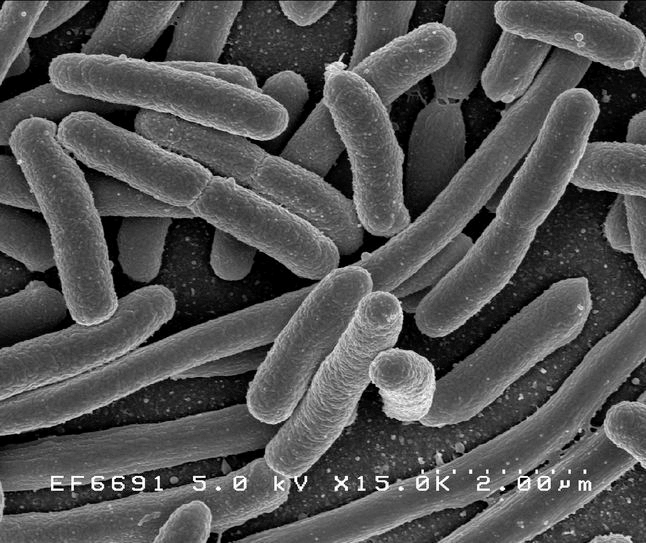
Пожалуй, это самая изученная клетка на планете. Её латинское название Escherichia coli (E.coli) в переводе означает эшерихия кишечная и связано с местом обитания бактерии (она живёт в нижнем отделе кишечника теплокровных) и именем открывшего её Теодора Эшериха. Но обычно её так не называют, а именуют на лабораторном жаргоне е-коли, кишпалкой или же совсем фамильярно — коляшкой. Коляшкины клетки прямые, размером примерно 1 на 3 мкм, объём одной бактерии составляет 2×10 –12 мл, но вмещает она многое. Во-первых, кольцевую молекулу ДНК, которая в тысячу раз длиннее самой клетки и, следовательно, очень плотно упакована. Молекула эта содержит столько генов, сколько необходимо для синтеза 4000 разных белков. Поступлений РНК от этих генов ожидают около 15 000 рибосом. Свой немалый геном кишечная палочка воспроизводит каждые 20 минут, ошибаясь с частотой 10 –8 –10 –10 . Это надо суметь: воспроизводиться так точно и с такой скоростью! Есть в клетках и плазмиды — свободноплавающие, не связанные с большой кольцевой хромосомой колечки ДНК, изучение которых привело к важнейшим достижениям в области биохимии и генной инженерии. Снаружи кишпалку защищает клеточная стенка, покрытая слизистой капсулой. Сквозь капсулу торчат короткие, похожие на волоски структуры, называемые пилями, — функция их пока не совсем понятна. Клетки некоторых штаммов перемещаются с помощью длинных жёстких жгутиков, играющих роль пропеллеров.
Как видите, кишечная палочка достаточно сложно устроена и предоставляет учёному богатое поле для работы и уникальные возможности. Некоторые штаммы E.coli словно специально созданы для лабораторных исследований. Хотя бактерия и обитает в кишечнике человека — среде, богатой органическими компонентами, её пищевые потребности относительно скромны: несколько простых солей и глюкоза, из которых она синтезирует около 5000 необходимых ей соединений. Кишпалка спор не образует, делится каждые 20 мин и при благоприятных условиях вырастает в жидкой среде до концентрации 2–5×10 9 клеток на миллилитр, а из плотной суспензии бактерий можно выделять разные вещества в количествах, достаточных даже для биотехнологических целей. На твёрдой поверхности бактерии образуют десятки тысяч колоний, которые можно быстро проанализировать с помощью специальных сред, красителей и антибиотиков (для сравнения заметим, что рассмотреть тысячи дрозофил одному человеку в короткий срок практически нереально), а это даёт возможность изучать очень редкие генетические события.
Но есть, конечно, и неудобства. Одно из них — явственно ощутимый дурной запах. Дело в том, что кишечные палочки синтезируют индол. Это вещество образуется и в кишечнике при гниении белков. Вместе с другим соединением, скатолом, оно обусловливает характерный запах фекалий. В чистом виде и малой концентрации индол содержится в цветах жасмина и апельсина, сообщая им чудесный аромат. А кишечная палочка индола образует много и пахнет соответственно, хотя лабораторные штаммы кишечника не видали отродясь.
В конце 70-х стало ясно, что в клетках Е.coli можно размножить и заставить работать почти любой эукариотический ген, главное — иметь этот ген. Тогда и расцвело пышным цветом клонирование ДНК. Учёные внедряли в кишечную палочку гены бактерий, грибов, насекомых, растений, животных и даже человека, так что палочка стала своеобразным символом генетического единства мира. Тогда же её стали называть живой пробиркой.
Когда генная инженерия делала первые шаги, обстановка вокруг неё была слегка паническая — генетически модифицированных объектов боялись. Хотя лабораторные штаммы для человека безвредны, кто знает, во что превратится кишпалка с чужим геном внутри. Так появились специальные штаммы, не способные существовать вне лаборатории: с тонкой стенкой, которая лопается при низкой концентрации солей, и нуждающиеся в некоторых веществах, которых они не найдут в окружающей среде и сами синтезировать не могут. Кстати, тонкая бактериальная стенка не только служит гарантией общественной безопасности, но и облегчает выделение клонированной ДНК или синтезированного белка.
Около 60% микрофлоры находится в желудочно-кишечном тракте. Любой сбой в слаженной работе микромира способен вызвать проблемы многих систем и функций.
1. Что такое дисбактериоз? Часто можно встретить другие обозначения — дисбиоз и синдром усиленного микробного роста.
2. Можно ли назвать дисбиоз и СИБР самостоятельными заболеваниями? Требуют ли они лечения?
СИБР и дисбиоз — это вторичные синдромы, сопутствующие многим патологическим процессам.
Нарушение баланса кишечной микрофлоры отмечается при синдроме раздраженного кишечника, диарее путешественников, антибиотико-ассоциированной, воспалительных заболеваниях кишечника и другой патологии. Однако это не означает, что СИБР и дисбиоз не нужно диагностировать и лечить. Расстройства микробиоценоза кишечника и увеличение числа условно-патогенной и патогенной микрофлоры кишечника (золотистый стафилококк, энтеропатогенная кишечная палочка, энтеробактер, протей, клебсиелла, синегнойная палочка, шигеллы, кампилобактер, клостридии, кандиды и др.) требуют терапии, т. к. вызывают и поддерживают местное воспаление, сопровождаются интоксикацией и могут привести к развитию сепсиса. При субкомпенсированном и декомпенсированном кишечном дисбиозе лечение обязательно.
3. В чем причины проблем с кишечной микрофлорой?
Дисбиоз развивается вследствие инфекционных заболеваний и постинфекционных состояний; после антибиотико-, гормоно- и
полихимиотерапии, применения слабительных средств и сорбентов; хирургического удаления части кишечника. Играют роль избыточное, несбалансированное и беспорядочное питание; дефицит пищевых волокон в рационе; употребление продуктов с обилием консервантов, красителей, ксенобиотиков; радиационные повреждения кишечника; гидроколонотерапия.
СИБР появляется при гипо- и анацидных состояниях желудка; лактазной и дисахаридазной недостаточности, целиакии; хроническом панкреатите и холецистите, воспалительных заболеваниях тонкой кишки (болезнь Крона, болезнь Уиппла, васкулиты); нейропатиях и миопатиях; опухолях кишечника и хронических запорах.
4. Как диагностировать нарушения микробиоценоза?
Поскольку в кишечнике живут более 500 видов бактерий (их общая масса может достигать 2,5 кг), определить нарушения количественного и качественного состава микрофлоры непросто. Применяются следующие методики:
классический бактериологический анализ кала (посев на дисбиоз) с определением основных видов микроорганизмов;
посев на бактериальные среды кишечного содержимого, полученного эндоскопически (для определения СИБР);
дыхательный тест с лактулозой, ксилозой, меченной изотопом углерода 14С;
бактериологическое исследование кала путем ПЦР, FISH-методом, изучение микробных метаболитов (индикан, фенол, паракрезол, аммиак и др.);
хромато-масс-спектрометрия родового состава микроорганизмов, позволяющая обнаружить живые и мертвые микроорганизмы и узнать их концентрации.+
5. Как проявляется дисбактериоз?
Симптомы неспецифичны; могут наблюдаться при заболеваниях желудочно-кишечного тракта, не сопровождающихся нарушением микробиоценоза. Основные признаки — диспепсический синдром (отрыжка, неприятный вкус во рту, повышенное газообразование, вздутие живота, урчание, понос, боли и зуд в области заднего прохода), синдром малдигестии (нарушение переваривания и всасывания жиров, мяса, углеводов), боль в животе, аллергические реакции (вздутие живота, жидкий пенистый стул, кожный зуд, крапивница, отек Квинке, бронхоспазм, полиартралгии).
Весьма характерно наличие внутренней интоксикации: слабость, быстрая утомляемость, отсутствие аппетита, головные боли, повышение температуры. При длительном течении развивается синдром мальабсорбции, проявляющийся поливитаминной недостаточностью, снижением массы тела, анемией.
За сутки в пищеварительном тракте образуется несколько литров газа, который в основном поглощается кишечной стенкой. Около 600 мл ежедневно выделяется через прямую кишку, а при избыточном росте бактерий его количество увеличивается до 2 л и более.+
6. Какое лечение необходимо при СИБР и дисбиозе?
Показания к уничтожению микробного загрязнения (к деконтаминации) — СИБР и наличие высоких титров условно-патогенной микрофлоры, представляющей угрозу переноса микробов в тонкую кишку. Для этого применяется несколько групп лексредств:+
препараты спорообразующей транзиторной флоры;
Антибиотики не должны всасываться из кишечника и подавлять рост нормальной микрофлоры. Этим требованиям отвечает рифаксимин — местный кишечный антисептик, который хорошо переносится и не вызывает бактериальной резистентности. Препарат имеет широкий спектр действия против условно-патогенных и патогенных грамположительных (стрептококки, стафилококки, энтерококк, туберкулезная палочка), грамотрицательных (шигелла, сальмонелла, иерсиния, протей, кишечная палочка, пептострептококк, холерный вибрион), аэробных бактерий, а также анаэробных грамположительных (клостридии, пептококк) и грамотрицательных (бактероиды, пилорический хеликобактер). Это лексредство с успехом используется для лечения острых кишечных инфекций, коррекции СИБР, санации толстой кишки при дисбактериозе и печеночной энцефалопатии. Рифаксимин применяется в течение недели по 400 мг 3 раза в сутки. При этом уровень выдыхаемого водорода снижается в 3–5 раз уже к третьему дню терапии, что свидетельствует о быстрой санации тонкой кишки.
Можно использовать и другие антибактериальные препараты: производные оксихинолов (интетрикс), нитрофуранов (нифуроксазид, или стопдиар), нитроимидазолы (метронидазол, тинидазол), энтерофурил. Метронидазол и тинидазол показаны при контаминации анаэробными микроорганизмами. Интетрикс и нифуроксазид обладают антимикробным действием по отношению к шигеллам, сальмонеллам, иерсиниям, кампилобактеру, протею, клебсиелле, патогенным коккам, а интетрикс также подавляет рост грибов и амеб. Длительность терапии при СИБР — 12–14 дней.
Эффективное средство лечения СИБР — энтерол, представляющий собой непатогенные дрожжевые грибы рода сахаромицеты булардии, полученные из тропических растений и плодов и обладающие генетически детерминированной устойчивостью по отношению почти ко всем группам антимикробных препаратов. Антимикробное действие энтерола установлено в отношении к широкому спектру условно-патогенных микроорганизмов и простейших. В то же время энтерол не подавляет рост облигатных микроорганизмов в полости кишки. Эти грибы обладают антивирусным и трофическим эффектом (синтезируют полиамины) и через 2–5 дней после окончания приема полностью выводятся из организма без побочных явлений. Энтерол используется в качестве антидиарейного и антисептического средства при острых кишечных инфекциях (в качестве альтернативы антибиотикам при невозможности их применения), антибиотико-ассоциированной диарее, псевдомембранозном колите, паразитарных диареях, дисбактериозе, СИБР.
При толстокишечном дисбиозе IV степени и неэффективности кишечных антисептиков необходимы антибиотики общерезорбтивного действия, предпочтительно фторхинолоны (офлоксацин, ципрофлоксацин, норфлоксацин, пефлоксацин); при псевдомембранозном колите — ванкомицин, метронидазол, энтерол, бацитрацин.
Показания к назначению антибиотиков: микробное загрязнение тонкой кишки; генерализованная форма дисбактериоза; выраженный интоксикационный синдром; упорный диарейный синдром; тяжелый иммунодефицит.
Применение бактериофагов при кишечном дисбиозе не оправдало возлагаемых на них надежд: оно провоцирует мутации бактерий.
Для снятия симптомов дисбиоза используют регуляторы кишечной моторики (дебридат, метеоспазмил, мотилиум, дицетел, мукофальк, имодиум), энтеросорбенты (смекта, энтеросгель, энтеродез).
7. Какие биологические препараты применяют для лечения дисбиоза?
Есть несколько групп биологических средств коррекции нарушений микрофлоры кишечника. Эубиотики, или пробиотики, содержат живые облигатные микроорганизмы; симбиотики — комбинацию из нескольких видов живых организмов; пребиотики — стимуляторы роста нормальных микроорганизмов; синбиотики — живые бактерии; пребиотические комплексы — рациональную комбинацию из пробиотиков, пребиотиков, сорбентов, витаминов, микроэлементов.
8. Как воздействуют пробиотики?
В широком смысле слова это живые микроорганизмы и вещества микробного и другого происхождения, оказывающие благоприятный эффект на физиологические функции, биохимические и поведенческие реакции организма через оптимизацию его микроэкологического статуса.
Выделяют 4 поколения пробиотиков. К 1-му относятся однокомпонентные (колибактерин, бифидумбактерин, лактобактерин), т. е. содержащие 1 штамм бактерий.
Препараты 2-го поколения (бактисубтил, биоспорин, споробактерин и др.), основанные на использовании неспецифических для человека микроорганизмов, являются самоэлиминирующимися антагонистами патогенной микрофлоры.
Препараты 3-го поколения включают поликомпонентные пробиотики, в составе которых несколько симбиотических штаммов бактерий одного вида (ацилакт, аципол и др.) или разных видов (линекс, бифиформ) с взаимоусиливающим действием.
К 4-му поколению относят иммобилизованные на сорбенте бифидосодержащие препараты (бифидумбактерин форте, пробифор). Сорбированные бифидобактерии эффективно колонизируют слизистую оболочку кишечника, оказывая более выраженное протективное действие, чем несорбированные аналоги.
Эффекты воздействия данных лексредств на организм человека:
синтез нутриентов и антиоксидантов (витаминов С, К, группы В, фолиевой кислоты, короткоцепочечных жирных кислот, бутирата, оксида азота);
защитная функция (колонизация слизистой толстого кишечника, выработка лизоцима, бактериоцинов, снижение продукции эндотоксинов, снижение мутагенности);
иммуномодулирующая (стимуляция макрофагов, синтеза IgA, подавление синтеза IgE, модулирование цитокинового ответа);
пищеварительная (расщепление углеводов, клетчатки, жиров, белков, деконъюгация желчных кислот);
цитопротективная (нейтрализация токсических субстратов и метаболитов, стимуляция регенерации и дифференцировки эпителия кишечника, антиканцерогенный эффект бутирата через регуляции апоптоза).
9. Что такое пребиотики?
Это препараты или БАД немикробного происхождения. Они не перевариваются в кишечнике, положительно влияют на организм, стимулируя рост и/или метаболическую активность нормальной микрофлоры кишечника. Типичные представители пребиотиков — соединения, относящиеся к классу низкомолекулярных углеводов: дисахариды, олигосахариды, которые широко распространены в природе. Пребиотики не должны подвергаться гидролизу пищеварительными ферментами и абсорбироваться в верхних отделах пищеварительного тракта. Они селективно стимулируют 1 вид или определенную группу микроорганизмов толстой кишки.
В качестве пребиотиков используют олигосахариды (соевый олигосахарид, фруктоолигосахариды); моносахариды (ксилоза); дисахариды (лактулоза); полисахариды (пектины, декстрин, инулин), пищевые волокна трав (псиллиум), злаковых (отруби, Рекицен-РД), фруктов; пептиды (соевые, молочные); ферменты (протеазы сахаромицетов и др.); аминокислоты (валин, аргинин, глутаминовая кислота); антиоксиданты (каратиноиды, глутатион, витамины А, С, Е, соли селена); ненасыщенные жирные кислоты; органические кислоты (уксусная, пропионовая, лимонная); другие вещества (лецитин, парааминобензойная кислота, лактоферрин, лектины, экстракты водорослей, растительные и микробные экстракты).
Пребиотики лучше использовать на начальных этапах дисбиоза, а также для его профилактики.
10. Назначают ли при дисбиозе фитотерапию?
Лечение лекарственными травами может стать профилактическим и вспомогательным методом коррекции. Наиболее известные растения, обладающие антибактериальным действием по отношению к определенным патогенным микроорганизмам:
абрикос — подавляет гнилостные микроорганизмы, протей, клебсиеллу, синегнойную палочку;
барбарис (берберин) — гемолитические стафилококки, стрептококки, дизентерийные бактерии, энтеробактер;
брусника (сок) — рост кандид;
земляника — золотистый стафилококк, энтеробактер;
клюква (ягоды) — гнилостные бактерии рода протей и клебсиеллы;
смородина черная — грибы и золотистый стафилококк, вирусы гриппа;
черника — стафилококк, шигеллы;
шиповник — грамположительные бактерии;
яблоки — патогенные кишечные палочки, вирусы гриппа А.
Их лечебный эффект несильный и наблюдается только после длительного воздействия.
В зависимости от формы и выраженности дисбиоза пациентам с нарушениями кишечной микрофлоры для домашнего лечения можно рекомендовать при:
стафилококковом дисбактериозе — эвкалипт, зверобой, аир, календулу, барбарис, мать-и-мачеху, исландский мох. В рационе должны присутствовать ягоды черники, рябины, земляники, малины; чеснок, хрен;
микотическом кандидозном дисбактериозе — липу, тимьян, почки березы, эвкалипт, мяту, мелиссу, фенхель, шалфей, аир, исландский мох, валериану, веронику, девясил, бадан. Надо употреблять в пищу бруснику, морковь, черемшу; дрожжевой, картофельный, тыквенный и рисовый экстракты;
гнилостном дисбактериозе — крапиву, бруснику, тмин, смородину, лапчатку прямостоячую, бадан, почки березы, чистотел, полынь горькую, маклею, лопух. Показаны абрикосы, ягоды смородины, рябины, брусники; топинамбур, красный сладкий перец;
протейном дисбактериозе — эвкалипт, календулу, аир, подорожник, зверобой, ольху, бадан, полынь, лапчатку прямостоячую. Полезны клюква, малина, смородина, перец, чеснок, лук.
Различают 3 степени нарушений микробиоценоза.
Легкая. Количество бифидофлоры снижено незначительно, анаэробы преобладают над аэробами, условнопатогенная флора представлена не более чем 2 видами в титрах до 10 6 .
Средняя. Увеличивается количество аэробов. Снижается титр бифидофлоры. Число анаэробов и аэробов примерно одинаковое. Появляются атипичные формы кишечной палочки, повышается титр условнопатогенных микроорганизмов.
Тяжелая. Количество аэробов превышает число анаэробов. Резко снижен титр бифидо и лактобактерий. Увеличено число условнопатогенной флоры — 10 7 и выше. Пациенты жалуются на расстройство стула, метеоризм; есть признаки интоксикации: повышенная температура, слабость, быстрая утомляемость.
Анатолий Близнюк, доцент кафедры поликлинической терапии БГМУ, кандидат мед.наук
Медицинский вестник, 25 июня 2014
03 февраля 2020
Герой февраля: кишечная палочка Escherichia coli
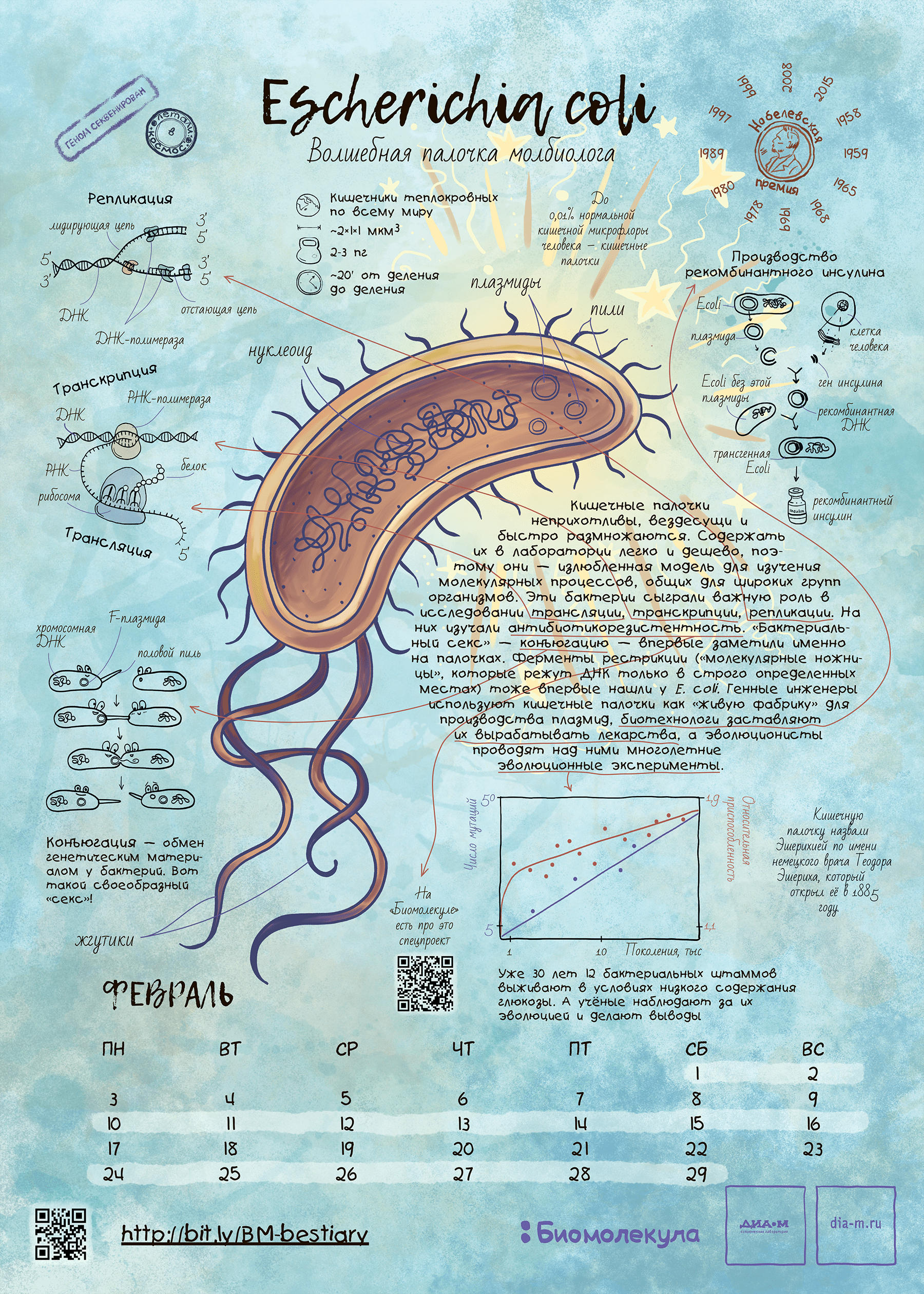
Скромная бактерия за полстолетия с момента ее открытия в конце XIX в. стала настоящей волшебной палочкой для молекулярной биологии. Сейчас результаты опытов с ее использованием занимают главы и тома профессиональных и популярных изданий. Конечно, в нашем путеводителе по модельным организмам E. coli должна была занять свое почетное место.
![]()
Двенадцать модельных организмов
Escherichia и Eschrichtius — Болезнь путешественников — Главная модельная бактерия — Учебник молекулярной генетики — Невезение с CRISPR/Cas
![]()
Рисунок 1а. Escherichia длиной 2 мкм
![]()
Рисунок 1б. Теодор Эшерих (1857–1911)
![]()
Рисунок 1в. Eschrichtius длиной 14 метров
![]()
Рисунок 1г. Даниэль Фредрик Эшрихт (1798–1863)
Клетки с относительно тонкой клеточной стенкой, не окрашивающиеся красителем генцианом фиолетовым (окраской бактерий по методу датского микробиолога Кристиана Грама).
Зачем же такую опасную бактерию сделали модельной? Дело в том, что в условиях культивирования кишечная палочка часто теряет патогенность, становится неспособной жить в естественных для себя условиях (то есть одомашнивается). И этим свойством в 1940-е годы воспользовались микробиологи, проведя с лабораторными штаммами E. coli (например, со знаменитым штаммом К12) много прорывных для науки экспериментов.
Так, манипулируя мутированными штаммами кишечной палочки, которые уже научились получать при помощи облучения, Джошуа Ледерберг и Эдуард Лаури Тейтем в 1947 году обнаружили способность разных штаммов обмениваться генетическим материалом и спасать друг друга от образовавшихся дефектов, проявлявшихся в неспособности расти на минимальной питательной среде. Так был открыт процесс конъюгации бактерий, который затем послужил важным инструментом для картирования бактериального генома . Ведь тогда это можно было делать только косвенными, микробиологическими методами — сама природа генетического кода была неизвестна.
Кстати, Джошуа Ледерберг был некоторое время мужем Эстер Ледерберг, первооткрывательницы бактериофага лямбда [3].
С начала 1950-х годов исследования по молекулярной генетике с использованием кишечной палочки и ее вирусов в качестве основного инструмента росли как снежный ком. Не будет преувеличением сказать, что к 70-м годам E. coli написала учебник молекулярной генетики! Вспомним открытие генетического кода, в котором участвовало несколько коллективов физиков и молекулярных биологов, в том числе Френсис Крик, Георгий Гамов и другие выдающиеся люди того времени [6]. Основные эксперименты по расшифровке кода велись на бесклеточных лизатах кишечной палочки.
Позднее обнаружилось, что E. coli хорошо подходит для зародившейся в 1960–1970-е годы биотехнологии [7]. Бактерия хорошо переносит введение в свою клетку гетерологичных (то есть чужеродных) генов и во многих случаях способна синтезировать их продукты без вреда для себя. Белки, полученные таким способом, стали называть рекомбинантными, и теперь они широко используются в медицине и других практических задачах.
Кишечная палочка — возможно, самый исследованный организм с точки зрения молекулярной биологии. Тем не менее у элементов ее генома до сих пор обнаруживают новые свойства. Это одновременно плохо (как же мало мы знаем!) и хорошо (будет чем заняться!). Совсем недавно на защите диссертации я услышал о том, как у одной из генных кассет эшерихии, участвующей в каскаде переработки сульфолипидов, также обнаружена и лактазная активность [8]. До этого такая активность была известна только у знаменитого лактозного оперона Жакоба и Моно, описанного в 1961 году!
Кажется, что E. coli — модельный организм без недостатков. Тем не менее биотехнологам не повезло, что у этой бактерии от природы нет системы бактериального иммунитета CRISPR/Cas [9], о которой я уже упоминал в эссе о бактериофаге лямбда [3]. Именно поэтому эту систему, ныне незаменимую в генной инженерии, открыли относительно поздно.
Кишечная палочка-выручалочка — это здорово (рис. 2). Но теперь пора переместиться в мир ядерных организмов. Удобным инструментом для молекулярной биологии и генетики эукариот оказались одноклеточные грибы — дрожжи — и гаплоидный плесневый гриб — нейроспора. Как они дошли до такой одноклеточной и гаплоидной жизни и что было открыто с их помощью — читайте в следующем материале нашего путеводителя по модельным организмам через месяц.
![]()
Благодарность
Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу. Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции
|