Анализ крови ифа лямблии и токсоплазмоз
Токсоплазмоз — широко распространенное инфекционное заболевание человека и животных, характеризующееся длительным хроническим течением, полиморфностью клинической картины (от бессимптомного носительства до летальных форм болезни) и возможностью внутриутробного инфицирования плода.
Возбудитель токсоплазмоза — Toxoplasma gondii — внутриклеточный паразит, размером 4—7 мкм. Если взглянуть на этот живой организм под микроскопом, он напоминает дольку апельсина (рис.1).
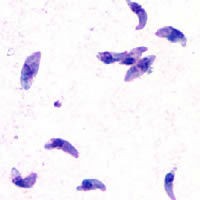
Рис. 1 Toxoplasma gondii –окрашенный препарат по Романовского-Гимзе
Можно ли заразиться токсоплазмозом от домашних животных? Да, ведь токсоплазмозом болеют около 60 видов птиц и 300 видов млекопитающих (одомашненных и диких), которые с фекалиями попадают во внешнюю среду выделяют цисты и приводят к заражению других организмов.
Но имея сложный путь развития (половой и бесполый) и тот факт, что половой процесс происходит только лишь в кишечнике животных семейства кошачьих, с образованием устойчивых форм (цист), которые долгое время сохраняются во внешней среде (до 2 лет), не боятся действия низких и высоких температур, высушивания. Бесполое размножение не приводит к образованию стойких форм паразита.
Источником инфекции выступают больные животные, которые выделяют паразитов со слюной, молоком, мочой, фекалиями. Люди лишь промежуточные хозяева этого простейшего.
Заражение возбудителем токсоплазмоза происходит:
- при употреблении в пищу сырого или плохо прожаренного мяса;
- при контакте с сырым или недостаточно термически обработанным мясом слизистой оболочки полости рта (многие хозяйки пробуют сырой фарш);
- при уходе за зараженными животными, например, уборка кошачьего туалета;
- при употреблении в пищу немытых овощей, фруктов, зелени, на которых могут быть цисты паразита;
- при пересадке внутренних органов или переливание крови.
В подавляющем большинстве случаев при токсоплазмозе наблюдается бессимптомное носительство паразита, сопровождающееся наличием специфических антител в крови. Инфицированность населения колеблется от 10 до 90%.
Клинические симптомы токсоплазмоза у человека отличаются разнообразием. Выделяют врожденный и приобретенный токсоплазмоз.
Врожденный токсоплазмоз протекает тяжелее всего. При заражении на ранних сроках беременности происходит внутриутробная гибель плода, так как у него формируются уродства, которые несовместимы с жизнью. Если инфицирование наступает во второй половине беременности, ребенок рождается с генерализованным поражением всех органов и систем. Для него характерны повышение температуры тела, желтушность кожи, слабость, низкий тонус мышц, увеличение печени, лимфатических узлов, селезенки, кожная сыпь, патологии нервной системы (энцефаломиелит). Также возможно развитие косоглазия, слепоты, нарушение формирования головного или спинного мозга.
Токсоплазмоз входит в группу TORCH- инфекций, считающихся потенциально опасными для внутриутробного развития плода. Только первичное заражение женщины во время беременности может привести к инфицированию плода. Таким образом, практически важным является вопрос о моменте инфицирования беременной: задолго до, непосредственно перед, либо во время беременности.
При попадании токсоплазм в организм человека через 7—14 дней начинается первичный гуморальный иммунный ответ — продуцируются специфические IgM. Максимальный уровень их концентрации достигается к 20— 30-му дню от момента инфицирования. Полное их исчезновение в большинстве случаев (около 70%) происходит в течение 3—4 месяцев, однако, возможно присутствие специфических IgM и более длительное время — до 1 года и более (около 10% случаев). Следовательно, присутствие в крови специфических IgM предполагает, но не доказывает свежее инфицирование, поскольку они могут находиться в крови от 3 мес. до 1,5 лет. Дифференцировать первичную инфекцию от паст-инфекции помогает комплексный подход к диагностике — это сопоставление данных всего спектра серологических маркеров инфекции, а именно:
- результатов выявления специфических IgM, IgA;
- определения индекса авидности IgG и концентрации IgG в динамике.
Анализ серологического профиля пациента позволяет определить вероятный срок инфицирования T.gondii.
В случае отрицательного результата беременные относятся к группе риска по инфицированию Toxoplasma gondii во время беременности и каждые 1—2 месяца должны обследоваться на токсоплазмоз. В случае положительного результата иммуноферментного анализа на поздние специфические антитела IgG у беременных важно определить срок инфицирования.
Приобретенный токсоплазмоз у человека чаще всего имеет латентное течение. Инкубационный период длится от 5 до 23 дней. Больные жалуются на высокую температуру тела, озноб, слабость, головные боли, болезненные ощущения в суставах и мышцах, увеличение печени, селезенки, шейных лимфатических узлов. Возможно развитие пневмонии, энцефалита, эндокардита, поражения глаз.
Течение хронического токсоплазмоза бессимптомное или характеризуется незначительными клиническими проявлениями на протяжении многих лет. Наиболее распространенные симптомы этой формы болезни:
- повышение температуры до субфебрильных цифр;
- слабость, которая возникает даже после сна, ухудшение памяти, апатия к окружающему миру, раздражительность;
- тупые головные боли;
- болезненные ощущения в мышцах и суставах, затруднение передвижения;
- увеличение в размерах селезенки, печени и лимфатических узлов;
- при поражении желудочно-кишечного тракта: тупые боли в животе, сухость во рту, снижение аппетита, метеоризм;
- патологии сердечно - сосудистой системы, которые сопровождаются снижением артериального давления, давящими болями в сердце и изменениями его ритма;
- нарушения эндокринной системы: болезни поджелудочной железы, сбои менструального цикла, импотенция;
- расстройства зрения, близорукость.
В то же время возможны и клинически выраженные варианты течения первичной инфекции (как правило, возникающие у лиц с нарушением иммунитета) с развитием энцефалита, миокардита, миозита, увеита, формированием хронической инфекции.
Весьма актуальна проблема генерализации латентного токсоплазмоза у ВИЧ-инфицированных с развитием тяжелого некротического энцефалита с большой вероятностью летального исхода.
Среди возможных осложнений токсоплазмоза выделяют: инфекционно-токсический шок, поражения центральной нервной системы (энцефалит, арахноидит, отек мозга, эпилептиформный синдром, параличи, парезы, отставание детей в развитии), болезни глаз (атрофия зрительного нерва), патологии сердца (эндокардит), недуги дыхательных органов (пневмония).
Так как клинические симптомы недуга очень разнообразны, диагностика токсоплазмоза на основании жалоб больного невозможна. Следует обязательно собрать эпидемиологический анамнез, выяснить, употреблял ли больной сырое иди недостаточно прожаренное мясо, контактировал ли с больными животными (в особенности кошками).
В лабораторной диагностике токсоплазмоза широко используются иммунологические методы, которые выявляют антитела к токсоплазмозу. Наиболее распространенным среди них является иммуноферментный анализ. Для его проведения у человека берут кровь на токсоплазмоз. Также можно применять и другие биологические жидкости. На основании выявления антител двух разных классов данное исследование позволяет судить о давности заражения, так как иммуноглобулины класса M появляются сразу после инфицирования и в течение года после него, а иммуноглобулины класса G сохраняются в крови на всю последующую жизнь.
Можно ли вылечить токсоплазмоз? У здоровых людей болезнь заканчивается полным выздоровлением с формированием иммунитета на всю дальнейшую жизнь и не имеет каких-либо последствий. Тяжелые поражения разных органов и систем при токсоплазмозе развиваются у людей с дефектами иммунитета, например, ВИЧ-инфицированных. Последствия токсоплазмоза особенно тяжелые при врожденной форме болезни. Она приводит к внутриутробной гибели плода или наличию у него выраженных патологий.
Профилактика токсоплазмоза также включает следующие мероприятия:
- тщательное мытье фруктов, овощей и зелени;
- употребление в пищу достаточно термически обработанных мясных блюд;
- мытье рук после земельных работ и ухода за животными;
- в период беременности следует избегать контакта с кошками;
- уничтожение мух, тараканов и грызунов, которые могут переносить цисты паразитов.
С целью предупреждения врожденного токсоплазмоза необходимо проводить обследование с определением уровня антител в крови всем женщинам, которые планируют беременность.

Иммуноферментный анализ (ИФА) — метод лабораторной диагностики, позволяющий обнаруживать специфические антитела и антигены при самых разных патологиях.
ИФА — один из самых распространенных и точных методов для выявления инфекций, передающихся половым путем, в частности ВИЧ, ВПЧ, гепатита В.

Для того чтобы результаты анализов были максимально достоверными, необходимо правильно подготовиться к их сдаче.

Спецпредложения, скидки и акции помогут существенно сэкономить на медицинском обследовании.
Контроль качества лабораторных исследований, осуществляемый по международным стандартам, — дополнительная гарантия точности результатов анализов.
Современная диагностика в медицине немыслима без высокочувствительных лабораторных анализов. Прежде для установления причин тех или иных симптомов врачи были вынуждены ориентироваться на косвенные признаки болезни, а также проводить многоступенчатые микроскопические исследования в попытке обнаружить возбудителя инфекции. Сегодня достаточно одного-единственного теста — такого как иммуноферментный анализ — чтобы подтвердить или опровергнуть первоначальный диагноз.
Основные понятия и принцип метода иммуноферментного анализа
Существует несколько разновидностей антител, каждая из которых вступает в действие на определенном этапе иммунного ответа. Так, первыми в ответ на проникновение антигена в организм синтезируются иммуноглобулины класса М (IgM). Содержание этих антител наиболее высоко в первые дни инфекционного процесса.
Следом за ними иммунная система выбрасывает в кровь иммуноглобулины класса G (IgG), которые помогают уничтожать антигены до полной победы над инфекцией, а также продолжают циркулировать по сосудам в дальнейшем, обеспечивая иммунитет к повторному заражению. На этом явлении основана вакцинация: благодаря прививкам, содержащим ослабленные антигены микробов и вирусов, в нашей крови появляется большое количество IgG, которые при контакте с реальной угрозой быстро подавляют инфекцию — до того, как она нанесет вред здоровью.
Как узнать, какие именно антигены или антитела присутствуют в организме человека? Когда врач предполагает, что причиной заболевания является определенная инфекция, или желает измерить концентрацию определенного гормона, он назначает пациенту иммуноферментный анализ.
ИФА бывает качественным и количественным. В первом случае подразумевается однозначный ответ: искомое вещество или найдено, или не найдено в образце. В случае с количественным анализом более сложная цепь реакций дает возможность оценить концентрацию антител в крови человека, что в сравнении с результатами предыдущих тестов даст ответ на вопрос о том, как развивается инфекционный процесс.
Бесспорные преимущества ИФА — высокая чувствительность и специфичность метода. Чувствительность — это возможность распознать искомое вещество, даже если его концентрация в образце невысока. Специфичность же подразумевает безошибочность диагностики: если результат положительный, значит, найдены именно те антитело или антиген, которые предполагались, а не какие-то другие.
Высокая степень технологичности проведения иммуноферментного анализа минимизирует влияние человеческого фактора, что снижает вероятность ошибки. Большинство используемых в современных лабораториях тест-систем и реактивов для ИФА выпускаются в промышленных условиях, что гарантирует точный результат.
В случае диагностики инфекционных заболеваний иммуноферментный анализ не может найти возбудителя и определить его специфичные свойства: он лишь указывает на наличие антител в крови у больного, косвенно свидетельствующих о присутствии чужеродного микроорганизма в теле человека.
ИФА — крайне точный, но не дешевый метод, поэтому обращаться к нему нужно с умом, а интерпретацией результатов должен заниматься квалифицированный врач.
Невозможно охватить полный список показаний к проведению ИФА. Вот наиболее распространенные цели анализа:
- Диагностика острых и хронических инфекционных заболеваний:
- IgM и IgG к вирусным гепатитам А, B, C, E, а также антигенов гепатитов В и С;
- IgG к ВИЧ;
- Ig M и IgG к цитомегаловирусной инфекции;
- Ig M и IgG к вирусу Эпштейна-Барр;
- Ig M и IgG к герпетическим инфекциям;
- Ig M и IgG к токсоплазмозу;
- Ig M и IgG к кори, краснухе, сальмонеллезу, дизентерии, клещевому энцефалиту и другим заболеваниям;
- IgG к паразитарным заболеваниям;
- Ig M и IgG к инфекциям, передающимся половым путем;
- IgG к хеликобактерной инфекции.
- Общая оценка показателей иммунитета человека и маркёров некоторых аутоиммунных заболеваний.
- Выявление онкологических маркёров (фактора некроза опухоли, простатспецифического антигена, раково-эмбрионального антигена и других).
- Определение содержания гормонов в сыворотке крови (прогестерона, пролактина, тестостерона, тиреотропного гормона и других).
Основной биоматериал для проведения ИФА — это сыворотка крови: в лаборатории у пациента берут образец крови из вены, из которого в дальнейшем удаляют форменные элементы, затрудняющие проведение анализа. В некоторых других случаях для анализа используется спинномозговая жидкость, околоплодные воды, мазки слизистых оболочек и т.д.
Для того чтобы избежать искажений в результатах, рекомендуется сдавать кровь натощак, а за две недели до исследования (если целью является диагностика хронических, скрыто протекающих инфекционных заболеваний) необходимо отказаться от приема антибиотиков и противовирусных препаратов.
При наличии необходимых реактивов и хорошей организации работы лаборатории результат анализа вы получите в течение 1–2 суток после забора крови. В некоторых случаях, при необходимости получения экстренного ответа, этот срок может быть сокращен до 2–3 часов.
- IgM — наличие этого класса иммуноглобулинов говорит об остром инфекционном процессе в организме. Отсутствие IgM может говорить как об отсутствии конкретного возбудителя в организме, так и о переходе инфекции в хроническую стадию.
- IgA при отрицательном результате теста на IgM чаще всего свидетельствует о хронической или скрыто протекающей инфекции.
- IgM и IgA (совместное присутствие) — два положительных результата говорят о разгаре острой фазы заболевания.
- IgG говорит либо о хронизации заболевания либо о выздоровлении и выработке иммунитета к инфекционному агенту.
В зависимости от содержания анализа в бланке могут быть представлены данные в виде таблицы с перечислением всех антител или антигенов с пометками об отрицательной или положительной реакции, либо будет указано количественное значение результата (отрицательный, слабоположительный, положительный или резко положительный). Последний вариант определяет, сколько антител содержится в анализируемом образце.
Еще один количественный показатель — индекс авидности антител, выраженный в процентах. Он указывает, сколько времени прошло от начала инфекционного процесса (чем выше индекс — тем больше).
Сегодня выпускаются тысячи видов тест-систем ИФА, позволяющих обнаруживать специфические антитела и антигены при самых разных патологиях. Поэтому этот анализ используется практически во всех медицинских отраслях. Диагноз, поставленный с помощью ИФА, — это гарантия назначения адекватной терапии и эффективного лечения заболевания.
Информативность ИФА делает этот анализ важным инструментом в работе многих медицинских центров. Но можно ли доверять такую диагностику государственным лабораториям или лучше самим выбрать, где провести такое исследование?

Токсоплазмоз - паразитарное заболевание, вызываемое представителем простейших токсоплазмой гондии. Наибольшую опасность оно представляет для беременных женщин, так как может привести к аномалиям развития плода и даже к его смерти.
МЕ/мл (международная единица на миллилитр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Не принимать пищу в течение 8-10 часов перед исследованием, можно пить чистую негазированную воду.
- Исключить физическое и эмоциональное перенапряжение за 24 часа до сдачи крови.
- Не курить в течение 3 часов до исследования.
Общая информация об исследовании
Т. гондии - это микроскопический паразит, основным хозяином которого является кошка. Также он может быть обнаружен в почве.
Т. гондии очень распространена. Она встречается во всем мире, а в некоторых странах инфицировано до 95 % населения. По данным ВОЗ, около 23 % людей старше 12 лет страдают токсоплазмозом. Заражение происходит при употреблении загрязненной пищи (особенно плохо приготовленного мяса) или воды, а также при уборке помета кошки, при передаче инфекции от матери к ребенку и в редких случаях во время трансплантации органов или переливания крови.
Окончательными хозяевами для т. гондии являются дикие и домашние кошки. После того как кошки заражаются, употребляя в пищу инфицированных птиц, грызунов или сырое мясо, т. гондии проходят половой цикл развития, приводящий к образованию яиц, заключенных в защитную оболочку. Первичное или повторное заражение т. гондии приводит к выраженным симптомам заболевания у людей с ослабленной иммунной системой, например у больных ВИЧ/СПИДом, проходящих курсы химиотерапии, пациентов после трансплантации органов или принимающих иммунодепрессанты. Могут поражаться глаза и нервная система, что вызывает головные боли, судороги, спутанность сознания, лихорадку, энцефалит, потерю координации и затуманенность зрения.
Когда заражается беременная женщина, вероятность того, что инфекция передастся будущему ребенку, составляет 30-40 %. Причем, если инфицирование происходит в начале беременности, оно может вызывать выкидыши, мертворождения или приводить к серьезным осложнениям у новорожденных, в том числе умственной отсталости, судорогам, слепоте и увеличению печени или селезенки. Многие инфицированные дети, особенно те, кто заразился ближе к появлению на свет, рождаются здоровыми, но спустя несколько лет у них развиваются тяжелые инфекции глаз, потеря слуха и задержка умственного развития.
Когда происходит контакт человека с т. гондии, его иммунная система реагирует, вырабатывая антитела против паразита. В крови может быть обнаружено два вида антител к токсолплазме: IgM и IgG.
Антитела IgG вырабатываются организмом через несколько недель после первичного инфицирования, чтобы обеспечить долгосрочную защиту. Уровень IgG нарастает во время активности инфекции, а затем стабилизируется, как только заболевание проходит и паразит становится неактивным. Однажды столкнувшись с т. гондии, человек на протяжении всей жизни будет иметь некоторые измеряемые количества антител IgG в крови.
Для чего используется исследование?
- Чтобы определить, была ли инфицированна т. гондии женщина, планирующая беременность, и есть ли у нее иммунитет к данной инфекции. Во время беременности исследование необходимо, если подозревается возможное заражение.
- Для выявления инфекции у людей с ослабленным иммунитетом, у которых подозревается токсоплазмоз, или у тех, у кого есть его выраженные симптомы.
Что означают результаты?
| Отрицательный результат | 1 - 3 МЕ/мл (либо равно 3) |
Причины положительного результата:
- активизация скрытой инфекции и/или хронической инфекции,
- текущая или ранее перенесенная инфекция.
Причины отрицательного результата:
- отсутствие инфицирования возбудителем в прошлом – если нет симптомов токсоплазмоза.
При подозрении на заражение исследование рекомендуется повторить через 10-14 дней, так как при первичном инфицировании антитела могут просто не успеть выработаться иммунной системой.

В Клиническом отделении №3 г. Кисловодска добавлены услуги УЗИ-диагностики
В организм человека цисты лямблий попадают через рот. Развитие лямблий происходит в тонком кишечнике. Полный цикл инвазии завершается высвобождением из организма-хозяина цист, которые во внешней среде остаются жизнеспособными длительное время.
Лямблии считаются причиной более 20 % острых кишечных заболеваний.
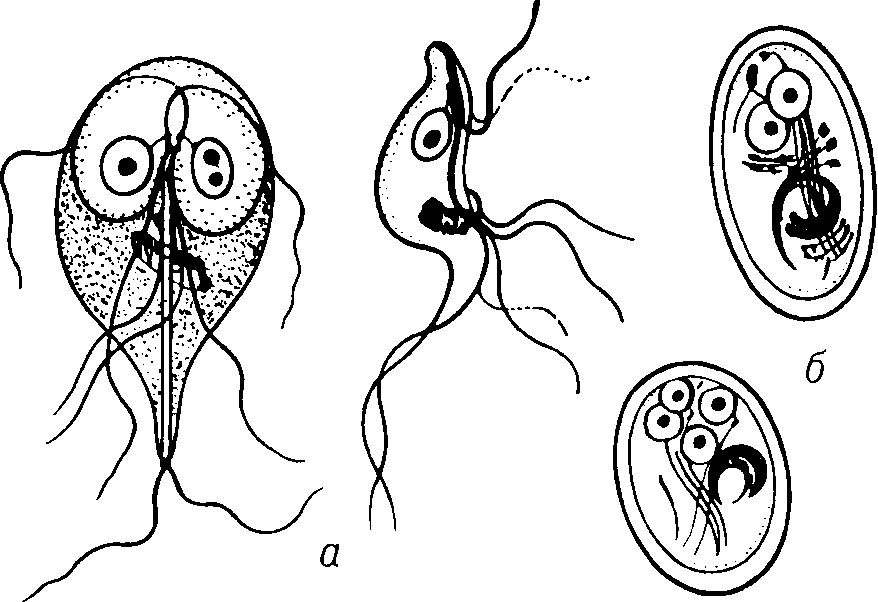
Инвазия G. lamblia слизистой оболочки тонкого кишечника может давать различную клиническую картину: от бессимптомного течения до уртикарных проявлений и диарейного синдрома, особенно тяжело протекающего при выраженной иммуносупрессии. Инфекция лямблиями может спонтанно исчезнуть через 6 недель, а может персистировать годами. При этом экскреция цист происходит с 10-20 дневными паузами.
Ярко выраженное заражение этими паразитами приводит к тяжелым кишечным расстройствам. При этом могут возникать нерезкие боли в животе, вздутие и урчание, расстройство стула, снижение аппетита, вялость, тошнота, иногда боли в правом подреберье, умеренная лихорадка.
- Также диагностическими признаками лямблиоза являются отрыжка тухлым, запах изо рта, горечь во рту, изжога.
У детей патологические явления наблюдаются чаще, чем у взрослых. Для детей особенно характерен синдром малабсорбции, вызывающий серьезные нарушения проницаемости слизистой тонкой кишки для жиров, углеводов, сахаров и витаминов. Это является причиной резкой потери веса и развития дистрофии у детей. Перечисленные выше симптомы могут присутствовать постоянно или иметь приходящий характер.
Трихинеллы — мелкие живородящие нематоды размером до 4 мм.
- Кишечная фаза. Личинки попадают в просвет кишки, где они созревают и начинают отрождать новые личинки.
- Миграционная фаза. Личинки попадают в ток крови и разносятся по всему организму.
- Мышечная фаза. Оседание личинок происходит в поперечнополосатых мышцах. Они распределяются неравномерно, предпочитая мимическую, дыхательную, жевательную мускулатуру, диафрагму, сгибатели конечностей.
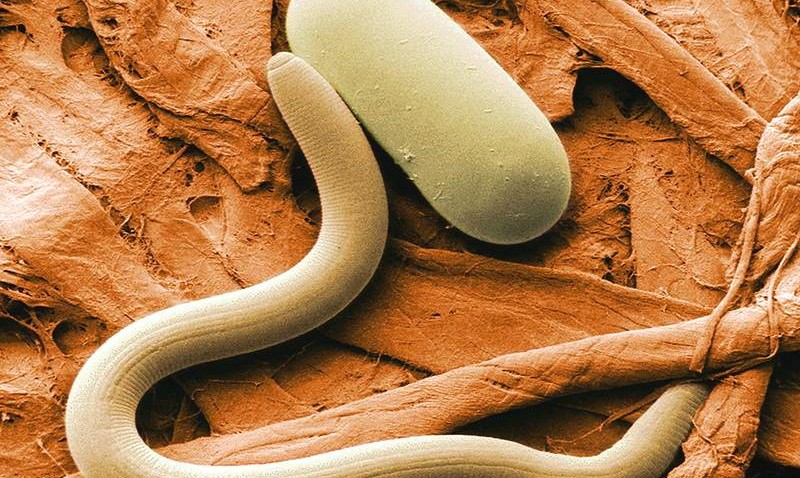
Основными клиническими проявлениями трихинеллёза является лихорадка, отёки, мышечные боли, эозинофилия. Отёк век и всего лица настолько характерен для трихинеллёза, что в народе болезнь получила название “одутловатка”. Мышечные боли возникают через 1–3 дня после появления отёков и являются также одним из характернейших симптомов. Чаще отмечаются боли в мышцах глазных яблок, жевательных, икроножных мышцах, сгибателях конечностей.
Абдоминальный синдром развивается с первых дней болезни и характеризуется разлитыми болями в животе, тошнотой, рвотой, редко поносами со слизью и кровью. Приступы болей сопровождаются высокой эозинофилией до 80–90 % и лейкоцитозом.
При тяжелом трихинеллёзе развиваются осложнения. Hа 1–2-ой неделе могут возникнуть язвенно-некротические поражения желудка и тонкого кишечника с последующей перфорацией и кровотечением. Hа 3–4 неделе — миокардит, пневмонит, морфологичекой основой которых являются распространенные васкулиты аллергического характера. Эти осложнения обычно и являются причиной смерти.
В диагностике трихинеллеза большое значение имеют серологические методы, основанные на выявлении специфических антител.
Описторхоз - заболевание, вызываемое паразитированием в печеночных ходах и в протоках поджелудочной железы гельминтов - кошачьей двуустки.
Заражение кошачьей двуусткой приводит к развитию хронического гепатита, панкреатита, цирроза печени, анемии.

Заражение человека и млекопитающих животных происходит при употреблении в пищу сырой, недостаточно прожаренной и слабо просоленной рыбы с метацеркариями гельминта.
- аллергические реакции
- механическое воздействие присосками и шипиками гельминтов с повреждением желчных и панкреатических протоков
- пролиферация железистого эпителия, которую следует рассматривать как предраковое состояние
В ранней фазе описторхоза могут быть повышение температуры тела, боли в мышцах и суставах, рвота, понос, болезненность и увеличение печени, селезенки, аллергические высыпания на коже. В поздней фазе описторхоза главной жалобой больных являются указания на боли в эпигастрии и правом подреберье; у многих они иррадиируют в спину и иногда в левое подреберье. Часто возникают головокружения, головные боли, диспептические расстройства. Некоторые больные указывают на бессонницу, частую смену настроения, повышенную раздражительность. Температура тела субфебрильная или нормальная.
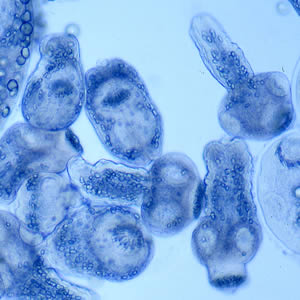
Попадая в печень, легкие, реже в почки, кости, мозг, личинки цепня формируют эхинококковый пузырь в форме кисты. Размеры и количество кист значительно варьируют. Эхинококковая киста растет на протяжении многих лет, отодвигая и сдавливая ткани хозяина.
При печеночной локализации кисты отмечается похудание, снижение аппетита, изжога, отрыжка, рвота. Проявления эхинококкоза легких определяются локализацией кисты. Даже небольшая киста, расположенная вблизи плевры, рано проявляет себя болевым синдромом, а при локализации у бронхиального ствола клинические симптомы проявляются кашлем и сосудистыми расстройствами. Эхинококкоз почек нередко диагносцируется лишь при выявлении эхинококкурии.
Осложнения при эхинококкозе встречаются часто (до 30%), иногда являясь первым клиническим проявлением заболевания. Нередки нагноения кисты (присоединение вторичной бактериальной инфекции при гибели эхинококка), сопровождающиеся усилением боли, лихорадкой, увеличением уровня лейкоцитов крови. Эхинококкоз легких может осложняться повторными легочными кровотечениями, острой сердечно-сосудистой недостаточностью. Наиболее грозным осложнением является разрыв кисты, который может быть спровоцирован ударом, поднятием тяжестей, грубой пальпацией.
При неосложненном эхинококкозе печени возможно медикаментозное лечение. При рецидиве или распространенном процессе показано оперативное лечение. Прогноз серьезный ввиду возможности развития угрожающих жизни осложнений.
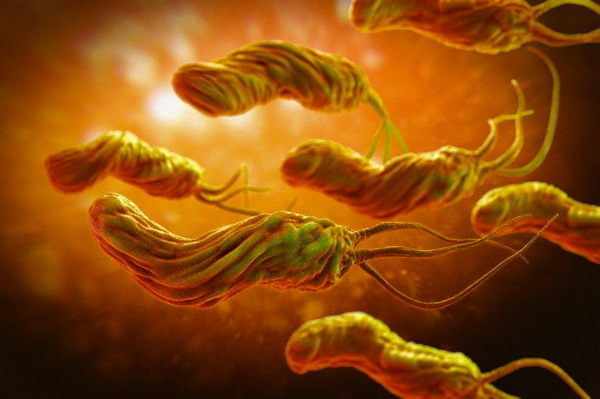
Helicоbacter pylori - грамотрицательная скрученная 5-образная бактерия. Одна из главных характеристик Н. pylori - ее способность производить большое количество уреазы. Данный микроорганизм существует под слоем желудочной слизи, где он защищен от кислой среды, создаваемой желудочным соком. Н. pylori играет важную роль в патогенезе гастрита и других заболеваний пищеварительной системы. Этот микроорганизм может повреждать эпителиальные клетки, вызывая воспалительные процессы, что при отсутствии соответствующего лечения способствует развитию хронического атрофического гастрита. У большинства больных в процесс вовлекается антральный отдел и тело желудка, постепенно развиваются атрофия желез, фиброзирование и кишечная метаплазия. Аутоиммунный механизм развития гастрита также инициируется хеликобактерной инфекцией.
Выявление специфических антител методом ИФА позволяет диагностировать заражение Н. pylori, связанное с гастритом, без гастродуоденоскопии. Получивший широкое распространение уреазный метод часто дает ложноположительные результаты вследствие возможного обсеменения биоптата слизистой оболочки желудка другими бактериями, обладающими уреазной активностью. Определение антител к Н. pylori является хорошим методом контроля эффективности лечения. Уровень антител определяется перед началом курса лечения и через 1-1,5 месяца после его окончания. Снижение уровня антител в крови больного или их исчезновение говорит об успешном лечении.

- Стадия локальной инфекции - развитие кожных реакций на участке кожи в месте присасывания иксодового клеща;
- Стадия диссеминации (распространения) боррелий по организму от места его первичного внедрения;
- Стадия органных поражений, как результат длительного патогенного воздействия возбудителей на органы и системы.
Часто органные поражения впервые выявляются у пациентов, которые в анамнезе не отмечали ни эритемы, ни факта укуса клеща, т.е. инфицирование прошло для них незаметно.
Кардинальные признаки боррелиозной инфекции
- основной признак: (псевдо) корешковые боли
- симптомы поражения ЦНС, обусловленные инфекционной интоксикацией (тошнота, нарушения сна, утомляемость);
- синдром хронической инфекционной интоксикации (постоянная слабость, повышении температуры тела, познабливание);
- неврологические дефициты
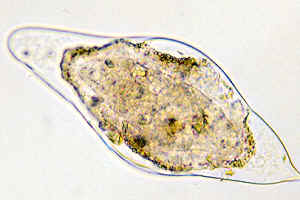
Шистосомозы — это гельминтозы, которые вызываются раздельнополыми трематодами. Промежуточными хозяевами являются моллюски, дефинитивным хозяином — человек. Одной из особенностей шистосом является то, что их взрослые особи паразитируют не в просвете кишечника, как большинство гельминтов, а преимущественно в венах мочевого пузыря, кишечника. Однако благодаря току крови они могут иметь и другую локализацию.
В сосудистом русле шистосомы откладывают яйца. Кровоток и спазм сосудов способствуют проникновению яйца через стенку сосуда и выходу его в окружающую ткань.
Источником шистосомоза является больной человек, выделяющий с испражнениями и мочой яйца гельминта, которые попадают в воду. Заражение происходит во время купания в водоемах, где имеются личинки шестосом – церкарии. Мочеполовым шистосомозом заражено более 39 млн человек. Кишечным шистосомозом заражено более 29 млн человек.
Все клинические формы шистосомозов характеризуются общностью патогенеза, одинаковой продолжительностью инкубационного периода и фазами развития болезни. В основе патогенеза шистосомозов лежат токсико-аллергические реакции как результат сенсибилизации организма продуктами жизнедеятельности и распада гельминтов, воздействие половозрелых паразитов и их личинок на ткани при их миграции, а также литические изменения тканей под воздействием ферментов, выделяемых паразитами в различных стадиях их развития. Различают шистосомоз мочеполовой, кишечный Менсона, кишечный интеркалатный и японский.
Помимо кишечника, печени и легких личинки аскарид проникают в мозг, глаза и другие органы. Они интенсивно питаются сывороткой крови и эритроцитами.
В период миграции личинок симптоматика заболевания обусловлена в основном аллергическими проявлениями. В кишечнике аскариды не прикрепляются, а удерживаются, упираясь своими концами в стенку кишки. Поэтому они весьма мобильны, могут спускаться и подниматься по ходу кишечника, проникать в желудок, а далее через пищевод и глотку — в дыхательные пути и даже лобные пазухи. Тяжелые проявления наступают при проникновении аскарид в печень, поджелудочную железу и другие органы.
В ранней фазе аскаридоза клинические проявления порой мало выражены. Иногда начало болезни проявляется с выраженного недомогания, появляется сухой кашель, иногда мокрота.
Поздняя (кишечная) фаза аскаридоза протекает с повышенной утомляемостью, изменением аппетита, тошнотой, иногда рвотой, болями в животе (в эпигастрии, вокруг пупка или в правой подвздошной области). У некоторых больных бывают поносы, у других запоры или их чередование.
Со стороны нервной системы при аскаридозе обычны головная боль, головокружение, повышенная умственная утомляемость. Наблюдаются беспокойный сон, ночные страхи. В некоторых случаях отмечаются изменения со стороны глаз — расширение зрачков, анизокория, светобоязнь, амблиопия. Со стороны сердечно-сосудистой системы у части больных аскаридозом отмечается снижение артериального давления.
Тохосага canis — нематода размером до 18 см, обычно паразитирующая у собак, волков, лисиц, песцов и других представителей семейства псовых, вызывающая заболевание с самой различной симптоматикой.
Основные пути заражения человека – контакт с загрязненной почвой и шерстью инфицированных животных. Заражение человека происходит при проглатывании инвазионных яиц токсокар. В проксимальном отделе тонкого кишечника из яиц выходят личинки, которые через слизистую оболочку проникают в кровоток.
Токсокароз - тяжёлое, длительное и рецидивирующее заболевание с полиморфизмом клинических проявлений, вследствие миграции личинок токсокар по различным органам и тканям. Личинки оседают в печени, лёгких, сердце, почках, поджелудочной железе, головном мозге, глазах и других органах и тканях.
При заражении большим количеством личинок обычно развивается висцеральная форма заболевания, проявляющаяся рецидивирующей лихорадкой, легочным синдромом, стойкой и длительной эозинофилией (до 80%), увеличением размеров печени, лимфаденопатией, гипергаммаглобулинемией, болями в животе, тошнотой, рвотой, диареей. У 32% больных заболевание сопровождается разнообразного типа высыпаниями на коже.
При заражении минимальным количеством личинок заболевание протекает субклинически, либо развивается глазной токсокароз. У детей заболевание проявляется косоглазием, снижением зрения, развитием гранулемы, кератита.
Риск передачи возбудителя плоду от матери, заразившейся в первом триместре беременности, равен 25%. Инфекция обычно приводит к самопроизвольным выкидышам, мертворождению или к серьезным заболеваниям плода. 75% младенцев, рожденных женщинами, которые были инфицированы в третьем триместре беременности, несут в себе скрытую (субклиническую) инфекцию, которая в конечном итоге (85% случаев) выливается в хориоретинит или неврологические осложнения.
В более старшем возрасте инфицирование может вызвать хроническое заболевание печени, неврологические нарушения и др. Для серодиагностики используют определение IgM- и IgG-антител. IgM-антитела обнаруживают при первичной инфекции или реактивации хронической. Токсоплазма - иммуносупрессирующий паразит, поэтому персистенция IgM у не прошедших лечения лиц может продолжаться многие месяцы. Количественное определение IgG помогает осуществлять контроль успешности лечения хронического токсоплазмоза. Возбудитель инфекции, Toxoplasтa goпdii, является широко распространенным паразитом. Инфицирование людей происходит при потреблении в пищу зараженного сырого мяса или при контакте с фекалиями, а также прямым путем через кровь при трансфузиях или внутриутробно у беременных.
Током крови аспергиллы могут заноситься в различные органы, образуя там специфические гранулемы, которые обычно абсцедируют. Из легочного аспергиллез превращается в генерализованный (септический) и нередко (свыше 50%) заканчивается гибелью больного.
- бронхолегочный аспергиллез;
- генерализованный (септический) аспергиллез;
- аспергиллез ЛОР-органов;
- аспергиллез глаза;
- аспергиллез кожи;
- аспергиллез костей;
- прочие формы аспергиллеза (поражение слизистых оболочек рта, гениталий, микотоксикозы)
Candida albicans — это типичный представитель дрожжеподобных грибов, находящихся в тонком кишечнике, половом тракте, полости рта, в пищеводе и гортани.
В норме существует баланс между Candida и другими бактериями и дрожжами в организме. Однако при определенных условиях возможно бурное размножение этого возбудителя, что приводит к ослаблению иммунитета и развитию инфекции, которая называется кандидоз.
Кандида может перемещаться по кровеносному руслу в различные части тела, в большинстве случаев — это полость рта, слуховой проход, полость носа, желудочно-кишечный тракт, влагалище. Поэтому кандидоз характеризуется разнообразными симптомами. Запоры, диарея, боли в животе, головные боли, затрудненное дыхание, литиаз, импотенция, нарушение памяти, зуд заднего прохода, нестабильность настроения, постоянная изжога, боли в мышцах и суставах, боли при глотании, постоянное подкашливание, чувство онемения на лице, конечностях, ощущение покалывания, акне, ночная потливость, выраженный зуд, заложенность придаточных пазух носа, чувство жжения в языке, белый налет на языке и в полости рта, выраженное ощущение усталости, инфекции влагалища, почек и мочевого пузыря, артриты, депрессия, снижение физической активности, снижение функции щитовидной железы, нарушение функции надпочечников и даже диабет.
Грибковая инфекция бурно размножается при ослаблении защитных функций организма. Кандидоз обычно возникает в определённые периоды: во время месячных, когда создаются благоприятные условия для роста грибков; в период овуляции при выработке гормона прогестерона, способствующего размножению грибков вообще и кандида в частности; во время беременности; при пользовании гормональными препаратами - будь то противозачаточные средства или стероиды; весной и летом в период обострения аллергии; во время применения антибиотиков, нарушающих обычные отношения микрообитателей нашего организма. Злоупотребление сладким, ожирение, нарушения в работе пищеварительной системы, страсть к узким синтетическим трусикам и сильно обтягивающим брюкам способствует развитию клинических признаков молочницы.
ВНИМАНИЕ. Рецидивирующая (частоповторяющаяся) молочница, не проходящая даже после неоднократных курсов лечения, свидетельствует о наличие половой инфекции.
В данной ситуации необходимо обратиться к специалисту (гинекологу или венерологу), и сдать анализы методом ИФА и ПЦР на основные заболевания, передающиеся половым путем.
- Alternaria tenius
- Aspergilus niger
- Aspergilus flavus
- Cladosporium herbar
- Penicillum tardum
- Penicillum expansum
- Rhizopus nigricans
- Candida albicans
- Candida kruzei
- Fusarium oxyspora
- Mucor pusillus
Определение ВСЕХ ПАРАЗИТАРНЫХ ИНФЕКЦИЙ проводится в условно-количественных единицах (с расчетом коэффициента позитивности для каждого показателя). Это дает возможность врачу четко отслеживать динамику процесса, объективно прогнозировать и оценивать эффективность проведенного лечения.
Читайте также:


