Опиаты-клиническая картина острого отравления
Основывается на характерной клинической картине(выявление кардинальных симптомов), реакции на специфическую(антидотную терапию), при возможности на данных анамнеза. При внутривенном введении опиатов могут быть обнаружены свежие следы по ходу подкожных вен. При пероральном приемевозможен коричневый налет у корня языка, при ингаляционном употреблении вероятно обнаружение следов порошка на губах или в носовых ходах.
Токсико-химическая диагностика. Определение алкалоидов опия в биологических жидкостях методами иммуноферментного анализа, в том числе экспресс-тестами (даже при терапевтических дозах), газовой хроматографии, совмещенной с масс-спектрометрией, жидкостной хроматографии высокого разрешения, тонкослойной хроматографии. Изолированное определение 6-моно-ацетилморфина - промежуточного метаболита героина, позволяет обнаружить прием этого вещества. Концентрации в крови различные. В моче морфин обнаруживается в течение48 часов,

Venena: опиаты – opiates - opiacés
кодеин в течение 72 часов. Синтетические опиаты, в частности метадон и бупренорфин, не дают перекрестных иммунохимических реакций с собст-
значение в диагностике
острых отравлений опиатами
имеет клиническая картина. Следует отметить, что кардинальные клини-
ческие признаки отравления опиатами(частота дыхательных движений в
минуту, степень угнетения сознания, размер зрачков) до и после введения
антидота или других средств, результаты токсико-химического исследо-
вания биологических сред на наличие опиатов должны быть тщательно
зафиксированы в направительных документах и в медицинской карте
стационарного больного (истории болезни). Указанные сведения имеют
особое значение для правильной диагностики и оценки эффективности
лечения, а также при экспертной оценке, в том числе правоохранитель-
ными органами. Диагноз острого отравления наркотическими вещества-
случаях тяжелого течения или
смертельного исхода, не-
редко приобретает отрицательное социальное значение и может быть абсолютной неожиданностью для родственников и близкого окружения больных, в связи с чем, возникает немало жалоб и судебных исков на правильность диагностики, обоснованность и адекватность лечебных мероприятий.
Целенаправленное выявление признаков позиционной компрессии мягких тканей (пальпация, измерение объема конечности). Ранним диагностическим признаком компрессии(до появления отека) может быть повышение в крови уровня ферментов(креатинкиназ, лактатдегидрогеназы, аспартатаминотрансферазы, аланинаминотрансферазы), миоглобинурия.
В случае смертельного исхода– судебно-медицинское исследование трупа (патоморфологическая диагностика и судебно-химическая экспертиза).
Дифференциальная диагностика
При отсутствии положительной реакции на антидот предполагаются: аноксическая энцефалопатия, черепно-мозговая травма, сочетанные интоксикации опиатами и этанолом, мепробаматом, фенотиазинами, барбитуратами и др., отравление психотропными веществами, фосфорорганическими соединениями (крайне тяжелой степени), отравление алкоголем с гипогликемией, отравление пресинаптическими a 2 -адреномиметиками (клонидин, гуанфацин и др.) или отравление морфиноподобными веществами, не отвечающими на обычные дозы налоксона(бупренорфин, декстропропоксифен). Нерезко выраженный миоз обнаруживают при соче-

Venena: опиаты – opiates – opiacés
танном отравлении с холинэргическими средствами(димедрол и др.) или при длительной церебральной аноксии. У лиц, употребляющих наркотические вещества, велика вероятность септического менингоэнцефалита.
В случае опийной интоксикации антидот действует очень быстро, в сравнимых дозах не оказывает никакого эффекта против медикаментов неопиоидного действия. При смешанных отравлениях опиатами и барбитуратами, алкоголем и другими веществами реакция на введение антидота может быть менее ярко выраженной, в зависимости от преобладающего в отравлении вещества.
Клиническую картину, сходную с отравлением опиатами, при отрицательном результате определения опиатов в моче, можно наблюдать при отравлении морфиноподобными веществами(метадоном, бупренорфином, декстропропоксифеном), морфиноподобными анестетиками (декстроморамид, фентанил).
Лечение
Острое отравление опиатами требует проведения неотложных мероприятий , осуществляемых на месте обнаружения больного, в машине скорой медицинской помощи, приемном и реанимационном отделениях больниц, специализированном токсикологическом отделении.
Налоксона гидрохлорид (Naloxone ® Narcan ® , Narcanti ® ) - продукт химической модификации молекулы морфинаспецифический, чистый антагонист опиатов (морфин и др.) и опиоидов (фентанила, декстропропоксифена, метадона, бупренорфина, нальбуфина), который применяется для полного или частичного устранения их действия, а также служит для диагностики при подозрении на острую передозировку этих соединений. Не оказывает никакого эффекта при угнетении дыхания, обусловленном другими причинами. При внутривенном введении налоксон быстро метаболизируется, метаболизм осуществляется в энтерогепатическом цикле: дезалкилирование с восстановлением6-кето-группы, глюкуронируется с образованием, в частности, 2-налоксон-глюкуронида. Элиминируется с мочой в чистом виде и в виде метаболитов (70% в течение 72 часов). Действие налоксона при внутривенном введении начинается через30 сек - 2-3 мин, при внутримышечном или подкожном введениичерез 3 мин.

Venena: опиаты – opiates - opiacés
Время полужизни в плазме составляет от45 до 90 мин. Продолжительность действия при внутривенном введении составляет от20 до 30 мин, при внутримышечном или подкожном введенииот 2,5 до 3 часов. Хорошо проникает через гематоэнцефалический(максимальная концентрация в структурах головного мозга достигается через15 мин, в 1,5 раза превышая плазматическую) и плацентарный барьеры.
В качестве начальной дозы вводят0,4-2 мг препарата(1,0-5,0) внутривенно. Обязательной реакцией на введение налоксона при отравлении опиатами является хотя бы кратковременное учащение дыхания, расширение зрачков, уменьшение степени угнетения сознания. Если желаемая степень антагонизации и улучшения дыхательных функций не достигается непосредственно после внутривенного вливания, то его можно повторять с интервалами в2-3 минуты. Отсутствие эффекта после 2-3 вливаний ставит под сомнение диагноз отравления опиатами. После введения (внутривенного, струйного) первичной дозы налоксона рекомендуется внутривенное капельное введение налоксона в дозе до2,4 мг (6,0) в 500 мл 5% р-ра глюкозы или0,9% р-ра натрия хлорида. Скорость инфузии определяется по реакции больного (рекомендуемая - 0,4 мг/30 мин).
Эффект от введения налоксона может быть непродолжительным, в связи с кратковременностью действия (30-45 мин), поэтому, в связи опасностью реморфинизации (повторное угнетение сознания и дыхания), да-
же после восстановления сознания необходимо наблюдение за больным (мониторинг дыхания и сознания) в течение 6-12 часов . Хоро-
ший пролонгированный поддерживающий эффект дает внутримышечное и подкожное введение налоксона.
Отсутствие достаточного эффекта от введения налоксона может быть обусловлено тяжелыми гипоксическими повреждениями головного мозга.
Несмотря на отсутствие доказанной причинно-следственной , связи указывается, что слишком быстрое введение налоксона у лиц, имеющих сердечное заболевание, может привести к артериальной гипотонии, отеку легких, вентрикулярной тахикардии, желудочковой фибрилляции, остановке сердца.
Для детей обычная начальная доза составляет0,01 мг/кг внутривенно, при необходимости введение продолжается. Существует специальная лекарственная форма для новорожденных (Narcan neonatal) , содержащая

Venena: опиаты – opiates – opiacés
При отравлении бупренорфином налоксон назначается(ограниченно) в дозе от 5 до 10 мг (эффект замедленный и частичный).
При отравлении метадоном налоксон вводят длительно(до 3 суток) с постепенным снижением дозы.
Угнетение дыхания при отравленииd-пропоксифеном требует введения больших доз налоксона.
При отравлении трамадолом налоксон применяется на протяжении 24 часов.
Коматозное состояние и угнетение дыхания при отравлении апоморфином устраняются налоксоном.
Симптомы отравления антидиарейными препаратами корригируются налоксоном.
Большие дозы налоксона способны вызвать опийный абстинентный синдром у лиц, злоупотребляющих наркотиками.
Налтрексон (Naltrexone hydrochloride), Antaxone ® - является спе-
цифическим антагонистом опийных рецепторов. Конкурентно связывается с опиоидными рецепторами всех типов и предупреждает или устраняет действие как эндогенных опиоидов, так и экзогенных опиоидных препаратов - наркотических анальгетиков и их суррогатов. Выпускается во флаконах, содержащих по 50 или 100 мг налтрексона гидрохлорида, в таблетках и в капсулах по50 мг. Сходен с налоксоном, но его действие более продолжительно. Время полусуществования в плазме налтрексона - 4 часа, а его метаболита 6- b -налтрексона - 13 часов. В дозе 50 мг блокирует фармакологические эффекты, вызванные внутривенным введением 25 мг героина в течение 24 часов, в дозе 100 мг - это действие удлиняется до 48 час, в дозе 150 мг - до 72 час. Применяется преимущественно для лечения опийной зависимости с целью поддержания у больного состояния, при котором опиоиды не смогут оказать характерного действия.
Налорфин (Nalorphine hydrochloride), Anarcon, Анторфин - по химическому строению близок к морфину. Модификация структуры привела к получению соединения, являющегося агонистом (анальгетическое действие) и антагонистом по отношению к опиатным рецепторам(ослабляет вызванное опиатами угнетение дыхания и снижение артериального давления, аритмии сердца). В качестве антидота применяется редко: его заменил налоксон. При отсутствии опиатов в организме может вызывать угнетение сознания и дыхания. Вводят внутривенно 0,5% раствора - 1-2 мл. При недостаточном эффекте инъекции повторяют через10-15 мин. Общая доза не должна превышать 8 мл.
2. Кислородотерапия. Искусственное дыхание с помощью маски или мешка Амбу, интубация трахеи, искусственная вентиляция легких, гипербарическая оксигенация (указывается на возможность выхода из

Рубрика: 6. Клиническая медицина
Дата публикации: 27.02.2018
Статья просмотрена: 389 раз
В данной работе отображены основные клинические особенности картины острых отравлений наиболее распространенными группами психоактивных веществами (ПАВ). Также представлена распространенность форм нарушения сознания, у лиц, различных возрастных групп, вызванная употреблением психоактивных веществ.
Ключевые слова: реанимация, токсикология, интоксикация, наркотики, психоактивные вещества.
Keywords: reanimation, toxicology, intoxication, drugs, hallucinogenic drug.
Произведенный анализ позволил выявить сохраняющуюся тенденцию нарушения сознания пациента, спровоцированную употреблением психоактивных веществам. В результате проведенных исследований, было выявлено, что среди всех факторов, вызывающих коматозное состояние человека, одним из наиболее преобладающих является именно фактор наркотической интоксикации, составляющий вместе с этиловой около 70 % от всех клинических случаев. Следует отметить тот факт, что практически все пациенты — люди трудоспособного возраста, и, следовательно, положение дел с необходимостью длительных дорогостоящих врачебных манипуляций — это не только неэффективное расходование бюджета здравоохранения Республики Беларусь, но и урон экономике страны в целом. Помимо финансовой стороны вопроса, немаловажным является тот факт, что длительность пребывания нарушения сознания на прямую влияет на вероятность осложнений со стороны общего здоровья и последующий выход на инвалидизацию. И напрямую влияет на объем затрачиваемых средств на пособия и пенсии по инвалидности.
Резюмируя вышеизложенное, можно констатировать, что сложившаяся ситуация, повышает требования к изучению проблемы диагностики неотложных состояний, вызываемых употреблением ПАВ. Ключевым моментом данного исследования является именно клинический анализ состояния пациента, так как современные виды наркотиков склонны к частому изменению химического состава, что затрудняет токсико-химическое определение их в биологических жидкостях.
Материалы и методы.
Анализируемый период включил в себя 73 факта оказания медицинской помощи пациентам с нарушенным сознанием на фоне отравления психоактивными веществами. Наиболее распространены следующие группы ПАВ: спайс, опиаты, каннабиноиды, амфетамин. Соотношение женщин и мужчин в данной группе пациентов — 7 человек (10 %) и 66 человека (90 %) соответственно. Возрастная ретроспектива представлена на рис. 1.
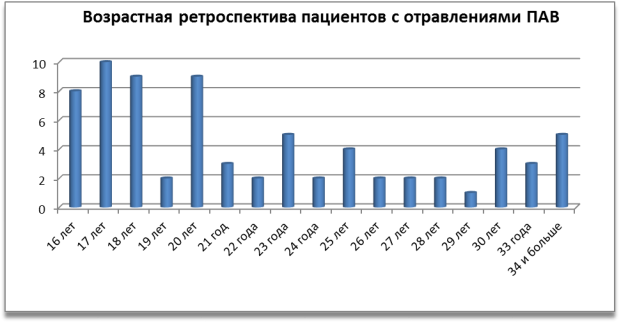
Рис. 1: Х — возраст пациентов, лет, У — численность пациентов, чел.
В тех случаях, когда не представляется возможным точно определить наименование вещества, вызвавшего острое отравление, диагноз ставят по ведущему клиническому синдрому. Таких синдромов 14: нарушение сознания, судорожные состояния, острое психотическое состояние, лихорадка, мидриаз, отек легких, центральное нарушение дыхания, экзотоксический шок, эксикоз, острая почечная или печеночная недостаточность, острая энцефалопатия, нарушения сердечного ритма и проводимости. Для пациентов с острыми отравлениями ПАВ основными синдромами являются: нарушение сознания (96 %), тахикардия (78 %), мидриаз (59 %), острое психотическое состояние (56 %).
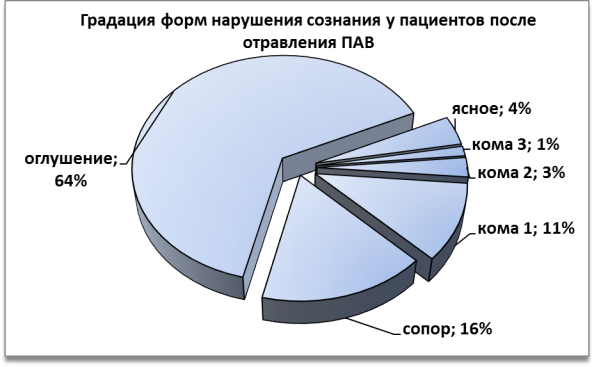
В соответствии с международными классификациями коматозных состояний, а также Приложением № 1 к приказу Министерства здравоохранения Республики Беларусь 18-XI 2008 № 1050 (форма № 0003/у-07) нарушения сознания делятся на 3 степени ком, оглушение и сопор. В настоящей работе сохранена указанная классификация с последующей детализацией по наиболее часто встречающимся клиническим признакам. На рис. 3 представлена градация частоты встречаемости указанных форм нарушения сознания, спровоцированная употребление ПАВ.
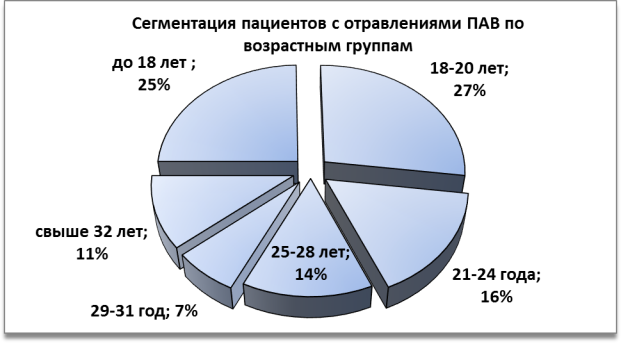
- Основная группа риска употребления ПАВ — молодежь в возрасте от 16 до 24 лет, при этом 25 % — несовершеннолетние. Наибольшую группу риска по проблематике алкогольных отравлений составляют лица работоспособного и репродуктивного возраста.
- Выявленная динамика крайне негативно сказывается на экономической и социально-демографической ситуации в Республике Беларусь.
- В клинической картине отравления ПАВ преобладают такие симптомы как: тахикардия, психомоторное возбуждение, тремор, расширение зрачков, атаксия, психоз, зрительные и слуховые галлюцинации, дезориентация. Соматические расстройства наблюдаются достаточно редко.
- Клиническая токсикология: Учебник. — 3–3е изд., перераб. и доп. — М.: Медицина, 1999. — 416 с.
- Е. А. Лужников. Экстремальная токсикология: руководство для врачей. — М.: ГЭОТАР — Медиа. — 2006. — 416 с.
- О. Г. Сыропятов, А. К. Напреенко, Н. А. Дзеружинская, О. В. Друзь, Н. Ю. Петрина. Неотложные состояния в наркологии: Учебное пособие. — Киев: Наук. Світ, 2013. — 53 с.
Употребление определенных веществ, способных изменять психическое состояние человека, практиковалось с древнейших времен. В разные эпохи у различных народов имелись свои предпочтения в выборе таких веществ, сегодня получивших название психоактивных (ПАВ)
Употребление определенных веществ, способных изменять психическое состояние человека, практиковалось с древнейших времен. В разные эпохи у различных народов имелись свои предпочтения в выборе таких веществ, сегодня получивших название психоактивных (ПАВ). Во всем мире, и наша страна не является исключением, употребление ПАВ (в ряде случаев при злоупотреблении разрешенными веществами — алкоголем, табаком, чаем, кофе и т. д.) остается острой и значимой проблемой.
Период эпизодического употребления ПАВ, по своей сути, представляет серию острых интоксикаций (отравлений), постепенно перетекающих в интоксикацию хроническую (табл. 1). Абсолютно предсказуемо, что в ряде случаев возможны тяжелые формы отравлений ПАВ, как правило — острых. Симптомы и тяжесть течения острых отравлений ПАВ напрямую зависят от вида, токсичности и дозы яда. Обычно при таких отравлениях требуются немедленная медицинская помощь и госпитализация в стационар токсикологического или реанимационного профиля.
В основе классификации всех острых отравлений (в том числе ПАВ) лежат нозологический, патогенетический и клинический принципы (рис. 1).
Нозологическая (этиологическая) классификация основана на названиях отдельных химических препаратов (кокаин), группы родственных веществ (опиаты) или целого вида химических соединений, одинаковых по происхождению (например, растительные или синтетические).
Перечень наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в РФ, приведен в таблице 2.
Таким образом, на современном этапе можно выделить 2 трактовки изучаемого явления: соматоневрологический, или общепатологический (терапевтический, неврологический, токсикологический), подход, согласно которому отравление рассматривается как интоксикация, наносящая вред всем органам и системам организма; психопатологический, или ментальный (психиатрический, наркологический), подход, когда то же явление рассматривается как опьянение.
Клиническая диагностика острых отравлений ПАВ основана на данных анамнеза и изучении клинической картины заболевания с применением лабораторных и инструментальных методов обследования больного. Последовательность оказания догоспитальной медицинской помощи пациентам с острыми отравлениями ПАВ схематично представлена на рисунках 2–4.
Чтобы быстрее обследовать больного и скорее приступить к лечебным мероприятиям, осмотр рекомендуется осуществлять в 3 этапа (рис. 4).
Отправной точкой для диагностики являются следующие симптомы доконтактной визуальной оценки состояния больного: размер зрачка, уровень изменения сознания, состояние кожных покровов и слизистых оболочек.
Исходя из ширины зрачка, отравления разделяют на условные группы: сужение зрачка — миоз; расширение — мидриаз; условная норма — без четкого изменения диаметра зрачка. Таким образом, предлагается начальный, отправной симптом.
Необходимо помнить, что в процессе развития отравления по мере углубления коматозного состояния и присоединения возможных осложнений перечисленные клинические критерии (в частности, диаметр зрачка) могут изменяться.
Например, возникшую в результате приема психоактивных веществ кому разделяют на осложненную и неосложненную. Неосложненная кома характеризуется непосредственным угнетающим влиянием токсического вещества на ткань мозга. Под осложненной комой чаще всего подразумевают присоединение токсического отека мозга, развивающегося по 2 механизмам: гидратация ткани мозга, за счет разности концентрации токсического вещества в нейронах и в окружающем пространстве; нарушение регионарного кровотока с образованием тромбов в микроциркуляторном русле в рамках ДВС-синдрома.
Таким образом, кома с отеком мозга может несколько изменять симптоматику, что объясняет некоторую вариабельность отдельных симптомов. Однако для обсуждения отдельных вариантов нужно хорошо представлять себе базовый симптомокомплекс.
После оценки состояния зрачка определяется уровень изменения сознания (угнетение или возбуждение). Особое внимание требуется уделить наличию судорог, как предвестников комы.
Для диагностики возможного эксикоза (что особо важно при отравлении стимуляторами ЦНС) и проведения дифференциального диагноза с патологией нетоксического характера надо оценить состояние слизистых оболочек и кожных покровов (сморщенная кожа, сухость слизистых оболочек ротовой полости и языка, сниженный тургор и т. д.).
Выявленная тетрада основных симптомов (оценка состояния зрачка, сознания, кожи и слизистых, а также наличие судороги) позволяет предварительно предположить отравление веществами, которые можно разделить на следующие группы: миоз с угнетением сознания (табл. 4) — опиаты, этанол; барбитураты и бензодиазепины; мидриаз с возбуждением (табл. 5) — кокаин, гашиш, амфетамин и его производные, ЛСД, грибы-галлюциногены; без четкого изменения диаметра зрачка и возбуждения (табл. 6) — фенциклидин.
При анализе клинической картины отравления психоактивными веществами важно выявить еще 8 симптомов (табл. 4–6).
На догоспитальном этапе лабораторная диагностика обычно ограничивается взятием биосред (надо указать время взятия биосред и данные пострадавшего) и полуколичественной оценкой уровня гликемии, глюкозурии, кетонурии. Вещественные доказательства (жидкости в бутылках, упаковки из-под лекарств, записки) необходимо собрать, так как они имеют не только медицинскую, но и юридическую ценность. При подозрении на острое отравление наркотическими веществами значительно облегчить диагностику могут иммунохроматографические экспресс-тесты на наличие ряда таких веществ в моче или слюне.
При проведении анализа следует надевать одноразовые резиновые или пластиковые перчатки, так как исследуемые образцы мочи могут содержать возбудителей инфекций.
Техника проведения анализа следующая. В чистую сухую емкость помещают исследуемый образец мочи таким образом, чтобы уровень ее не превышал 1-1,5 см. Затем вскрывают упаковку полоски (разорвать вдоль прорези), а извлеченную полоску погружают вертикально тем концом, на котором обозначены стрелки, в мочу до уровня ограничительной линии на 30–60 с. Извлеченную из мочи тест-полоску следует положить на ровную, чистую, сухую поверхность и по истечении 5 мин визуально оценить результат реакции.
Интерпретация исследования крайне проста, выявление 2 параллельных розовых полос свидетельствует об отрицательном анализе, выявление же только одной розовой полосы в контрольной зоне подтверждает положительный результат.
При отсутствии полос в течение 5 мин пробу следует повторить с помощью новой полоски.
Возможности экспресс-тестов отражены на упаковке. Каждая полоска позволяет определить в моче наличие одного ПАВ. Например, положительную реакцию при тестировании дают: при определении опиатов и/или их метаболитов — родственные морфину соединения: этилморфин, гидроморфон, мерперидин, морфин-3-глюкуронид, героин. При помощи данной методики можно выявлять оговариваемую концентрацию иных наркотических веществ, их метаболиты, а также структурно-родственные соединения таких средств, как метадон, барбитураты, бензодиазепины, каннабиноиды, РСР, амфетамины и др.
В тех случаях, когда не представляется возможным точно определить наименование вещества, вызвавшего острое отравление, диагноз ставят на основании ведущего клинического синдрома, представленного в таблице 7.
Последовательность лечебных мероприятий при острых отравлениях (в том числе ПАВ) схематично представлена на рисунке 5.
Промывание желудка через зонд наиболее эффективно в первый час отравления, поэтому если больного невозможно сразу же госпитализировать, эту процедуру производят на месте отравления.
Для предотвращения аспирации рвотных масс в дыхательные пути и предупреждения повреждения легких промывание желудка проводят после предварительной интубации трахеи трубкой с раздувной манжеткой. Больным, находящимся в бессознательном состоянии (например, при тяжелых отравлениях снотворными препаратами), промывания повторяют 2–3 раза в течение первых суток с момента отравления. Это необходимо, поскольку при коме резко замедляется всасывание токсического агента, и в желудочно-кишечном тракте обычно депонируется значительное количество невсосавшегося вещества. Кроме того, некоторые вещества (морфин, бензодиазепины) выделяются слизистыми оболочками желудка, а затем вновь всасываются. Наконец, находящиеся в складках слизистых оболочек желудка таблетированные лекарственные препараты могут не растворяться в течение длительного времени.
После промывания в качестве слабительного средства с целью ускорения выделения содержимого кишечника в желудок вводят 100–150 мл 30% раствора сульфата натрия или сульфата магния (при отравлениях водорастворимыми ядами) либо 100 мл вазелинового масла (при отравлениях жирорастворимыми ядами).
Адсорбцию находящихся в желудочно-кишечном тракте ТВ проводят активированным углем внутрь. Взвесью активированного угля (2–4 столовые ложки на 250–400 мл воды) промывают желудок, уголь вводят через зонд до и после промывания в виде кашицы (1 столовую ложку порошка или 5–10 таблеток — 50–100 мг активированного угля растворяют в 5–10 мл воды). Возможна очистительная клизма.
Если ТВ были введены в полость организма, их также промывают прохладной водой или сорбентами с помощью клизмы или спринцевания.
Для удаления из организма всосавшегося яда уже на догоспитальном этапе проводят детоксикацию организма. Основной метод детоксикации — форсирование диуреза, включающего 3 этапа: предварительную водную нагрузку; внутривенное введение мочегонных средств; заместительное введение растворов электролитов.
Параллельно определяют: почасовой диурез путем постановки мочевого катетера; концентрацию ТВ в крови и моче; содержание электролитов в крови; гематокрит (соотношение форменных элементов и плазмы крови).
Противоядия (антидоты) рекомендуется использовать как можно раньше, поскольку они непосредственно влияют на действие и метаболизм попавшего в организм ТВ, его депонирование или выведение и тем самым ослабляют действие яда.
Выделяют 4 группы специфических противоядий, из которых для купирования отравлений ПАВ обычно применяют лишь 2 первых: химические (токсикотропные); фармакологические (симптоматические); биохимические (токсикокинетические); антитоксические иммунопрепараты.
В основе действия фармакологических противоядий лежит фармакологический антагонизм веществ (например, аминостигмина и атропина или других холинолитиков, налоксона и опиатов, флумазенила и бензодиазепинов).
Таким образом, именно фармакологические антидоты составляют наиболее значимую группу медикаментозных препаратов для лечения острых отравлений ПАВ, из которых наибольшего внимания требуют налоксон, флумазенил, а также аминостигмин и ему подобные средства.
Налоксон (наркан, нарканти) — полный антагонист опиатных рецепторов. Выпускается в ампулах по 1 мл раствора — 0,04% (0,4 мг/мл), 0,1% (1 мг/мл), а также для новорожденных — 0,002% (0,02 мг/мл). Препарат вытесняет опиаты из специфичных рецепторов, быстро восстанавливает угнетенное дыхание и сознание и поэтому особо показан на догоспитальном этапе даже при невозможности интубации трахеи и искусственной вентиляции легких. Предпочтительнее (для достижения мгновенного эффекта) вводить налоксон внутривенно струйно, на изотоническом растворе хлорида натрия (однако возможно раздельное или комбинированное его введение — подкожное, внутримышечное или эндотрахеальное) в начальной дозе 0,4–0,8 мг. Затем дозу подбирают методом титрования, максимальная доза налоксона — 10 мг.
Продолжительность антагонистического действия налоксона составляет 30–45 мин, поэтому при ухудшении состояния может потребоваться его дополнительное введение. В ряде случаев после достижения терапевтического эффекта целесообразно закрепить результат внутримышечным или внутривенным капельным введением дополнительной дозы 0,4 мг.
При длительном пребывании больного в состоянии тяжелой гипоксии или возможной аспирации (признаки рвоты), а также введении налоксона можно получить нежелательный эффект в виде выраженного психомоторного возбуждения и отека легких через 30–60 мин. Поэтому в таких случаях введению налоксона должны предшествовать интубация трахеи (после премедикации атропином) и искусственная вентиляция легких.
Если введение налоксона обеспечивает улучшение или восстановление самостоятельного дыхания и повышение уровня сознания, это свидетельствует об отравлении ПАВ (героином, алкоголем, фенциклидином, есть литературные сведения об эффективности при отравлении барбитуратами и даже бензодиазепинами). Скорее всего, этот список неокончательный. Отсутствие эффекта от введения налоксона дает основание искать другую причину угнетения сознания и дыхания или сопутствующую патологию.
Флумазенил (анексат, мазикон, ромазикон) — антагонист бензодиазепиновых рецепторов — применяется у больных с тяжелым отравлением препаратами бензодиазепинового ряда. Антидот выпускается в виде 0,01% раствора (0,1 мг/мл) и вводится внутривенно струйно в дозе 0,3–0,5 мг на изотоническом растворе натрия хлорида; при отсутствии положительного эффекта (восстановление сознания) в течение нескольких минут введение можно повторить в той же дозе. Специфичность действия позволяет использовать анексат с дифференциально-диагностической целью. Максимальная разовая доза составляет 2 мг. Противопоказаниями для использования препарата являются сочетанные отравления бензодиазепиновыми производными и трициклическими антидепрессантами, а также случаи передозировки бензодиазепинов у больных эпилепсией.
При отравлениях, вызванных ПАВ с холинолитическим действием (к которым относятся нейролептики, трициклические антидепрессанты, антигистаминные), в качестве антидота применяют ряд антихолинэстеразных средств, предшественником которых является всем хорошо известный физостигмин (эзерин). К таким противоядиям относятся галантамин и аминостигмин.
Галантамина гидробромид (нивалин) является препаратом короткого действия, применяется в виде 0,5% раствора и вводится внутривенно по 4–8 мл.
Аминостигмин — антидот длительного действия — вводится внутримышечно по 1-2 мл в виде 0,1% раствора.
Первые 2 антидота (налоксон и флумазенил) используются в схеме лечения коматозных состояний (рис. 6).
Таким образом, применение фармакологических противоядий на догоспитальном этапе является важным и необходимым лечебно-диагностическим мероприятием, позволяющим повысить качество оказания неотложной помощи, сократить число выездов бригад СМП и госпитализаций.
По вопросам литературы обращайтесь в редакцию.
В. Г. Москвичев, кандидат медицинских наук
И. В. Духанина, кандидат медицинских наук
А. Л. Верткин, доктор медицинских наук, профессор
МГМСУ, ННПОСМП, Москва
Читайте также:


