Изменение миокарда при отравлениях
Полный текст:
1. Элленхорн М. Дж.
2. Лужников Е. А., Суходолова Г. И.Клиническая токсикология. М.: Медицина; 2008.
3. SnookС. P., Sigpaldason K., Kristinsson J.Severe atenalol and diltiazem overdose. J. Toxicol. Clin. Toxicol. 2000; 38 (6): 661—665.
5. Моисеев В. С., Киякбаев Г. К.Проблема классификации кардиомио-патий. Кардиология 2009; 49 (1): 65—70.
6. Мартынов А. И.Интенсивная терапия. М.: ГЭОТАР-Медицина; 1998.
7. Стародубцев А. К., Архипова Д. Е., Сычев Д. А.Функциональные изменения /3-адренорецепторов миокарда у больных с хронической сердечной недостаточностью. Эксперим. и клин. фармакология 2005; 68 (6): 59-66.
8. Desjars P., Pinaud M., Potel G. et al.A reappraisal of norepinephrine therapy in human septic shock. Crit. Care Med. 1987; 15 (2): 134—137.
9. Yuan T. M., Kerns W. P., Tomaszewski C. A. et al.Insulin-glucose as adjunctive therapy for severe calcium channel antagonist poisoning. J. Toxicol. Clin. Toxicol. 1999; 37 (4): 463—474.
10. Яцинюк Б. Б.Методика катетеризации яремной вены и техника измерения центрального венозного давления у крыс. В кн.: Фундаментальные науки — практике здравоохранения. Омск; 2001.
11. Карпицкий В. В., Словесное С. В., Рерих Р. А.Определение сердечного выброса у мелких лабораторных животных методом тетрополярной реографии. Патол. физиология и эксперим. терапия 1986; 1: 74—77.
12. Фархутдинов Р. Р., Лиховских В. А.Хемилюминесцентные методы исследования свободно-радикального окисления в биологии и медицине. Уфа; 1998.
13. Гланц С.Медико-биологическая статистика. М.; 1998.
14. Архипенко Ю. В.Повышение резистентности мембранных структур сердца, печени и мозга при адаптации к периодическому действию гипоксии и гипероксии. Бюл. эксперим. биологии и медицины 2005; 140 (9): 257—260.
15. Афанасьев В. В.Неотложная токсикология. М.: ГЭОТАР-Медиа; 2009.
16. Долгих В. Т.Повреждение и защита сердца при острой смертельной кровопотере. Бюл. СО РАМН 2001; 1: 73—81.
17. Корпачева О. В., Долгих В. Т.Изменение основного энергетического субстрата как способ защиты миокарда от ишемического повреждения при экспериментальной механической травме сердца. Патол. физиология и эксперим. терапия 2008; 4: 16—18.
18. Шейх-Заде Ю. Р., Галенко-Ярошевский П. А., Чередник И. Л.Фибрилляция предсердий: новое объяснение старого явления. Бюл. эксперим. биологии и медицины 2002; 134 (7): 4—8.
19. Pereska Z.QT-marker of poisoning severity after acute exposure to anticholinesterase insecticides. [EUROTOX 2001, Istanbul, 13-16 Sept., 2001]. Toxicol. Lett. 2001; 123 (1): 96.
20. Кечкер М. И.Руководство по клинической кардиографии. М.; 2000.
21. Сазонтова Т. Г., Архипенко Ю. В.Значение баланса прооксидантов и антиоксидантов — равнозначных участников метаболизма. Па-тол. физиология и эксперим. терапия 2007; 3: 2—18.
22. Garbe T. R., Yukawa H.Common solvent toxicity: autoxidation of respiratory redox-cyclers enforced by membrane derangement. Z. Naturforsch. C. 2001; 56 (7—8): 483—91.
23. Ласукова Т. В., Арбузов А. Г., Маслов Л. Н. и соавт.ЭкстрактGanodermalucidumпри диастолической дисфункции сердца и возникновение необратимых повреждений кардиомиоцитов в условиях ишемии и реперфузии изолированного сердца. Патол. физиология и эксперим. терапия 2008; 1: 22-25.
24. Афанасьев С. А., Роговская Ю. В., Фалалеева Л. П. и соавт.Сравнительная оценка ремоделирования сердца крысы после экспериментального стеноза коронарной артерии и криодеструкции. Бюл. экс-перим. биологии и медицины 2009; 147 (6): 631—634.
25. Бояринов Г. А., Григорьев Е. В., Плотников Г. П. и соавт. Медикаментозная профилактика реперфузионных повреждений при тром-болитической терапии инфаркта миокарда. Общая реаниматология 2010; VI (1): 64—68.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
УДК 340.6_615.015.6_615.099.091
Ю.С. Исмаилова, А.Ж. Алтаева, А.Н. Бекишева,
Б.Ж. Анаятова, С.Г. Умбеталиев, Н.В. Селивохина
Казахский Национальный Медицинский Университет
им. С. Д. Асфендиярова. Кафедра патологической анатомии.
Министерства здравоохранения Республики Казахстан
В статье представлены результаты морфологических изменений миокарда лиц, умерших от хронической наркотической интоксикации морфином. Аутопсийное исследование при судебно-медицинской экспертизе выявило в миокарде морфологические признаки токсического влияния наркотика. Отмечены выраженные расстройства кровообращения, очаговое повреждение кардиомицитов с наличием контрактур и очагов миоцитолизиса, признаки гипертрофии и атрофии кардиомиоцитов. Характерным признаком являлся некоронарогенный кардиосклероз.
Ключевые слова: судебно-медицинская экспертиза, хроническая наркотическая интоксикация, патоморфология миокарда.
Проблемы заболеваемости и смертности от наркомании актуальны как для врачей наркологов (токсикологов), так и для судебно-медицинских экспертов, так как по данным токсикологического отделения ГБСНП города Алматы прогрессирует количество не смертельных отравлений наркотиками, а также летальных исходов от острого отравления наркотическими веществами [1]. В судебно-медицинской экспертизе количество случаев смертельных отравлений наркотическими веществами, особенно морфином, ежегодно увеличивается в структуре насильственной смерти [2, 3].
В практической работе судебно-медицинских экспертов возникают ситуации, при которых предполагаемое на аутопсии отравление наркотическим веществом не подтверждается при последующем химико-токсикологическом исследовании. Поэтому важное значение имеют результаты судебно-гистологического (патоморфологического) исследования, выявляющие патологические изменения органов, свидетельствующие об интоксикации наркотическими веществами [4].
При хронической наркотической интоксикации поражаются все органы и системы, в том числе и сердечнососудистая система. Поэтому патоморфологические изменения в нём оказывают непосредственное влияние на вариант танатогенеза, а также позволяют установить непосредственную причину смерти и длительность употребления наркотиков. Вопрос экспертной оценки патоморфологических изменений миокарда при интоксикации морфином с учетом возраста потерпевших остается актуальным до настоящего времени [5, 6, 7].
Целью нашей работы являлось изучение патоморфологических изменений миокарда у лиц молодого возраста, умерших от острого отравления морфином на фоне хронической наркотической интоксикации.
Материал и методы исследования. Объектами исследования были 142 сердца, изъятые при проведении судебно-медицинских экспертиз у умерших от отравления морфином, в возрасте от 15 до 30 лет, при жизни страдавших наркотической зависимостью. На аутопсии из различных отделов сердца брали кусочки миокарда (правое и левое предсердие, межпредсердная перегородка, правый и левый желудочек, межжелудочковая перегородка, верхушка), маркировали и фиксировали в 10 % растворе нейтрального формалина. Парафиновые срезы окрашивали гематоксилином и эозином, пикрофуксином по Ван Гизону, фуксином на эластические волокна по Вейгерту, по Маллори. Окрашенные срезы исследовали в проходящем свете в мультиголовочном микроскопе Axio Zeiss A1 и в поляризованном свете микроскопа Leica DM 750Р.
1 Тойбаев Г. М. Токсикологическая ситуация по г. Алматы в период времени с 1999 по 2010 года // Вестник КазНМУ. – Алматы: — 2012. — (выпуск посвященный 1-й годовщине БСНП г. Алматы) — С. 76-85.
2 Поданева В. И., Абдраимов М. А., Жунисов С. С., Райымбердиева Ж. Ш. Анализ смертельных отравлений в г. Алматы за 1996-1999гг., //Судебная медицина в Казахстане. – Алматы: — 2003. — № 7. — С. 40-41.
4 Пиголкин Ю.И., Должанский О. В., Голубева А. В. Судебно-медицинская диагностика хронической наркотической интоксикации по морфологическим данным // судебно-медицинская экспертиза. – М.: — 2012. — №1. — С. 34-37.
5 Hantson P., Beauloye C. Myocardial metabolism in toxin-induced heart failure and therapeutic implications // Clin. Toxicol (Phila). — 2012 Mar. — 50(3):166-71.
6 Kul´bitskiĭ B.N., Larev Z.V., Fedulova M.V., Denisova O.P., Bogomolov D.V. Pathology of the heart conducting system in the thanatogenesis of sudden death from alcoholic cardiomyopathy and coronary heart disease // Sud.med.ekspert. — 2012 Mar.-Apr. — 55(2):62-5.
7 Bogomolova I.N. Bogomolov D.V. Shpekht Dlu., Kul´bitskiĭ B.N. The characteristic morphological changes of the internal organs in certain forms of combined poisoning. Sud.med.ekspert. — 2012. 55 (2). – P.18-21.
Ю.С. Исмаилова, А.Ж. Алтаева, А.Н. БекІшева,
Б.Ж. Анаятова, С.Г. Умбеталиев, Н.В. Селивохина
Опий есірткімен созылмалы улану кезіндегі миокардтағы
Түйін: Мақалада морфинмен созылмалы улану нәтижесінде өлген адамдардың миокардындағы морфологиялық өзгерістерді зерттеу нәтижелері берілген. Аутопсиялық материалды сот-медициналық сараптау кезіндегі миокардта есірткі әсерінен дамитын морфологиялық өзгерістер көрсетілді. Нақтылап айтқанда қан айналымының ерекше бұзылыстары, кардиомиоциттердің ошақты бұзылыстары, контрактуралық өзгерістері, ошақты миоцитолизі, гипертрофиялық немесе атрофиялық өзгерістері табылды. Коронарогендік емес кардиосклероздың дамуы осы жағдайларға тән белгі деп қарастыруға болады.
Кілт сөздер: сот-медициналық сараптау, морфинмен созылмалы улану, миокард патоморфологиясы
Y.S. Ismailova, A. Zh. Altayeva, A.N. Bekisheva,
B. Zh. Anayatova, S. G. Umbetaliev, N.V. Selivohina
Morphological changes of myocardium at chronic drug intoxication
Resume: The article presents the results of morphological changes of myocardium of people who died because of the chronic narcotic intoxication. The autopsy researches of forensic medical evaluation revealed the morphological indications of toxic influence in myocardium. Clear blood circulation disorders, focal damage of myocardium cells with contractures and myocytolysis along with hypertrophy and atrophy of myocardium cells have been observed. Non-coronary sclerosis is shown as a characteristic feature.
Keywords: forensic medicine expert operation, chronic narcotic intoxication (poisoning), myocardium patomorphology.
Рисунок 1 — Контрактурная дегенерация кардиомиоцитов при острой наркотической интоксикации.
Окраска гематоксилин и эозин.
Микроскопия в проходящем свете
Рисунок 2 — Диапедезные кровоизлияния в миокарде острой наркотической интоксикации.
Микроскопия в проходящем свете
Рисунок 3 — Сетчатый кардиосклероз с компенсаторной гипертрофией кардиомиоцитов при хронической наркотической интоксикации
Окраска пикрофуксином по ван Гизон. Увеличение Х100
Микроскопия в проходящем свете
Рисунок 4 — Нарушение тинкториальных свойств кардиомиоцитов при острой интоксикации

Кафедра судебной медицины и кафедра патологической анатомии Рязанского медицинского института им. И.П. Павлова
УДК 615.917:547.262] .07:616.127-091-07
PATHOMORPHOLOGIC ALTERATIONS IN THE MYOCARDIUM IN ALCOHOLIC INTOXICATION
A study of 25 cases. Severe dystrophic, dyscirculatory, and destructive changes were demonstrated. Author suggests that even small amounts of alcohol in patients with cardiovascular diseases may hamper the compensatory process and play the role of the direct cause of death.
библиографическое описание:
Патоморфология сердечной мышцы при алкогольной интоксикации / Казанцева Г.П. // Судебно-медицинская экспертиза. — М., 1975. — №1. — С. 24-28.
код для вставки на форум:
Известно, что алкоголь является сильнейшим цитотоксическим ядом, вызывающим -грубые морфологические и функциональные изменения внутренних органов. По сведениям В.Н. Александровского и Г.С. Галкиной (1970), С.Г. Вайнштейна и соавт. (1970), Streian и соавт. (1971) и др., алкогольное отравление сопровождается различными изменениями со стороны сердечно-сосудистой системы (нарушения ритма сердца, остановка сердца, ишемический синдром, падение артериального давления). Особенно отчетливо эти нарушения выявляются у людей, страдающих атеросклерозом или гипертонической болезнью, хотя ряд исследователей наблюдали развитие острой коронарной недостаточности и инфаркта миокарда после приема алкоголя на фоне интактных коронарных сосудов (О.И. Глазова и В.В. Новосельская, 1964; В.А. Шакуль и А.Н. Кишиневский, 1967; В.А. Кононяченко, 1967).
Учитывая важность кардиальных нарушений в клинике алкогольной интоксикации, мы поставили задачу исследовать влияние этанола на морфологическую структуру миокарда в плане изучения механизма развития этих изменений и танатогенеза скоропостижной смерти после приема алкоголя.
Исследовали 25 случаев смертельного отравления алкоголем. В 8 наблюдениях обнаружен коронарокардиосклероз на фоне общего атеросклероза или гипертонической болезни. В качестве контроля использовали случаи железнодорожной и черепно-мозговой травмы, повешения и утопления при отсутствии алкоголя в крови.
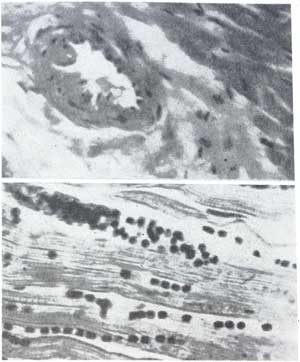
Рис. 1. Утолщение и деструкция стенки
межмышечной артерии со слущиванием
эндотелия в просвет сосуда. В отечном
периваскулярном пространстве скопление
лейкоцитов и мононуклеаров.
Окраска гемотоксилин-эозином.
Ув. 140Х.
Выраженное капиллярное полнокровие
с явлениями стаза.
Окраска по Маллори. Ув. 200 X.
В изученных случаях отравления концентрации алкоголя в крови и моче колебались (в пределах 3—5 мг%, а их соотношение соответствовало стадии элиминации или диффузионного равновесия.
Гистологически исследовали кусочки из различных отделов сердца (верхушка, боковая и задняя стенки левого желудочка, перегородка, правый желудочек), а также из других внутренних органов для общей характеристики наблюдений. После фиксации в 10% нейтральном формалине и по Шабадашу готовили парафиновые и замороженные срезы, которые окрашивали гематоксилин-эозином, по Селье, Маллори, гистохимически выявляли нейтральные и кислые мукополисахариды, гликоген, свободные NH2-группы и липиды.
При исследовании сердца в случаях алкогольного отравления обращала на себя внимание выраженная патология со стороны мелких интрамуральных сосудов (рис. 1) — просвет их сужен, стенки набухшие, гомогенизированы либо разрыхлены, со слущиванием эндотелия в просвет и вакуолизацией мышечных элементов. Местами наблюдалось неравномерное утолщение сосудистой стенки с накоплением кислых мукополисахаридов, которые при окраске срезов толуидиновым синим или тионином дают гамма-метахромазию. В периваскулярном пространстве встречались небольшие кровоизлияния, лимфостазы, скопление лимфоцитов и мононуклеаров, белковой жидкости, отмечался отек межуточной ткани. Набухание и разрыхление стенок с очаговой гамма-метахромазией при окраске толуидиновым синим и вакуолизацией мышечных элементов наблюдались со стороны крупных коронарных сосудов миокарда и эпикарда. Вокруг сосудов и между мышечными волокнами отмечалось разрастание соединительной ткани. При сопутствующих соматических заболеваниях, сопровождающихся коронарокардиосклерозом, явления склероза сосудов эпикарда и миокарда были ярче выражены, встречались довольно крупные поля фиброза. Во всех случаях отравления алкоголем, как показано на рис. 1, выраженное полнокровие с расширением всех капилляров, явлениями стаза и мелкими кро
воизлияниями в одних отделах сердца сочеталось с запустением сосудов в других.
Значительные морфологические изменения наблюдали и со стороны мышечных волокон. Толщина их неравномерная, гипертрофированные волокна чаще встречались вокруг склерозированных сосудов. Саркоплазма мышечных волокон неравномерно воспринимала красители:
можно было видеть участки оксифильные, базофильные и бледные, почти не окрашенные эозином. Реакция с нингидрин-реактивом Шиффа характеризовалась неравномерностью окраски на свободные NH2-группы в различных мышечных волокнах и в пределах одного волокна. Поперечная исчерченность сохранилась лишь частично, а в большинстве мышечных волокон отсутствовала. Саркоплазма таких клеток набухшая, гомогенизирована, дает яркую ШИК-положительную реакцию. Скопление волокон, претерпевающих некробиотичеокие изменения, чаще отмечалось вокруг дилатированных вен, там же обнаруживались клетки с явлениями кариолизиса и глыбчатого распада саркоплазмы (рис. 2). В очагах некробиоза и коагуляционного некроза мышечных волокон отмечалось скопление лейкоцитов. Часто встречались волокна в состоянии сегментации и фрагментации. При сопутствующих коронарокардиосклерозе и гипертонической болезни этот процесс захватывал обширные поля. Встречались мышечные волокна на различных стадиях колликвационного некроза: ядро отсутствует, протоплазма светлая, заполнена вакуолями (рис. 3). На месте погибших волокон, а также вокруг сосудов отмечалось разрастание соединительной ткани.
Ядра мышечных волокон имели различную форму и величину: мелкие, пикнотичные и крупные, вакуолизированные, с бледной кариоплазмой. В некоторых волокнах отмечались ядра с перераспределением хроматинового вещества по спирали, а в истонченных волокнах изредка встречалось явление атрофической пролиферации ядер. В саркоплазме в перинуклеарной области отмечалось отложение мелкозернистого липофусцина. В миокарде пожилых людей липофусцина было больше, и он приобретал бурый оттенок.
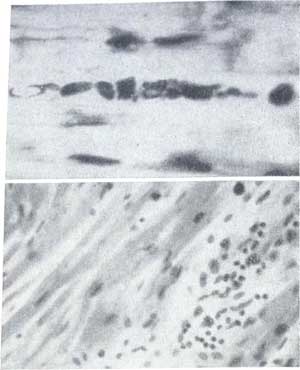
Рис. 2. Глыбчатый распад ШИК-гомогенной
субстанции некротизированного волокна.
Окраска по Гочкисс. Ув. 200X.
Разрушение некротизированных мышечных
клеток клетками инфильтрата.
Окраска гематоксилин-эозином. Ув. 120Х
При обработке срезов по методу Селье наблюдалась распространенная фуксинофилия мышечных волокон во всех отделах миокарда. Отмечалась очаговая фуксинофилия миофибрилл, набухших вставочных пластин, гомогенных участков саркоплазмы. Часто фуксинофилия распространялась на весь сегмент или захватывала несколько мышечных сегментов. Скопление фуксинофильных волокон отмечалось под эпикардом, эндокардом, вблизи дилатированных сосудов. Гомогенная фуксинофилия или оранжефилия при окраске по методу Селье отмечалась в мышечных волокнах, претерпевающих некробиотические изменения. В этих же волокнах наблюдалась яркая ШИК-положитель-ная реакция в параллельных срезах. Периваскулярные и межмышечные коллагеновые волокна окрашивались местами в малиновый или фиолетовый цвет. Окраска по Маллори характеризовалась менее распространенной оранжефилией мышечных волокон.
При окраске Суданом черным местами в межмышечных прослойках отмечалось скопление жировой ткани. Ожирение сердца с постоянством наблюдалось в правом желудочке. Многие мышечные волокна содержали капли свободных липидов.
Таким образом, во всех случаях алкогольного отравления наблюдали однотипные патоморфологические изменения со стороны сердца. Выражены дизорические расстройства и деструктивные изменения в стенках сосудов, что сопровождается повышением сосудистой проницаемости, образованием экстравазатов, скоплением белковых масс в периваскулярном пространстве и огрубением стромы миокарда при хроническом употреблении алкоголя. Описанные изменения обусловливают коронарную недостаточность миокарда. Надо полагать, что не менее важным в механизме развития дистрофических изменений мышечных волокон является прямой гистотоксический эффект этанола, так как известно, что алкоголь легко проникает через клеточные мембраны и нарушает внутриклеточной метаболизм. Повреждение мышечных волокон сердца выражается в изменении тинкториальных свойств саркоплазмы, потере поперечной исчерченности, деструкции ядер, обеднении гликогеном, липофаперозе. Неравномерность окраски мышечных волокон на NH2-группы, гомогенная фуксинофилия и оранжефилия при реакциях Селье, Маллори свидетельствуют о глубоком повреждении с денатурацией и нарушением структурной организации молекул миозина (Ю.Л. Сутулов, 1967). Значительное количество мышечных клеток находится в состоянии фрагментации, некробиоза и коагуляционного или колликвационного некроза. В случаях с сопутствующими соматическими заболеваниями дистрофические изменения мышечных волокон были глубже и обширнее, ярче выражались явления склероза в сердце.
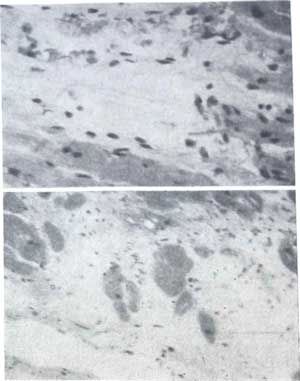
Рис. 3. Миоцитолиз в двух соседних
мышечных волокнах.
Окраска гематоксилин-эозином. Ув. 140X.
Замещение погибших мышечных волокон
соединительной тканью. Та же окраска.
Ув. 120Х.
Нам представляется, что в развитии патологических изменений мышцы сердца, кроме дисциркуляторного и прямого гистотоксического эффекта этанола на миокард, определенную роль играет вовлечение его в общий адаптационный синдром (опосредованное воздействие нервно-рефлекторным путем и через эндокринную систему). По сведениям Anton (1965), Davis и соавт. (1967), В.А. Опалевой-Стеганцевой и соавт. (1969), Myrsten A.-L. и соавт. (1971) и др., прием алкоголя, как всякая стрессовая ситуация, возбуждает симпатико-адреналовую систему, в крови и моче увеличивается содержание катехоламинов. Сердце же обладает высокой способностью абсорбировать адреналин из крови (Raab, 1959). Катехоламины значительно увеличивают потребность сердечной мышцы в кислороде и, следовательно, еще больше нарушают равновесие между местным снабжением кислородом и его потреблением, что в свою очередь ведет к нарушению электролитного равновесия. Одновременно повышение экскреции кортикостероидов, наблюдающееся при алкогольной интоксикации (Fazekas, 1964; В.И. Шишов, 1971; Suzuki и соавт., 1972), усиливает дисбаланс электролитов и деструктивное действие катехоламинов. Морфологическим доказательством стресс-реакции в миокарде является ряд признаков, описанных К.М. Даниловой (1963) и обнаруженных нами в гистологической картине сердца при отравлении алкоголем. К ним относятся фуксинофильное набухание дисков, некробиоз и микронекроз мышечных волокон, отек миокарда с лимфостазами и кровоизлияниями.
Некробиотические изменения и микронекрозы мышечных волокон в наших наблюдениях имеют много общего с описанным многочисленными авторами адреналиновым повреждением миокарда. По данным Ю.Г. Целлариус и Л.А. Семеновой (1972), развитие коагуляционного и колликвационного некрозов мышечных волокон происходит в пределах первых суток после воздействия повреждающего агента, а разрушение и резорбция некротизированных клеток — в течение вторых — третьих и четвертых суток.
Декомпенсация сердечной деятельности, обусловленная повреждением мышечных волокон под влиянием алкоголя, по-видимому, является причиной госпитализации больных или смертельного исхода при явлениях острой сердечно-сосудистой недостаточности даже на 2-е и 3-й сутки после принятия алкоголя.
Таким образом, при отравлении алкоголем в сердце наблюдаются глубокие дистрофические, дисциркуляторные и деструктивные изменения, которые и являются, на наш взгляд, материальным субстратом функциональных расстройств сердечной деятельности при острой алкогольной интоксикации. Это позволяет предположить, что даже малые концентрации этанола в условиях нарушенного метаболизма (атеросклероз, гипертоническая болезнь и другие соматические заболевания, сопровождающиеся коронарокардиосклерозом) могут привести к срыву процессов компенсации и явиться непосредственной причиной смерти.
Методические рекомендации по судебно-медицинской экспертизе отравления алкоголем / Клевно В.А., Максимов А.В., Кучук С.А., Григорьева Е.Н., Заторкина О.Г., Кислов М.А., Крупина Н.А., Лысенко О.В., Тарасова Н.В., Плис С.С. — 2019.
Особенности некоторых морфологических и биохимических изменений печени при острой алкогольной интоксикации в эксперименте / Алябьев Ф.В., Серебров Т.В., Толмачева С.К., Долбня А.Д., Налтакян А.Г., Стрельцова Н.Ю., Паксюткина А.В., Возняк А.В. // Избранные вопросы судебно-медицинской экспертизы. — Хабаровск, 2019. — №18. — С. 137-138.
Морфофункциональная характеристика коры надпочечников при остром отравлении угарным газом в состоянии алкогольного опьянения / Алябьев Ф.В., Толмачева С.К., Долбня А.Д., Налтакян А.Г., Стрельцова Н.Ю., Сапега А.С., Паксюткина А.В., Возняк А.В. // Избранные вопросы судебно-медицинской экспертизы. — Хабаровск, 2019. — №18. — С. 39-40.
В статье представлены результаты морфологических исследований миокарда в поляризованном свете у людей, умерших от острой интоксикации морфином. Выявлены различные варианты повреждения кардиомиоцитов с преимущественной локализацией в левом желудочке в виде контрактур и внутриклеточного миоцитолизиса.
Морфологическими критериями острых повреждений миокарда в патологоанатомической практике являятся дистрофические, некробиотические и некротические изменения кардиомиоцитов. Важное клиническое значение имеят патоморфологические изменения миокарда, такие как дистрофия и некробиоз, предшествуящие некрозу. Именно дистрофические и некробиотические изменения кардиомиоцитов лежат в основе очаговых метаболических повреждений и инфаркта миокарда [1 - 3· Так называемые метаболические повреждения имеят все большее клиническое значение в диагностике патологии миокарда. Выявление ранних стадий повреждения миокардиальных клеток в наиболее полном объеме возможно при использовании метода поляризационной микроскопии, позволяящей выявлять правильно ориентированные структуры, поляризуящие свет [4, 5.
Применение поляризационной микроскопии для диагностики ранних стадий повреждения миокарда базируется на способности основного функционального элемента кардиомиоцитов - миофибрилл к двулучепреломления, что и позволяет обнаруживать патологические изменения. Поляризационная микроскопия изучает гистологические структуры, обладаящие способностья к двоякому лучепреломления (анизотропия), т.е. раздвоения светового луча при прохождении его через анизотропнуя среду. При поляризованном свете колебания световых волн происходят в определенной плоскости, а в обычном свете - в различных плоскостях. Этот метод позволяет диагностировать изменения кардиомиоцитов уже при нарушении энергетического обмена, что сразу же влияет на состояние сократительного аппарата миофибрилл. В своя очередь, изменение структуры миофибрилл определяет тинкториальные особенности саркоплазмы измененных кардиомиоцитов [6 - 8].
Материалы и методы исследования. Материалом для исследования являлись сердца лядей, умерших при острой интоксикации морфином, не имевших какой-либо тяжелой соматической патологии, в возрасте от 15 до 19 лет.
На аутопсии из сердца умерших вырезали кусочки миокарда из левого и правого желудочка, межжелудочковой перегородки и папиллярных мышц, фиксация материала осуществляли в 10 % нейтральном формалине. Гистологический материал для микроскопического исследования готовили по общепринятой методике. Парафиновые срезы окрашивали гематоксилином и эозином, заклячали в полистерол, а также использовали неокрашенные срезы. Кусочки ткани миокарда вырезали и ориентировали на блоках так, чтобы мышечные волокна имели продольное направление, так как миофибриллы в поляризованном свете обнаруживаят характернуя поперечнуя исчерченность, обусловленнуя чередованием анизотропных (А) и изотропных (I) дисков. А-диски в поляризованном свете выглядят светлыми в связи с выраженным свойством положительного двулучепреломления, I - диски выглядят темными, так как почти лишены способности к двулучепреломления.
Результаты исследования и их обсуждение: При остром отравлении морфином в миокарде в поляризованном свете выявлены изменения, характеризуящиеся сегментарными контрактурами II и III степени (рисунок 1).
В окрашенных гематоксилином и эозином серийных срезах в указанных мышечных волокнах выявлялась ацидофилия с усилением окраски эозином. При II степени контрактур отмечено сближение дисков А с истончением I - дисков. Полное исчезновение изотропных дисков и слияние анизотропных дисков А в сплошной конгломерат выявлено при контрактуре III типа повреждения.
В кардиомицитах в состоянии некробиоза при поляризационной микроскопии выявлялась сплошная анизотропия. Имели место и субсегментарные контрактуры с множественными очаговыми контрактурами отдельных групп саркомеров.
В таких клетках в поляризованном свете отсутствовала поперечная исчерченность, а в участках контрактур определялись светящиеся полосы или множественные анизотропные глыбки (рисунок 2).
В ряде наблядений наиболее распространенными явились повреждения кардиомиоцитов в виде внутриклеточного миоцитолизиса. Миоцитолизис характеризовался очагами исчезновения анизотропии в параллельно лежащих мышечных клетках, происходило исчезновение миофибрилл на некотором протяжении кардиомиоцитов, что придавало миокарду своеобразный мозаичный вид (рисунок 3).
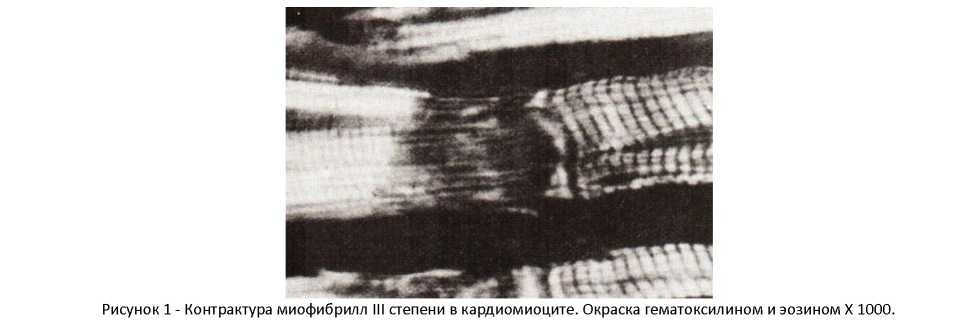

Часть ядер подвергалась кариолизису. Иногда отмечался глыбчатый распад миофибрилл с очаговым лизисом и контрактурами отдельных групп саркомеров. В световой микроскопии выявлялось интенсивное окрашивание саркоплазмы с деформацией ядер, гиперхроматозом, кариопикнозом. В поляризованном свете в очагах глыбчатого распада миофибрилл исчезала поперечная исчерченность, появлялись анизотропные глыбки, которые чередовались с участками без анизотропных структур.
Выводы: проведенные исследования миокарда в поляризованном свете при остром отравлении морфином позволили установить что, очаговые метаболические повреждения мышцы сердца, как правило, развиваются вторично, являясь осложнением основного заболевания в данном случае острого отравления морфином, с развитием острой сердечной недостаточности. Среди многочисленных заболеваний осложненных метаболическим повреждением миокарда, одну из лидирующих позиций занимают различные острые и хронические отравления, в том числе и наркотическими веществами.
Наиболее частой локализацией выявленных нами метаболических повреждений миокарда явился левый желудочек, в основном его субэндокардиальный слой. В очагах метаболических повреждений преобладали контрактуры III степени, которые морфологически характеризовались тяжелыми, а также необратимыми повреждениями кардиомиоцитов. Выявленный в миокарде внутриклеточный миоцитолизис клеток с очаговой дезагрегацией и лизисом миофибрилл кардиомиоцитов является морфологическим маркером повреждающего токсического действия морфина.
СПИСОК ЛИТЕРАТУРЫ
Читайте также:


