![]()
Фото - Нэля САДЫКОВА |
Как ваша печень справилась с последствиями праздничных застолий, в состоянии ли она приспособиться к современной генно-модифицированной пище и трансжирам?
О своем видении процессов, происходящих в этом важном очистительном органе, говорит президент Казахстанской ассоциации медицинской лабораторной диагностики, профессор, завкафедрой КазНМУ им. С. Д. Асфендиярова Мустафа РЫСУЛЫ.
– Помните миф о древнегреческом титане Прометее, который похитил огонь у богов и передал его в помощь людям, и как за это он был прикован к скале и обречен на вечные мучения. Каждый вечер к нему прилетал орел и клевал его печень. На другой день печень отрастала заново, и опять орел клевал ее. Но бессмертный Прометей так и не умирал.
Иносказательно это и есть показатель регенерации печени. Действительно, печень – уникальный орган, который способен к самовосстановлению. Ведь другие органы орел не клевал. А мог бы склевать и сердце, и легкие… Но тогда бы Прометей попросту умер. А его наказали так, чтобы он долго мучился, но не умирал… Как говорят гепатологи, в этой легенде скрыт глубокий медицинский смысл!
– Итак, встретили мы новый, 2017 год, дали поклевать свою печень всяким яствам: пили шампанское, водку, коньячок, целых две недели кушали мясо, оливье, пирожные, бешбармак, и что. Бежим сдаваться доктору? Делаем биохимический анализ крови на печеночные тесты?
– Бежим, но не сразу, а через три-семь дней. Потому что у печени есть своя особенность – количество ферментов (белковые молекулы, ускоряющие химические реакции в живых системах), которые позволяют переработать поступающие в организм вещества, тем больше, чем больше токсичных веществ в него попадает. И еще несколько дней после обильных праздничных трапез и возлияний печень продолжает усиленно вырабатывать эти ферменты. Самые главные среди них – так называемые маркерные ферменты: АЛТ (аланинаминотрансфераза, или АлАТ) и АСТ (аспартатаминотрансфераза, или АсАТ). Это белки, которые отвечают за работу печени по обезвреживанию инородных веществ, в том числе и лекарств. Плюс они производят некую переработку поступивших веществ, переводят токсичные в нетоксичные. Их количество в крови измеряется в единицах на литр.
Есть еще такой фермент, как щелочная фосфатаза. Ее уровень всегда повышается, когда происходит застой желчи. В общем, каждый фермент выполняет свою функцию. И при диагностике они и являются индикаторами повышенной нагрузки на печень.
– А если все же пойти на обследование сразу после обильных застолий.
– Тогда врач, увидев такие ваши анализы, может сказать, что ваша печень больна. А вы ему скажете: “Да нет же, просто я вчера пил!”. Если накануне обследования человек пил алкоголь, то все показатели у него будут повышены. При этом его печень может и не быть больной, просто она среагировала на то, что попало в пищеварительную систему.
– То есть она выработала то количество ферментов, которое может справиться с этой пищей?
– Именно так. Вы дали ей лишнюю нагрузку, и она пытается ее осилить, вот и вырабатывает ферменты. Но если вы забудете сказать врачу о том, что много пили и ели накануне, а он поставит диагноз и начнет вас лечить, это очень плохо. Мало того что печени придется справляться с большим количеством потребленной пищи и алкоголя, так теперь ее нагрузят еще и лекарствами, которые тоже уничтожают ее. Недаром печень называют лабораторией организма. Все поступающие в нее вещества проходят контроль. К молекулам этих веществ либо присоединяется нужный белок, чтобы транспортировать их по назначению, либо печень обезвреживает их и уничтожает, если это токсины.
– То есть, чтобы достоверно узнать, здорова ли печень, надо дать ей тайм-аут в виде воздержания от усиленного питания?
– Конечно. И при условии, что вы больше не пьете алкоголь, не едите шашлыки, острую, жареную пищу и вообще не переедаете. Тогда биохимический печеночный анализ покажет истинное ее состояние. И если при этом уровень ферментов АЛТ и АСТ окажется выше нормы, то человеку надо обратиться к доктору. Ведь зачастую он может и не ощущать признаков того, что болен. Хотя обычно страдания печени сопровождаются слабостью, утомляемостью, тяжестью в правом подреберье.
– И желтизной тела?
– Нет, желтизна – это уже чистый гепатит. А пока человек чувствует некоторую слабость после нескольких дней переедания – это показатель того, что в данный момент печень не в порядке. Ее надо поберечь и перейти на облегченную диету. Тогда она сама быстро восстановится. Потому что это еще не болезнь, а обратимое явление, показатель того что идет нарушение функций печени на уровне этих ферментов. В стадию болезни это переходит позднее.
– Получается, что после новогодних праздников непременно надо устроить разгрузку организму, каникулы для печени?
– Да. Не голодать полностью, но сократить еду до минимума. И перейти на легкую пищу. Это могут быть преимущественно овощи, а также курица, рыба, нежирная телятина, мясо кролика. Никаких жареных шашлыков, никакой острой пищи или донеров! Утром вы можете съесть маленький бутерброд и выпить чаю. И этого достаточно. Через три-четыре часа еще съесть булочку или одно яйцо. К вечеру закусить несладкой овсяной печенюшкой и запить ее лучше несладким чаем. Вот и всё. Какое-то время вы будете чувствовать себя не совсем комфортно, зато организм очистится, и все эти разборки в нем утихнут. Обычно дня два-три хватает, чтобы вернуть все в норму. Тогда вы снова станете активным, сбросите 200–300 граммов лишнего веса. Это очень хорошо для организма, который борется за каждый лишний грамм. И разумеется, никакого алкоголя. А то, бывает, люди есть перестают, а пить – нет. А алкоголь в момент вернет повышение и АЛТ, и АСТ.
– Чем ее лечат?
– По сути, печень лечить не надо. Она сама себя хорошо восстанавливает. Надо просто ей не вредить. А все эти капли и препараты, которые рекламируют по телевидению, не помогут. Печень – достаточно мощный и умный орган и может долго вас спасать. Раз в неделю вы можете что-то нарушить, для нее это не проблема. Она долгое время может работать в плохих условиях и выдерживать большие нагрузки. Ее можно травить алкоголем и лекарствами, различными ядами и генно-модифицированными продуктами. Она работает, даже когда остается всего 25 процентов от всей ее ткани. Это высокий показатель надежности. Но ничто не вечно в этом мире. И если нарушать благополучие печени каждый день, естественно, она не выдержит! Легенду о Прометее знают все, но мало кто придает значение ее глубокому смыслу.
А в целом биохимические исследования крови, печеночные тесты проводят чаще всего на АЛТ, АСТ, а также на билирубин, щелочную фосфатазу и ГГТ (гаммаглутамилтрансфераза – это показатель замедленного продвижения желчи в печени и желчевыводящих путях). Он может быть также тестом на хронический алкоголизм. И все нарушения уровня этих ферментов показывают, что способности печени к детоксикации организма снижаются.
– И вот что интересно, американские ученые провели исследование в Европе, Азии и Америке. В нем участвовало 1 200 человек, практически здоровых, у которых печень страдает, но болезни еще нет. И когда подсчитали средние показатели ее ферментов, то увидели, что на самом деле они повысились, хотя у этих людей не было клиники, не было заболевания. Поэтому сейчас предлагается считать, что прежние нормы уровня ферментов печени устарели и их надо менять в сторону повышения. Это происходит в связи с тем, что жизнь людей изменилась. Население планеты стало потреблять больше новых веществ, к которым печень стала приспосабливаться и держать свои ферменты на определенном уровне активности. Чтобы они могли справляться с той едой, которая приходит к нам сейчас, с тем количеством искусственных жиров, генетически модифицированных продуктов, всяких искусственных добавок. Это своеобразная акция приспособления печени к новым условиям жизни людей. И теперь американская ассоциация гастроэнтерологов предлагает пересмотреть нормативы печеночных тестов на АЛТ и АСТ в сторону их повышения.
– Верно ли это?
– Да, в последние годы наблюдается тенденция к повышению показателей этих тестов на ферменты АЛТ и АСТ на 5–10 процентов по сравнению с общепринятой нормой и без клинической картины заболеваний печени.
– А не получится ли так, что человек постепенно и сам генно-модифицируется?
– Это вполне возможно. Конечно, люди так быстро, как мыши или мушки дрозофилы, не меняются. Результаты будут видны через столетия. Но это уже первый признак, что человечество меняется. А то, что происходит при этом в других органах, например, в головном мозге, мы пока не знаем. Но, безусловно, смена одного показателя автоматически ведет к смене других показателей.
Поэтому людям в современном мире необходимо внимательно следить за диетой, стараться исключать продукты, которые содержат искусственно измененные при помощи генной инженерии растительные и животные белки. И, естественно, в таких экстремальных условиях не стоит губить печень алкоголем. Она и без того испытывает большие нагрузки. И самое опасное, когда печень, страдая долгое время, постепенно подвергается циррозу (болезненное рубцевание), а ее отмирающие ткани затвердевают и перестают выполнять свои функции.
![]()
Алкогольное поражение печени — алкогольный (токсический) гепатит — состояние, характеризующееся гисто-морфологочискими (т.е структурными) изменениями паренхимы печени с нарушением их функций.
Токсическое действие алкоголя на печень оказывается четыремя путями, которые все имеют место в клинической ситуации:
- Прямое токсическое действие, связанное с влянием этанола и продуктами его метаболизма на мембранный аппарат клеток и ферментативную активность;
- Нарушение моторной функции, сопровождающейся застоем желчи и ее цитолитическим (т.е. разрушающим) действием на клетки и последующей реакции иммунной системы с развитием воспаления;
- Аутоимунная реакция (собственно гепатит);
- Окислительный стресс, вызывающий нарушения в системе клеточных ферментов, что усугубляет течение процесса.
Хотя печень является частью ЖКТ, алкогольное поражение этого органа происходит через непосредственное действие, поскольку биотрансформация этанола в основном происходит в печени, а также опосредовано, через изменение микробного состава жкт.
В пересчёте на чистый этанол порог токсичности для печени составляет 90 г в сутки в перерасчете на чистый этанол.
Даже при однократномупотреблении алкоголя может наблюдаться картина транзиторного некроза гепатоцитов, проявляемая или непроявляемая клиническими симптомами. Маркерным ферментом, позволяющим заподозрить данное состояние, служит гамма-глутамилтрансфераза (ГГТ). ГГТ -фермент, с наибольшей активностью и представленностью в печени, почках и поджелудочной железе, участвующих в обмене аминокислот. В крови здорового человека уровень ГГТ ниже: для женщин — до 32 Ед/л., для мужчин — до 49 Ед/л. У новорожденных норма ГГТ в 2—4 раза выше, чем у взрослых.
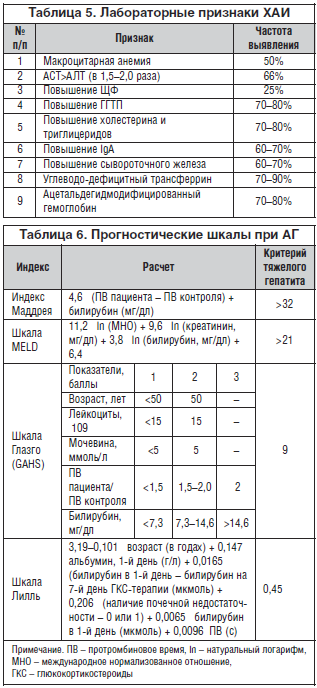
При хронической интоксикации этанолом (в том числе при употреблении слабо-алкогольных напитков и пива) повышаются и другие печеночные ферменты (транспептидазы), в том числе аланинаминотрансфераза (АЛТ) и аспартатаминотрансфераза (АСТ). Для предциррозных стадий характерно преобладание АСТ над АЛТ (понижается, так называемый коэффициент де Ритиса — отношение уровня АСТ к АЛТ. Значение коэффициента в норме составляет 1,33±0,42 или 0,91-1,75, снижение ниже уровня 0,9 — уверенное подтверждение разрушения клеток печени и является прогностически неблагоприятным). В последнее время важным методом выявления злоупотребления алкоголем используют определение углеводдефицитного (десиализированного) трансферрина сыворотки крови — соединения трансферрина с ацетальдегидом (продуктом метаболизма этанола), приводящего к накоплению железа в печени (специфиность 70–90%) и ацетальдегидмодифицированного гемоглобина (специфичность 70–80%). Множественные очаги некрозов ведут к фиброзу и, в конечном итоге, циррозу печени. Цирроз развивается, по меньшей мере, у 10 % лиц с алкогольным поражением печени (см. ниже).
Распространенность алкогольного поражения печени имеет прямую зависимость от уровня потребления алкоголя, например этот уровень в Европе в среднем составляет до 9,8 л (ВОЗ, 1995).
Исследования в Канаде показали, что, при увеличении годового потребления алкоголя на 1 л на душу населения, общий показатель по всем циррозам возрастал у мужчин на 17 %, а у женщин на 13 %. Аналогичные данные полученны в США, где стойкую алкогольную зависимость имеют 10-12% населения, а алкогольная болезнь печени (стеатоз) составляет 34 %, из неё примерно 17 % приходится на стеатогепатиты и 5% на цирроз. Данные иследований методом опроса среди тех, кто регулярно употребляет алкоголь свидетельствуют, что в год пьющий гражданин в среднем выпивает по 8,7 литров вина, 5,7 л спирта и 78 литров пива.
В РФ потребление алкоголя составляет примерно 13 л на человека в год, и около 10 млн россиян больны хроническим алкоголизмом.
В таблице приводятся усредненные данные по количеству потребляемого этанола на душу населения в год:
Крепкие спиртные напитки
При этом мировое потребление алкоголя неуклонно продолжает расти.
Алкогльная болезнь печени развивается в 12–20% случаев. В то же время 80% летальных исходов связаны с избыточным употреблением алкоголя и его токсичных суррогатов, приводящих к тяжелой соматической патологии (печеночная кома, острая сердечная недостаточность, желудочно-кишечные кровотечения, инфекции и др. В Украине по данным официальной статистики примерно 40 000 смертей в год напрямую зависят от злоупотребления этанола.
К факторам риска развития АБП относят: дозы алкоголя, характер и длительность злоупотребления; генетический полиморфизм этанолметаболизирующих ферментов; пол (у женщин склонность к развитию АБП выше); неполноценное питание (дефицит пищевых веществ); применение гепатотоксических лекарственных препаратов, метаболизирующихся в печени; инфицирование гепатотропными вирусами; иммунные факторы.
Метаболизм этанола. В организме человека метаболизм алкоголя проходит в три этапа при участии алкогольдегидрогеназы (АДГ), микросомальной этанолокислительной системы (МЭОС) и пироксисом [1, 2, 3]. Формирование АБП во многом обусловлено наличием генов, кодирующих ферменты, участвующие в метаболизме этанола — АДГ и альдегиддегидрогеназа (АлДГ) [1, 4]. Эти ферменты строго специфичны и локализуются преимущественно в печени. При попадании в желудок 12–25% введенного в организм алкоголя окисляется под воздействием желудочной АДГ, конвертирующей этанол в ацетальдегид, тем самым редуцируя количество алкоголя, поступающего в систему портального кровотока и соответственно в печень. Более низкая активность желудочной АДГ у женщин, чем у мужчин, отчасти объясняет тот факт, что они более чувствительны к токсическому воздействию алкоголя. Следует учитывать снижение уровня АДГ желудка при приеме блокаторов Н2-гистаминовых рецепторов, что может привести к значительному увеличению концентрации алкоголя в крови.
Этанол, поступая по системе портального кровотока в печень, подвергается воздействию печеночной фракции АДГ, коферментом которой является никотинамиддинуклеотид (NAD+), в результате чего происходит образование ацетальдегида, играющего важную роль в развитии АБП, и восстановление кофермента до NАD*H. АДГ, являясь цитоплазматическим ферментом, участвует в окислении этанола при тканевой концентрации алкоголя не более 10 ммоль/л.
У человека существует три основных гена, кодирующих АДГ: АДГ1, АДГ2, АДГ3. Полиморфизм на локусе АДГ2, наиболее вероятно, приводит к значительным различиям в метаболизме этанола. Так, изофермент АДГb2 (аллель АДГ2*1), обеспечивающий усиленное образование ацетальдегида, чаще встречается у лиц монголоидной расы, что объясняет их меньшую толерантность к алкоголю, проявляющуюся гиперемией лица, потливостью, тахикардией, а также раскрывает причины более высокого риска формирования АБП. На следующем этапе ацетальдегид под воздействием цитозольного АлДГ1 и митохондриального АлДГ2 ферментов в NAD-зависимых реакциях метаболизируется до уксусной кислоты. Около 10–15% этанола метаболизируется в микросомах гладкого эндоплазматического ретикулума с помощью МЭОС, включающей цитохром P 450 2E1, здесь же происходит метаболизм многих лекарственных препаратов. Увеличение алкогольной нагрузки приводит к повышению чувствительности к лекарственным веществам, образованию токсических метаболитов и токсическому поражению печени при использовании терапевтических доз препаратов. Наконец, каталазы, содержащиеся в пироксисомах, также могут участвовать в метаболизме этанола.
Патогенез. Токсическое воздействие этанола находится в прямой зависимости от концентрации в крови ацетальдегида и ацетата. При окислении этанола происходит повышенный расход кофермента NAD+, увеличение соотношения NAD*H / NAD+, что играет важную роль в формировании жировой дистрофии печени. Увеличение концентрации NAD*H приводит к возрастанию синтеза глицеро-3-фосфата, способствует эстерификации жирных кислот, синтезу триглицеридов, сопровождается снижением скорости b-окисления жирных кислот, приводит к их накоплению в печени.
Ацетальдегид обладает гепатотоксическим действием, которое проявляется в результате усиления процессов перекисного окисления липидов (ПОЛ), образования соединения с другими белками и ферментами, что приводит к нарушению функции фосфолипидных клеточных мембран. Комплекс соединений ацетальдегида с белками, в том числе с тубулином, вызывает изменения структуры микротрубочек гепатоцитов, образуя так называемый алкогольный гиалин, и способствует нарушению внутриклеточного транспорта, ретенции белков и воды, развитию баллонной дистрофии гепатоцитов.
Избыточное образование ацетальдегида и жирных кислот приводит к уменьшению активности митохондриальных ферментов, разобщению процессов окисления и фосфорилирования, снижению синтеза аденозинтрифосфата, а также усиливает синтез цитокинов (в частности, трансформирующего фактора роста — TGFb). Последний способствует трансформации клеток Ито в фибробласты, которые продуцируют коллаген. Другим механизмом коллагенообразования является стимуляция клеток Купфера продуктами ПОЛ.
Наряду с этим в развитии АБП предполагается роль гена ангиотензиногена (АГТ) — белка, синтезирующегося в печени, и ангиотензина II. Установлен их профиброгенный эффект [5], обнаружено повышение уровня ангиотензина II плазмы крыс в зависимости от алкогольной мотивации [6].
В патогенезе АБП велика роль иммунных механизмов. Выявлены нарушения гуморального иммунитета: повышение уровня сывороточных иммуноглобулинов (преимущественно иммуноглобулина класса А), их отложение в стенке печеночных синусоидов, образование в низких титрах антиядерных и антигладкомышечных антител, а также антител к алкогольному гиалину и др.
Нарушение клеточного иммунитета связано с сенсибилизацией Т-клеток ацетальдегидом, влиянием иммунных комплексов, повышенным образованием цитотоксических Т-лимфоцитов. В результате взаимодействия иммунокомпетентных клеток высвобождаются провоспалительные цитокины (в том числе и фактор некроза опухоли — TNFa) и индуцируемые им интерлейкины (IL-1, IL-2, IL-6, IL-8), что при участии активных форм кислорода и оксида азота приводит к повреждению различных клеток-мишеней, а в конечном итоге — к развитию полиорганных нарушений.
Одновременно у больных, страдающих АБП, обнаруживают избыточный рост бактерий в тонкой кишке, что способствует увеличению синтеза эндотоксина — липополисахарида оболочки грамотрицательных микробов. При попадании в кровь портальной системы эндотоксин наряду с другими отрицательными факторами (метаболиты ПОЛ) стимулирует активность купферовских клеток, синтез провоспалительных цитокинов, особенно TNFa, при активном влиянии которого усиливается развитие воспаления и фиброзирующих процессов в печени.
Целью терапии АСГ является предотвращение формирования фиброза и цирроза печени (ингибирование воспаления и фиброза в ткани печени, снижение активности процессов ПОЛ и биохимических показателей, выведение токсических метаболитов, уменьшение эндотоксемии), улучшение качества жизни и лечение ассоциированных с АСГ состояний (хронический холецистит, панкреатит, язвенная болезнь желудка и двенадцатиперстной кишки и др.) . Тяжесть печеночной недостаточности тесно взаимосвязана с интенсивностью желтухи, гипераммониемии. Источниками последней являются пищевые белки, кровь, изливающаяся в просвет пищеварительного тракта (чаще при кровотечении из варикозно-расширенных вен пищевода). Под влиянием пищеварительных соков и ферментов из белков образуется аммиак. В условиях нарушения дезинтоксикационной функции печени аммиак не подвергается разрушению и попадает в общий кровоток, оказывая токсическое действие на головной мозг. Степень тяжести печеночной недостаточности определяет выраженность нервно-психических расстройств. На ранних стадиях выявляют психическую депрессию или, наоборот, эйфорию, которые часто сменяют друг друга. Позднее происходят изменения неврологического статуса: нарушение координации движения, речи, заторможенность сознания. В финальной стадии болезни развивается коматозное состояние, тяжесть которого целесообразно определять по шкале Глазго.
Целью воздействия на эндогенную токсемию, связанную с бактериальным обсеменением тонкой кишки, целесообразно в программу лечения пациентов с алкогольным стеатозом печени, АСГ включать применение пребиотиков, улучшающих метаболизм кишечных бактерий. Под влиянием пребиотических препаратов у больных компенсированным ЦП алкогольной этиологии отмечено снижение избыточной бактериальной пролиферации в тонкой кишке, сопровождающееся уменьшением выраженности печеночной энцефалопатии.
Данные мета-анализа свидетельствуют что лактулоза способна в значительной степени предотвращать выраженность алкогольной энцефалопатии у больных с алкогольным поражением печени. Неабсорбируемый дисахарид -лактулоза — начал применяться в лечении ПЭ с конца 60-х годов как безопасная альтернатива антибиотику неомицину. На основании двух небольших РКИ, где в качестве контроля применяли неомицин, было сделано заключение, что эффективность лактулозы в лечении ПЭ не отличается от эффективности неомицина [42, 43]. Однако эффективность самого неомицина в лечении ПЭ никогда не была подтверждена. В 80-е годы в практику лечения ПЭ был введен другой синтетический дисахарид – лактитол. Его эффективность сравнивалась с эффективность лактулозы. Дальнейшие исследования и метаанализ показали, что лактитол и лактулоза одинаково эффективны в лечении ПЭ, при этом частота побочных эффектов (метеоризм, диарея, тошнота) была ниже для лактитола. С 80-х годов неабсорбируемые дисахариды рассматривались как стандарт для лечения ПЭ. Эти данные подтверждены в 2009 г. В ходе мета-анализа рандомизированных исследований рифаксимина (неабсорбируемого деривата рифамицина) в сравнении с невсасывающимися дисахаридами (в частности, лактулозой) при лечении пациентов с печёночной энцефалопатией сравнивались положительные и отрицательные моменты указанных двух вариантов терапии.
Было идентифицировано 7 рандомизированных контролируемых исследований, из которых 5 исследований соответствовали критериям включения в мета-анализ (общее число включенных пациентов — 264).
В ходе проведённого мета-анализа не было выявлено существенных различий в улучшении у пациентов с печёночной энцефалопатией при использовании рифаксимина и невсасывающихся дисахаридов (относительный риск (ОР) 1,08; 95% доверительный интервал (ДИ), 0,85-1,38; р=0,53]. Показатель ОР составил 0,98 (95% ДИ, 0,85-1,13; р=0,74) для острой печёночной энцефалопатии (n=157) и 0,87 (95% ДИ, 0,40-1,88; р=0,72) для хронической энцефалопатии (n=96). Также не было выявлено достоверных различий влияния рифаксимина и невсасывающихся дисахаридов на диарею (ОР=0,90; 95% ДИ 0,17-4,70; р=0,90), однако при использовании рифаксимина достоверно реже отмечались боли в животе (ОР=0,28; 95% ДИ 0,08-0,95; р=0,04).
Таким образом, рифаксимин не превосходит невсасывающиеся дисахариды при лечении острой или хронической энцефалопатии как при использовании короткого курса, так и при длительном применении.
Сравнительная эффективность неабсорбируемых дисахаридов, плацебо и отсутствия вмешательства при ПЭ (модифицировано по B.Als-Nielsen, L.Gluud, C.Gluud, 2004).
Кроме того, как выяснилось в ходе экспериментальных исследований (Козловский В.А., 2011) лактулоза, способна сама по себе уменьшать выраженность влияния этанола на развитие алкогольной интоксикации.
При изучении на животных длительность угнетения ЦНС в группе животных получавших и не получавших лактулозу, достоверно отличалась. У животных, получавших лактулозу до острого отравления в дозе 500 мг/кг длительность бокового положения (т.е. наркотического сна) на 27% была меньше, чем у группы не леченных животных. Комбинация эталонного сорбента энтеросгеля и лактулозы оказывала еще более значимое влияние на уменьшение выраженности алкогольного отравления.
Свойство лактулозы ускорять элиминацию ацетальальдегида и этанола в крови и кишечнике при длительном применении известно с 2003 г. Этот механизм объясняется пребиотическим эффектом за счет нормализации колонизации микрофлоры кишечника, которая в состоянии продуцировать альдегид — и алкогольдегидрогеназу.
Однако, механизм действия лактулозы на степень острого отравления сложно объяснить ее стандартным пребиотичеким действием. Врядли возможно предположить колонизацию микроорганизмов за 15 минут введения лактулозы. Вероятнее всего, возможен прямой механизм взаимодействия лактулозы с этанолом, или стимуляция ферментов семейства цитохромов под влиянием лактулозы.
Последнее предположение опровергается исследованиями Lhoste E.F (2001), показавшим отсутствие влияния лактулозы на ситему цитохромов.
Если механизм алкогольпротекторного действия лактулозы в комбинации с энтеросгелем понятен, то сам по себе впервые установленный антиалкогольный эффект лактулозы требует детального изучения.
Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции