Современные методы лечения кандидозов


В статье приведены литературные данные по возможности использования как традиционных, так и альтернативных методов лечения кандидоза. Как альтернативный метод лечения кандидоза мы рекомендуем аутовакцинотерапию.

Богомолова, Н.С. Кандидозы в хирургической клинике: видовой состав возбудителей, чувствительность к антибиотикам, превентивная терапия / Н.С. Богомолова [и др.] // Анестезиология и реаниматология. – 2011. - №5. – С. 43-48.
Вознесенский, А.Г. Клиническая фармакология противогрибковых препаратов / А.Г. Вознесенский // Гедеон Рихтер в СНГ. – 2001. - № 2(6). – С. 50-53.
Волосач, О.С. Метод комбинированной иммунотерапии пациентов с хроническими воспалительными заболеваниями, осложненными кандидозом : инструкция по применению № 084-0909 : утв. 17.09.2009 г. / Министерство здравоохранения Республики Беларусь ; сост. О.С. Волосач, В.М. Цыркунов, С.Б. Позняк, С.М. Дешко. – Гродно, 2009. – 11 с.
Воробьев, А.А. Принципы классификации и стратегия применения иммуномодуляторов в медицине / А.А. Воробьев // Журн. микробиологии, эпидемиологии и иммунологии. – 2002. - №4. – 93-98.
Воробьева, Л.И. Противоопухолевая аутовакцина в комплексном лечении больных раком яичников / Л.И. Воробьева [и др.] // Тез. докл. 3 съезда онкологов и радиологов СНГ, Минск, 25-28 мая 2004 г. – Минск, 2004. – Ч. 2. – С. 195-196.
Кажина, М.В. Стафилококковая аутовакцинотерапия при дисбиозе половых путей (клинико-экспериментальное обоснование) : научное издание / М.В. Кажина, С.Б. Позняк; Грод. гос. мед. ун-т. – Гродно, 2002. – 127 с.
Котова, Т.В. Клиническая эффективность вагинальной озонотерапии и раствора гуминовых соединений в комплексном лечении рецидивирующего кандидозного вульвовагинита / Т.В. Котова, Р. Чандра-Д’Мелло, Г.О. Гречканев // Медицинский альманах. – 2013. - №6. – С. 75-78.
Кузнецова, Ю.К. Лечение микст-инфекции кожи / Ю.К. Кузнецова, Н.С. Сирмайс // Вестн. дерматологии и венерологии. – 2013.- №5. – С. 132-137.
Лисовская, С.А. Взаимодействие Candida albicans и бактерий ассоциантов при кандидозах различной локализации / С.А. Лисовская, Е.В. Халдеева, Н.И. Глушко // Проблемы медицинской микологии. – 2013. - №2. – С. 40-43.
Львов, А.Н. Комбинированная наружная терапия дерматозов сочетанной этиологии : клинический разбор / А.Н. Львов // Дерматология. – 2013.- №2. – С. 8-14.
Мадова, И.О. Острый вульвовагинальный кандидоз: старая проблема – новое решение // И.О. Мадова [и др.] //Клиническая дерматология и венерология. – 2012. - №4. – С. 53-57.
Медуницин, Н.В. История, принципы конструирования комбинированных вакцин и проблемы вакцинопрофилактики при их применении / Н.В. Медуницин // Журн. микробиологии, эпидемиологии и иммунологии. – 2001. - №1. – С. 90-94.
Мелинти, Е.В. Современные методы профилактики и лечения вульвовагинального кандидоза / Е.В. Мелинти // Новая аптека. – 2013. - №5. – С. 40-41.
Новиков, Д.К. Основы иммунокоррекции : учеб. пособие для вузов / Д.К. Новиков [и др.] ; под ред. Д.К. Новикова. – Витебск, 1998. – 107 с.
Позняк, С.Б. Применение аутовакцины при гнойно-воспалительных заболеваниях, осложненных кандидозом / С.Б. Позняк, В.И. Третьякевич // Клинич. медицина.– 1981. - №10. – С. 80-81.
Сергеев, А.Ю. Грибковые инфекции : руководство для врачей / А.Ю. Сергеев, Ю.В. Сергеев. –2-е изд. – М. : Изд-во БИНОМ, 2008. – 480 с.
Симбарская, М.Л. Иммуномодулирующая терапия в комплексном лечении рецидивирующего кандидозного вульвовагинита / М.Л. Симбарская [и др.] // Проблемы медицинской микологии. – 2012. - №3. – С. 32-37.
Синчихин, С.П. Роль комплексного местного и системного лечения при патологических вагинальных выделениях у женщин / С.П. Синчихин, О.Г. Черникина, О.Б. Мамиев. – Рос. вестн. акушера-гинеколога. – 2013. - №5. – С. 63-65.
Чеботарь, И.В. Исследование действия антимикотических препаратов на биопленки, сформированные грибами рода Candida / И.В. Чеботарь, В.В. Паршиков // Акушерство и гинекология. – 2013. - №5. – С. 98-102.
Чистякова, В.Р. Отомикозы в детском возрасте : руководство для врачей / В.Р. Чистякова, И.В. Наумова. – М. : Медицинское информационное агенство, 2001. – 176 с.
Шабашова, Н.В. Хронический кандидоз кожи и слизистых оболочек и иммуногенетические механизмы врожденной чувствительности макроорганизма к Candida spp. / Н.В. Шабашова // Проблемы медицинской микологии. – 2012. - №4. – С. 20-28.
Bacci, A. Dendritic cells pulsed with fungal RNA induce protective immunity to Candida albicans in hematopoietic transplantation / A. Bacci [et al.] // J. Immunol. – 2002. – Vol. 168, №6. – P. 2904-2913.
Bradbury, J. Mucosal infection yields to new approaches / J. Bradbury // The Lancet. – 2000. – №356. – P. 1132.
Bromuro, C. Interplay between protective and inhibitory antibodies dictates the outcome of experimental disseminated candidiasis in recipients of Candida albicans / C. Bromuro [et al.] // Infect. Immunol. – 2002. – Vol. 70, №10. – P. 5462-5470.
Elahi, S. A therapeutic vaccine for mucosal candidiasis / S. Elahi, R. Clancy, G. Pang // Vaccine. – 2001. – Vol. 19, №117. – P. 2516-2521.
Frattarelli, D.A.C. Antifugals in systemic neonatal candidiasis / D.A.C. Frattarelli [et al.] // Drugs. – 2004. – Vol. 64, №9. – P. 949-968.
Halasa, J. Treatment with an autovaccine of a patient with catarrhal rhinitis, nasal polips and infectious bronchial asthma / J. Halasa, B. Millo // Process. of intern. sympos. : The role of bacteria and viruses in bronch. asthma. – Zakopane, March 19- 20, 1991. – P. 145-147.
Ibrahim, A.S. Vaccination with recombinant N-terminal domain of Als1p improves survival during murine disseminated candidiasis by enhancing cell-mediated not humoral immunity / Ibrahim A.S. [et al.] // Infect. Immunol. – 2005. – Vol. 73, №2. – P. 999-1005.
Jia, Y. Calcium-activated-calcineurin reduces the in vitro and in vivo sensitivity of flconazole to Candida albicans via RTA2P / Y. Jia [et al.] // PLoS One. – 2012. – Vol.7, № 10. – P. 48369.
Kucharska, E. Attempts to demonstrate changed reactivity to histamine in laboratory animals after repeated and increasing doses of staphylococcal vaccine / E. Kucharska, L. Szymniak, J. Halasa // Process. of intern. sympos. : The role of bacteria and viruses in bronch. asthma, Zakopane, March 19-20, 1991. – P. 125-129.
Kul’ko, A.B., Mitokhin S.D., Moroz A.M. Respiratory tract mycotic infections in phthisiological practice: species composition and susceptibility of the Candida albicans isolates to antifungal agents / A.B. Kul’ko, S.D. Mitokhin, A.M. Moroz // Antibiot. Khimioter. – 2005. – Vol. 50, №4. – P. 14-17.
Mirza, M.A. In vitro/in vivo performance of different complexes of itraconazole used in the treatment of vaginal candidiasis / M.A. Mirza [et al.] // Brazilian Journal of Pharmaceutical Sciences. – 2012. – Vol.48, №4. – P. 759-77.
Mochon, A.B. Is a vaccine needed against Candida albicans? / A.B. Mochon, J.E. Cutler // Med. Mycol. – 2005. – Vol. 43, №2. – P. 97-115.
Peptides which mimic Candida carbohydrate epitopes and their use in a vaccine: Patent US 6391587 A 61 K 39/00 A 61 K 9/127 / J.E. Cutler, P.M. Glee, B.L. Granger; – № 09/334921; 17.06.1999; 21.05.2002.
Rusch, V. Results of an open, non-placebo controlled pilot study investigating the immunomodulatory potential of autovaccine / V. Rusch, D. Ottendorfer, K. Zimmermann // Arzneimittelforschung. – 2001. – Vol. 51, №8. – P. 690-697.
Sevilla, M.J. A fungicidal monoclonal antibody protects against murine invasive candidiasis / M.J. Sevilla [et al.] // Infect. Immunol. – 2006. – Vol. 74, №5. – P. 3042-3045.
Shuhtin, V.V. Clinical and laboratory characteristics of HIV-infected patients with disorders of the skin in the Odessa Region / V.V. Shuhtin [et al.] // Journal of Health Sciences. – 2013. – Vol. 3, №6 (16). – P. 283-294.
Suenobu, N. Nasal vaccination induces the ability to eliminate Candida colonization without inflencing the preexisting antigen specifi Ig E Abs: a possibility for the control of Candida-related atopic dermatitis / N. Suenobu, M.N. Kweon, M. Kiyono //Vaccine. – 2002. – Vol. 20, №23-24. – P. 2972- 2980.
Toubas, D. Epidemiology of invasive candidiasis / D. Toubas // Revue Francophone des Laboratoires. – 2013. – Vol. 2013, №450. – P. 27-36.
Vonk, A.G. Host defense against disseminated Candida albicans infection and implications for antifungal immunotherapy / A.G. Vonk, M.G. Netea, J.W. van der Meer // Expert. Opin. Biol. Ther. – 2006. – Vol. 6, №9. – P. 891- 903.
Wang, Y.B. Analysis of ERG 11 gene mutation in Candid albicans / Y.B. Wang [et al.] // Di Yi Jun Yi Da Xue Xue Bao. – 2005. – Vol. 25, №11. – P. 1390-1393.
Zhang, M.X. Mannan-specifi immunoglobulin G antibodies in normal human serum mediate classical pathway initiation of C3 binding to Candida albicans / M.X. Zhang, D.M. Lupan, T.R. Kozel // Infect. Immunol. – 1997. – Vol. 65, №9. – P. 3822-3827.
- На текущий момент ссылки отсутствуют.
Урогенитальный кандидоз — это грибковое заболевание слизистых оболочек и кожи мочеполовых органов, вызываемое дрожжеподобными грибами рода Candida. В настоящее время описано более 170 биологических видов дрожжеподобных грибов, из них возбудителями урог
Урогенитальный кандидоз — это грибковое заболевание слизистых оболочек и кожи мочеполовых органов, вызываемое дрожжеподобными грибами рода Candida.
В настоящее время описано более 170 биологических видов дрожжеподобных грибов, из них возбудителями урогенитального кандидоза являются: C. albicans — в 80% (за рубежом — в 45–70%), C. glabrata — в 15–30%, C. tropicalis, C. krusei, C. parapsilosis — в 4–7% случаев.
Заболевание поражает и мужчин и женщин, однако чаще встречается у женщин репродуктивного возраста. По распространенности кандидозный вульвовагинит стоит на втором месте среди всех вульвовагинальных инфекций. Пик заболеваемости отмечается в 20–45 лет.
Половой путь передачи инфекции встречается в 30–40% случаев. Чаще (60–70%) заболевание обусловлено эндогенной инфекцией. При беременности заболеваемость возрастает на 10–20%, риск передачи инфекции новорожденному в родах составляет примерно 70–85%.
К факторам риска обычно относят беременность, применение гормональной контрацепции и заместительной гормонотерапии (особенно гормональными препаратами первого поколения), длительное и бессистемное использование антибиотиков, иммунодепрессантов, цитостатиков и некоторых других препаратов. Однако необходимо отметить, что антибактериальные средства выступают как фактор риска только на фоне существующего кандидоносительства и их влияние кратковременно. Нарушения углеводного обмена, обусловленные сахарным диабетом, способствуют упорному течению урогенитального кандидоза с частыми рецидивами, плохо поддающимися терапии.
Иммунодефицитные состояния, системные заболевания, приводящие к иммунной недостаточности, также провоцируют возникновение и рецидивы урогенитального кандидоза. Особенно тяжело протекает кандидаинфекция у ВИЧ-инфицированных пациентов. Нередко в терминальной стадии СПИДа развивается генерализованная кандидаинфекция.
К основным патогенетическим факторам традиционно относят дисбаланс микрофлоры влагалища, повышение концентрации эстрогена и прогестинов в тканях, нарушение местного иммунитета половых путей.
Вульвовагинальный кандидоз — наиболее часто употребляемое название заболевания, поскольку его основными клиническими проявлениями являются вульвит и вагинит. Однако по локализации выделяют также кандидозный цервицит, кольпит, уретрит, бартолинит. По характеру течения заболевания различают:
- острый (свежий, спорадический) кандидоз (протекает не более 2 мес);
- хронический, в том числе: а) рецидивирующий (не менее 4 эпизодов в год); б) персистирующий (симптомы заболевания сохраняются постоянно, несколько уменьшаясь после лечения).
Острый генитальный кандидоз характеризуется ярко выраженной воспалительной картиной. Основные жалобы и симптомы при кандидозном вульвовагините — зуд и жжение, постоянные или усиливающиеся во второй половине дня, вечером, ночью, после длительной ходьбы, а у пациентов с атопической предрасположенностью — под действием множества разных факторов. В области вульвы и половых губ зуд, как правило, интенсивный, сопровождается расчесами. Сильный, постоянный зуд нередко ведет к бессоннице, неврозам. Чувство зуда и жжения, боли, особенно в области расчесов, препятствует мочеиспусканию и может приводить к задержке мочи. Болезненность и чувство жжения во влагалище усиливаются во время коитуса и приводят к появлению страха перед половым сношением и расстройству половой жизни (диспареунии).
Следующий симптом — лейкорея. Бели не обильны, белого цвета, густые (сливкообразные) или хлопьевидные, творожистые, пленчатые, имеют нерезкий, кисловатый запах. Редко бывают водянистыми, с творожисто-крошковатыми вкраплениями. Могут отсутствовать полностью.
При поражении близлежащих кожных покровов отмечаются гиперемия, мацерация кожи, отдельные пустулезные элементы, зуд в области заднего прохода.
У пациентов, имеющих предрасположенность, кандидоз нередко рецидивирует, т. е. наблюдаются возвраты болезни после полного угасания клинических проявлений и восстановления нарушенных функций слизистой в процессе лечения. Если такие рецидивы наблюдаются не менее 4 раз в год, то заболевание классифицируется как хронический рецидивирующий вульвовагинальный кандидоз. Тактика лечения в этом случае отличается от таковой при спорадических эпизодах.
Другая форма течения хронической инфекции — персистирующий вульвовагинальный кандидоз, при котором клинические симптомы сохраняются постоянно и лишь несколько стихают после лечения. Рецидивы следует отличать от обострений, которые развиваются не после болезни, а на фоне сохраняющейся клинической симптоматики. Разумеется, и подход к лечению в этом случае несколько иной, чем при других формах.
Если ранее хронизацию и рецидивирование заболевания объясняли реинфицированием (либо эндо-, либо экзогенным), то в настоящее время причиной этих явлений считают состояние макроорганизма, так как постоянно выделяется один и тот же штамм гриба.
К вторичному вульвовагинальному кандидозу обычно относят случаи возникновения инфекции на фоне существующего неинфекционного поражения половых органов при красном плоском лишае, болезни Бехчета, пемфигоиде.
Как правило, симптомы кандидоза развиваются быстро, за неделю до менструации и несколько стихают во время менструации. При хронической персистирующей форме нарастает их интенсивность.
В плане дифференциальной диагностики схожие симптомы имеют две другие наиболее частые инфекции влагалища — бактериальный вагиноз и трихомониаз.
Симптомы бактериального вагиноза, как правило, возникают в первую неделю менструального цикла и самостоятельно проходят в середине цикла. Рецидив бактериального вагиноза иногда следует за рецидивом вагинального кандидоза.
Для острого трихомониаза характерны зуд и более выраженное жжение. Выделения, как правило, более обильные, жидкие, пенистые.
Микроскопия нативного препарата или окрашенного мазка — наиболее простой и доступный метод выявления гриба, его мицелия и спор. Культуральная диагностика рекомендуется лишь в некоторых случаях:
- для подтверждения диагноза при отрицательном результате микроскопии и наличии типичной клиники;
- для видовой идентификации при подозрении на нетипичную этиологию;
- для определения чувствительности к антимикотикам (обычно вместе с видовой идентификацией).
Выделение более 1•10 4 КОЕ/мл при отсутствии клиники расценивают как бессимптомную колонизацию (кандиданосительство), лечение при этом не назначается (10–25% населения являются транзиторными носителями Candida в полости рта, 65–80% — в кишечнике, 17% — в детрите гастродуоденальных язв). Однако при наличии предрасполагающих (провоцирующих) факторов (например, антибиотико-, химио-, лучевая, стероидная и др. иммуносупрессивная терапия) часто проводят профилактическое (превентивное) лечение. Широко применяемым профилактическим препаратом служит нистатин. Однако он эффективен для профилактики кандидоза только в просвете кишечника. Системная абсорбция его не более 3–5%, поэтому он не способен воздействовать на грибы, находящиеся не в просвете кишечника. Для профилактики урогенитального кандидоза предпочтение отдается местным формам антимикотиков (вагинальным таблеткам и свечам, растворам и мазям). В профилактике кандидоза у лиц, страдающих тяжелыми заболеваниями, которые рассматриваются в качестве предрасполагающих факторов (сахарный диабет), реально эффективными могут быть только системные азольные препараты и амфотерицин.
Противокандидозные препараты включают:
- полиены — нистатин, леворин, амфотерицин;
- имидазолы — кетоконазол, клотримазол, миконазол, бифоназол, изоконазол;
- триазолы — флуконазол, итраконазол;
- прочие — флуцитозин, нитрофунгин, декамин, препараты йода и др.
Большинство случаев вульвовагинального кандидоза поддается терапии местными противогрибковыми средствами и антисептиками.
Преимуществом местных средств является безопасность, так как системная абсорбция практически невелика, в то же время создаются очень высокие концентрации антимикотика непосредственно в области поражения, т. е. на поверхности слизистой.
Вагинальные кремы рекомендуются для лечения вульвитов, таблетки и суппозитории — вагинитов.
При лечении беременных женщин местные антимикотики по показаниям можно назначать только во II и III триместрах. Системные антимикотики при беременности не рекомендуются.
Довольно часто при кандидозном вульвовагините отмечаются сопутствующие инфекции или нарушение влагалищного микробиоценоза. В таких случаях используются комбинированные препараты, которые отличаются высокой клинической эффективностью и могут с успехом применяться в терапии вульвовагинитов смешанной этиологии. Среди таких препаратов наибольшей популярностью пользуются:
- травокорт — изоконазола нитрат + дифторкортолона-21-валерат;
- клион-Д — миконазол + метронидазол;
- макмирор комплекс 500 — нистатин + нифурател;
- полижинакс — нистатин + неомицин + полимиксин;
- тержинан — нистатин + неомицина сульфат + тернидазол + преднизолон.
Однако за рубежом комбинированные формы не рекомендуются к применению, так как, по мнению некоторых исследователей, они ухудшают фармакокинетику за счет конкуренции составляющих комбинированного препарата. В таких случаях предпочтение отдается сочетанию местного лечения с системным.
В терапии вульвовагинального кандидоза используются также местные антисептики:
- растворы соды, борной кислоты, тетрабората натрия, марганцовокислого калия (для спринцеваний и тампонов), анилиновых красителей (для смазывания в зеркалах);
- суппозитории — повидон-йодин (бетадин, вокадин, йодоксид) — на ночь;
- вагинальные капсулы — борная кислота 600 мг/сут;
- кортикостероидные кремы (I и II класса).
При выраженном вульвите назначают теплые ванночки с содой и местные кортикостероидные кремы I и II классов. Отличных результатов в ходе терапии удается достигнуть, применяя при выраженном вульвите крем травокорт, который содержит антимикотик изоконазол в сочетании с кортикостероидом II класса дифлукортолона-21-валератом. Такое оптимальное сочетание позволяет быстро купировать симптомы у женщин и особенно у мужчин. Этот крем удобен в применении, так как назначается всего 1 раз в сутки (на ночь) у женщин и 2 раза (утром и вечером) — у мужчин. Травокорт не имеет запаха и не пачкает белье.
Высокоактивные кортикостероидные мази III и IV классов не рекомендуются, так как могут привести к обострению, усилению симптомов. Патогенетическая терапия включает также использование антигистаминных препаратов и кетотифена.
В упорных случаях и при диссеминированном кандидозе предпочтение отдается системной терапии, а в ряде случаев — сочетанию системного и местного лечения.
При беременности и лактации использовать системные препараты не рекомендуется, а существующие в некоторых работах ссылки на положительные результаты не доказаны достаточным количеством наблюдений и научных исследований.
Продолжительность системной терапии при неосложненном вульвовагинальном кандидозе минимальна (однократный прием, или прием пероральных препаратов не более 5 дней).
Общей рекомендацией по лечению осложненных форм является удлинение курса терапии (объем местной и системной терапии увеличивается вдвое).
На основании собственного опыта нами предложены схемы терапии неосложненного и осложненного вульвовагинального кандидоза (табл.).
Наши наблюдения свидетельствуют о том, что наиболее адекватными являются методы профилактики рецидивов при помощи как местных, так и системных препаратов.
- Начальный курс: микофлюкан (флуконазол) по 50 мг ежедневно в течение 14 дней или по 150 мг 1 раз в 3 дня в течение 2 нед (всего на курс 14 таблеток по 50 мг или 5 таблеток по 150 мг).
- Профилактический курс: микофлюкан (флуконазол) по 150 мг 1 раз в неделю в течение 3–4 мес.
Начальный курс проводится такой же, как при хроническом рецидивирующем кандидозе. Поддерживающая терапия состоит в постоянном приеме противокандидозных препаратов: флуконазол (микофлюкан), таблетки по 150 мг,1–2 раза в месяц в течение 12–24 мес.
В лечении устойчивого к антимикотикам кандидоза, если терапия оказалась неэффективной, требуется повторно подтвердить диагноз, производя посев и выделение возбудителя с последующим определением его вида и чувствительности к противогрибковым препаратам. Выбор системного или местного антимикотика и его дозы далее осуществляется в соответствии с результатами исследования.
После повторного подтверждения диагноза возможен переход на местную терапию антимикотиками или антисептиками, назначаемыми в высоких дозах, часто и длительными курсами.
Целесообразно также использование витаминных комплексов, содержащих биотин.
Н. В. Кунгуров, доктор медицинских наук, профессор
Н. М. Герасимова, доктор биологических наук, профессор
И. Ф. Вишневская
Уральский НИИ дерматовенерологии и иммунопатологии Минздрава России, г. Екатеринбург
Оппортунистические инфекции, включая микозы органов пищеварения, представляют собой актуальную проблему современной гастроэнтерологии. Диагностика и лечение кандидоза пищевода в ряде случаев сопряжены с определенными трудностями.
Патогенез
Дрожжеподобные грибы рода Candida — одноклеточные микроорганизмы размерами 6-10 мкм. В различных условиях они образуют бластоспоры (клетки-почки) и псевдомицелий (нити удлиненных клеток). Дрожжи рода Candida широко распространены в окружающей среде: в почве, питьевой воде, пищевых продуктах, на коже и слизистых оболочках человека и животных. Исход контакта с дрожжеподобными грибами рода Candida обусловлен состоянием системы антифунгальной резистентности индивида. В большинстве случаев такой контакт формирует транзиторное кандидоносительство. В то же время у лиц с нарушениями в системе антифунгальной резистентности контакт может сформировать как персистирующее носительство и как кандидоз.
Перечисленным факторам патогенности естественным образом противостоят многочисленные факторы:
- целостность слизистой оболочки и мукополисахариды слизи;
- антагонизм дрожжеподобных грибов и бактерий пищеварительного тракта;
- активность пищеварительных ферментов и фунгистатического действия неспецифических гуморальных факторов, таких как лизоцим;
- функция клеток фагоцитарного ряда — полиморфноядерных лейкоцитов;
- специфический антифунгальный гуморальный ответ (реализуется за счет синтеза В-клетками специфических противокандидозных антител).
Дефекты в описанной выше системе антифунгальной резистентности являются факторами, способствующими возникновению кандидоза.
1. Физиологические иммунодефициты (детский, старческий возраст, беременность).
2. Генетически детерминированные (первичные) иммунодефициты.
4. Онкологические заболевания, особенно на фоне лучевой и химиотерапии.
5. Аллергические и аутоиммунные болезни, особенно на фоне лечения глюкокортикостероидами.
6. Заболевания эндокринной системы, в первую очередь, сахарный диабет, аутоиммунный полиэндокринный синдром, гипотиреоз, ожирение и др.
7. Дисбиоз на фоне антибиотикотерапии.
9. Трансплантация органов и тканей.
Внедрение грибов рода Candida чаще наблюдается в участках, представленных многослойным эпителием (полость рта, пищевод) и значительно реже - в однослойный эпителий (желудок, кишечник).
На практике клиницисту приходится сталкиваться, преимущественно, с кандидоносительством, частота которого у здоровых лиц достигает в полости рта 25%, а в кишечнике — до 65–80%.
Диагностика
Объем обследования органов пищеварения при кандидозе включает изучение анамнеза и клинической картины, оценку рутинных клинических тестов, эндоскопические исследования, микологические (культуральные, морфологические и серологические) и иммунологические тесты.
Кандидоз пищевода встречается у больных общего профиля в 1–2% случаев, у больных сахарным диабетом 1 типа — в 5–10% случаев, у больных СПИДом — в 15–30% случаев.
Среди местных факторов риска называют ожог, ахалазию, дивертикулез, полипоз пищевода.
Характерными жалобами являются дисфагия, одинофагия, ретростернальный дискомфорт, однако встречается и латентное течение.
Симптомы кандидоза пищевода могут нарушить акт глотания, что в свою очередь, приводит к нарушению питания и значительному снижению качества жизни.
Показаниями для эндоскопического исследования с целью исключения кандидоза пищевода является: группа риска, клинические признаки эзофагита и верифицированный кандидоз других локализаций.
Среди всего разнообразия визуальных признаков кандидоза пищевода можно выделить три группы типичных изменений:
2. Фибринозный (псевдомембранозный) эзофагит. Наблюдают бело-серые или бело-желтые рыхлые налеты в виде округлых бляшек диаметром от 1 до 5 мм, выступающие над ярко гиперемированной и отечной слизистой оболочкой. Контактная ранимость и гиперемия слизистой оболочки заметно выражены.
Схожие эндоскопические изменения могут наблюдаться при рефлюкс-эзофагите, пищеводе Барретта, герпес-эзофагите, плоских лейкоплакиях, красном плоском лишае, ожоге или опухоли пищевода, поэтому диагностика кандидоза пищевода основана на эндоскопическом исследовании и лабораторном изучении биопсийных материалов из пораженных участков.
Культуральный микологический метод основан на посеве биоматериалов слизистых оболочек на среду Сабуро. Преимущество данного метода — в возможности видовой идентификации грибов рода Candida и тестировании культуры на чувствительность к антимикотикам. Культуральное исследование биоматериалов слизистых оболочек с определением вида возбудителя становится строго необходимым при рецидивирующем течении кандидоза или резистентности к стандартной антимикотической терапии.
Осложнения
Кандидоз пищевода опасен своими осложнениями: стриктурой, кровотечением, перфорацией и диссеминацией микотического поражения.
Развитие стриктуры пищевода отмечают у 8–9% пациентов с кандидозным эзофагитом. Чаще они локализованы в верхней или средней трети грудного отдела пищевода и вызывают перманентную дисфагию.
Хроническое кровотечение вызвано контактной ранимостью слизистой оболочки, оно малоинтенсивное, приводит к анемии.
Клиническая картина перфорации пищевода характеризуется, кроме интенсивного болевого синдрома, развитием пневмомедиастинума и подкожной эмфиземы в области шеи.
Лечение
В план ведения пациентов с кандидозом пищевода необходимо включить диагностику и коррекцию фоновых заболеваний, других очагов кандидозной инфекции, рациональную антифунгальную терапию и иммунокоррекцию. Также необходимо исключение злокачественных опухолей, рентгенография легких, фиброколоноскопия, дополнительно для мужчин — УЗИ предстательной железы, дополнительно для женщин — УЗИ молочных желез и малого таза с консультацией гинеколога.
Лечение кандидоза пищевода основано на применении антифунгальных препаратов:
- полиеновые антимикотики (амфотерицин В, нистатин и натамицин);
- азольные антимикотики (кетоконазол, флуконазол, итраконазол, вориконазол, позаконазол);\
- эхинокандины (каспофунгин, анидулафунгин, микафунгин).
Цель лечения кандидоза слизистых оболочек верхних отделов пищеварительного тракта — устранение симптомов и клинико-лабораторных признаков заболевания, а также предотвращение рецидивов.
Нужно подчеркнуть, что при кандидозе пищевода местная терапия неэффективна. У больных с выраженной одинодисфагией, которые не способны глотать, должна использоваться парентеральная терапия.
Несмотря на высокую эффективность флуконазола у пациентов с сохраняющимся иммунодефицитным состоянием высока вероятность рецидивов кандидоза пищевода. Необходимо помнить, что безрецидивного течения кандидоза можно достичь только у больных с полной коррекцией фонового состояния. Так, например, при СПИДе рецидивы кандидоза прекращаются только при успешной антиретровирусной терапии, обеспечивающей снижение вирусной нагрузки и увеличение числа CD4-лимфоцитов.
Зав. эндоскопическим отделением
Новополоцкой городской больницы
Кожушкевич А.Ю.
Приемная главного врача
(+375 214) 50-62-70
(+375 214) 50-62-11 (факс)
Канцелярия
(+375 214) 50-15-39 (факс)
Известно, что грибковые инфекции занимают одну из ключевых позиций среди заболеваний слизистой оболочки полости рта по распространенности среди населения и тяжести возможных осложнений для организма пациента.
В последние годы во всем мире, и особенно в развитых странах, наблюдается значительное увеличение числа грибковых заболеваний, вызываемых дрожжеподобными грибами рода Candida.
Согласно последним исследованиям, кандидоз слизистой оболочки рта относится к наиболее распространенным заболеваниям, что подтверждается увеличением его распространенности среди других заболеваний слизистой оболочки рта до 63% [30].
Основываясь на данных современных литературных источников, лечение кандидоза должно быть комплексным, с повторными курсами и индивидуальным подходом. При проведении лечебных мероприятий учитывают этиологию, характер и продолжительность заболевания 17.
Кандидоносительство статистически определяется у 5% младенцев, у лиц же пожилого возраста этот показатель увеличивается до 60% [6]. Однако истинное проявление патогенных свойств грибов рода Candida зависит главным образом от состояния макроорганизма. Главную роль в развитии кандидоза играет ослабление иммунной системы. Именно состояние функциональной системы ротовой полости у каждого индивидуума с учетом его возраста, гигиенических навыков и других факторов характеризует экосистему в целом. Кандидоз возникает, как правило, на фоне более или менее выраженного иммунодефицита или дисбаланса иммунной системы [14].
Развитию кандидоза могут способствовать тяжелые сопутствующие заболевания: злокачественные новообразования, ВИЧ-инфекция, туберкулез, эндокринопатии (сахарный диабет, гипотиреоз, гипопаратиреоз, гипо- и гиперфункция надпочечников). Заболевания желудочно-кишечного тракта, особенно пониженная кислотность желудочного сока и ахилия, часто обусловливают развитие кандидоза слизистой оболочки рта.
Возникновению кандидоза слизистой оболочки полости рта способствует длительное лечение кортикостероидными препаратами, цитостатиками, которые подавляют иммунную систему организма и усиливают вирулентность дрожжеподобных грибов [15].
Однако следует отметить, что используемые большинством пародонтологов антисептики при их разведении ротовой жидкостью явно снижают свою активность, а некоторые антисептики, например, хлоргексидин, оказывают побочное действие [6,13,23 и др.]. Что касается применяемых в настоящее время иммунотерапевтических препаратов, то иммуномодулятор левамизол обладает пирогенными свойствами [24], а имудон эффективен лишь при легких формах заболеваний пародонта [3].
Вследствие широкого применения антибиотиков за последние годы значительно увеличилось количество больных кандидозом слизистой оболочки рта. Длительный прием антибиотиков нарушает состав резидентной микрофлоры полости рта, в результате чего формируется дисбактериоз. Происходят угнетение резидентной микрофлоры полости рта и резкий рост вирулентности условно патогенных грибов рода Candida, вызывающих заболевание слизистой оболочки рта (суперинфекция, аутоинфекция). Прием антибиотиков может вызвать также дисбактериоз кишечника, следствием чего являются гипо- и авитаминозы В, В2, В6, С, РР, что в свою очередь отрицательно сказывается на функциональном состоянии слизистой оболочки рта (она становится подверженной влиянию кандидозной инфекции).
В настоящее время, с учетом всего вышеперечисленного, кандидоз рассматривается как иммуннодефицитное состояние, возникшее в результате существенной разбалансировки экосистемы в целом. Такое представление о заболевании обуславливает принципиальную необходимость комплексного лечения кандидоза, в состав которого будут непременно включаться:
- мероприятия, направленные на устранение местных проявлений заболевания;
- мероприятия для системного лечения проявлений кандидоза;
- мероприятия, направленные на восстановление и нормализацию функций иммунной системы.
Материалы и методы исследования
Таблица 1. Общее количество пациентов
| Возраст | Количество пациентов | ||
| муж. | жен. | Всего | |
| 20-30 | 5 | 7 | 12 |
| 31-40 | 10 | 8 | 18 |
| 41-50 | 9 | 11 | 20 |
| Общее число | 24 | 26 | 50 |
По мнению Шумского А.В. (2009), системная терапия кандидоза слизистой оболочки рта назначается при определенных показаниях: хронический гиперпластический кандидоз, эрозивно-язвенная форма кандидоза, кандидоз рта на фоне сахарного диабета, иммунодефицитного состояния, при неэффективной местной терапии [32].
В схему местного лечения входит комплекс мероприятий, включающих профессиональную гигиену полости рта, санацию рта, ортопедическое лечение, коррекцию протезов и др. [7].
По данным современных литературных источников, используемые в лечении кандидоза противогрибковые средства подразделяются на полиеновые антибиотики (нистатин), азольные соединения (флуконазол), аллиламиновые средства (нафтифин и тербинафин), смешанные вещества (антисептики, щелочные полоскания и анилиновые красители) [31].
Антисептическим препаратом из группы четвертичных аммониевых соединений является Мирамистин ® , который обладает широким спектром антимикробного действия, включая госпитальные штаммы, резистентные к антибиотикам.
Рис. 1. Бензилдиметил[3-(миристоиламино)пропил] аммоний хлорид, моногидрат
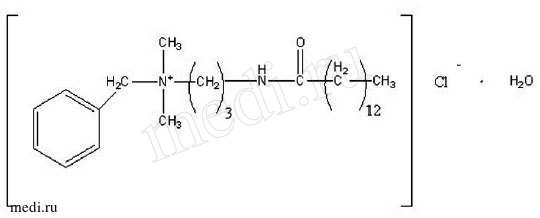
Активное вещество препарата -бензилдиметил[3-(миристоиламино) пропил]аммоний хлорид, моногидрат - относится к классу поверхностно-активных веществ (см. рис. 1).
Проведенные экспериментальные исследования показали, что препарат оказывает выраженное бактерицидное действие в отношении грамположительных (Staphylococcus spp., Streptococcus spp., Streptococcus pneumoniae и др.), грамотрицательных (Pseudomonas aeruginosa, Escherichia coli, Klebsiella spp. и др.), аэробных и анаэробных бактерий, определяемых в виде монокультур и микробных ассоциаций, включая госпитальные штаммы с полирезистентностью к антибиотикам. Оказывает противогрибковое действие на аскомицеты рода Aspergillus и рода Penicillium, дрожжевые (Rhodotorula rubra, Torulopsis glabrata и т.д.) и дрожжеподобные грибы (Candida albicans, Candida tropicalis, Candida krusei, Pityrosporum orbiculare (Malassezia furfur) и т.д.), дерматофиты (Trichophyton rubrum, Trichophyton mentagrophytes, Trichophyton verrucosum, Trichophyton schoenleini, Trichophyton violacent, Epidermophyton Kaufman-Wolf, Epidermophyton floccosum, Microsporum gypseum, Microsporum canis и т.д.), атакже на др. патогенные грибы в виде монокультур и микробных ассоциаций, включая грибковую микрофлору с резистентностью кхимиотерапевтическим препаратам (см. рис. 2) [1, 9].
Рис. 2. Преобладающий механизм действия мирамистина
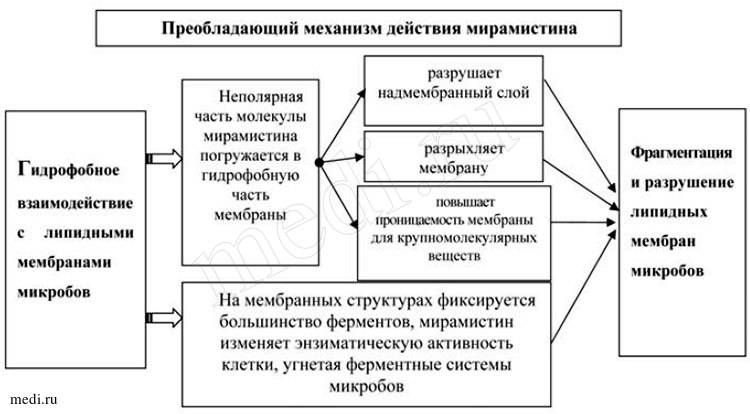
Кроме того, мирамистин характеризуется низкой токсичностью, отсутствием аллергизирующего и раздражающего действия. Мирамистин ускоряет репаративную активность, а также усиливает действие антибиотиков, снижая устойчивость бактерий и грибов к ним; обладает противовоспалительным действием; эффективно действует на патогенные микроорганизмы, не оказывая при этом отрицательного действия на ткани организма человека; повышает местный иммунитет - стимулирует защитные реакции в месте применения за счет активации поглотительной и переваривающей функции фагоцитов; потенцирует активность моноцитарно-макрофагальной системы (см. рис. 2) [25].
В ходе исследования мирамистин применялся для лечения кандидоза слизистой оболочки полости рта в виде бактерицидной повязки. Курс лечения кандидоза составил 21 день.
Спектр антимикробного действия мирамистина довольно широк и включает грамположительные (стрептококки, стафиллококки), грамотрицательные (гонококки, эшерихии, вибрионы, спирохеты, шигеллы, сальмонеллы), а также вирусы гриппа, герпеса, грибы рода Candida и простейшие [9, 11, 12, 20, 33].
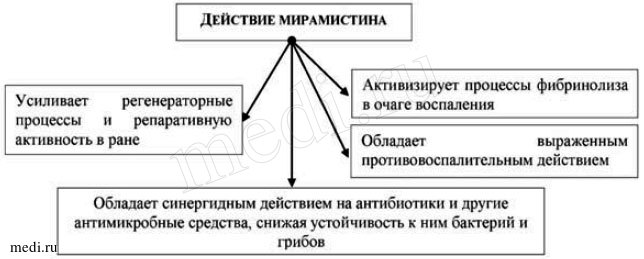
Изучение фармакодинамических свойств мирамистина показало, что наряду с антимикробным действием препарат стимулирует репаративные процессы и функциональную активность иммунокомпетентных клеток, оказывая иммуномодулирующее действие в патологическом очаге [18]. При комбинированном применении мирамистина с антибиотиками он замедляет развитие резистентности микрофлоры к антибиотикам [21]. Мирамистин устойчив во внешней среде. Действие мирамистина представлено на рис. 3.
Рис. 3. Действие мирамистина
Конечно, нельзя исключать и возможность общего воздействия на обменные процессы. Поэтому автор статьи рекомендует включать в комплекс терапии расшлаковку (детоксикацию) ЖКТ (полисорб, лактофильтрум, активированный уголь), лечение дисбактериоза (нормофлорин-Л и нормофлорин-Б, биовестин-лакто) [2].
Таблица 2. Количественное определение состояния индексов индивидуальной гигиены полости рта до лечения
| Возраст | Индексы индивидуальной гигиены полости рта | |||
| Silness-Loe | РМА | Kotzschke | SBI | |
| 20-30 | 0,95 | 30% | II степень | 4 |
| 31-40 | 1,5 | 45% | II степень | 4 |
| 41-50 | 2,6 | 60% | II степень | 4 |
| Средний показатель | 1,68 | от 30% до 60% (средняя степень тяжести гингивита) | II степень | 4 |
Таблица 3. Количественное определение состояния индексов индивидуальной гигиены полости рта при лечении кандидоза в динамике
| Возраст | Индексы индивидуальной гигиены полости рта | |||||||
| Silness-Loe | РМА | Kotzschke | SBI | |||||
| 3 нед. | 3 мес. | 3 нед. | 3 мес. | 3 нед. | 3 мес. | 3 нед. | 3 мес. | |
| 20-30 | 0,3 | 0,2 | 6% | 5% | I степень | I степень | 1 | 1 |
| 31-40 | 0,8 | 0,7 | 16% | 14% | I степень | I степень | 1 | 1 |
| 41-50 | 1,6 | 1,4 | 22% | 20% | I степень | I степень | 1 | 1 |
| Средний показатель | 0,9 | 0,77 | от 6% до 22% | от 5% до 30% | I степень | I степень | 1 | 1 |
| легкая степень тяжести гингивита | ||||||||
Таблица 4. Количественные данные исследования применения мирамистина в комплексе с медикаментозной терапией при лечении пациентов с диагнозом кандидоз слизистой оболочки полости рта*
| Кол-во пациентов** | Отсутствие признаков заболевания | ||
| Через 3 нед.*** | Через 3 мес.*** | ||
| Число пациентов | 50 человек | 84% (43 человек) | 90% (45 человек) |
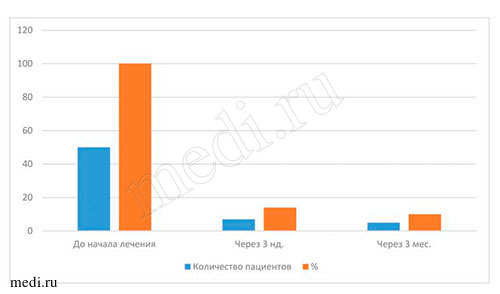
Таблица 5. Данные бактериологического исследования материала при применении мирамистина в комплексе с медикаментозной терапией при лечении пациентов с диагнозом кандидоз слизистой оболочки полости рта*
| Динамика изменения количества пациентов с наличием грибов рода Candida | |||
| До начала лечения | Через 3 нед.** | Через 3 мес.** | |
| Число пациентов | 50 | 7 | 5 |
| % | 100 | 14 | 10 |
Результаты исследования и их обсуждение
Оценка эффективности лечения складывалась из совокупности субъективных и объективных данных, полученных в процессе исследования. В качестве субъективных данных рассматривались наличие или отсутствие жалоб у пациента, а также оценка врачом клинической картины заболевания.
Оценка основных показателей пародонтологического статуса включала: количественное определение уровня гигиены полости рта с использованием индекса РМА, индекса Silness-Loe (Silness I., Loe H.), индекса Kotzschke (1975), индекса кровоточивости десневой борозды (SBI) (Muehlemann, Son, 1971) [28].
Оценка гигиенического состояния полости рта проводилась по количеству зубного налёта. Индекс гигиены Silness-Loe основан на определении количества мягкого зубного налёта в придесневой борозде. Папиллярно-маргинально-альвеолярный индекс предназначен для оценки тяжести гингивита. Наличие воспалительных заболеваний пародонта является одним из показателей кандидоза. Индекс Kotzschke (1975) фиксирует кровоточивость по данным анамнеза. Индекс кровоточивости десневой борозды (SBI) (Muehlemann, Son, 1971) учитывает кровотечение из десневой борозды, возникающее при зондировании, а также гиперемию, припухлость и отек десны (см. табл. 2-3 и рис. 4-5).
Рис. 4. Количественное определение индекса Silness-Loe
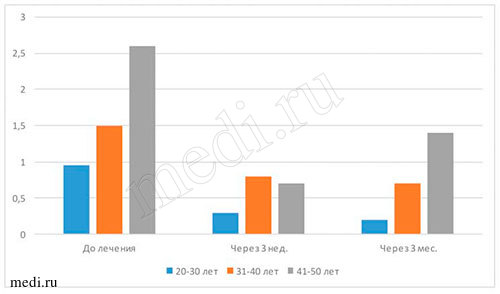
Рис. 5. Количественное определение индекса РМА
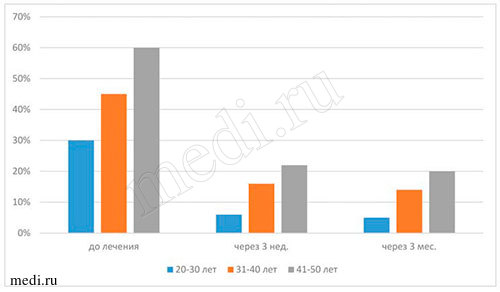
Рис. 6. Данные бактериального посева на определение содержания грибов рода Candida и отсутствие почкующегося мицелия на дорсальной поверхности языка во всех возрастных группах исследуемых при применении мирамистина в комплексе с медикаментозной терапией пациентов с диагнозом кандидоз слизистой оболочки полости рта
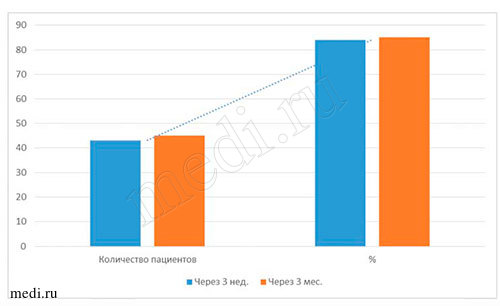
Рис. 7. Данные бактериологического исследования материала при применении мирамистина в комплексе с медикаментозной терапией пациентов с диагнозом кандидоз слизистой оболочки полости рта
Изучение динамики воспалительного процесса на фоне лечения в различных возрастных группах пациентов свидетельствует о следующем:
- кровоточивость десен при чистке зубов(индекс Kotzschke) - до начала лечения II степень, после лечения - снизилась до I степени; припухлость и отек десен отсутствовали, отмечались незначительная гиперемия десен и кровотечение из десневой борозды при зондировании (индекс SBI до начала лечения соответствовал 4, а после лечения равен 1); снизилось количество мягкого зубного налета в придесневой борозде (индекс Silness-Loe - до начале лечения - 1,68, а в конце лечения - 0,9); индекс РМАдо начала лечения находился в интервале от 30% до 60%, в конце лечения - от 6% до 22% (до начала лечения отмечалась средняя степень гингивита, а в конце лечения - легкая степень гингивита).
Следует отметить, что числовые значения вышеуказанных показателей через 3 месяца после лечения незначительно снизились.
Наиболее объективными показателями эффективности лечения пациентов всех возрастных групп с диагнозом кандидоз слизистой оболочки полости рта являются результаты, полученные при бактериологических исследованиях материала на определение содержания грибов рода Candida на дорсальной поверхности языка. По полученным данным, во всех исследуемых возрастных группах пациентов до начала лечения мирамистином грибы рода Candida были выявлены у 100% (50 человек), через 3 нед. - приближались к норме (14% - у 7 чел.), через 3 мес. - отмечены единичные проявления (10% - 5 человек). Данные, полученные через 3 нед. и 3 мес. после курса лечения, свидетельствуют о прогрессирующей динамике лечения мирамистином в комплексе с другими препаратами (см. выше) пациентов с диагнозом кандидоз слизистой оболочки полости рта во всех возрастных группах. По моему мнению, незначительное количество грибов рода Candida на дорсальной поверхности языка у пациентов всех возрастных групп могло быть обусловлено многими факторами, например, ремиссией заболевания, возрастными изменениями организма, особенностями иммунитета, географией проживания,экологией местности и т.д. (см. табл. 4-5 и рис. 6-7).
Заключение
Применение мирамистина в комплексе с медикаментозной терапией кандидоза полости рта в течение 3 мес. уменьшает тяжесть воспалительного процесса и образование зубного налета и обеспечивает стойкий положительный клинический эффект, что подтверждается длительной нормализацией цитологических и микробиологических показателей.
Данные, полученные при проведенном исследовании, ярко свидетельствуют о том, что при лечении кандидоза слизистой оболочки полости рта необходимо воздействовать не только на возбудителя инфекционного процесса, но и на все предрасполагающие факторы заболевания. Терапия, направленная на все звенья патологического процесса, позволяет повысить эффективность лечения и, кроме того, способствует достижению длительного периода ремиссии заболевания.
Читайте также:


