Можно ли использовать мирамистин при молочнице у ребенка
Известно, что грибковые инфекции занимают одну из ключевых позиций среди заболеваний слизистой оболочки полости рта по распространенности среди населения и тяжести возможных осложнений для организма пациента.
В последние годы во всем мире, и особенно в развитых странах, наблюдается значительное увеличение числа грибковых заболеваний, вызываемых дрожжеподобными грибами рода Candida.
Согласно последним исследованиям, кандидоз слизистой оболочки рта относится к наиболее распространенным заболеваниям, что подтверждается увеличением его распространенности среди других заболеваний слизистой оболочки рта до 63% [30].
Основываясь на данных современных литературных источников, лечение кандидоза должно быть комплексным, с повторными курсами и индивидуальным подходом. При проведении лечебных мероприятий учитывают этиологию, характер и продолжительность заболевания 17.
Кандидоносительство статистически определяется у 5% младенцев, у лиц же пожилого возраста этот показатель увеличивается до 60% [6]. Однако истинное проявление патогенных свойств грибов рода Candida зависит главным образом от состояния макроорганизма. Главную роль в развитии кандидоза играет ослабление иммунной системы. Именно состояние функциональной системы ротовой полости у каждого индивидуума с учетом его возраста, гигиенических навыков и других факторов характеризует экосистему в целом. Кандидоз возникает, как правило, на фоне более или менее выраженного иммунодефицита или дисбаланса иммунной системы [14].
Развитию кандидоза могут способствовать тяжелые сопутствующие заболевания: злокачественные новообразования, ВИЧ-инфекция, туберкулез, эндокринопатии (сахарный диабет, гипотиреоз, гипопаратиреоз, гипо- и гиперфункция надпочечников). Заболевания желудочно-кишечного тракта, особенно пониженная кислотность желудочного сока и ахилия, часто обусловливают развитие кандидоза слизистой оболочки рта.
Возникновению кандидоза слизистой оболочки полости рта способствует длительное лечение кортикостероидными препаратами, цитостатиками, которые подавляют иммунную систему организма и усиливают вирулентность дрожжеподобных грибов [15].
Однако следует отметить, что используемые большинством пародонтологов антисептики при их разведении ротовой жидкостью явно снижают свою активность, а некоторые антисептики, например, хлоргексидин, оказывают побочное действие [6,13,23 и др.]. Что касается применяемых в настоящее время иммунотерапевтических препаратов, то иммуномодулятор левамизол обладает пирогенными свойствами [24], а имудон эффективен лишь при легких формах заболеваний пародонта [3].
Вследствие широкого применения антибиотиков за последние годы значительно увеличилось количество больных кандидозом слизистой оболочки рта. Длительный прием антибиотиков нарушает состав резидентной микрофлоры полости рта, в результате чего формируется дисбактериоз. Происходят угнетение резидентной микрофлоры полости рта и резкий рост вирулентности условно патогенных грибов рода Candida, вызывающих заболевание слизистой оболочки рта (суперинфекция, аутоинфекция). Прием антибиотиков может вызвать также дисбактериоз кишечника, следствием чего являются гипо- и авитаминозы В, В2, В6, С, РР, что в свою очередь отрицательно сказывается на функциональном состоянии слизистой оболочки рта (она становится подверженной влиянию кандидозной инфекции).
В настоящее время, с учетом всего вышеперечисленного, кандидоз рассматривается как иммуннодефицитное состояние, возникшее в результате существенной разбалансировки экосистемы в целом. Такое представление о заболевании обуславливает принципиальную необходимость комплексного лечения кандидоза, в состав которого будут непременно включаться:
- мероприятия, направленные на устранение местных проявлений заболевания;
- мероприятия для системного лечения проявлений кандидоза;
- мероприятия, направленные на восстановление и нормализацию функций иммунной системы.
Материалы и методы исследования
Таблица 1. Общее количество пациентов
| Возраст | Количество пациентов | ||
| муж. | жен. | Всего | |
| 20-30 | 5 | 7 | 12 |
| 31-40 | 10 | 8 | 18 |
| 41-50 | 9 | 11 | 20 |
| Общее число | 24 | 26 | 50 |
По мнению Шумского А.В. (2009), системная терапия кандидоза слизистой оболочки рта назначается при определенных показаниях: хронический гиперпластический кандидоз, эрозивно-язвенная форма кандидоза, кандидоз рта на фоне сахарного диабета, иммунодефицитного состояния, при неэффективной местной терапии [32].
В схему местного лечения входит комплекс мероприятий, включающих профессиональную гигиену полости рта, санацию рта, ортопедическое лечение, коррекцию протезов и др. [7].
По данным современных литературных источников, используемые в лечении кандидоза противогрибковые средства подразделяются на полиеновые антибиотики (нистатин), азольные соединения (флуконазол), аллиламиновые средства (нафтифин и тербинафин), смешанные вещества (антисептики, щелочные полоскания и анилиновые красители) [31].
Антисептическим препаратом из группы четвертичных аммониевых соединений является Мирамистин ® , который обладает широким спектром антимикробного действия, включая госпитальные штаммы, резистентные к антибиотикам.
Рис. 1. Бензилдиметил[3-(миристоиламино)пропил] аммоний хлорид, моногидрат
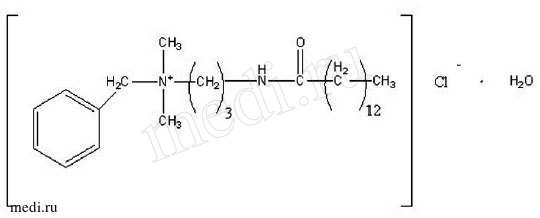
Активное вещество препарата -бензилдиметил[3-(миристоиламино) пропил]аммоний хлорид, моногидрат - относится к классу поверхностно-активных веществ (см. рис. 1).
Проведенные экспериментальные исследования показали, что препарат оказывает выраженное бактерицидное действие в отношении грамположительных (Staphylococcus spp., Streptococcus spp., Streptococcus pneumoniae и др.), грамотрицательных (Pseudomonas aeruginosa, Escherichia coli, Klebsiella spp. и др.), аэробных и анаэробных бактерий, определяемых в виде монокультур и микробных ассоциаций, включая госпитальные штаммы с полирезистентностью к антибиотикам. Оказывает противогрибковое действие на аскомицеты рода Aspergillus и рода Penicillium, дрожжевые (Rhodotorula rubra, Torulopsis glabrata и т.д.) и дрожжеподобные грибы (Candida albicans, Candida tropicalis, Candida krusei, Pityrosporum orbiculare (Malassezia furfur) и т.д.), дерматофиты (Trichophyton rubrum, Trichophyton mentagrophytes, Trichophyton verrucosum, Trichophyton schoenleini, Trichophyton violacent, Epidermophyton Kaufman-Wolf, Epidermophyton floccosum, Microsporum gypseum, Microsporum canis и т.д.), атакже на др. патогенные грибы в виде монокультур и микробных ассоциаций, включая грибковую микрофлору с резистентностью кхимиотерапевтическим препаратам (см. рис. 2) [1, 9].
Рис. 2. Преобладающий механизм действия мирамистина
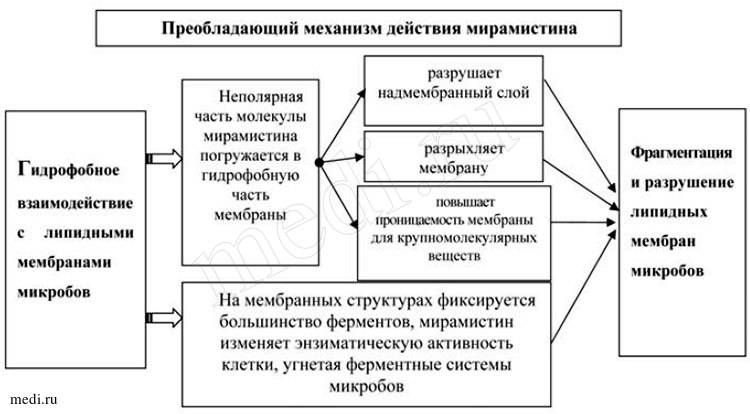
Кроме того, мирамистин характеризуется низкой токсичностью, отсутствием аллергизирующего и раздражающего действия. Мирамистин ускоряет репаративную активность, а также усиливает действие антибиотиков, снижая устойчивость бактерий и грибов к ним; обладает противовоспалительным действием; эффективно действует на патогенные микроорганизмы, не оказывая при этом отрицательного действия на ткани организма человека; повышает местный иммунитет - стимулирует защитные реакции в месте применения за счет активации поглотительной и переваривающей функции фагоцитов; потенцирует активность моноцитарно-макрофагальной системы (см. рис. 2) [25].
В ходе исследования мирамистин применялся для лечения кандидоза слизистой оболочки полости рта в виде бактерицидной повязки. Курс лечения кандидоза составил 21 день.
Спектр антимикробного действия мирамистина довольно широк и включает грамположительные (стрептококки, стафиллококки), грамотрицательные (гонококки, эшерихии, вибрионы, спирохеты, шигеллы, сальмонеллы), а также вирусы гриппа, герпеса, грибы рода Candida и простейшие [9, 11, 12, 20, 33].
Изучение фармакодинамических свойств мирамистина показало, что наряду с антимикробным действием препарат стимулирует репаративные процессы и функциональную активность иммунокомпетентных клеток, оказывая иммуномодулирующее действие в патологическом очаге [18]. При комбинированном применении мирамистина с антибиотиками он замедляет развитие резистентности микрофлоры к антибиотикам [21]. Мирамистин устойчив во внешней среде. Действие мирамистина представлено на рис. 3.
Рис. 3. Действие мирамистина
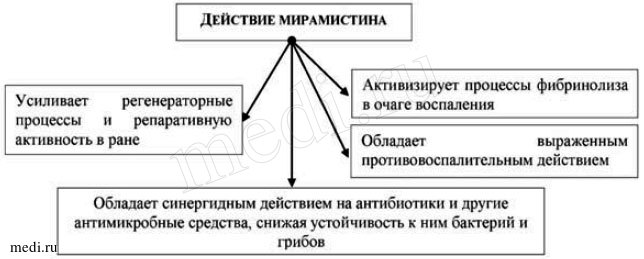
Конечно, нельзя исключать и возможность общего воздействия на обменные процессы. Поэтому автор статьи рекомендует включать в комплекс терапии расшлаковку (детоксикацию) ЖКТ (полисорб, лактофильтрум, активированный уголь), лечение дисбактериоза (нормофлорин-Л и нормофлорин-Б, биовестин-лакто) [2].
Таблица 2. Количественное определение состояния индексов индивидуальной гигиены полости рта до лечения
| Возраст | Индексы индивидуальной гигиены полости рта | |||
| Silness-Loe | РМА | Kotzschke | SBI | |
| 20-30 | 0,95 | 30% | II степень | 4 |
| 31-40 | 1,5 | 45% | II степень | 4 |
| 41-50 | 2,6 | 60% | II степень | 4 |
| Средний показатель | 1,68 | от 30% до 60% (средняя степень тяжести гингивита) | II степень | 4 |
Таблица 3. Количественное определение состояния индексов индивидуальной гигиены полости рта при лечении кандидоза в динамике
| Возраст | Индексы индивидуальной гигиены полости рта | |||||||
| Silness-Loe | РМА | Kotzschke | SBI | |||||
| 3 нед. | 3 мес. | 3 нед. | 3 мес. | 3 нед. | 3 мес. | 3 нед. | 3 мес. | |
| 20-30 | 0,3 | 0,2 | 6% | 5% | I степень | I степень | 1 | 1 |
| 31-40 | 0,8 | 0,7 | 16% | 14% | I степень | I степень | 1 | 1 |
| 41-50 | 1,6 | 1,4 | 22% | 20% | I степень | I степень | 1 | 1 |
| Средний показатель | 0,9 | 0,77 | от 6% до 22% | от 5% до 30% | I степень | I степень | 1 | 1 |
| легкая степень тяжести гингивита | ||||||||
Таблица 4. Количественные данные исследования применения мирамистина в комплексе с медикаментозной терапией при лечении пациентов с диагнозом кандидоз слизистой оболочки полости рта*
| Кол-во пациентов** | Отсутствие признаков заболевания | ||
| Через 3 нед.*** | Через 3 мес.*** | ||
| Число пациентов | 50 человек | 84% (43 человек) | 90% (45 человек) |
Таблица 5. Данные бактериологического исследования материала при применении мирамистина в комплексе с медикаментозной терапией при лечении пациентов с диагнозом кандидоз слизистой оболочки полости рта*
| Динамика изменения количества пациентов с наличием грибов рода Candida | |||
| До начала лечения | Через 3 нед.** | Через 3 мес.** | |
| Число пациентов | 50 | 7 | 5 |
| % | 100 | 14 | 10 |
Результаты исследования и их обсуждение
Оценка эффективности лечения складывалась из совокупности субъективных и объективных данных, полученных в процессе исследования. В качестве субъективных данных рассматривались наличие или отсутствие жалоб у пациента, а также оценка врачом клинической картины заболевания.
Оценка основных показателей пародонтологического статуса включала: количественное определение уровня гигиены полости рта с использованием индекса РМА, индекса Silness-Loe (Silness I., Loe H.), индекса Kotzschke (1975), индекса кровоточивости десневой борозды (SBI) (Muehlemann, Son, 1971) [28].
Оценка гигиенического состояния полости рта проводилась по количеству зубного налёта. Индекс гигиены Silness-Loe основан на определении количества мягкого зубного налёта в придесневой борозде. Папиллярно-маргинально-альвеолярный индекс предназначен для оценки тяжести гингивита. Наличие воспалительных заболеваний пародонта является одним из показателей кандидоза. Индекс Kotzschke (1975) фиксирует кровоточивость по данным анамнеза. Индекс кровоточивости десневой борозды (SBI) (Muehlemann, Son, 1971) учитывает кровотечение из десневой борозды, возникающее при зондировании, а также гиперемию, припухлость и отек десны (см. табл. 2-3 и рис. 4-5).
Рис. 4. Количественное определение индекса Silness-Loe
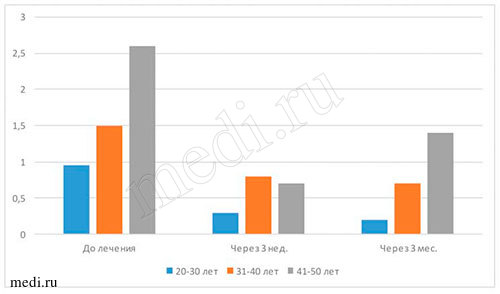
Рис. 5. Количественное определение индекса РМА
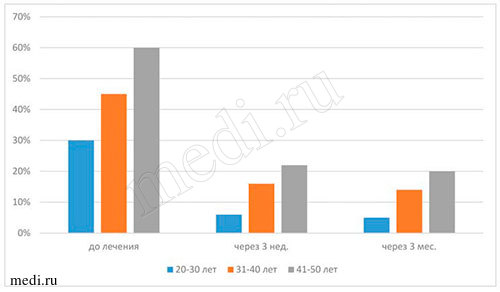
Рис. 6. Данные бактериального посева на определение содержания грибов рода Candida и отсутствие почкующегося мицелия на дорсальной поверхности языка во всех возрастных группах исследуемых при применении мирамистина в комплексе с медикаментозной терапией пациентов с диагнозом кандидоз слизистой оболочки полости рта
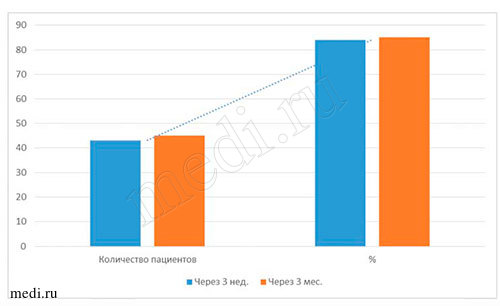
Рис. 7. Данные бактериологического исследования материала при применении мирамистина в комплексе с медикаментозной терапией пациентов с диагнозом кандидоз слизистой оболочки полости рта
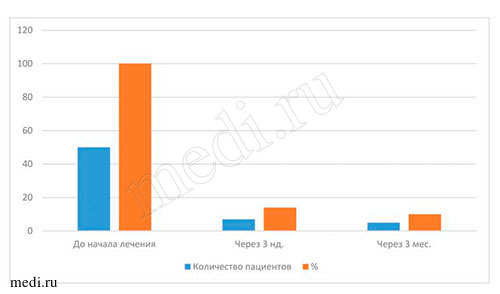
Изучение динамики воспалительного процесса на фоне лечения в различных возрастных группах пациентов свидетельствует о следующем:
- кровоточивость десен при чистке зубов(индекс Kotzschke) - до начала лечения II степень, после лечения - снизилась до I степени; припухлость и отек десен отсутствовали, отмечались незначительная гиперемия десен и кровотечение из десневой борозды при зондировании (индекс SBI до начала лечения соответствовал 4, а после лечения равен 1); снизилось количество мягкого зубного налета в придесневой борозде (индекс Silness-Loe - до начале лечения - 1,68, а в конце лечения - 0,9); индекс РМАдо начала лечения находился в интервале от 30% до 60%, в конце лечения - от 6% до 22% (до начала лечения отмечалась средняя степень гингивита, а в конце лечения - легкая степень гингивита).
Следует отметить, что числовые значения вышеуказанных показателей через 3 месяца после лечения незначительно снизились.
Наиболее объективными показателями эффективности лечения пациентов всех возрастных групп с диагнозом кандидоз слизистой оболочки полости рта являются результаты, полученные при бактериологических исследованиях материала на определение содержания грибов рода Candida на дорсальной поверхности языка. По полученным данным, во всех исследуемых возрастных группах пациентов до начала лечения мирамистином грибы рода Candida были выявлены у 100% (50 человек), через 3 нед. - приближались к норме (14% - у 7 чел.), через 3 мес. - отмечены единичные проявления (10% - 5 человек). Данные, полученные через 3 нед. и 3 мес. после курса лечения, свидетельствуют о прогрессирующей динамике лечения мирамистином в комплексе с другими препаратами (см. выше) пациентов с диагнозом кандидоз слизистой оболочки полости рта во всех возрастных группах. По моему мнению, незначительное количество грибов рода Candida на дорсальной поверхности языка у пациентов всех возрастных групп могло быть обусловлено многими факторами, например, ремиссией заболевания, возрастными изменениями организма, особенностями иммунитета, географией проживания,экологией местности и т.д. (см. табл. 4-5 и рис. 6-7).
Заключение
Применение мирамистина в комплексе с медикаментозной терапией кандидоза полости рта в течение 3 мес. уменьшает тяжесть воспалительного процесса и образование зубного налета и обеспечивает стойкий положительный клинический эффект, что подтверждается длительной нормализацией цитологических и микробиологических показателей.
Данные, полученные при проведенном исследовании, ярко свидетельствуют о том, что при лечении кандидоза слизистой оболочки полости рта необходимо воздействовать не только на возбудителя инфекционного процесса, но и на все предрасполагающие факторы заболевания. Терапия, направленная на все звенья патологического процесса, позволяет повысить эффективность лечения и, кроме того, способствует достижению длительного периода ремиссии заболевания.
Показания

Мирамистин – непримечательный флакон с насадкой-распылителем. Но сколько всего он умеет! Если посмотреть на список показаний, то можно сказать, что препарат помогает буквально от всего. От всего, что имеет инфекционную природу. Или собирается стать таковой. Ожоги, раны, вирусы, операции и многое другое – сфера применения Мирамистина. Он снимает воспаление и оказывает противомикробный эффект. Особенно приятно, что простой состав характеризуется практическим отсутствием противопоказаний, побочных реакций, и прием препарата может быть назначен с самого рождения.

Рисунок 1 - Мирамистин отлично справляется с ожогами
Мирамистин – отечественный антисептический препарат широкого спектра действия, который применяют для профилактики и лечения бактериальных, грибковых и вирусных инфекций. Первоначально препарат предназначался для дезинфекции отсеков на советских космических кораблях и станциях. А сейчас Мирамистин отлично показал себя при профилактике и терапевтическом лечении ран, гнойно-септических процессов, появление которых сопровождает хирургию и травматологию. Мирамистин эффективно борется с патогенными микроорганизмами, поэтому применим в гинекологии, урологии, стоматологии, отоларингологии и других отраслях медицины.
Но не стоит думать, что Мирамистин просто оказывает противомикробное действие, он довольно силен и борется даже с теми штаммами, которые нечувствительны к другим антибиотикам. Мирамистин взаимодействует с аскомицетами, дрожжевыми и дрожжеподобными грибами, дерматофитами, некоторыми другими патогенными грибами. И что особенно важно, Мирамистин способен влиять на вирусы иммунодефицита человека, герпеса и др. То есть демонстрировать противовирусный эффект. А еще лекарство довольно активно по отношению к патогенам, которые провоцируют болезни, передающиеся половым путем (ЗППП).
Мирамистин предотвращает инфицирование ожогов, ран, так как ускоряет поглощение гнойного выделяемого, стимулирует процесс регенерации тканей и проявление защитных реакций организма.
И все эти замечательные свойства практически не вызывают аллергических проявлений или раздражающего действия на кожу. Вот что значит средство разрабатывалось для космической промышленности.
Показания
Спектр применения Мирамистина довольно широк. Итак, лечащий врач может назначить применение мирамистина в следующих случаях:
- В травматологии и хирургии: профилактика нагноения, лечение гнойных ран. Используется в процессе терапии гнойно-воспалительных заболеваний опорно-двигательного аппарата.
- В акушерстве и гинекологии: лечение и профилактика нагноений ран и травм, полученных во время родов, лечение воспалительных и инфекционных процессов половых органов (вульвовагинит, эндометрит).
- В венерологии и дерматологии: лечение и профилактика дерматомикозов, пиодермий, также используется при микозов стоп, кандидозе кожи и слизистых в частности, от молочницы.
- В урологии: лечение уретрита (острая и хроническая форма) и уретропростатита.
- В стоматологии: профилактика инфекционно-воспалительных процессов, происходящих в полости рта. Лечение стоматита, гингивита, пародонтита. Также Мирамистином проводится гигиеническая обработка съемные протезы.
- В оториноларингологии: применяется при гайморите, при отите, ларингите, фарингите, тонзиллите хронической формы. Назначается мирамистин при ангине. В частности, средство применяется в комплексной терапии при фарингите, хроническом тонзиллите, а также при ангине у детей с трехлетнего возраста.
- Комбустиология: лечение поверхностных и глубоких ожогов II и IIIA степени, подготовка ожоговых ран к дерматопластике.
- Раствор используется для индивидуальной профилактики развития заболеваний, которые передаются человеку половым путем (сифилис, гонорея, хламидиоз, трихомониаз, генитальный герпес, генитальный кандидоз и др.).
Единственным противопоказанием к применению Мирамистина является повышенная чувствительность или непереносимость компонента/-ов препарата.
Действующее вещество Мирамистина – Бензилдиметил [3 — миристоиламино) пропил] аммоний хлорид моногидрат — 100 мг. Дополнительный компонент – очищенная вода.
Побочные реакции во время применения Мирамистина довольно редки. Чаще всего это аллергическая реакция – ощущение слабого жжения в месте, на которое попал Мирамистин. Подобное проявление не требует отмены или замены препарата.
Применение Мирамистина как антисептического препарата довольно широко. Кроме областей, приведенных в таблице ниже, лекарство назначают при лечении прыщей, в качестве профилактики гриппа и простудных заболеваний, при опрелостях.

Рисунок 2 - Как правильно применят мирамистин
Следует учитывать, что Мирамистин может вызывать раздражение слизистой оболочки носа.
Любое назначение препарата, указание дозировки и продолжительности курса производит лечащий врач.
Тонзиллиты, фарингиты и ларингиты.
От 4 до 10 дней.
Верхнечелюстная пазуха промывается достаточным количеством препарата.
Показано полоскание горла и/или орошение (10-15 мл) 3-4 раза/сут.
Стоматит, гингивит, пародонтит.
До наступления ремиссии.
Полоскание ротовой полости 10-15 мл препарата, 3-4 раза/сут.
Хирургия, травматология, комбустиология.
2-3 раза/сут. орошают поверхность ран и ожогов, рыхло тампонируют раны и свищевые ходы, фиксируют марлевые тампоны, смоченные препаратом.
- КЛЮЧЕВЫЕ СЛОВА: кандидоз, вульвовагинит, постменопауза, антисептик, девушки-подростки, Мирамистин
В настоящее время вульвовагинальный кандидоз занимает одно из ведущих мест в структуре акушерско-гинекологической заболеваемости и второе место среди инфекций влагалища, уступая лишь бактериальному вагинозу. Ежегодно в мире регистрируется около 2 млн случаев вульвовагинального кандидоза, который поражает, как правило, женщин репродуктивного возраста, но может встречаться также у детей, молодых девушек и женщин в постменопаузе. Новые схемы лечения и четкие знания этиологии и патогенеза данного заболевания не привели к снижению заболеваемости. В связи с этим поиск новых и оптимизация имеющихся схем и способов лечения по-прежнему актуальны.
Вульвовагинальный кандидоз – инфекционное заболевание, вызванное дрожжеподобными грибами рода Candida, насчитывающими более 170 видов. Только 20 штаммов относятся к истинным возбудителям вагинального кандидоза, среди которых лидирует Candida albicans, на долю этого штамма приходится 80–90% случаев кандидоза [1]. Второй по распространенности штамм – Candida glabrata [2]. Вульвовагинальный кандидоз, вызванный данным возбудителем, нередко протекает в хронической рецидивирующей форме. Кроме того, Candida glabrata значительно чаще выделяется при вульвовагинальном кандидозе на фоне сахарного диабета и ВИЧ-инфекции. Следует отметить, что в 7% случаев Candida glabrata устойчива к препаратам имидазолового ряда, применяемым местно [2]. Остальные случаи вульвовагинального кандидоза вызваны преимущественно Candida tropicalis, Candida parapsilosis, Candida krusei.
К особенностям вульвовагинального кандидоза относятся частые рецидивы, возможность генерализации процесса, развитие резистентности к терапии антимикотиками, а также ограниченные возможности терапии беременных и новорожденных.
Среди факторов риска развития вульвовагинального кандидоза – иррациональная антибиотикотерапия (зачастую длительный и бесконтрольный прием антибиотиков), а также прием гормональных контрацептивов с высоким содержанием эстрогенного компонента. Эстрогены повышают способность связывания дрожжеподобных грибов с эпителиальными клетками влагалища с последующим размножением гриба и развитием заболевания [3].
У 75% женщин наблюдается по крайней мере один эпизод вульвовагинального кандидоза в течение жизни. Каждая вторая пациентка переносит заболевание не менее двух раз, у 10–20% отмечаются рецидивы, в половине случаев каждые два-три месяца [4]. Одна из причин рецидивов – устойчивость бактерий к антибактериальным и антимикотическим препаратам вследствие способности бактерий образовывать биопленку – трехмерную упорядоченную структуру, которая препятствует доступу антисептиков к нижним слоям клеток микроорганизмов, снижая эффективность терапии. Результаты бактериологического исследования вагинального отделяемого пациенток, страдающих хроническим вульвовагинитом и воспалительными заболеваниями органов малого таза, свидетельствуют о том, что слизистая влагалища колонизирована анаэробными и аэробными микроорганизмами, включая возбудителей вульвовагинального кандидоза, объединенными в биопленки.
Биопленки, как правило, состоят из микроорганизмов разных видов, что осложняет выбор эффективного антисептика и антибиотика. Важное требование к антибиотикам и антисептикам – конечный результат противомикробного действия, который может быть бактерицидным и бактериостатическим. При лечении хронических инфекций, связанных с формированием микробных биопленок, необходимо использовать препараты с бактерицидным и фунгицидным действием, так как иммунная система не в состоянии справиться с биопленкой и полностью ее элиминировать.
По мнению некоторых авторов [4], недостаточная эффективность терапии объясняется тем, что у акушеров-гинекологов не хватает фармакологических знаний о взаимодействии лекарственных средств и грибов in vivo. Разработка новых эффективных и удобных схем терапии, способных не только обеспечить эрадикацию грибов, но и предупредить возникновение рецидивов, – одно из приоритетных направлений развития современной фармацевтической науки.
Вульвовагинальный кандидоз у подростков
Среди гинекологических заболеваний подросткового возраста хронический вульвовагинит занимает одно из лидирующих мест, так как обнаруживается у 60–70% девочек, особенно у сексуально активных, обращающихся к гинекологам [6]. Изменение состава нормальной вагинальной микрофлоры у подростков может быть обусловлено влиянием различных экзогенных и эндогенных факторов, включающих иммунодефицитные состояния, иррациональную антибиотикотерапию, санитарно-гигиенические погрешности или инфекции, передаваемые половым путем [7]. В течение многих лет клиницисты, занимающиеся проблемой неспецифических вульвовагинитов, высказывали различные мнения об этиологии и микробиологической характеристике данного заболевания, что отразилось на методах лечения, иногда включающих системную антибиотикотерапию [8]. Однако и в этом случае частота рецидивов достигала 40–65% [4], а в 20% случаев развивался вульвовагинальный кандидоз.
Вульвовагинальный кандидоз характеризуется рецидивирующим течением, тенденцией к возрастанию этиологической роли грибов, не относящихся к виду Candida albicans, сочетанием кандидоинфекции с возбудителями инфекций, передаваемых половым путем [9]. Антибиотики широкого спектра действия элиминируют нормальную влагалищную флору, которая обеспечивает резистентность вагинального биотопа благодаря конкуренции за питательные субстраты и подавлению лактобактериями прикрепления Candida к клеткам эпителия и их размножения. В настоящее время показано, что к вульвовагинальному кандидозу предрасполагают не только пероральные антибиотики, но и препараты локального действия, содержащие йод, метронидазол и др. [3].
Мирамистин – катионное поверхностно-активное вещество. К катионным антисептикам относятся химические соединения разной природы, имеющие в своей структуре сильно основные функциональные группы, среди которых важную роль играют свободные или замещенные аминогруппы, иминогруппа, гуанидиновая группировка [11]. Основные группы этих антисептиков в слабокислой среде приобретают положительный заряд и, взаимодействуя с отрицательно заряженными цитоплазматическими мембранами бактерий, вызывают их повреждение и последующую гибель [12].
Мирамистин® в лечении вульвовагинального кандидоза
В многочисленных научных статьях описаны эффективность применения препарата Мирамистин®, его высокая антимикробная активность и широкий спектр действия. Препарат характеризуется выраженным бактерицидным действием в отношении грамположительных (Staphylococcus spp., Streptococcus spp., Streptococcus pneumoniae и др.), грамотрицательных (Pseudomonas aeruginosa, Escherichia coli, Klebsiella spp. и др.), аэробных и анаэробных бактерий, включая госпитальные штаммы с полирезистентностью к антибиотикам. Мирамистин® оказывает противогрибковое действие, демонстрируя эффективность в отношении аскомицетов рода Aspergillus и рода Penicillium, дрожжевых (Rhodotorula rubra, Torulopsis gabrata и т.д.) и дрожжеподобных грибов (Candida albicans, Candida tropicalis, Candida krusei, Pityrosporum orbiculare и т.д.), дерматофитов (Trichophyton rubrum, Trichophyton mentagrophytes и т.д.), а также других патогенных грибов в виде монокультур и микробных ассоциаций, включая грибковую микрофлору с резистентностью к химиотерапевтическим препаратам [13].
У большинства госпитальных штаммов нет резистентности к Мирамистину. Он стимулирует репаративные процессы, а в малых концентрациях обладает выраженным местным иммуномодулирующим действием, которое обусловливает дополнительный положительный терапевтический эффект при урогенитальных инфекциях [14]. Кроме этого Мирамистин® способен повышать чувствительность микробных агентов к действию антибактериальных и антимикотических препаратов.
Изучение возможности повышения эффективности и безопасности лечения вульвовагинального кандидоза у подростков путем применения 0,01%-ного раствора бензилдиметил-[3-(миристоиламино)пропил] аммония хлорида моногидрата (Мирамистин®), флаконы 50 мл в комплекте с гинекологической насадкой, в комплексном лечении данного заболевания.
Материал и методы
Под наблюдением находились 72 девочки в возрасте от 16 до 19 лет, обратившихся в гинекологическое отделение Ростовского научно-исследовательского института акушерства и педиатрии по поводу хронического вульвовагинального кандидоза и имеющих не менее четырех эпизодов обострения в течение одного года. Хотя жалобы пациенток (зуд, жжение, творожистые выделения, дизурические явления, диспареуния) и клинические проявления вульвовагинального кандидоза (отечность, гиперемия слизистых оболочек экто- и эндоцервикса, уретры, эрозии и трещины, дерматит перигенитальной области) весьма характерны, диагноз ставился только после получения результатов лабораторной диагностики.
При первом визите (до назначения лечения) проводилось бактериоскопическое и бактериологическое исследование вагинального отделяемого. Через две недели после окончания лечения (второй визит) проводился бактериологический контроль. Воспалительную реакцию слизистых оболочек влагалища оценивали по количеству лейкоцитов. Качественная и количественная оценка всех ассоциантов микробиоценоза генитального тракта осуществлялась с использованием бактериологического и бактериоскопического исследований, иммуноферментного анализа и полимеразной цепной реакции. Видовую идентификацию облигатных и факультативных анаэробов, микроаэрофилов, включая генитальные микоплазмы, гарднереллы, грибы и трихомонады, проводили с помощью компьютерной программы и идентификационных наборов фирмы Becton Dickinson BBL Crystal System. С помощью полимеразной цепной реакции выявляли хламидии, трихомонады, вирусы, гонококки, иммуноферментного анализа – антигены возбудителя хламидиоза. Данные исследования проводились для верификации диагноза и формирования клинически однородной группы.
При микроскопии нативного или окрашенного по Граму материала, полученного путем мазков со слизистой оболочки влагалища, обнаруживались дрожжевые почкующиеся клетки и/или псевдомицелий и мицелий Candida spp. Во всех случаях проводилась видовая идентификация возбудителя.
Для лечения острого вульвовагинального кандидоза использовались системные антимикотические препараты (флуконазол, итраконазол, кетоконазол). В качестве местной терапии – раствор бензилдиметил-[3-(миристоиламино)пропил] аммония хлорида моногидрата (Мирамистин®), вводимый интравагинально при помощи гинекологической насадки (первая группа, n = 38) в объеме 10 мл на одну процедуру один раз в сутки в течение десяти дней (в соответствии с инструкцией к препарату), или полиеновые препараты для местного (интравагинального) применения (пимафуцин) в виде вагинальных свечей (вторая группа, n = 34).
В настоящем исследовании нами апробирована новая форма выпуска препарата Мирамистин® – флаконы емкостью 50 мл в комплекте с гинекологической насадкой. Данная форма предлагается для проведения профилактических и лечебных процедур в форме влагалищных орошений. Насадка изготовлена из мягкого пластика, удобна и создает минимум неприятных ощущений для пациентки. Благодаря специальной конструкции и боковым отверстиям лекарственный раствор равномерно распределяется не только в верхней части, но и по всей длине насадки, что обеспечивает удобное проведение и эффективность лечебной процедуры.
Результаты исследований пациенток первой и второй клинических групп сравнивались с показателями 20 здоровых пациенток аналогичного возраста (средний возраст 17,8 (16,1–18,9) года), составивших контрольную группу.
Результаты и их обсуждение
До начала лечения (первый визит) при бактериоскопическом исследовании вагинального отделяемого у пациенток первой группы обнаруживались повышенное количество лейкоцитов, смешанная кокко-бациллярная микрофлора и споры грибка Candida albicans.
По данным сравнительного анализа выявленных дисбиотических изменений, в обеих группах нарушения микробиоценоза носили преимущественно воспалительный характер, были связаны с угнетением облигатной микрофлоры, активным размножением анаэробов и не имели межгрупповых различий. Изучение этиологической структуры микробиоценоза показало, что в группе контроля возбудители специфических инфекций и вирусы не регистрировались (табл. 1). Структура микробиоценоза влагалища до лечения в первой и второй группах не различалась и характеризовалась снижением численности облигатных микроорганизмов во влагалищном биотопе по сравнению со здоровыми пациентками в группе контроля (см. табл. 1).
Угнетение облигатного компонента микробиоценоза сопровождалось интенсивной колонизацией влагалищного биотопа условно патогенными микроорганизмами. Отличительной особенностью микробиоценоза влагалища пациенток первой и второй групп явилось превалирование в его составе облигатных анаэробов. Удельный вес этих микроорганизмов в общем биоценозе составил 60,5% в первой группе и 64,7% во второй, что превышало показатели контрольной группы в 12 и 13 раз соответственно (р
Читайте также:


