Аспергиллез стандарты диагностики и лечения

Эта публикация переработана автором оригинальной статьи, чтобы пояснить пациентам, что же такое аспергиллезная инфекция легких. Использован собственный опыт ведения более 100 пациентов с аспергиллезом в условиях стационара НИИ пульмонологии.
В этой статье не будут представлены тяжелые формы аспергиллезной инфекции, которая встречается у пациентов с иммунодефицитом или после трансплантации органов. Мы затронем аллергические, не инвазивные формы аспергиллёзной инфекции – это АБЛА, бронхиальную астму с гиперчувствительностью к аспергиллам.
Аспергиллы – это плесневые грибы, свободно проживающие рядом с нами. Они необходимая часть биосферы. Плесневые грибы распространены повсеместно. И неизбежно при вдыхании воздуха человек может контактировать со спорами грибов. Не все из них могут нанести вред человеку. Плесневые грибы Aspergillus в основном населяют верхний слой почвы, где есть перегной. Так же они встречаются в домах людей — старый пол, обои, протекающие краны в ванной, теплицы и т.п. Но не все люди даже при контакте с грибами могут заболеть. Для неблагоприятного развития ситуации, прежде всего у человека, должен быть иммунологический дефект — снижена защита или имеется аллергическая реакция на плесневые грибы (например, при длительном контакте с плесенью). И количество плесневых спор попавших в дыхательные пути человека должно быть значительным.
Как развивается АБЛА?
Впервые аллергический бронхолегочный аспергиллез (АБЛА) был описан в 1952 г. Термин АБЛА стал широко известен среди пульмонологов и аллергологов. Это заболевание не всегда четко диагностируется или пропускается вовсе. В эпоху отсутствия современной иммунологии, КТ диагностики легких этот факт был объясним. По моим наблюдениям невысокая диагностика АБЛА связана с тем, что заболевание считалось редко встречаемым. При этом бронхолёгочный аспергиллез включает в себя ряд схожих симптомов и проявлений, характерных для других болезней.
АБЛА возникает при колонизации плесневыми грибами аспергиллами (A. fumigatus) дыхательных путей с обязательной комбинированной аллергической реакцией организма. Это не просто аллергическая реакция, которая выражается в аллергическом насморке, чихании или даже атопической астме. Это сложный воспалительный процесс, приводящий к мощному выбросу медиаторов воспаления, эозинофильному воспалению и повреждению тканей легкого.
Колонизация гриба становится возможной из-за повреждения стенок бронха, снижению иммунной защиты. Это позволяет плесневому грибу активно размножаться. При прорастании грибов, по аналогии с обычными грибами в лесу, из спор образуются т.н. гифы (или если угодно аналог грибницы). Прорастая, гифы разрушают стенки бронхов, защитные и эвакуаторные способности бронхов резко снижаются, нарушается отхаркивание мокроты, создаются условия для размножения грибов. Все процессы вместе еще больше снижают защитные возможности иммунитета пациента. В норме макрофагам человека удается быстро справиться и удалить из организма споры грибов.
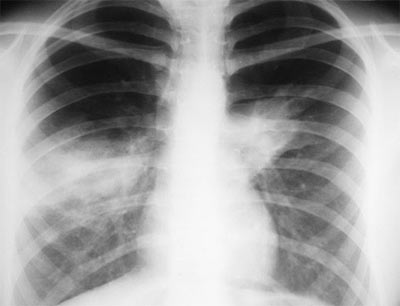
На фото рентгенография легких у пациента с АБЛА.
Сочетание бронхиальной астмы (синдром бронхиальной обструкции) плюс выявление специфических антител к грибам рода аспергиллюс, с большой достоверностью указывают на наличие у пациента АБЛА. Проведение накожных аллерго-проб к плесневым грибам Aspergillus помогает подтвердить диагноз.
Можно выделить несколько ситуаций у пациента, требующих исключения диагноза АБЛА:
- Устойчивая к лечению бронхиальная астма или тяжелая гормонозависимая БА.;
- Эозинофильные инфильтраты в легких;
- Сочетание бронхиальной астмы с инфильтратами в легких и/или с бронхоэктазами.
Бронхиальная астма с гиперчувствительностью к аспергиллам
Бронхиальная астма с гиперчувствительностью к аспергиллам (БА)- это обычная бронхиальная астма, которая обостряется при контакте с аллергенами – плесневыми грибами. При этом у пациента отсутствуют легочные эозинофильные инфильтраты, отсутствует лихорадка, высокие значения эозинофилов и антител.
Для лечения грибковой БА мы используем стандарты по лечению бронхиальной астмы, которые освещены отдельно на нашем сайте. Противогрибковой терапии не применяют.
Можно ли вылечить аспергиллез?
Да, своевременно поставленный диагноз и назначенное лечение всегда дает положительный результат.
Комбинации современных противогрибковых средств, ингаляционно или системно, позволяют эффективно сражаться с грибковой инфекцией в легких. Грамотно подобранная терапия противовоспалительными средствами, позволить контролировать обструктивный синдром у пациентов с АБЛА.
";Проблемы медицинской микологии";-2002.- том.4, №1.
Аспергиллёзная инфекция; подходы к её диагностике и лечению
Н.П. Елинов, В.С. Митрофанов, Р.М. Чернопятова
НИИ медицинской микологии им.П.Н.Кашкина Санкт-Петербургской медицинской академии последипломного образования, Россия
Оппортунистические микозы занимают особое место среди всех грибковых заболеваний, поскольку их возникновение и последующее развитие патологических процессов происходят у иммунокомпрометированных пациентов. В настоящее время врачи различных специальностей и, прежде всего, врачи - микологи стремятся разработать стандарты диагностики и лечения соответствующих заболеваний. Согласованные действия в этом направлении предприняты в отношении кандидоза, что было отражено в соответствующих публикациях и в решениях 4-х Кашкинских чтений в июне 2001 г. [1,2].
Представляемые в настоящей статье материалы включают базисные сведения об аспергиллах и вызываемых ими заболеваниях, о диагностике и лечении аспергиллёза различными лекарственными средствами 5. Эти материалы могут послужить основой для подготовки соответствующих рекомендательных документов, полезных для медицинской общественности нашей страны.
Возбудители аспергиллёза являются гиалогифомицетами или, точнее, лейкогифомицетами [16], у которых тканевые формы состоят, как правило, из бесцветных (гиалиновых), септированных элементов, иногда ветвящихся или, реже, округлых, тогда как в культуре аспергиллы - белые по цвету до периода спорообразования, или плодоношения. Этиологическими агентами аспергиллёза называют немногим более 20 видов из около 200, описанных в литературе [17], названия которых принадлежат их анаморфам. Все аспергиллы относят к аскомицетовым микромицетам (например, по характеру строения клеточной стенки), независимо от того - имеется или нет информация о выявлении телеоморфы у данного вида. К настоящему времени известны следующие телеоморфы рода Aspergillus: Chaetosartorya, Dichlaena, Eurotium, Emericella, Fennellia, Hemicarpenteles, Neosartorya, Petromyces, Sclerocleista, Warcupiella (Ascomycota, Euascomycetes, Eurotiales: Trichocomaceae) [17].
Поскольку у большинства видов аспергиллов ещё не известен половой цикл развития, постольку на практике изучают их вегетативную и бесполую репродукцию, то есть воспроизведение вегетативно - за счёт участков мицелия и его ветвления или репродукционно - за счёт специализированных клеток размножения - конидий, возникающих на конидиеносцах, или конидиофорах. Следует помнить, что патогенными являются аспергиллы в анаморфном состоянии, и если их случайно выявляют в виде телеоморф (например, A. repens, A. nidulans) в посевах патологического материала, то это может произойти только на питательных средах in vitro. В большинстве случаев и на обычно применяемых в лабораторных условиях средах (агар Сабуро, сусло-агар и др.) аспергиллы вырастают в анаморфном состоянии.
В качестве возбудителей аспергиллёза описаны следующие виды: A. amstelodamii, A. candidus, A. carneus, A. clavatus, A. conicus, A. deflectus, A. fischeri, A. flavipes, A. flavus,A. fumigatus,, A. nidulans, A. niger, A. niveus, A.. ochraceus, A. oryzae, A. parasiticus, A. repens, A. restrictus, A. ruber, A. sydowi, A. terreus, A. ustus, A. versicolor. Наиболее распространённым видом является A. fumigatus.
В основу дифференциации аспергиллов на виды положены: форма и строение конидий, тип конидиогенеза, характер пигментации и цвет окраски колоний.
В таксономических целях чаще применяют агаризованную среду Чапека-Докса, приготавливаемую весо-объёмным методом на деминерализованной воде, в которую (из расчёта на 1 л) вносят: 30 г сахарозы, 3 г натрия нитрата, 1 г калия дигидрофосфата, 0,5 г калия хлорида, 0,5 г магния сульфата, 0,01 г железа сульфата и 15 г агар-агара; стерилизуют при 121 о С в течение 15 минут.
Ниже мы приводим выборочно некоторые таксономические характеристики часто выделяемых в лабораторных условиях видов аспергиллов [см. 4] (таблица 1).
Таксономические характеристики некоторых аспергиллов, выросших на среде
длина 1,5 - 3 мм, ширина
20-30мкм, гладкостен-ный, неокра-шенный, плавно пере-ходящий в головку
булавовидная,плодоносная часть его занима-ет около 250 мкм длины; диа-метр голов-ки 40-60 мкм
Эллипсовид-ные, толсто- стенные, гладкие
3-4,5 х 2,5- 3,5 мкм; у некоторых штаммов могут быть крупнее
желтый до желтовато-зелёного или, с возрастом, зе-лёного
длина 400-850 мкм (редко - до 1500 мкм), не окрашен-ный, толс-тостенный, грубошеро-ховатый
удлинённая - до шаро-видной, 25-45 мкм, ре-же - 10-65 мкм в диа-метре
Шаровидные, гладкие - до шиповатых, 3-6 мкм в
белый, зелё-ный, до серо-зелёного; на косячках сре-ды - серые с возрастом. Оборотная сторона коло-
ний вариабе-льна по цвету
мкм) шири-на - 5-8 мкм,
щённая сверху, ко-нидиофор
к головке; диаметр 20-30 мкм; сте-ригмы пара-
ллельные конидиенос-цу, располо-
эллиптичес-кие, шиповат-ые, редко -
ным; оборот-ная сторона -
коричнева-тым оттенком в
От светло-коричневого до ярко-коричневого, редко – оранжево-коричневые.
Длиной 100-250 мкм, ширина 4,5-6 мкм, бесцветный, гладкий, извилистый
Полукруглая или куполо-подобная, плавно переходящая в конидие-носец, 10-16 мкм в диаметре
Шаровидные до слегка эллиптичес-ких, гладкие 1,8-2,4 мкм в диаметре
Из приведенных в таблице 1 видов аспергиллов первый и четвертый могут быть причиной аллергических состояний, второй, хорошо растущий при 37 о С, - обычным патогеном для людей (некоторые его штаммы продуцируют токсины – афлатоксины); третий ( A. fumigatus ), развивающийся и при температуре 45 о С, является частым и убиквотным патогеном для людей; четвертый ( A. niger ) – выступает нередко причиной отомикоза и как вид (наряду с A. terreus) , колонизирует открытие полости тела человека.
В целях определения аспергиллов весьма полезен труд Рейпера и Феннелла [18]. Аспергиллы хорошо растут на обычных питательных средах в анаморфном состоянии, то есть в паразитической форме и, как правило, в сроки от трех до пяти дней они образуют из вегетативных гиф конидиеносцы, опирающиеся на так называемые опорные клетки (Рис.1). Конидиеносцы завершаются головками или пузырьками, на которых располагаются в один ряд (или более) стеригмы с конидиями (Рис.2). Конидии образуются на стеригмах при созревании. Они одноклеточные, сухие, гидрофобные, легко диспергирующиеся в воздушных потоках, благодаря чему могут попадать в дыхательные пути человека. Если же изоляты аспергиллов не образуют конидий, то для быстрой идентификации гриба прибегают к определению экзоантигена аспергилла.
В случаях, когда, по тем или другим причинам, оказывается трудным идентифицировать изолят на видовом уровне, тогда важно найти микромицет в свежевзятом клиническом материале при микроскопии и повторно изолировать тот же гриб из того же образца клинического материала (или из многих других мест в организме). В тканевых срезах аспергиллы обычно представлены в форме гиалиновых нитей с параллельными клеточными стенками и четкими регулярными септами; диаметр нитей мицелия – от 3 до 6 мкм. Нити ветвятся дихотомически под острым углом (Рис.3.).
Гифы в ткани могут быть окрашены гематоксилином и эозином, если ткани хорошо зафиксированы и не являются некротическими. Живые гифы чаще базофильны (до амфофильных), тогда как мацерированные или некротизированные ткани эозинофильны. Предположительный “гистологический диагноз” должен всегда подтверждаться культурально или иммунологически. Не следует забывать о том, что трудно дифференцировать гифы аспергиллов от гиф других оппортунистических лейко(гиало)гифомицетов, например, Fusarium spp . и Scedosporium apiоspermum. Если в каких-либо тканях разовьются конидиальные головки, то по ним будет легче поставить диагноз заболевания и определить возбудитель, сравнив его по морфологии с чистой культурой.
Элементы мицелия могут приобретать и необычные формы – сферические, искривленные, укороченные, с плохо просматривающимися септами. В подобных случаях необходимо быть настороженным, чтобы не принять фрагменты мицелия как принадлежащие какому-либо зигомицету.
Уже было сказано, что иммунологические методы оказываются полезными, например, при определении циркулирующих аспергиллезных антигенов; в равной мере они могут быть использованы и для определения аспергиллезных антител.
В случае образования аспергиллемы в легких возникает необходимость дифференцировать ее от сходного по форме грибного шара (fungus ball) в том случае, если патогеном выступает Pseudoallescheria boydii , а культуры из патологического материала не получены.
При инвазивном аспергиллезе быстрая серологическая диагностика исключительно важна, поскольку необходимо раннее лечение этой тяжелой формы микоза. Циркулирующие антигены аспергиллов определяют с помощью радиоиммунологического метода (RIA-Radioimmunoassay) или ELISA-метода (Enzyme-Linked Imunosorbent Assay). В последние годы используют ПЦР (полимеразную цепную реакцию), хотя в ряде случаев отмечают достаточно высокий процент ложно-положительных результатов (до 25%) ПЦР у пациентов при фактическом отсутствии у них аспергиллеза [19].
Достаточно информативна и специфична непрямая реакция иммунофлюоресценции антител (от 80 до 100%).
Клинические формы аспергиллеза и их диагностика
Аспергиллез разнообразен по клиническим проявлениям и, очевидно, поэтому отсутствует единая клиническая классификация, которая полностью удовлетворяла бы запросы медицинских микологов, тем не менее, многие авторы признают 3 основные формы аспергиллеза: инвазивный с вовлечением различных органов и систем, легочную аспергиллему и аллергический бронхолегочный аспергиллез (АБЛА).
Другие авторы [17] выделяют семь форм аспергиллеза: аспергиллема, инвазивный аспергиллез, токсический аспергиллез, астматический аспергиллез, альвеолярный инфильтративный аспергиллез, АБЛА, церебральная аспергиллема. С учетом таких клинических симптомов, как диспное, астматические признаки, геморрагии, накопление иммуноглобулинов типов G и E (IgG, IgE), эозинофилию, рентгенологические данные, выделение возбудителя в культуре, то минимум из них отмечают при токсическом аспергиллезе – диспное; астматические признаки и накопление IgE – при астматическом аспергиллезе; диспное, рентгенологические изменения в легких, возможное некоторое накопление IgG и получение культуры микромицета из патологического материала – при инвазивном аспергиллезе; диспное, умеренное возрастание уровня IgG, некоторая эозинофилия, изменения в рентгенологических данных и получение возбудителя в культуре из патологического материала - при альвеолярном инфильтративном аспергиллезе; почти аналогичную предыдущей симптоматику отмечают при АБЛА, за исключением эозинофилии, но при некотором возрастании уровня IgE. При аспергиллеме возможны геморрагии и выделение культуры патогена, рост уровня IgG и, слабее - IgE, имеют место рентгенологические изменения в легких.
Церебральную аспергиллему можно рассматривать как одну из наиболее частых вторичных локализаций инвазивного аспергиллеза центральной нервной системы (ЦНС), возникающей в результате гематогенного распространения Aspergillus sp. с последующими окклюзией внутричерепных кровеносных сосудов и некрозами тканей. Клинический диагноз при этом подтверждается обнаружением патогена в гистологическом препарате из биоптата, если биопсия была возможной, а также выявлением антигена в спинномозговой жидкости (СМЖ); нарушения иммунной системы при этом оказываются мало выраженными. Церебральная аспергиллема может быть оценена как внутричерепной абсцесс [20].
Согласно Международной классификации грибковых заболеваний 10-го пересмотра (1995) обсуждают следующие формы аспергиллеза [21]:
, MD, Wayne State University School of Medicine
Last full review/revision November 2017 by Sanjay G. Revankar, MD

(См. также Обзор грибковых инфекций (Overview of Fungal Infections) и Практические рекомендации по болезням, спровоцированным грибами рода Aspergillus (Practice Guidelines for Diseases Caused by Aspergillus) Американского общества инфекционистов (Infectious Diseases Society of America)).
Патофизиология
Инвазивные инфекции обычно приобретаются при вдыхании спор или иногда прямым внедрением через поврежденную кожу.
К основным факторам риска аспергиллеза относятся:
Продолжительная нейтропения (обычно >7 дней)
Долгосрочная терапия кортикостероидами в больших дозах
Трансплантация органа (особенно пересадка костного мозга с реакцией "трансплантат против хозяина" [ТПХ])
Наследственные заболевания, связанные с функцией нейтрофила (например, хроническое гранулематозное заболевание)
Грибы рода Aspergillus склонны поражать открытые места, такие как полости в легких, что вызвано предыдущими заболеваниями легких (например, расширение бронхов, опухоль, туберкулез), пазухи или наружные слуховые проходы (отомикоз). Такие инфекции склонны быть локально инвазивными и вызывать деструкцию, хотя иногда происходит системное распространение, особенно у пациентов с ослабленным иммунитетом и нейтропенией или иммуносупрессией на фоне приема кортикостроидов. Тем не менее, аспергиллез является редким среди пациентов с ВИЧ-инфекцией.
A. fumigatus является наиболее распространенной причиной инвазивной легочной болезни; A. flavus чаще всего вызывает инвазивную внелегочную инфекцию, вероятно, потому что у этих пациентов иммунитет ослаблен сильнее, чем у пациентов, зараженных A. fumigatus.

В результате очаговой инфекции, что обычно развивается в легких, иногда формируется аспергиллома, присутствует характерный рост запутанных масс гифов, с эксудатом фибрина и небольшим количеством клеток воспаления, как правило, заключенный в капсулу из волокнистой ткани. Иногда есть локальная инвазия в ткань на периферии полости, но обычно грибы только проживают в пределах полости без заметного локального внедрения.
Иногда встречается хроническая форма инвазивного аспергиллеза, особенно у пациентов, которые длительное время принимают кортикостероиды, и пациентов с хроническим гранулематозным заболеванием, которое характеризуется наследственным дефектом фагоцитов.
Вид Aspergillus может также вызвать эндофтальмит после травмы или операции на глазах, или путем гематогенной диссиминации, и может инфицировать внутрисосудистые и внутрисердечные протезы.
Первичный поверхностный аспергиллез нехарактерен, но может развиться при ожогах; под герметичной повязкой; после травмы роговицы (кератит); или в носовых пазухах, ротовой полости, носу или наружном слуховом проходе.
Аллергический бронхолегочный аспергиллез – это реакция гиперчувствительности на A. fumigatus, которая приводит к воспалению легких, не связанному с грибковой инвазией тканей.
Клинические проявления
Острый инвазивный легочный аспергиллез обычно вызывает кашель, часто с кровохарканьем, плевритической болью в грудной клетке и одышкой. Без лечения инвазивный легочной аспергиллез может привести к быстро прогрессирующей и в конечном счете смертельной дыхательной недостаточности.
Хронический легочной аспергиллез может проявляться умеренными, вялотекущими симптомами, несмотря на выраженное заболевание.
Внелегочный инвазивный аспергиллез возникает у пациентов с тяжелым иммунодефицитом. Он начинается с поражения кожи, синусита или пневмонии и может вовлекать печень, почки, головной мозг и другие ткани; часто приводит к скорой смерти.
Аспергиллез в носовых пазухах может сформировать аспергиллому или вызвать аллергический грибковый синусит или хроническое, медленное инвазивное гранулематозное воспаление с лихорадкой, ринитом и головной болью. У пациентов могут быть некрозы кожи над носом или пазухами, изъязвления нёба и десен, симптомы пещеристого тромбоза пазухи или легочные или диссеминированные поражения.
Клинически аспергиллезные мицетомы протекают бессимптомно, хотя могут вызвать мягкий кашель, а иногда и кровохарканье.
Диагностика
Обычно грибковая культура и гистопатология образцов ткани
Определение антигена галактоманнана в образцах сыворотки и бронхоальвеолярного лаважа
Поскольку вид Aspergillus распространен в окружающей среде, положительные культуры мокроты могут быть связаны с загрязнением или с неинвазивной колонизацией у пациентов с хроническим заболеванием легких; положительные культуры являются существенными показателями главным образом тогда, когда мокрота получена у пациентов с увеличенной восприимчивостью из-за иммуносупрессии или есть сильное подозрение из-за типичных результатов томографии. Наоборот, культуры мокроты пациентов с аспергилломами или инвазивным легочным аспергиллезом часто отрицательны, потому что полости часто огорожены от воздухоносных проходов и потому что инвазивное заболевание прогрессирует главным образом путем внедрения в сосуды и развития инфарктов тканей.
Проводится рентгенографическое обследование грудной клетки; однако КТ грудной клетки – гораздо более чувствительный метод и должна назначаться пациентам с высоким риском (т.е., с нейтропенией). КТ носовых пазух, если есть подозрение на синусит. Подвижный грибок в пределах полостного поражения характерен для обоих, хотя большинство поражений очаговые и твердые. Иногда томография выявляет симптом нимба (туманная тень, окружающая узелок) или образование каверн в пределах некротического поражения. У некоторых пациентов отмечаются диффузные генерализованные легочные инфильтраты.
Для подтверждения диагноза требуются, как правило, посев и гистопатология образца ткани; гистопатология помогает отличить инвазивную инфекцию от колонизации. Образец, как правило, отбирается из легких во время бронхоскопии или чрескожной биопсии и из пазух при передней риноскопии. Поскольку тест-культуры занимают время, и результаты гистологического исследования могут быть ложно-отрицательными, большинство решений по лечению основываются на весомых клинических доказательствах. При аспергилезном эндокардите от большого разрастания часто отсоединяются заметных размеров эмболы, которые могут закупорить кровеносные сосуды и обеспечить образцы для диагноза.
Обнаружение антигенов, таких как галактоманнан, может быть специфичным, но в сыворотке оно часто не является достаточно чувствительным, чтобы идентифицировать большинство случаев на их ранних стадиях. При инвазивном легочном аспергиллезе тест на галактоманнан в образцах бронхоальвеолярного лаважа значительно чувствительней, чем в сыворотке, и часто является единственным вариантом для пациентов с тромбоцитопенией, которым биопсия противопоказана. Гемокультуры почти всегда отрицательны, даже в редких случаях эндокардита.
Клинические рекомендации по диагностике и лечению острого почечного повреждения
Настоящие рекомендации разработаны рабочей группой профильной комиссии по нефрологии Министерства здравоохранения Российской Федерации в составе:
Андрусев А.М., к.м.н.
Ватазин А.В., д.м.н., профессор
Гуревич К.Я., д.м.н., профессор
Захарова Е.Н., к.м.н.
Земченков А.Ю., д.м.н., профессор
Томилина Н.А., д.м.н., профессор
Шилов Е.М., д.м.н., профессор
2. ВАЛИДИЗАЦИЯ И ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
3. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ ОСТРОГО ПОЧЕЧНОГО ПОВРЕЖДЕНИЯ
4. ПРИЧИНЫ ОСТРОГО ПОЧЕЧНОГО ПОВРЕЖДЕНИЯ
5. ДИАГНОЗ ОСТРОГО ПОЧЕЧНОГО ПОВРЕЖДЕНИЯ
6. ПРЕДОТВРАЩЕНИЕ И ЛЕЧЕНИЕ ОСТРОГО ПОЧЕЧНОГО ПОВРЕЖДЕНИЯ
7. ЗАМЕСТИТЕЛЬНАЯ ПОЧЕЧНАЯ ТЕРАПИЯ
8. ПРОФИЛАКТИКА И ПРОГНОЗ
KDIGO (Kidney Disease: Improving Global Outcomes) — улучшение глобальных результатов лечения заболеваний почек
NGAL – липокалин, ассоциированный с желатиназой нейтрофилов
АД – артериальное давление
АНЦА – антитела к цитоплазме нейтрофилов
ГИТ – гепарин-индуцированная тромбоцитопения
ЗПТ – заместительная почечная терапия
ИГД – интермиттирующий гемодиализ
КИ-ОПП – контраст-индуцированное острое почечное повреждение
ОИТ – отделение интенсивной терапии
ОКН – острый канальцевый некроз
ОПН – острая почечная недостаточность
ОПП – острое почечное повреждение
ОРИТ – отделение реанимации и интенсивной терапии
ОЦК – обьем циркулирующей крови
ПД – перитонеальный диализ
ПЗПТ – постоянная заместительная почечная терапия
СПОН – синдром полиорганной недостаточности
ХБП – хроническая болезнь почек
ЦВД – центральное венозное давление
ЧСС – число сердечных оскращений
Острое почечное повреждение (ОПП) – синдром стадийного нарастающего острого поражения почек от минимальных изменений почечной функции до ее полной утраты. ОПП весьма часто развивается у больных в критическом состоянии и, будучи в таких случаях независимым фактором риска смерти, ассоциируется с высокой летальностью. Последняя, несмотря на значительный прогресс медицинской науки и практики, на протяжении последних трех десятилетий практически не изменилась, оставаясь в диапазоне от 28 до 90%, что зависит от этиологии и тяжести ОПП, характера основной и сопутствующей патологии, возраста больных, профиля отделения интенсивной терапии и ряда других факторов. Среди больных, нуждающихся в заместительной почечной терапии (ЗПТ), показатели летальности максимальные и достигают 50–70% [9, 13].
Важность изучения и совершенствования лечения ОПП определяется: значительной опасностью синдрома; высокой частотой и разнообразием причин развития; реальной возможностью частичного или полного восстановления почечной функции больного с сохранением работоспособности и качества жизни при своевременной диагностике и грамотном лечении.
Настоящие рекомендации по диагностике, лечению и профилактике ОПП являются руководством для практических врачей, осуществляющих ведение и лечение данных пациентов. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Рекомендации составлены на основании анализа литературы из доступных международных медицинских баз данных и согласованы с Практическими Клиническими рекомендациями KDIGO, 2012г. [12].
Данные рекомендации носят общий характер и не содержат специфических протоколов лечения. Они составлены таким образом, чтобы предоставить врачам информацию и помочь в принятии решения в конкретной клинической ситуации. Их не следует рассматривать в качестве стандартов лечения, и при выборе лечебной тактики они не должны толковаться как единственно возможное руководство к действию. Отклонения в повседневной клинической практике неизбежны, так как клиницисты должны принимать во внимание нужды отдельного больного, доступные ресурсы и ограничения, имеющиеся в конкретном лечебном учреждении [12].
2. ВАЛИДИЗАЦИЯ И ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
| Степень*
Качество доказательной базы
3. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ ОСТРОГО ПОЧЕЧНОГО ПОВРЕЖДЕНИЯ В результате этой работы, для определения ОПП в последние годы применялись две сходные классификации, основанные на уровне креатинина сыворотки и величины диуреза. Так, одним из выводов II согласительной конференции стала выработка критериев острого почечного повреждения ОПП (RIFLE критерии) [4], в которой предусмотрены три уровня почечного повреждения: R (Risk) риск почечной дисфункции, I (Injury) повреждение почек, F (Failure) недостаточность почечной функции, два варианта клинических исходов L (Loss) утрата почечной функции и E (End-stage renal disease) – терминальная почечная недостаточность. Критерии RIFLE были основаны на изменениях концентрационной функции почек, степени снижении клубочковой фильтрации или увеличении уровня сывороточного креатинина и критериях мочеотделения. В 2012 году Международной организацией по улучшению глобальных результатов лечения заболеваний почек (KDIGO) [12] было предложено единое определение, включающее присутствие любого из следующих признаков: — увеличение креатинина сыворотки крови ³ 0.3 мг/дл (³ 26.5 мкмоль/л) в течение 48 час ИЛИ — увеличение креатинина сыворотки крови более, чем в 1.5 раза от известного или предполагаемого в течение последних 7 дней исходного значения ИЛИ — диурез менее 0.5 мл/кг/час в течение 6 час. *ОПП диагностируется при наличии хотя бы одного из критериев Тяжесть ОПП по KDIGO предлагается оценивать следующей классификацией (таблица 3). (1.А) Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу. Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции
|

