Синдром рамсея ханта возникает при герпетическом поражении
Представлены литературный обзор по постгерпесной невралгии и клинический случай неблагоприятного исхода ветряной оспы в виде сформировавшегося постзостерного ганглионита лицевого и тройничного нервов — синдрома Рамсея–Ханта, нейропатии большого затылочног
The literature overview on post-herpes neuralgia was given, and a clinical case of adverse outcome of chicken pox as a formed post-zoster ganglionitis of facial and trifacial nerves — Ramsay Hunt syndrome, neuropathy of greater occipital nerve, was presented. The strategy of the therapy was discussed.
Актуальной проблемой современной медицины является постгерпетическая невралгия, что связано с ростом числа герпесвирусных заболеваний с формированием болевого синдрома в случае поражения ганглиев. Частота опоясывающего герпеса после перенесенной ветряной оспы с формированием невралгии в различных странах мира составляет от 0,4 до 1,6 случая заболевания на 1000 пациентов в год в возрасте до 20 лет.
Вирусы герпеса широко распространены в природе, являясь самыми древними возбудителями болезней человека. Такая способность длительно сохраняться во времени связана с их свойством переходить в латентное состояние и интегрироваться в геном хозяина, трансформируясь в другую качественную форму. Герпесвирусы отличаются широким разнообразием путей передачи инфекции, способны поражать любые органы и системы человеческого организма, вызывать острую, латентную и хронические формы заболевания. В современной классификации, в зависимости от типа клеток, вовлеченных в инфекционный процесс, характера репликации вирусов, структуры их генома, эти вирусы делятся на три подсемейства — α-, β- и ν-герпесвирусы [1–3]. Представителями α-герпесвирусов являются вирус простого герпеса 1-го, 2-го типов (ВПГ 1-го типа, 2-го типа) и вирус ветряной оспы — опоясывающего лишая — вирус варицелла-зостер (ВГЧ 3-го типа). К β-герпесам относится ВГЧ 5-го типа — цитомегаловирус. К ν-герпесам относят ЭБВ — ВГЧ 4-го типа, ВГЧ 6-го, 7-го и 8-го типов.
Вирус варицелла-зостер (ВГЧ 3-го типа), вызывая всем хорошо известную детскую инфекцию — ветряную оспу, может приводить к серьезным поражениям периферической нервной системы — ганглионевритам и ганглиорадикулитам.
Доказано, что в условиях даже одного субклона для вирионов характерны полиморфизм и антигенная вариабельность. Поэтому ВГЧ 3-го типа у одних людей вызывает ветряную оспу, а у других — опоясывающий герпес, поражая у одних только кожу, у других — слизистые оболочки, а инфицируя эндоневральные и периневральные клетки ольфакторных волокон и попадая в паренхиматозные клетки обонятельной луковицы, может проникать в центральную нервную систему (ЦНС). Полагают, что такой путь передачи — единственный способ проникновения в ЦНС нейротропных вирусов при инфекциях с низким уровнем вирусемии. Так, первично или после перенесенной ветряной оспы вирус через кожу и слизистые, далее лимфогенным и гематогенным путем проникает в ганглии, межпозвонковые узлы и задние корешки спинного мозга, где долгое время может персистировать в латентном состоянии. Вирус инфицирует ветви обонятельного или тройничного нервов, достигает луковицы обонятельного тракта или гассерова узла, что клинически проявляется острым ганглионитом [4].
При снижении иммунологической реактивности под влиянием различных факторов, таких как иммунодефицитное состояние, обострение хронических заболеваний, прием иммунодепрессантов, интоксикации, латентная инфекция может активизироваться. Активация вируса сопровождается развитием ганглионита (межпозвонковых ганглиев или ганглиев черепных нервов, а также задних корешков). При данном заболевании поражаются региональные, чувствительные ганглии с развитием корешковых болей, парастезий, сегментарных нарушений чувствительности, что отмечается практически у каждого больного [5].
По локализации выделяют поражения: тригеминального (гассерова узла); коленчатого; шейных; грудных; пояснично-крестцовых ганглиев [5].
По МКБ-10 классифицируют:
- опоясывающий лишай с другими осложнениями со стороны нервной системы (B02.2);
- постгерпетический ганглионит узла коленца лицевого нерва (G53.0);
- полиневропатию (G63.0);
- невралгию тройничного нерва (G53.0).
Следствие поражения коленчатого узла (ганглия коленца) вирусом опоясывающего лишая (herpes zoster) описали: в 1907 г. американский невролог J. R. Hunt, а в 1912 г. французские неврологи Dejerine, Souques, Sicard. Проявления заболевания начинаются остро, с общих симптомов интоксикации и повышения температуры. У части больных может наблюдаться поражение лицевого нерва и невралгия тройничного нерва с продолжительностью до нескольких недель. J. R. Hunt (1907) подробно описал четыре клинические формы этого заболевания, которое в дальнейшем стало называться синдромом Ханта. В случаях очень распространенного ушного зостера последний захватывает не только наружный слуховой проход, ушную раковину, сосцевидный отросток, но и барабанную перепонку, которая иногда очень тяжело страдает. В таких случаях поражается область, иннервируемая V, VII и Х парами, причем поражение этих нервов сопровождается поражением ганглиев, соответственных черепных нервов или же анастомозов, связывающих конечные разветвления всех вышеперечисленных нервов [6, 7].
При ганглионите гассерова узла отмечаются мучительные боли и высыпания в зоне иннервации I, II, III или всех ветвей тройничного нерва. По мнению ряда авторов герпетические ганглиониты гассерова узла встречаются чаще, чем ганглиониты межпозвонковых узлов.
У большинства больных с данной локализацией процесса наблюдаются повышение температуры и отек лица на пораженной стороне, а также болезненность в точках выхода тройничного нерва. Невралгия (от др.-греч. νεuρον — жила, нерв +aλγος — боль) — поражение периферических нервов, характеризующееся приступами боли в зоне иннервации какого-либо нерва. В отличие от неврита при невралгии нет двигательных нарушений и выпадения чувствительности [7–9].
Постзостерная (постгерпетическая) невралгия (ПГН) возникает примерно у 10–15% пациентов, страдающих опоясывающим лишаем. Развитию постзостерной невралгии предшествуют одновременно общая нечувствительность пораженного дерматома и сильная боль в начальной фазе опоясывающего лишая. ПГН описывается как постоянная мучительная, жгучая боль различной интенсивности, иногда сопровождаемая внезапными кратковременными приступами дизестезии, такими как пощипывание и пронзительная боль.
Болевой синдром имеет выраженную вегетативную окраску в виде жгучих, приступообразных, резких болей, усиливающихся в ночное время. В дальнейшем боли рецидивируют и беспокоят больного в течение многих месяцев и лет, вызывая потерю трудоспособности, нарушая сон, изменяя его психический и эмоциональный статус, формируя постоянный синдром — постгерпетической невралгии. Затяжной, тяжелый характер заболевания с длительным, выраженным алгическим синдромом способствует формированию личностных расстройств психики [10].
Больная Арина К., 20.06.1992 г. рожд. История болезни № 18230.
Анамнез жизни. Девочка родилась от первой беременности, протекавшей без патологии, срочных родов, весом 3650 г, длиной 53 см. Ранний постнатальный период протекал без патологии, на грудном вскармливании до 6 мес. Развитие соответствовало возрасту. Аллергологический анамнез не отягощен. Прививки проводились согласно НКП, патологических реакций в поствакцинальном периоде не отмечалось. Перенесла в 2,5 года коклюш, в 4 года — энтеровирусную миалгию. Девочка проживала в Краснодарском крае.
В 2002 г. на фоне усиления болевого синдрома той же локализации проведена терапия ацикловиром с положительным эффектом. В 2003 г. отмечался очередной приступ более интенсивных и продолжительных болей в области глаз, шеи, ушей, со слезотечением, упорной головной болью. Диагностирован синдром Рамсея–Ханта. Получен кратковременный эффект от терапии ацикловиром внутривенно. Через 2 недели приступ повторился, но меньшей интенсивности. В течение 2003 г. проводилась месячным курсом терапия Вифероном-2, Т-активином, девочка редко посещала школу из-за повторных приступов болевого синдрома. Консультирована была в Москве в Госмедакадемии им. И. М. Сеченова, где психиатром диагностирован ипохондрический синдром.
В феврале 2004 г. обратилась за помощью на нашу кафедру, где при осмотре подтвержден синдром Рамсея–Ханта после перенесенной ветряной оспы и герпес зостер, что требовало исключения других фоновых персистирующих герпесвирусных инфекций и оценки иммунного статуса.
При неврологическом обследовании отмечались жалобы на головокружение, сопровождавшееся тошнотой, боли в затылочно-околоушной и периорбитальной зонах. Отмечены слабость конвергенции, значительная сглаженность носогубной складки справа, гиперестезия в зоне С2-С3 справа; болезненность в области большого затылочного нерва справа; повороты головы в стороны были ограничены; общий тон настроения сниженный, девочка установочно фиксирована была на своих ощущениях.
Рентгенологически в области шейного отдела позвоночника патология не выявлена.
При осмотре окулистом выявлялись спазм аккомодации, приобретенная миопия.
Проведено серологическое и молекулярно-генетическое обследование на весь спектр герпесвирусных инфекций, получены положительные результаты на вирус Эпштейна–Барр, ВГЧ 1-го, 6-го типов при исследовании крови, мочи и слюны методами иммуноферментного анализа (ИФА) и полимеразной цепной реакции (ПЦР), что указывало на медленную персистирующую герпесвирусную инфекцию, включая варицелла-зостерную инфекцию.
ИФА на anti-IgG к вирусу варицелла-зостер — 1:16000; anti-IgG — к HSV1–1:24000; anti-IgG к EBV (к VCAg — 1:160; к EAg — 1:80); в слюне: DNA HHV-6 — положит., DNA EBV — положит., DNA СMV — положит; в моче: DNA HHV-6 — положит., DNA EBV — положит., DNA СMV — положит., DNA HSV1 — положит.; в крови — отр.
В иммунном статусе выявлена недостаточность клеточного иммунитета: снижение CD 19+ , CD 20+ , CD 4+ , ИРИ — до 0,89. Показатели иммуноглобулинов А, М и G в пределах нормы.
Консультирована и обследована иммунологом в НИИ иммунологии РАМН, где установлено вторичное иммунодефицитное состояние на фоне медленно текущей персистирующей герпесвирусной инфекции.
При исследовании общих анализов крови, мочи, биохимического анализа крови патология не выявлена.
Таким образом, с учетом данных анамнеза заболевания и результатов объективного обследования у больной был диагностирован синдром Рамсея–Ханта (ганглионит с поражением ядер лицевого и тройничного нервов, нейропатией большого затылочного нерва), который развился на фоне хронической смешанной персистирующей ГВИ: HVZ, HSV1, СMV и HHV 6-го типа со сформировавшимся вторичным иммунодефицитным состоянием. Сопутствовал астеноипохондрический синдром на фоне хронического болевого синдрома. Следует отметить несвоевременность назначения противовирусной терапии, которая первично не была применена в остром периоде заболевания ветряной оспой, протекавшей тяжело, и в рецидивирующем характере течения, что требовало уточнения фоновой патологии, обусловившей неблагоприятный исход этой инфекции.
Учитывая кратковременность эффекта на предшествующую противовирусную и гормональную терапию, на клинической базе нашей кафедры — в Морозовской городской детской клинической больнице решено было в комплексную терапию включить курс высокоактивных в/в иммуноглобулиновых препаратов (пентаглобина, октагама — 22,5 г на курс), миелопида интраназально, Т-активина 100 мг в/м на 1 мес; с противовоспалительной целью — в/в получала фосфоглив прерывистым курсом — 3 мес, гепон интраназально 2 недели, нейропсихотропные препараты: амитриптилин 1/2 табл. на ночь, Финлепсин 1/2 табл. 2 раза — до 3 мес, Кавинтон 1 табл. 3 раза в сутки 1 мес, Фенибут 1 табл. 3 раза на время стационарного лечения. На фоне указанной терапии состояние больной значительно улучшилось. Так как девочка переехала на постоянное жительство в Москву, было продолжено наблюдение в катамнезе на нашей кафедре и в неврологическом центре. За время 5-летнего наблюдения у девочки интенсивность и частота повторных приступов болевого синдрома значительно уменьшились на фоне повторных курсов нейротропных и иммунотропных препаратов, включая и противовирусную терапию Фамвиром. Это способствовало включению больной в нормальный режим обучения в школе и параллельно в музыкальной школе (чего она была лишена в течение нескольких лет). Обучение продолжила в музучилище.
В современном стандарте и протоколе лечения и профилактики ветряной оспы и опоясывающего герпеса приводятся следующие рекомендации.
При среднетяжелой и тяжелой формах ветряной оспы или опоясывающего лишая, а также при иммунодефицитных состояниях, в том числе пациентам, получающим иммуносупрессивную терапию цитостатиками или глюкокортикостероидами, страдающим фоновой энцефалопатией, независимо от формы тяжести в качестве этиотропной терапии применяют противовирусные препараты.
Препарат выбора при ветряной оспе:
- Ацикловир внутрь по 0,2 г (детям до 2 лет); по 0,4 г (детям 2–6 лет); по 0,8 г (детям старше 6 лет) 4 раза в сут, 7 дней.
Препарат выбора при опоясывающем лишае:
- Валацикловир внутрь по 1 г 3 раза в сут, 7 дней.
При тяжелой форме противовирусные препараты назначаются парентерально:
- Ацикловир в 100 мл 0,9% раствора хлорида натрия в/в капельно по 5–10 мг/кг.
Препарат выбора при опоясывающем герпесе для местного применения:
- Валацикловир (мазь или крем) на пораженные участки 5 раз в сут с интервалом 4 ч, 5–10 дней + Глицирризиновая кислота (крем) на пораженные участки 5 раз в сут с интервалом 4 ч, 5–10 дней.
При развитии энцефалита или менигоэнцефалита, а также при тяжелых атипичных формах с целью интенсификации этиотропной терапии вводятся стандартные иммуноглобулиновые препараты: иммуноглобулин человека нормальный (IgG + IgA + IgM) в/в капельно 5 мл/кг 3–5 введений (при необходимости через 1 неделю курс повторить) или иммуноглобулин человека нормальный в/в капельно 5–8 мл/кг 1 раз в сут, 3–5 введений.
Проводится терапия антигистаминными препаратами наряду с антипиретиками (парацетамол, ибупрофен), при болевом синдроме назначаются анальгетики.
В настоящее время используется вакцина Варилрикс, вводится по 0,5 мл подкожно или внутримышечно.
Одна доза вакцины Варилрикс назначается детям в возрасте от 12 месяцев и до 13 лет, а две дозы назначаются подросткам с 13 лет и взрослым с интервалом между дозами 6–10 недель — такая схема вакцинации обеспечивает 95% оптимальную защиту против ветряной оспы.
Вакцина Варилрикс может назначаться одновременно с другими детскими вакцинами, такими как корь–краснуха–паротит, что делает ее прекрасным кандидатом для универсальной массовой вакцинации.
Показана для однократной постэкспозиционной профилактики в период до 96 часов после контакта с вирусом (предпочтительно в течение 72 часов). Это уменьшает тяжесть ветряной оспы и является обоснованной стратегией предотвращения вспышек.
Вакцина Варилрикс™ может храниться в обычном холодильнике при температуре 2–8 °C до 2 лет.
В мире применяется вакцина Зоставакс, которая применяется у взрослых с целью профилактики опоясывающего герпеса.
Применение своевременного комплексного системного подхода в лечении основных причин заболевания постзостерного ганглионита с использованием противовирусных, иммунотропных препаратов, нейротропных, а также и препаратов, воздействующих на болевой синдром, позволяет уменьшить степень инвалидизации подобной категории больных.
Существующие мифы о том, что ветряная оспа является легкой детской инфекцией, развеиваются, когда эта инфекция наслаивается на персистирующую другую герпесвирусную инфекцию, на иммунодефицит, органическую сосудистую патологию головного мозга и др., часто предопределяющих неблагоприятный исход заболевания.
Поэтому вопрос о назначении противогерпетической терапии в подобных случаях решается в пользу назначения таковой даже при легкой форме ветряной оспы.
Принципиально важной остается недооценка значимости профилактики этой инфекции, где до настоящего времени существует расхожее, ничем не подкрепленное мнение о том, что:
- ветряная оспа — не опасная инфекция;
- с введением прививок возрастает риск развития опоясывающего лишая;
- вакцина не дает желаемого эффекта;
- введение вакцины чревато высоким риском осложнений и т. д.
Авторам этой статьи очень хочется привлечь внимание педиатров и врачей общей практики к проблеме лечения и профилактики ветряной оспы у детей и взрослых, так как, переболев ею однажды даже в легкой форме, продолжаем в себе носить этот вирус на протяжении всей жизни с огромным риском потерять беременность, родить инвалида или заболеть тяжелой неврологической патологией.
Литература
- Гранитов В. М. Герпесвирусные инфекции. НГМА, 2001. С. 80.
- Деконенко Е. П. Вирус герпеса и поражение нервной системы // Рос. мед. журнал. 2002. № 2. С. 46–49.
- Диагностика герпесвирусных инфекций человека: меморандум совещания ВОЗ // Бюл. ВОЗ. 1991. № 3. С. 11–18.
- Редькин Ю. В., Одокиенко А. Ю. Современные подходы в фармакотерапии рецидивирующей герпетической инфекции // Экспериментальная и клиническая фармакология. 2005. Т. 68, № 6. С. 67–71.
- Опоясывающий герпес / Под ред. А. А. Кубановой. М.: ДЭКС-Пресс, 2010. 24 с.
- Thakur R., Philip A. G. Treating herpes zoster and postherpetic neuralgia: аn evidence-based approach // Journal of Family Practice. 2012. Vol. 61. № 9. S9–15.
- Hunt J. R. On herpetic inflammations of the geniculate ganglion: a new syndrome of its complications // [The] Journal of nervous and mental disease, 1907; 34: 73–96.
- Hunt J. K. The sensory field of the facial nerve: a further contribution to the simptomatology of the geniculate ganglion // Brain. 1915. Vol. 38. P. 418–446.
- Bhupal H. K. Ramsay Hunt syndrome presenting in primary care. Practitioner 2010. 254 (1727). С. 33–53.
- Максимова М. Ю., Синева Н. А., Водопьянов Н. П. Постгерпетические невралгии (невропатии), обусловленные опоясывающим герпесом // Фарматека. 2013. № 10. С. 58–62.
Ф. С. Харламова* , 1 , доктор медицинских наук, профессор
В. Ф. Учайкин*, доктор медицинских наук, профессор, академик РАН
И. М. Дроздова**
А. Е. Анджель**
* ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ГБУЗ Морозовская ДГКБ ДЗМ, Москва
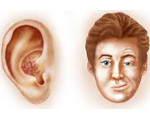
Синдром Рамсея Ханта — герпетическое поражение лицевого коленчатого узла с развитием ганглионита. Клинические проявления включают общеинфекционную симптоматику, одностороннюю пузырьковую сыпь и боли в области ушной раковины, парез лицевого нерва. Возможны расстройства слуха, вестибулярные нарушения. Диагноз выставляется на основании клинических данных, герпетическая этиология подтверждается ИФА, ПЦР, дополнительно проводится исследование иммунного статуса. Лечение комплексное, состоит из противовирусной терапии, антиэпилептических, седативных, витаминных, сосудистых фармпрепаратов.
Общие сведения

Причины синдрома Ханта
Главным этиофактором заболевания выступает герпесвирусная инфекция. Возбудителем является вирус герпеса 3-го типа — варицелла-зостер. Основные пути проникновения инфекции в организм – контактный и воздушно-капельный. Полиморфизм и антигенная вариабельность вирионов в пределах одного клона обуславливают различные клинические формы первичного поражения: ветряную оспу, опоясывающий лишай. Другой специфической особенностью герпесвирусов является способность переходить в латентное состояние, что позволяет им длительно персистировать в нервных ганглиях в форме латентно-ассоциированных транскриптов.
Активация вирусов происходит при недостаточности иммунологических защитных механизмов макроорганизма. Провоцирующими иммунодефицит факторами становятся иммунодепрессивная терапия онкопатологии и аутоиммунных процессов, длительное лечение кортикостероидами, хронические соматические болезни (хронический пиелонефрит, бронхит, сердечная недостаточность), эндокринные нарушения (сахарный диабет, гипотиреоз), тяжёлые травмы.
Патогенез
При первичном инфицировании часть герпесвирусов варицелла-зостер не уничтожается иммунной системой, а по периневральным пространствам проникает в коленчатый узел лицевого нерва, где длительно сохраняется в латентном состоянии. На фоне иммуносупрессии происходит реактивация вирусов, что сопровождается развитием воспалительной реакции. Ганглионит вызывает дисфункцию нейронов коленчатого узла, отвечающих за вкусовую чувствительность, сенсорное восприятие кожи наружного уха, слухового прохода, позадиушной области. Распространение воспаления на проходящие мимо ганглия моторные волокна лицевого нервного ствола обуславливает выпадение двигательной функции — парез мимической мускулатуры на стороне поражения.
В острой фазе заболевания поражаются преимущественно толстые волокна типа А, в норме активирующие клетки желатиновой субстанции задних рогов спинного мозга. Нейроны субстанции обладают ингибирующим воздействием на модуляцию болевых импульсов. Таким образом, поражение А волокон влечёт за собой нарушение механизма формирования боли на спинальном уровне, лежащее в основе сохранения упорной прозопалгии после перенесённого острого зостерного ганглионита. Устойчивый болевой синдром отмечается преимущественно у больных старшего возраста, что связано с уменьшением толщины нервных волокон вследствие естественного старения.
Классификация
Синдром Рамсея Ханта встречается в различных клинических вариантах, включающих также сочетанное поражение лицевого и преддверно-улиткового нервов. Понимание формы заболевания, стадии его клинического течения необходимо при выборе лечебной тактики. Согласно клинической классификации выделяют четыре основных формы синдрома:
- Хант I — высыпания в зоне, иннервируемой коленчатым ганглием, не сопровождаются неврологической симптоматикой.
- Хант II — герпетические высыпания протекают с парезом лицевого нерва.
- Хант III — лицевой парез и пузырьковая сыпь сочетаются с ухудшением слуха.
- Хант IV — к проявлениям, характерным для синдрома Ханта III, присоединяются вестибулярные расстройства.
В течении заболевания различают три клинических периода:
- Общеинфекционный — характеризуется общей симптоматикой: слабостью, вялостью, подъёмом температуры.
- Кожный — период появления типичной герпетической сыпи.
- Невропатический — отличается преобладанием невралгического болевого синдрома.
Симптомы синдрома Ханта
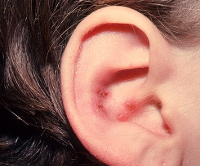
Типичное начало – как при классической вирусной инфекции. Синдром манифестирует общим недомоганием, повышением температуры тела до субфебрильных и фебрильных цифр, цефалгией, чувством разбитости, общей слабости. Спустя 1-2 суток на коже ушной раковины, передних 2/3 языка, мягком нёбе с поражённой стороны появляются герпетические высыпания. Элементы сыпи представляют собой пузырьки, наполненные прозрачным или геморрагическим содержимым. Отмечается мышечная слабость в поражённой половине лица, приводящая к его асимметрии. Наблюдается перекос лица в здоровую сторону, на стороне ганглионита сглаживается носогубная складка, опускается угол рта. Парез редко достигает большой выраженности.
Прозопалгия возникает с первых дней болезни или спустя несколько дней после появления высыпаний. Боли локализуются в области уха, иррадиируют в затылок, шею, периорбитальную зону. Выявляется гиперестезия слухового прохода, околоушной области, сменяющаяся гипестезией. В ряде случаев сенсорные нарушения охватывают всю половину лица. Вовлечение в патологический процесс слуховой части преддверно-улиткового нерва приводит к развитию тугоухости, появлению звона в ушах. При распространении герпетического поражения на вестибулярный нерв к клинической симптоматике присоединяются проявления вестибулярной атаксии: головокружение, неустойчивость, горизонтальный нистагм.
С течением времени пузырьковые высыпания подсыхают, образуются отшелушивающиеся корочки. Главным клиническим симптомом становится прозопалгия. Болевые ощущения носят глубинный распирающий, жгучий характер, сопровождаются локальной вегетативной дисфункцией: отёчностью, слезотечением, инъекцией сосудов склеры. Возможен постоянный умеренный болевой синдром с периодической флюктуацией боли. Типичной особенностью постгерпетической невропатии является зависимость выраженности болевых ощущений от психоэмоционального состояния пациента, климатических условий.
Осложнения
Синдром Рамсея Ханта отличает преимущественно благоприятное течение. Осложнения возникают при хронизации прозопалгии. Хронические боли обуславливают нарушения сна, расстройства эмоциональной, психологической сферы. Пациенты становятся раздражительными, эмоционально лабильными, общий фон настроения понижается. При отсутствии корректного лечения прозопалгии и психологической поддержки возможно развитие невротических проявлений: депрессии, ипохондрии, неврастении. Резистентный к терапии болевой синдром приводит к стойкому снижению трудоспособности.
Диагностика
Типичная клиническая картина пузырьковых высыпаний в сочетании с невритом лицевого нерва позволяет неврологу без труда установить клинический диагноз. Поскольку фоном развития синдрома Ханта является иммунодепрессивное состояние, необходима консультация иммунолога для диагностики и выявления причин иммунодефицита. При обнаружении невротических расстройств показана консультация психолога, психиатра. Основу диагностического поиска составляют:
- Неврологический осмотр. Выявляет снижение мышечной силы мимической мускулатуры половины лица, элементы гиперпатии, в зависимости от давности заболевания — гипер/гипестезию околоушной области, слухового прохода. Вестибулярная атаксия характеризуется неустойчивостью в позе Ромберга, усиливающейся при поворотах головы, закрывании глаз.
- Исследование слуха. Показано, если синдром протекает со снижением слуха. Консультация отоларинголога с проведением аудиометрии даёт возможность определить степень тугоухости, исключить иные причины её возникновения.
- Лабораторные исследования. В первые дни болезни в анализе крови отмечается умеренный лейкоцитоз, незначительное ускорение СОЭ. Проводится ИФА и ПЦР-диагностика опоясывающего герпеса, подтверждающие герпетическую этиологию коленчатого ганглионита.
- Иммунологическое обследование. Позволяет оценить состояние иммунной системы. Включает исследование клеточного иммунитета, уровня иммуноглобулинов. Зачастую диагностирует вторичный иммунодефицит.
Синдром Рамсея Ханта необходимо дифференцировать от тройничной невропатии, невралгии языкоглоточного нерва. В отличие от синдрома Ханта в указанных случаях отоалгические боли провоцируются сокращением жевательных мышц при разговоре, приёме пищи. Тройничная невралгия характеризуется наличием триггерных точек, соответствующих местам выхода ветвей тройничного нерва на лицо. Следует учитывать, что в некоторых случаях невралгия Ханта может сопровождаться умеренной болезненностью данных точек.
Лечение синдрома Ханта
В остром периоде обязательно проведение этиотропной противовирусной терапии. Применяется валацикловира гидрохлорид, ацикловир, при тяжёлом течении препараты вводятся внутривенно капельно. При иммунодефиците показана иммунотерапия человеческим иммуноглобулином, фармпрепаратами тимуса. В нейропатическом периоде проводится комплексное лечение прозопалгии, включающее:
- Антиконвульсанты: карбамазепин, габапентин. Действие противосудорожных препаратов основано на снижении возбудимости нервных волокон, угнетении распространения по ним болевого импульса
- Седативные средства. Наиболее эффективны антидепрессанты (амитриптилин), возможно назначение нейролептиков (тиоридазина, хлорпротиксена), транквилизаторов (диазепама).
- Витамины группы В: тиамин, пиридоксин. Благоприятно влияют на трофику нервной ткани, способствуют нормализации проводящей функции нервных волокон.
- Препараты для улучшения микроциркуляции (пентоксифиллин, никотиновая кислота). Стимулируют кровоснабжение нервного ствола, что улучшает его питание, способствует восстановлению нормального функционирования.
- Антихолинэстеразные средства (неостигмин). Необходимы при наличии прозопареза. Потенцируют восстановление силы мимических мышц путём улучшения нервно-мышечной передачи.
- Физиотерапию. Лазеро- и магнитотерапия уменьшают выраженность воспалительных изменений. Рефлексотерапия проводится для устранения болевого синдрома и восстановления двигательной функции мимических мышц.
Прогноз и профилактика
В большинстве случаев при своевременно начатой терапии синдром Рамсея Ханта имеет благоприятный для выздоровления прогноз. Неполная элиминация вируса в ходе противовирусного лечения обуславливает отдельные рецидивы заболевания. Упорное течение прозопалгии наблюдается преимущественно в пожилом возрасте. Специфическая профилактика заключается в проведении детям вакцинации против ветряной оспы. Дополнительной мерой, способной предупредить синдром Ханта, является активное противовирусное лечение больных ветрянкой. Немаловажное профилактическое значение имеет здоровый образ жизни, позволяющий поддерживать высокий уровень иммунитета.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.

Читайте в новом номере
Боль в области лица после перенесенной вирусной герпетической инфекции представляет собой достаточно актуальную проблему вповседневной клинической практике ивызывает трудности нетолько при проведении дифференциальной диагностики, ноипри подборе адекватной терапии имедицинской реабилитации [1].
ПГН — самое частое осложнение инфекции, особенно у пожилых людей и пациентов с нарушением иммунитета. Herpes zoster, или опоясывающий лишай, — это острое болезненное состояние. После перенесенной в детстве ветряной оспы вирус Varicella zoster остается в организме в латентном состоянии, локализуясь преимущественно в сенсорных ганглиях, расположенных в задних корешках спинальных нервов и чувствительных корешках тройничного нерва. При реактивации ( иногда после вакцинации) вирус вызывает образование характерной везикулярной сыпи, расположенной по дерматомному типу, в зоне иннервации соответствующего сенсорного нерва. У 50% больных сыпь встречается на туловище, у 20% пациентов — на голове, у 15% — на руках и у 15% — на ногах. Через несколько дней сыпь трансформируется в пустулезную, затем образуются корочки, и к концу 3 нед. заболевания она исчезает [3].
Хотя у некоторых пациентов острая фаза опоясывающего герпеса протекает бессимптомно, в большинстве случаев развивается ПГН. Это осложнение наблюдается у 50% больных старше 60 лет. В основе боли, связанной с ПГН, лежат воспалительные изменения или повреждения ганглиев задних корешков спинного мозга и периферических нервов в пораженных зонах тела. Если поражен задний корешок или его ганглий, в соответствующей зоне иннервации также происходят характерные патологические изменения. ПГН возникает при поражении корешков задних рогов спинальных нервов, чаще всего торакальных и тройничного нервов.
По данным исследования, проведенного среди 27 658 пациентов общей врачебной практики, распространенность ПГН в Великобритании составляет 70 случаев на 100 тыс. населения, а ежегодная заболеваемость — 11 новых случаев на 100 тыс. населения. Однако есть определенные трудности в сравнении данных о ПГН из различных исследований, поскольку авторами используются неоднородные критерии этого осложнения.
Наиболее часто ПГН определяют как боль, сохраняющуюся:
- в течение 3 мес. после появления сыпи;
- после исчезновения сыпи.
Тригеминальная ПГН (ПГТН) — постоянная или периодически возникающая лицевая боль в течение не менее 3 мес. от дебюта герпетической инфекции, имеет достаточно высокую распространенность и вызывает трудности при проведении дифференциальной диагностики и терапии [4].
Невралгия обусловлена снижением иммунных свойств в пожилом возрасте и активацией длительно сохранявшегося в организме вируса ветряной оспы. Varicella virus по лимфатическим путям достигает тригеминального ганглия, поражает сенсорный корешок тройничного нерва и преимущественно первую, офтальмическую ветвь тройничного нерва вследствие наименьшей ее миелинизации.
Выделяют несколько стадий заболевания: продромальную, проявляющуюся неспецифическими общеинфекционными симптомами, односторонней сыпью с последующим заживлением кожи с формированием депигментации.
Для невролога важной является диагностика продромальной фазы ПГТН, когда высыпаний еще нет, но болевой синдром уже появился. Предположить вероятную продрому опоясывающего герпеса можно, выявив розовые пятна на коже, в зоне которых имеют место зуд, жжение, боль и отек лица. Спустя 3–5 дней эритрематозный фон исчезает, и возникают пузырьки на здоровой коже. После появления высыпаний постановка диагноза не представляет трудностей [5].
Среди лиц, перенесших острую герпетическую инфекцию, только у 10–20% в дальнейшем развивается ПГН. Причем в 50% случаев заболевают лица после 60 лет. Факторами риска возникновения ПГН являются: пожилой возраст, женский пол, наличие и выраженность боли в продромальной стадии и остром периоде, а также выраженность кожных высыпаний и последующих рубцовых изменений [6].
Основной жалобой больных ПГТН является постоянная лицевая боль, которая возникает после отпадания корочек (после заживления кожи на месте высыпаний) в течение 1,5–2 мес. в 15% случаев, а у 25% пациентов — в течение года.
При синдроме Ханта пациенты в первую очередь обращают внимание на парез лицевой мускулатуры, а боль в области уха, языка и в глубине полости рта носит второстепенный характер. Парез мимических мышц у больных синдромом Ханта в зависимости от уровня локализации сопровождается нарушением слезо- и слюноотделения и вкусовых ощущений на передних 2/3 языка [9, 10].
В настоящее время выделяют 4 варианта течения синдрома Ханта.
вариант — герпетическая инфекция коленчатого узла без неврологических проявлений. — герпетический ганглионит коленчатого узла с периферическим парезом лицевой мускулатуры. вариант — герпетическая инфекция коленчатого узла с нарушением функции лицевого и нерва. вариант характеризуется поражением коленчатого узла, сопровождается периферическим парезом мимических мышц, шумом в ухе, снижением слуха на стороне поражения и вестибулярными симптомами.
Однако в клинической практике более целесообразно использовать упрощенную классификацию синдрома Ханта. Синдром Ханта 1 является формой опоясывающего герпеса при поражении коленчатого узла и имеет несколько синонимов, таких как: невралгия коленчатого узла, синдром коленчатого узла, ганглионит коленчатого узла, геникуляторная невралгия, herpes zoster oticus.
Расстройства слюноотделения при этом варианте синдрома не носят выраженного характера за счет компенсаторного усиления секреции слюны околоушной слюнной железой, иннервируемой языкоглоточным нервом [11]. Болевой синдром обычно регрессирует в течение нескольких недель после дебюта заболевания, тогда как нарушение функции мимической мускулатуры (хотя обычно в минимальном объеме, постневритическая контрактура) может сохраняться длительное время [12].
Синдром Ханта 2 представляет собой множественное герпетическое поражение ганглиев черепных нервов: , языкоглоточного, редко — блуждающего нерва, а также ганглиев и разветвлений 2–3 шейных спинномозговых нервов. Герпетические высыпания дополнительно локализуются на волосистой части головы. Нарушение слюноотделения более выражено, чем при синдроме Ханта 1, и проявляется ксеростомией. Возникают горизонтальный нистагм, головокружение и атаксия. С первых же часов заболевания развивается периферический парез лицевой мускулатуры.
Алгоритм клинической диагностики ПГН включает анализ следующих проявлений.
1. Локализация герпетических высыпаний (или участков трофических изменений кожи после заживления).
Для ПГН тройничного нерва характерны рубцы в области лба и волосистой части головы на фоне гипер- или гипопигментации кожи.
При синдроме Ханта 1 герпетические высыпания локализованы на барабанной перепонке, в области наружного слухового прохода, ушной раковины, на мягком небе, небных миндалинах и передних 2/3 языка.
2. Характер и локализация болевого синдрома.
вариант синдрома Ханта 1 проявляется умеренным болевым синдромом в глубине наружного слухового прохода с ретроаурикулярной иррадиацией, регрессирующий в течение нескольких недель после дебюта заболевания.
Сочетание перманентного и пароксизмального компонентов лицевой боли характерно как для ПГН тройничного нерва, так и для , и вариантов синдрома Ханта 1, кроме того, эти варианты дополнительно характеризуются иррадиацией боли в затылок и шею.
3. Триггерные участки.
Триггерные участки специфичны для ПГН тройничного нерва и локализованы на коже головы, лба и век. Боль, как правило, представляет собой единичные малоинтенсивные прострелы, которые провоцируются соприкосновением ресниц или прикосновением к коже лба на стороне поражения (симптом расчески).
4. Болезненность точек выхода тройничного нерва.
Болезненность в области надглазничной вырезки, реже — подглазничного отверстия типична для ПГН тройничного нерва в отличие от синдрома Ханта 1.
5. Сенсорные и вегетативные расстройства.
Для ПГН тройничного нерва характерны чувствительные расстройства в виде интенсивного жжения и зуда, а также таких проявлений, как аллодиния, гипестезии, дизестезии, гипералгезия в области лба и волосистой части головы.
вариант синдрома Ханта 1 сопровождается гипестезией уха, а вариант — снижением вкусовых ощущений на передних 2/3 языка, гипестезией ипсилатеральной части языка, ксеростомией и нарушением слезоотделения. вариант синдрома Ханта 1 характеризуется снижением слуха.
7. Горизонтальный нистагм, головокружение и атаксия. Данные клинические проявления, как правило, обнаруживаются при варианте синдрома Ханта 1.
В современном лекарственном арсенале врача имеется достаточное количество эффективных препаратов для лечения ПГТН [13, 14].
Направления лечения постгерпетической прозапалгии.
I. Противовирусная терапия.
Исследования нового перорального противовирусного препарата (валацикловира) продемонстрировали укорочение острой фазы герпеса и снижение частоты стойкого болевого синдрома.
Полученные результаты подтверждают, что раннее лечение специфическими противовирусными препаратами реально снижает частоту развития ПГН.
Согласно современной классификации, противогерпетические препараты разделяют на следующие классы:
1. Средства этиотропной фармакотерапии:
- противовирусные химиопрепараты (аномальные нуклеозиды): ацикловир, валацикловир (Валогард) и др.;
- препараты интерферонов: природные и рекомбинантные;
- индукторы интерфероногенеза: амизон и др.
2. Средства патогенетической терапии (иммунотропные средства):
- препараты, реставрирующие Т- и клеточного иммунитета: тималин и др.;
- иммуноглобулины: обычный и противогерпетический.
3. Герпетические вакцины и др.
Валацикловир — противовирусное средство, представляющее собой сложный эфир ацикловира. Ацикловир является аналогом пуринового нуклеозида (гуанин).
Первая стадия фосфорилирования требует активности ферментов. Для ВПГ таким ферментом является вирусная тимидинкиназа, которая присутствует в пораженных вирусом клетках. Активация ацикловира специфическим вирусным ферментом в значительной степени объясняет его селективность.
Процесс фосфорилирования ацикловира (превращение из моно- в трифосфат) завершается клеточными киназами. Ацикловиртрифосфат конкурентно ингибирует вирусную и, будучи аналогом нуклеозида, встраивается в вирусную ДНК, что приводит к облигатному разрыву цепи, прекращению синтеза ДНК и, следовательно, блокированию репликации вируса.
У пациентов с сохраненным иммунитетом ВПГ с пониженной чувствительностью к валацикловиру встречаются крайне редко, но иногда могут быть обнаружены у пациентов с тяжелым нарушением иммунитета, например с трансплантатом костного мозга, у больных, получающих химиотерапию по поводу злокачественных новообразований, и у .
Резистентность обычно обусловлена дефицитом тимидинкиназы, что приводит к чрезмерному распространению вируса в организме хозяина. Иногда снижение чувствительности к ацикловиру обусловлено появлением штаммов вируса с нарушением структуры вирусной тимидинкиназы или . Вирулентность этих разновидностей вируса напоминает таковую у его дикого штамма.
Рекомендуемая доза Валогарда для терапии ПГН составляет 1000 мг 3 р./сут в течение 7 дней. В более тяжелых случаях дебюта заболевания лечение следует начинать как можно раньше, а его продолжительность должна быть увеличена с 7 до 10 дней.
Важно! Идеальным условием эффективной терапии ПГТН является назначение препарата Валогард в продромальном периоде или сразу после появления первых симптомов заболевания!
В соответствии с рекомендациями EFNS (2006), лечебные мероприятия для купирования боли при ПГН включают препараты первого ряда, к которым относятся: трициклические антидепрессанты (амитриптилин) и локальные средства, содержащие 2,5 и 5,0% лидокаин [14].
При нормальном иммунном статусе и выраженном болевом синдроме, резистентном к анальгетикам, можно использовать кортикостероиды и/или симпатические блокады.
В клинической практике терапия постгерпетических прозопалгий представляет собой трудную задачу, особенно у лиц пожилого и старческого возраста.
Значительная распространенность прозопалгий, сложность и стойкость нарушения функций, сопровождающихся порой длительной утратой трудоспособности, делают реабилитацию пациентов, страдающих данной патологией, одной из важнейших проблем.
Современные методологические подходы к реабилитации пациентов с ПГТН отличает соблюдение следующих принципов.
1. В настоящее время целесообразным считается максимально раннее начало реабилитации. Нейрореабилитация как неотъемлемая составная часть лечебного процесса не может рассматриваться только как долечивание; ее использование вторым этапом после завершения лечения малоэффективно. Целесообразное сочетание лечебных и реабилитационных мероприятий — рациональная профилактика функциональных нарушений, связанных непосредственно с лечением, а при их комплексном совмещении возможно сокращение общих сроков излечивания больных с болевыми синдромами в области лица.
3. Важным моментом является индивидуализация реабилитационных программ, составленная членами мультидисциплинарной команды.
4. Не менее значима социальная установка — повышение уровня адаптации пациента с целью улучшения качества жизни.
5. Ключевая рекомендация состоит в необходимости осуществления реабилитационных программ мультидисциплинарной командой, в состав которой входят невролог, физиотерапевт, рефлексотерапевт, психотерапевт и кинезотерапевт.
В силу полиморфности причин развития болевого синдрома нередко необходимо активное участие стоматолога, клинического фармаколога, нейрохирурга, вертебролога и других специалистов.
6. В целях повышения эффективности проведения медицинской реабилитации болевых синдромов в области лица реализована концепция эффективного взаимодополняющего сочетания консервативных методов, направленных на устранение причин, препятствующих полноценной реабилитации больных. Следует учитывать, что чем больше компонентов этого порочного круга становятся мишенями для лечения, тем выше вероятность его успеха.
7. Оценка статуса пациента и мониторинг эффективности реабилитационных мероприятий должны базироваться на клинических данных с применением стандартных количественных тестов, данных нейровизуализации (компьютерная и томография) и результатов нейрофизиологического обследования (транскраниальная магнитная стимуляция, вызванные потенциалы, электронейромиография).
Следует отметить, что в последние предложены новые технологии терапии и идеологии медицинской реабилитации пациентов, страдающих ПГН. При этом первоочередными задачами специалистов, занимающихся данной проблемой, должны являться совершенствование знаний о патогенезе, клинической картине, диагностике и терапии ПГТН, а также использование новых инновационных технологий при проведении медицинской реабилитации этой категории больных [15].
Эффективную терапию ПГН может обеспечить назначение Валогарда в дозе 1000 мг 3 р./сут в течение 7 дней в продромальном периоде или сразу же после появления первых симптомов заболевания.
Только для зарегистрированных пользователей
Читайте также:


