Порок сердца из-за герпеса
Тябут Тамара Дмитриевна, профессор кафедры кардиологии и ревматологии Бел МАПО, доктор медицинских наук
Год здоровья. Прочитай и передай другому
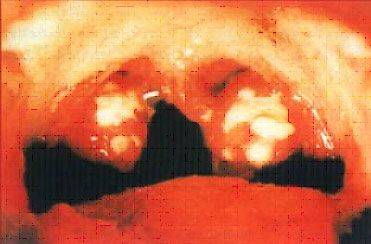
Тонзиллит, вызванный бета-гемолитическим стрептококком.
При наличии хронического тонзиллита в лакунах скапливается большое количество гноя, состоящего из погибших микробов, белых кровяных телец - лейкоцитов, других клеток (гнойно-казеозные пробки). В гнойном содержимом лакун размножаются болезнетворные микробы. Продукты жизнедеятельности микробов из миндалин попадают в кровь и приводят к развитию тонзиллогенной интоксикация, проявляющейся утомляемостью, болями в мышцах и суставах, головными болями, снижением настроения, субфебрилитетом. Миндалины превращаются в хранилище инфекционных агентов, откуда они могут распространяться по организму и быть причиной воспалительных процессов. Частые болезни еще более ослабляют иммунитет, что приводит к дальнейшему развитию тонзиллита. Так формируется порочный круг заболевания.
Хронический тонзиллит опасен осложнениями, связанными с распространением инфекции по организму. К ним относятся паратонзиллярные абсцессы, ·поражение сердца (тонзилогенная миокардиодистрофия, острая ревматическая лихорадка), сосудов, почек.
Тонзиллогенная миокардиодистрофия относится к часто развивающимся, но гораздо реже диагностируемым поражениям сердечной мышцы при хроническим тонзиллите. Она вызывается токсинами бактерий, находящихся в миндалинах, и продуктами местного воспаления и распада тканей.
Клинические признаки тонзиллогенной дистрофии миокарда обусловлены нарушением деятельности вегетативной нервной системы (вегетативной дисфункцией) и нарушением различных видов обмена в сердечной мышце (электролитного, белкового), следствием которых является нарушение образования энергии в сердечной мышце. На ранних этапах развития тонзилогенная миокардиодистрофия проявляется высокой частотой сердечных сокращений - тахикардией, перебоями в работе сердца - экстрасистолией, одышкой при интенсивных физических нагрузках, нарушением общего самочувствия больных. При поздней диагностике появляются признаки сердечной недостаточности, уменьшается объем нагрузки, вызывающей одышку, появляются более тяжелые нарушения ритма и проводимости. При своевременной диагностике и лечении внесердечного фактора - хронического тонзиллита, вызвавшего перечисленные изменения в сердечной мышце, они обратимы и постепенно структура и функции сердечной мышцы
восстанавливаются.
Наибольшую опасность для прогноза и качества жизни пациентов представляет поражение сердца при острой ревматической лихорадке.
Острая ревматическая лихорадка (ОРЛ) - постинфекционное осложнение тонзиллита (ангины) или фарингита, вызванных бета - гемолитическим стрептококком группы А, в виде системного воспалительного заболевания соединительной ткани с преимущественной локализацией патологического процесса в сердечно-сосудистой системе (кардит), суставах (мигрирующий полиартрит), мозге (хорея) и коже (кольцевидная эритема, ревматические узелки), развивающегося у предрасположенных лиц, главным образом молодого возраста (7-15 лет). В Российской Федерации и в РБ заболеваемость ревматической лихорадкой составляет от 0,2 до 0,6 случаев на 1000 детского населения. Первичная заболеваемость ОРЛ в России в начале ХХI века составила 0,027 случая на 1000 населения. Частота впервые выявленной хронической ревматической болезни сердца (ХРБС), которая включает пороки сердца и специфические изменения клапанов (краевой фиброз), выявляемые при ультразвуковом исследовании сердца - 0,097случаев на 1000 населения, в том числе ревматических пороков сердца - 0,076 случаев на 1000 взрослого населения. Имеющиеся статистические различия между частотой первичной заболеваемости острой ревматической лихорадкой и хронической ревматической болезнью сердца свидетельствует о наличии большого количества не диагностированных острых форм болезни.
Временной интервал между перенесенным острым стрептококковым тонзиллитом, фарингитом, обострением хронического тонзиллита и возникновением проявлений острой ревматической лихорадки составляет 3-4 недели. При острой ревматической лихорадке могут поражаться все структуры сердца - эндокард, миокард, перикард. Поражение миокарда (мышцы сердца) встречается всегда. Проявлениями поражения сердца могут быть сердцебиение, одышка, связанная с физической нагрузкой или в покое, боли в области сердца ноющего характера, которые в отличие о стенокардии не имеют четкой связи с физической нагрузкой и могут сохраняться длительный период времени, сердцебиение, перебои в работе сердца, приступообразные нарушения ритма - мерцательная аритмия, трепетание предсердий. Обычно поражение сердца сочетается с суставным синдромом по типу артралгий - болей в крупных суставах (коленных, плечевых, голеностопных, локтевых) или артрита (воспаления) этих же суставов. Для воспаления суставов характерны боль, изменения формы сустава, вызванные отеком, покраснение кожи в области пораженного сустава, местное повышение температуры и нарушение функции сустава в виде ограничения объема движений. Мелкие суставы поражаются гораздо реже. Воспалительный процесс в суставах носит мигрирующий характер и быстро проходит на фоне правильного лечения. Поражение сердца и суставов обычно сопровождается повышением температуры тела, слабостью потливостью, нарушением трудоспособности. У части пациентов встречаются поражения нервной системы, кожные сыпи по типу кольцевидной эритемы и подкожные ревматические узелки.
Для постановки диагноза острой ревматической лихорадки существуют диагностические критерии, которые включают клинические, лабораторные и инструментальные данные, а также информацию о перенесенной инфекции, вызванной бета-гемолитическим стрептококком группы А, его ревматогенными штаммами. Своевременно поставленный диагноз позволяет добиться выздоровления больного при проведении терапии антибиотиками, глюкокортикоидными гормонами, нестероидным противовоспалительными препаратами. Однако, при поздно начатом лечении, несоблюдении пациентами двигательного режима, наличии генетической предрасположенности, не санированной очаговой инфекции (декомпенсированный тонзиллит, кариес) исходом острой ревматической лихорадки может быть хроническая ревматическая болезнь сердца с пороком сердца или без него. Порок сердца возникает как исход воспалительного поражения клапанов сердца. Наличие порока сердца ревматической этиологии требует отнесения пациента к группе высокого риска развития инфекционного эндокардита, наиболее тяжелой формы поражения сердца, связанного с инфекционными агентами.
Острая ревматическая лихорадка относится к заболевания, при которых профилактика имеет важное значение для снижения как первичной заболеваемости, так и повторных эпизодов болезни (повторная острая ревматическая лихорадка).
Первичная профилактика имеет своей целью снижение первичной заболеваемости и включает комплекс медико-санитарных и гигиенических мероприятий, а так же адекватное лечение инфекций, вызванных бета-гемолитическим стрептококком группы А. Первое направление включает мероприятия по закаливанию, знакомство с гигиеническими навыками, санацию хронических очагов инфекции, в первую очередь - хронического тонзиллита и кариеса. Миндалины тщательно санируют повторными полосканиями и промываниями растворами антибактериальных средств, вакуум-аспирацией патологического содержимого лакун. Если это не дает желаемого результата обсуждается вопрос хирургического лечения - удаления миндалин. В каждом конкретном случае выбор тактики лечения определяет врач отоларинголог и терапевт, кардиолог или ревматолог.
Адекватное лечение ангины и фарингита направлено на подавление роста и размножения стрептококка в организме при развитии стрептококкового фарингита, ангины, тонзиллита. Основу лечения составляет антибиотикотерапия в сочетании с противовоспалительными средствами, которые должны проводиться не менее 10 дней с обязательным контролем общего анализа крови, мочи, а по показаниям биохимического анализа крови при возникновении признаков болезни, при окончании лечения и через месяц от появления первых признаков болезни. Лабораторное исследование, проведенное в эти сроки, позволяет правильно поставить диагноз, определить эффективность лечения, и что самое главное, не пропустить начало развития осложнения в виде острой ревматической лихорадки.
Вторичная профилактика имеет своей целью предупреждение развития повторной острой ревматической лихорадки и прогрессирования заболевания у лиц, перенесших ОРЛ. Она проводится у пациентов, не имеющих аллергии к препаратам пенициллинового ряда. Лекарственным средством, используемым для профилактики у взрослых является бензатинбензилпенициллин (экстенциллин, ретарпен) в дозе 2 400 000 ЕД 1 раз в 3 недели внутримышечно. Профилактические режимы зависят от возраста пациента и исхода острой ревматической лихорадки. В соответствии с рекомендациями Ассоциации ревматологов России вторичная профилактика включает следующие режимы:
Наиболее тяжелым и прогностически неблагоприятным заболеванием сердца, связанным с инфекцией считается инфекционный эндокардит - заболевание, характеризующееся развитием воспалительного процесса на клапанном или пристеночном эндокарде, включающее поражение крупных внутригрудных сосудов, отходящих от сердца, возникающее вследствие воздействия микробной инфекции. Наиболее часто это различные бактерии- стрептококки, стафилококки, энтерококки, кишечная палочка, синегнойная палочка и многие другие. Описано 119 различных возбудителей, приводящих к развитию заболевания.
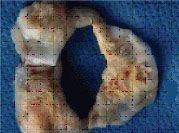
Аортальный клапан
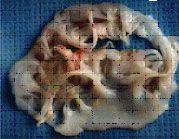
Митральный клапан
Так выглядят клапаны сердца при развитии инфекционного эндокардита.
Наложения из микробов, клеток крови нарушают их функцию,
разрушают клапан и зачастую требуют экстренного хирургического лечения.
Распространенность инфекционного эндокардита в начале 21 века составляла 2- 4 случая на 100 000 населения в год. Отмечается повсеместный рост заболеваемости, наиболее выраженный в старших возрастных группах и составляющий 14, 5 случая на 100 000 населения в возрасте 70-80 лет. Диагностика заболевания сложна. При первом обращении к врачу диагноз ставится только у 19 - 34,2% больных. Средний срок от первичного обращения до постановки диагноза составляет не менее 1,5 - 2 месяцев.
Выделяют группу больных с высоким риском развития инфекционного эндокардита, в которую входят:
- пациенты с ранее перенесенным инфекционным эндокардитом,
- пациенты с протезированными клапанами сердца,
- пациенты с синими врожденными пороками,
- пациенты после хирургических операций на аорте, легочных сосудах
- пациенты с приобретенными пороками сердца, в первую очередь ревматической этиологии (ХРБС).
Кроме этого выделена группа умеренного (промежуточного) риска, объединяющая пациентов со следующими заболеваниями:
- Пролапс митрального клапана, обусловленный миксоматозной дегенерацией или другими причинами с регургитацией 2-3 степени или пролапсы нескольких клапанов
- Нецианотичные врожденные пороки сердца (исключая вторичный ДМПП)
- Бикуспидальный (двухстворчатый)аортальный клапан
- Гипертрофическая кардиомиопатия (идиопатический гипертрофический субаортальный стеноз).
Установлено, что для развития инфекционного эндокардита необходимо попадание возбудителя в кровь. Наиболее частой причиной этого могут быть стоматологические манипуляции, сопровождающиеся повреждением десны и кровоточивостью. При наличии кариеса или заболеваний десен, бактериемия (наличие возбудителя в крови) может возникать достаточно часто.
Официальный сайт
Не секрет, что беременность является серьезным испытанием для женского организма. Часто во время беременности у женщины обостряются хронические заболевания, снижается иммунитет и поэтому будущая мама становится особенно уязвимой для всякого рода инфекционных заболеваний. Среди инфекций есть относительно безобидные для матери и плода (например, ОРЗ) и очень опасные (вплоть до ВИЧ).
Но есть группа инфекций, особенность которых заключается в том, что, будучи относительно безобидными для взрослых, и даже для детей, они становятся чрезвычайно опасными для беременных.
По первым буквам латинских названий входящих в нее инфекций эту группу принято называть TORCH-инфекциями или инфекциями TORCH-комплекса.
Расшифровывается аббревиатура TORCH следующим образом:
- Т — токсоплазмоз (toxoplasmosis)
- О — другие инфекции (others)
- R — краснуха (rubella)
- С — цитомегаловирусн ая инфекция (cytomegalovirus )
- H — герпес (herpes simplex virus)
Загадочная буква О — others (другие) — подразумевает такие влияющие на плод инфекции, как гепатит В и гепатит С, сифилис, хламидиоз, гонококковая инфекция, листериоз. Недавно в этот перечень включили ВИЧ-инфекцию, ветряную оспу, энтеровирусную инфекцию.
Однако, как правило, в группу ТОРЧ-инфекций включают только четыре перечисленных заболевания: токсоплазмоз, краснуха, цитомегаловирус и герпес. При этом варианте буква О аббревиатуры расшифровывается как вторая буква слова toxoplasmosis.
Особенность ТОРЧ-инфекций в том, что при первичном заражении ими во время беременности они могут оказывать пагубное действие на все системы и органы плода, особенно на его центральную нервную систему, повышая риск выкидыша, мертворождения и врожденных уродств ребенка, формирования пороков его развития, вплоть до инвалидности.
Часто поражение беременной женщины инфекциями торч-комплекса является прямым показанием к прерыванию беременности.
Кровь на наличие антител к TORCH-инфекция м правильнее всего сдавать еще до наступления беременности, при ее планировании.
Повторим, что наиболее опасным для плода является первичное заражение торч-инфекциями на фоне беременности, особенно на ранних ее сроках, поэтому если при обследовании на torch-инфекци и до беременности в крови женщины обнаруживаются антитела к этим инфекциями, то женщина может спокойно беременеть — ее ребенку с этой стороны ничто не угрожает. Если же перед беременностью антител к инфекциям ТОРЧ-комплекса не обнаруживается, значит, беременной женщине необходимо будет принимать дополнительные меры для того, чтобы обезопасить то них себя и своего будущего малыша.
Единственная ситуация, при которой токсоплазмоз представляет собой серьезнейшую опасность — это первичное заражение токсоплазмозом во время беременности.
Важно также то, что опасность представляет только токсоплазмоз, которым женщина заразилась во время текущей беременности. Это значит, что если женщина уже переболела токсоплазмозом до беременности (не менее чем за полгода до нее) ее будущему ребенку токсоплазмоз не угрожает. Более того, в трагической ситуации, когда из-за токсоплазмоза во время беременности женщина теряет ребенка, через полгода она может беременеть, уже не опасаясь токсоплазмоза.
Если же во время беременности заражение токсоплазмозом все же произошло, то многое зависит то того, на каком сроке беременности токсоплазмы попали в организм беременной женщины. Чем более ранним был срок беременности — тем больше риск тяжелых последствий при заражении плода токсоплазмозом, но, в то же время, тем меньше вероятность того, что это заражение произойдет.
И, наоборот, на более поздних сроках беременности процент передачи токсоплазмоза плоду очень высок (около 70%), но риск тяжелых поражений плода снижается.
Коварство краснухи в том, что заражение часто происходит во время инкубационного периода, когда болезнь еще никак себя не проявляет и человек не знает о том, что он болен. Однако после перенесенного заболевания краснухой организм человека вырабатывает устойчивый иммунитет, поэтому вторичного заражения краснухой не происходит.
При заражении краснухой беременной женщины эта безобидная инфекция становится смертельно опасной для плода. В начальной стадии беременности вирус краснухи чаще всего поражает нервную ткань плода, ткани глаза, сердце. В первом триместре краснуха беременной является показанием к прерыванию беременности. Если же заражение краснухой произошло во втором или третьем триместре беременности, то таких непоправимых последствий для плода, как правило, не возникает, но, тем не менее, возможно его отставание в росте и другие нарушения. В таких случаях проводится общеукрепляющая терапия, профилактика недостаточности плаценты.
Наконец, при заражении краснухой на последнем месяце беременности ребенок может родиться с проявлениями краснухи, после чего она протекает у него так же, как у детей, заразившихся после рождения, и тяжелых последствий обычно не вызывает.
Цитомегаловирусн ая инфекция — это обнаруженное только в ХХ веке вирусное инфекционное заболевание, возбудителем которого является цитомегаловирус (ЦМВ).
Цитомегаловирус может передаваться половым путем, через кровь, при грудном вскармливании. Влияние ЦМВ на человека зависит, прежде всего, от состояния иммунной системы: при здоровом иммунитете ЦМВ практически не представляет опасности, если же иммунитет снижен, то цитомегаловирус активизируется и может поражать практически все системы и органы зараженного человека. Большинство инфицированных ЦМВ людей переносят инфекцию, даже не замечая ее. Антитела к ЦМВ устойчивы и сохраняются на всю жизнь, повторных заболеваний почти никогда не возникает.
Однако так же, как в случае с остальными торч-инфекциями, если первичное заражение цитомегаловирусо м происходит при беременности, последствия могут быть катастрофическим и. Проблема усугубляется тем, что риск внутриутробной передачи ЦМВ довольно велик — цитомегаловирусн ая инфекция занимает одно из первых мест по внутриутробно му инфицированию плода. Причем инфицирование плода может произойти разными путями, и не, только от больной матери, но и от отца во время зачатия, так как в мужской сперме тоже содержится ЦМВ.
Однако чаще всего ЦМВ попадает в организм плода либо через плаценту, либо через плодные оболочки, то есть из организма матери. Заражение ребенка может произойти и во время родов, при прохождении через инфицированные родовые пути матери, и при кормлении грудью, но этот вариант гораздо менее опасен и к тяжелым последствиям для ребенка, как правило, не ведет.
При внутриутробном заражении цитомегаловирусн ая инфекция может привести к внутриутробной гибели плода или рождению ребенка с врожденной цитомегаловирусн ой инфекцией.
Врожденная цитомегаловирусн ая инфекция может проявиться сразу после рождения ребенка такими пороками развития как недоразвитый головной мозг, водянка головного мозга, гепатит, желтуха, увеличение печени и селезенки, пневмония, пороки сердца, врожденные уродства.
Родившийся ребенок может страдать задержкой психического развития, глухотой, эпилепсией, церебральным параличом, мышечной слабостью.
Иногда врожденная цитомегаловирусн ая инфекция проявляется только на 2—5-м году жизни инфицированного ребенка слепотой, глухотой, речевым торможением, отставанием в умственном развитии, психомоторными нарушениями.
Все это приводит к тому, что первичная цитомегаловирусн ая инфекция у беременной на ранних сроках беременности является показанием к искусственному прерыванию беременности.
Если же женщина была заражена цитомегаловирусн ой инфекцией ранее, а во время беременности произошло ее обострение, то таких страшных последствий не возникает: женщине назначается лечение антивирусными препаратами и иммуномодулято рами.
Следовательно, как и в случаях всех torch-инфекций, анализ на антитела к цитомегаловиру су необходимо сдать до наступления беременности. Если антитела не будут обнаружены, то женщине будет рекомендовано проводить ежемесячное исследование крови, которое не позволит упустить первичное заражение, наиболее опасное для плода.
Последней из инфекций ТОРЧ-комплекса является герпес. Строго говоря, герпес - это даже не болезнь, а целая группа вирусных инфекционных заболеваний. Известны две группы вирусов герпеса — герпес I и II типов.
В случае запущенного хронического течения болезни герпес обоих типов может проявляться поражениями не только кожи и слизистых, но и центральной нервной системы, глаз, внутренних органов.
При первичном заражении герпесом во время беременности, особенно на начальной ее стадии, когда закладываются все органы и системы будущего ребенка, герпесная инфекция может быть смертельно опасной для плода.
В этом случае втрое повышается риск неразвивающейся беременности и выкидышей, возможно развитие уродств у плода. Если заражение генитальным герпесом происходит во второй половине беременности, то увеличивается вероятность появления врожденных аномалий плода, таких как микроцефалия, патология сетчатки, пороки сердца, врожденная вирусная пневмония. Могут произойти преждевременные роды.
Кроме того, заражение плода ВПГ во внутриутробны й период может стать причиной тяжелых ситуаций, связанных с гибелью ребенка после рождения, детского церебрального паралича, эпилепсии, слепоты, глухоты.
Ребенок может заразиться герпесом не только внутриутробно, но и во время родов, проходя родовыми путями инфицированной матери. Это происходит, если во время беременности у женщины обостряется генитальный герпес, а высыпания локализуются на шейке матки или в половых путях. В случае если за четыре недели до родов у беременной женщины обнаруживается вирус герпеса, то роды, как правило, проводятся путем планового кесарева сечения, для того чтобы свести к минимуму риск инфицирования новорожденного.
Вывод напрашивается сам собой: обследование пары, планирующей беременность, на герпес, также должно проводиться еще до наступления беременности.
Если вирус герпеса будет обнаружен, врач назначит лечение, после которого инфекция не будет беспокоить ни будущую маму, ни будущего малыша. При необходимости лечение герпеса назначается и во время беременности, для этого, как правило, используются противовирусные средства, подавляющие активность вируса герпеса, а также препараты, укрепляющие иммунитет беременной женщины, особенно стимулирующие выработку организмом интерферона.
По данным ВОЗ заболевания, передаваемые вирусом герпеса, занимают 2-е место (15,8%) после гриппа (35,8%) как причина смерти от вирусных инфекций.
На территории России и в странах СНГ от хронической герпетической инфекции страдает не менее 22 миллионов человек [5]. Среди вирусных инфекций, поражающих генитальные органы, герпетическая инфекция встречается наиболее часто. Этому возбудителю принадлежит преобладающая роль в этиологии спонтанных абортов и преждевременных родов, в нарушении эмбрио- и органогенеза, врожденной патологии новорожденных.
Почти треть населения Земли поражена герпетической инфекцией и у 50% из них ежегодно наблюдаются рецидивы заболевания, так как иммунитета против этой вирусной инфекции нет. Имеются данные, что к 5 летнему возрасту около 60% детей уже инфицировано вирусом герпеса, а к 15 годам - почти 90% детей и подростков. Большинство людей являются пожизненными вирусоносителями. Причем в 85-99% случаев первичная инфекция у них протекает бессимптомно и только в 1-15% - в виде системной инфекции.
Около 90% городского населения во всех странах мира инфицировано одним или несколькими типами вируса герпеса, а рецидивирующие герпесные инфекции наблюдаются у 9-12% жителей разных стран. Инфицированность и заболеваемость постоянно растут, опережая естественный прирост населения Земли. Особенно быстро увеличивается число зарегистрированных случаев генитального герпеса (увеличилось на 168% за последнее десятилетие).
При обследовании студентов одного из колледжей США у 1-4% лиц были выявлены антитела к вирусу простого герпеса 1 и 2 типов; среди студентов университета - у 9%; лиц, посещающих клинику по планированию семьи - 22%, среди беременных женщин (не имеющих в анамнезе генитальный герпес) - 32% и лиц, посещающих клинику по поводу лечения заболеваний, передаваемых половым путем - в 46% случаев (Frenkel М., 1993).
Под герпетической инфекцией понимают болезни, характеризующиеся высыпаниями на коже, и/или слизистых оболочках в виде сгруппированных на отечно-эритематозном основании пузырьков и протекающие с поражением внутренних органов.
Этиология: герпес вирусы - "ползучие" ДНК, содержащие вирусы размером 150-300 нм.
Классификация:
Группа вирусов герпеса включает следующие подгруппы:
1. Вирус простого герпеса (ВПГ) - herpes simplex:
1.1. ВПГ 1 типа (ВПГ-1) клинически проявляется в виде герпеса губ, полости рта, глаз, генитального герпеса.
1.2. ВПГ 2 типа (ВПГ-2) - генитальный герпес и генерализованный герпес новорожденных.
2. V. Varicella Zoster - ветряная оспа и опоясывающий герпес (лишай).
3. Вирус Эпштейна-Барра - инфекционный мононуклеоз и лимфома Беркета.
4. Цитомегаловирус (ЦМВ) - цитомегалия.
Вирус простого герпеса.
Воротами инфекции являются губы, кожа, слизистые оболочки (в том числе и глаз). После инфицирования ВПГ-инфекция восходит по периферическим нервам до ганглиев, где и сохраняется пожизненно. Латентная герпетическая инфекция ВПГ-1 персистирует в ганглии тройничного нерва, а ВПГ-2 - в ганглии крестцового сплетения. При активации вирус распространяется по нерву к первоначальному очагу поражения [1].
Считается, что распространение герпетической инфекции поддерживается не цепочкой непрерывных заражений, а периодической активацией латентной инфекции, переходящей в клинически выраженные формы под влиянием факторов, снижающих функционирование иммунной системы (грипп, переохлаждение, лечение иммунодепрессантами, стресс и др.)
ВПГ-1.
Пути передачи: от больного человека здоровому при прямом контакте (чаще через поцелуй), воздушно-капельный, через предметы обихода, трансплацентарный, фекально-оральный и половой. ВПГ-1 можно выделить из слюны у 2-2,5% внешне здоровых лиц. Около 5% здоровых людей имеют вирус простого герпеса во рту, носоглотке, слезной жидкости, а иногда в спинномозговой жидкости и выделяют с фекалиями.
Герпес губ.
Клинически проявляется в виде группы пузырьков 1-3 мм в диаметре, расположенных на отечном гиперемированном основании. Пузырьки заполнены серозным содержимым и сгруппированы вокруг рта, на губах, крыльях носа. Иногда наблюдается распространенная герпетическая сыпь на коже рук, ягодиц.
Заболевание склонно к рецидивированию. Появление сыпи зачастую сочетается с головной болью, недомоганием, субфебрилитетом, чувством жжения, покалывания, зуда. Регрессируя, пузырьки ссыхаются с образованием корочки, либо вскрываются с образованием эрозий. Выздоровление наступает через 7-10 дней.
Лечение: мази ацикловир, зовиракс, госсипол, теброфеновая, а при корочках - тетрациклиновая или эритромициновая мазь.
Герпес полости рта протекает в виде герпетического стоматита и проявляется высыпаниями на слизистой оболочке полости рта в виде везикул, которые вскрываются с образованием эрозий с серовато-белым налетом (афтозный стоматит).
Лечение: обработка слизистых полости рта 0,1% раствором 5-йод-дезоксиуридина (керицид), таблетки ацикловир 200 мг 5 раз в сутки в течение 5 дней.
Герпес глаз протекает в виде кератитов (поверхностных или глубоких). Заболевание склонно к длительному рецидивирующему течению. Болезнь часто приводит к стойкому помутнению роговицы и снижению остроты зрения. Самыми опасными осложнениями являются: перфорация роговицы, эндофтальмит, повышение внутриглазного давления, развитие катаракты.
Лечение: таблетки ацикловир 200 мг 5 раз в сутки в течение 5 дней; закапывание раствора человеческого лейкоцитарного интерферона на конъюнктиву глаз, иммуностимуляторы.
ВПГ-2, генитальный герпес.
Основной путь передачи - половой. Заражение обычно происходит в том случае, когда у партнера, являющегося источником инфекции, наблюдается рецидивирование инфекции. Наряду с выраженными формами заболевания больше распространены асимптомные и не диагностируемые генитальные заболевания, обусловленные ВПГ-2. Такие больные становятся резервуаром и носителями вирусной инфекции, заражая других. Так, среди взрослого населения США их насчитывается 65-80% [1]. Асимптоматическое выявление ВПГ более определяется у женщин, чем у мужчин и более типично для ВПГ-2, чем ВПГ-1 [9].
Клиника.
1. Первичный генитальный герпес у лиц, не имевших контакта с ВПГ, характеризуется генитальными и экстра генитальными поражениями. Чаще всего процесс протекает на больших и малых половых губах, слизистой влагалища и шейки матки, в области балано-препуционной бороздки, крайней плоти, слизистой головки полового члена и мочеиспускательного канала [7]. После скрытого периода, длящегося от 1 до 5 дней, появляются боль, зуд в местах поражения, выделения. У 60% больных наблюдается повышение температуры, головные и мышечные боли, в 23% случаев - увеличение паховых и бедренных лимфоузлов. На пораженных участках возникают мелкие, 1-3 мм в диаметре серозные пузырьки, сидящие на гиперемированном основании. Вначале прозрачное, содержимое пузырьков становится мутным, гноевидным. Вскрываются пузырьки с образованием ярко-красной эрозии, покрываясь тонкой корочкой, которая по мере эпителизации отпадает. Заживление происходит без рубцов, но остается временная гиперемия или пигментация. Средняя продолжительность местных проявлений 10-12 дней.
Поражение мочеиспускательного канала начинается внезапно с выделения слизи в виде "утренней капли", почти бесцветной. Больные жалуются на расстройство мочеиспускания, боли, чувство жара, иногда зуда или жжения в области наружных гениталий [9]. Через 1-2 недели симптомы исчезают, но у большинства больных возникают рецидивы болезни с интервалами от нескольких недель до нескольких лет.
2. Вторичный генитальный герпес протекает легче, и выздоровление наступает быстрее. Высыпанных элементов мало. Рецидивы при ВПГ-2 проявляются раньше и чаще, чем при ВПГ-1.
Анализ сывороток различных групп населения показал очень высокое содержание антител против ВПГ-2 у пациентов с инвазивной карциномой шейки матки (в 83% случаев, против 20% в контрольной). Врачи должны более тщательно обследовать больных с герпетической инфекцией гениталий, как на вирусное, так и злокачественное заболевание шейки матки [4].
Вторичный генитальный герпес способствует возникновению рака головки полового члена.
Лечение: зависит от формы и периода заболевания.
При первичном генитальном герпесе местно 5% мазь или крем ацикловир, таблетки ацикловир по 200 мг 5 раз в день в течение 5 дней или внутривенное введение ацикловира 5мг/кг каждые 8 часов в течение 5 дней, бонофтоновая, теброфеновая или оксолиновая мази 6 раз в сутки в течение 15-20 дней, иммуностимуляторы.
При поражении уретры - введение каплями раствора интерферона [2].
При эрозиях - примочки или суппозитории с интерфероном, виферон.
При рецидивирующем генитальном герпесе:
- эпизодическое лечение каждого обострения: наружно 5% крем ацикловир 5 раз в день в течение 10 дней, иммуностимуляторы,
- при 6 и более обострений в год - продолжительная терапия ацикловиром по 200 мг 4-5 раз в день в течение 3 месяцев, иммуностимуляторы.
1. Неонатальная герпетическая инфекция у детей почти всегда связана с ВПГ-1, который поражает ротовую полость и лицо. Передача возбудителя чаще всего происходит при родах во время прохождения через родовые пути. Большинство женщин, родивших зараженных детей, не имеют в анамнезе герпетических заболеваний. В клинической картине преобладают явления энцефалита (лихорадка, вялость, снижение аппетита, судороги), характерно поражение кожи и внутренних органов (печени, легких, надпочечников),
Профилактика заключается в 100% обследовании супругов и беременных женщин для выявления антител к вирусам герпеса. При явных клинических проявлениях генитального герпеса у беременной - рождение ребенка кесаревым сечением.
Прогноз - сомнительный, смертность достигает 90%.
2. Трансплацентарно или путем восходящей инфекции, особенно после преждевременного разрыва оболочек, а также путем передачи вирусов со спермой через инфицированную яйцеклетку, развивается внутриутробное инфицирование, на 50% обусловленное ВПГ-2. Наибольшее число заболеваний у новорожденных встречается при первичной инфекции у матери на поздних сроках беременности [6]. Это может привести к молниеносной диссеминирующей инфекции плода и послужить причиной нарушения органогенеза и возникновения уродств или обусловливает самопроизвольное преждевременное прерывание беременности, мертворождение и раннюю детскую смертность. Дети могут рождаться с недоразвитостью головного мозга, гепатитом, желтухой, менингитом, отложением кальция в головном мозге, поражением глаз, зрительного нерва, клеток крови, надпочечников и др. Такие дети, как правило, нежизнеспособны.
Вирус Зостер.
1. Ветряная оспа - развивается при отсутствии предшествующего иммунитета. Возбудитель передается воздушно-капельным путем. Чаще болеют дети. После исчезновения клинических проявлений вирус в организме сохраняется пожизненно.
2. При резком снижении защитных сил организма вирус персистирует, что манифестно проявляется в виде клиники ветряной оспы (у лиц, уже переболевших ей). Затем наступает (атентный период, характеризующийся развитием вирусов в ганглиях периферической нервной системы, и развивается клиника, широко известная под названием опоясывающий лишай [11]. Появляется сильное чувство жжения, стреляющие боли, покалывания. Боли часто симулируют клинику стенокардии, аппендицита и др. Вскоре на отечном гиперемированном основании развиваются многочисленные пузырьки с серозным содержимым. Высыпания локализуются по ходу нервов (чаще межреберных и тройничных). Присоединяются резкие, жгучие боли такой интенсивности, что больные кричат, вынуждены искать положение тела, при котором боли менее сильные. Пузырьки сливаются в буллы, появляются очаги некроза. Длительность заболевания 3-4 недели, после чего сыпь исчезает, боль может оставаться несколько месяцев или лет.
Больных с опоясывающим герпесом нужно наиболее тщательно обследовать на выявление онкологических заболеваний.
Лечение: местно в остром периоде жидкий анальгин и флуцинар; мази госсипол, теброфеновая, Ацикловир по 800 мг 5 раз в день в течение 7-10 дней и иммунокорректоры. После однократно перенесенного заболевание не повторяется.
Вирус Эпштейна-Барра.
С этим вирусом связано развитие инфекционного мононуклеоза. Заболевание часто дает малигнизацию в лимфому Беркета. Встречается больше в странах Африки и Азии, поражая детей 2-15 лет. Процесс протекает в верхней челюсти, яичниках, орбитах глаз, почках, селезенке, периферических лимфоузлах [12]. Лечение по схеме полихимиотерапии агрессивных лимфом.
Вирус Цитомегалии.
Инфекционный процесс характеризуется поражением слюнных желез с образованием в тканях гигантских клеток с внутриядерными включениями, ассоциирован с ВИЧ [10]. Для передачи возбудителя требуется длительный и тесный контакт [8].
Основной путь передачи - половой. Вирус обнаруживается в слюне, моче, крови, грудном молоке, сперме (очень много). Выделяется со слюной до 4 недель, с мочой - до 2-х лет.
Заболевание протекает бессимптомно или с небольшой клиникой. При внутриутробном заражении дети рождаются с недоразвитым головным мозгом, с массивными отложениями кальция в нем, водянкой головного мозга, гепатитом, желтухой, увеличением печени и селезенки, пневмонией, пороками сердца, поражением миокарда, паховой грыжей, врожденными уродствами и др.
Лечение: ацикловир внутривенно 5 мг/кг веса (10 мг/кг) 3 раза в день в течение 10 дней в сочетании с иммуностимулирующей терапией.
Читайте также:


