Полудан при генитальном герпесе
Опасность биологического оружия
До Великой Отечественной Войны в Советской России особых успехов в изучении и лечении генитального герпеса не наблюдалось. Лечили герпес фукорцином и другими малоэффективными средствами. И только в послевоенные годы в Подмосковье и Ленинграде нашими учёными под электронным микроскопом было изучено строение вируса. В 1954 году тов. Сталин умер. На смену Ему пришел Хрущев, фаворитом которого был "акадэмик Лысенко". Его наукотворчество отбросило советскую микробиологию на десятилетия назад. До конца 60 гг серьезно проблемой генитального герпеса в СССР практически никто не занимался. В 1967 году брежневское правительство обнаружило гигантское отставание СССР в области микробиологии. Совершенно секретными постановлениями Совмина были учреждены несколько организаций -"почтовых ящиков", которые занялись, в частности, изучением данной проблемы. В то время Советское правительство боялось, что вирус простого герпеса будет использован американскими империалистами, в качестве биологического оружия. Тем более, что все предпосылки для этого есть.
Защита мирного населения от ВПГ
ГНЦ Прикладной Микробиологии в дальнем Подмосковье и ГНЦ Вирусологии и Биотенологии "Вектор" в Новосибирске, Институт Вирусологии им. Д. И. Ивановского РАМН в Москве и ряд других гражданских институтов вплотную занялись защитой мирного населения от ВПГ. К концу 70-началу 80 гг прошлого века были достигнуты определенные успехи. Как гласил вышедший 5 сентября 1984 г. приказ Минздрава СССР № 1030 "Об организации лечебно-профилактических мероприятий по борьбе с герпетическими заболеваниями": установлена возможность внутриутробного заражения плода путем передачи инфекции от больной. Хронический герпес гениталий находится в тесной связи с раком шейки матки, что предопределяет онкологический аспект проблемы.(От автора: Тогда ещё не знали, что вирус папилломы человека является причиной рака шейки матки и всё валили на бедный герпес).
Организация помощи больным герпесом
Врачи различных специальностей
-стоматологи и дерматовенерологи,
- онкологи и инфекционисты часто встречаются в своей работе с проявлениями герпетической инфекции. В последние годы усилилось внимание к изучению и внедрению в практику профилактических и лечебных препаратов при герпетической инфекции. Создан ряд новых отечественных препаратов различного действия: повышающих специфическую (противогерпетическая культуральная инактивированная поливакцина) и неспецифическую (индукторы интерферона - полудан и мегасин) реактивность организма больных, а также обладающих этиотропным воздействием (химиопрепараты - теброфен, флореналь, бромуридин). Вместе с тем, в организации диагностики, лечения и оказания квалифицированной консультативно-диагностической помощи больным герпесом, имеются серьезные недостатки. Врачи терапевты, офтальмологи, стоматологи, дерматовенерологи, гинекологи и инфекционисты недостаточно знакомы с вопросами диагностики, клиники, лечения и профилактики данного заболевания. В специализированных больницах, отделениях, женских консультациях и кожвендиспансерах при проведении дифференциальной диагностики не всегда учитывается возможность наличия у больного герпетической инфекции, не проводится диспансеризация больных герпесом гениталий.
В те годы предполагалось открыть на всей территории СССР консультативно-диагностические центры для больным герпесом. К 1985 году учёные должны были завершить научные разработки и с 1986 года начать промышленный выпуск сухой противогерпетической вакцины, а Центральный научно-исследовательский институт санитарного просвещения Минздрава СССР предусмотреть в планах редакционно-издательской деятельности института подготовку и выпуск материалов для массовой санитарно-просветительной работы по лечению и профилактике герпеса.
Не удачен был и выбор учреждения для организации всесоюзного центра по герпесу: Институт вирусологии им. Д. И. Ивановского РАМН всегда занимался фундаментальными исследованиями вируса и методов его диагностики. По использующимся научным методам диагностики до сих пор нет равных этому учреждению. Однако помощь практическим врачам, составление методических разработок для них не было коньком этого уважаемого научного учреждения.
После того, как в 1996 году действующий в то время министр здравоохранения Царегородцев приказал учитывать в системе государственной статистики случаи генитального герпеса, количество больных за несколько лет перевалило с десятков до сотен тысяч человек. Минздрав России не мог безучастно стоять в стороне, поэтому 01 июля 1999 г. приказом за № 254
"Об организации Научно-методического центра по проблемам герпетических инфекций кожи, слизистых оболочек, урогенитального тракта и папилломавирусных инфекций Минздрава России" возложил функцию всероссийского герпетического центра на ЦНИКВИ. Основными направлениями деятельности центра стали:
1. Оказание консультативно-диагностической и лечебно-профилактической помощи пациентам, страдающим папилломавирусной и герпетической инфекциями и нарушениями репродуктивной функции.
2.Координация научных исследований по разрабатываемым проблемам в Российской Федерации.
3. Проведение научных исследований в соответствии с утвержденными научными направлениями с целью разработки и внедрения в практику здравоохранения научно обоснованных методов диагностики, лечения и профилактики.
4. Подготовка и повышение квалификации специалистов в соответствии с утвержденными Минздравом России программами последипломного образования.
5. Определение текущей и перспективной потребности здравоохранения в специальной медицинской технике и лекарственных препаратах, предназначенных для диагностики и терапии урогенитальных инфекций и бесплодия.
6. Издание справочных материалов и собственных научных трудов.
7. Международное научно-техническое сотрудничество по проблеме в рамках согласованных с Минздравом России международных научно-технических программ.
8. Организацию и проведение съездов, конференций и семинаров по актуальным проблемам вирусных инфекций урогенитального тракта и ассоциированным нарушениям репродуктивной функции.
Однако для хорошей работы даже врачам требуется хорошее материальное обеспечение деятельности.
Но в любом случае, за последние 20 лет работу государственных органов здравоохранения по предотвращению распространения половых инфекций, включая генитальный герпес, следует признать неудовлетворительной. Санитарно-просветительная работа ведётся на крайне низком уровне, информационные материалы для пациентов практически не издаются.
Как лечат?
Единых стандартов лечения до сих пор нет. Поэтому есть доктора, которые лечат заболевание кто во что горазд:
- жидким азотом, чтобы и без того тяжелая жизнь медом не казалась.
Порой их знания о лечении базируются на литературе 70-80 гг прошлого века или на рекламных брошюрах компаний производителей иммуномодуляторов и пищевых добавок. В России нет стандартов лечения герпесвирусных инфекций. Существующие временные отраслевые стандартны по некоторым заболеваниям не утверждены Госстандартом России, поэтому носят исключительно рекомендательный характер. Таким образом, защитить свои права при некачестном лечении практически невозможно.
Первый вопрос к какому же врачу обратиться? Пациент по своему усмотрению может обратиться:
- мужчина - к урологу,
-женщина - к гинекологу.
Иди же к дерматовенерологу. В случае частых рецидивов (>6 раз в год) следует обращаться к врачу аллергологу-иммунологу, т.к. скорее всего либо иммунодефицит, либо другая половая инфекция является причиной частых рецидивов. В любом случае, если уролог или гинеколог сомневаются в диагнозе "герпес", то нужно обратиться к дерматовенерологу, т.к. по врачебным канонам именно эти специалисты лучше всего разбираются в половых инфекциях. На приём к врачу лучше прийти вместе с половым партнёром, даже если его ничего не беспокоит. У большинства (до 80%) людей с герпесом болезнь протекает практически бессимптомно.
В случае если у Вас герпес протекает с видимыми симптомами, а у партнёра болезнь никак себя не проявляет, то лечить следует только того партнёра, у которого ЕСТЬ симптомы болезни. В противном случае вы только выбросите деньги на ветер.
Лечение
В США и Европе для лечения генитального герпеса разрешены только 3 лекарственных препарата. Их эффективность доказана во многих двойных слепых рандомизированных плацебоконтролируемых исследованиях.
Вот эти лекарства:
Для лечения первого в жизни (первичного) эпизода генитального герпеса нужно использовать мощные противовирусные препараты. По данным исследования, при раннем назначении валацикловира при первичном эпизоде герпеса, в последующем рецидивы у пациентов бывают реже. В случае, если валацикловир Вы не можете позволить себе по причинам финансового характера, можно использовать таблетированный ацикловир. Желательно, чтобы субстанция (активное вещество из которого производят препарат) не была бы индийского производства. При первичной атаке препараты принимают внутрь от 5 до 10 дней. Мази и кремы для лечения генитального герпеса не годятся, они не могут снизить заразность и победить вирус. Следует понимать, что в кишечнике всасывается 10-20% ацикловира, 67% валацикловира. валацикловир обеспечивает в крови недостижимые для ацикловира концентрации. Ацикловир тормозит активность вируса, валацикловир - блокирует вирус.
В последующем, если рецидивы у Вас редки (до 6 раз в год) можно принимать химиотерапевтические средства (ацикловир, валацикловир, фамцикловир) только в момент вспышки. Ранний приём указанных препаратов позволяет снять зуд, болезненность, отёк, приостановить размножение вируса. В ряде случаев рецидив не развивается. Если приём препаратов начат позднее 48-60 часов от момента вспышки, то выраженного эффекта ждать не стоит. Противовирусные препараты помогут лишь ускорить заживление язвочек.
Если Вы всё же решили использовать мазь, ни в коем случае не наносите её руками, т.к. можно занести вирус на кисти рук. Пользуйтесь косметическими палочками. В момент рецидива при посещении туалета и манипуляциях с гениталиями тщательно соблюдайте правила личной гигиены. Мойте руки с мылом до и после контакта с половыми органами.
Необходимость в супрессивной терапии появляется у людей, частота герпеса у которых - шесть и более вспышек в год. Таким людям может быть назначен:
Которые принимают постоянно и длительно.
Основными противопоказаниями к приёму препаратов является:
- аллергия к ацикловиру,
-составным частям таблетки
Дело в том, что ацикловир, валацикловир и фамвир являются не лекарствами, а предлекарствами и поступают в организм в неактивной форме. Во время вспышки вирус активизирует эти лекарства. Если вирус "спит", то и лекарства не взаимодействуют с организмом, они просто выводятся с мочой и калом, при этом не влияя на печень, почки, не вызывая дисбактериоза кишечника (это не антибиотики). По данным исследований эти лекарства не влияют на потенцию и возможность иметь детей. Крайне редко встречается при супрессивной терапии ацикловиром наблюдается диффузное облысение. Это побочное действие описано в аннотации и после отмены лекарства тут же проходит. У других препаратов такого побочного нет. Все препараты относятся к средствам рецептурного отпуска и должны назначаться врачом.
Иммуномодулирующая терапия
Что же касается иммуномодулирующей терапии, то она должна назначаться врачом аллергологом-иммунологом после изучения состояния иммунной системы - иммунограммы. В части случаев у людей с очень частыми рецидивами причиной является иммунодефит. Он может быть постоянным или транзиторным (преходящим). Транзиторные иммунодефициты случаются при смене погоды: зима-осень, зима-весна, а также под действием внешних факторов:
-некоторых лекарственных средств,
-переохлаждение или перегрев.
В этом случае снижение действия защитной системы организма позволяет вирусу активизироваться. Использование иммуномодулирующих препаратов, назначенных врачом, позволяет скорректировать состояние иммунной системы и снизить частоту рецидивов.

В своей практической деятельности врачи многих специальностей встречаются с заболеваниями, вызванными вирусами семейства Herpesviridae, которые широко распространены в человеческой популяции. Они способны поражать практически все органы и системы организма хозяина, вызывая латентную, острую и хроническую формы инфекции при этом, спектр клинических проявлений, развитие которых они обусловливают, чрезвычайно широк [7]. Особого внимания заслуживает рецидивирующая форма герпетической инфекции (ГИ), относящаяся к числу наиболее распространенных психосоматических кожных заболеваний. Хроническое течение, зуд, частая локализация и характер высыпаний на лице или интимно значимых участках кожного покрова сопровождаются изменениями эмоциональной сферы. В свою очередь, состояния стресса, восприятие самим пациентом проявлений болезни оказывает влияние на интенсивность и частоту рецидивов простого герпеса (ПГ) [24].
Многочисленные исследования в области проблемы ГИ, особенно вызванные вирусами простого герпеса (ВПГ) 1 и 2 типов, не теряют своей актуальности в настоящее время [21, 16].
Серьёзной проблемой является высокая инфицированность здорового населения, преимущественно молодого, трудоспособного возраста. В мире ежегодно заражаются от 16 до 800, а в России – от 40 до 80 человек на 100 тыс. населения. В настоящее время заболеваемость ПГ крайне высока, по статистике ВОЗ, она занимает второе место среди вирусных поражений, уступая лишь гриппу. ВПГ-1 инфицировано около 90 % взрослого населения планеты, распространенность ВПГ-2 колеблется от 7 до 40 %. В США ежегодно регистрируется до 98 млн случаев лабиального герпеса и 20 млн случаев рецидивирующего герпеса гениталий, 500 тыс. случаев офтальмогерпеса и более 5 тыс. случаев герпетического энцефалита, около 1 тыс. случаев герпеса новорожденных. По мнению ведущих специалистов, в нашей стране ежегодная заболеваемость герпесом губ составляет 10 млн, герпесом кожи – 1 млн, офтальмогерпесом – 250 тыс. случаев. Рецидивирующими формами герпеса страдают от 10 до 20 % населения, а ежегодный прирост увеличивается на 15–17 % [3, 13, 23].
Литературные данные свидетельствуют, что большинство населения Земли инфицировано ВПГ-1, ВПГ-2 или тем и другим вирусом одновременно. Первичная инфекция, ассоциированная с ВПГ-1 или ВПГ-2, может протекать в клинически выраженной форме в очаге инфицирования (например, в орофациальной или генитальной области) либо как бессимптомная или нераспознанная инфекция. Генитальная форма простого герпеса может быть связана с ВПГ-1, так же как и лабиальная форма – с ВПГ-2. После первичного инфицирования у 50–75 % больных отмечается рецидивирующее течение простого герпеса. В течение первых 12 месяцев после инфицирования ВПГ-2 рецидив возникает у 80 % пациентов, ВПГ-1 – у 55 % [15, 26].
Современная медицина не располагает методами лечения, позволяющими элиминировать ВПГ из организма человека. Целью лечения герпеса является: 1) подавление репродукции ВПГ в период обострения (купирование рецидива); 2) снижение частоты и длительности рецидивов заболевания, тяжести их течения; 3) формирование адекватного иммунного ответа и его длительное сохранение с целью блокирования реактивации ВПГ в очагах персистенции.
Всё разнообразие методов терапии и профилактики обострения герпесвирусных инфекций можно сгруппировать в направления этиотропного, патогенетического и симптоматического лечения с применением химиотерапии, иммунотерапии и комплексного лечения [1, 7, 11].
Большое внимание уделяется антигерпетическим соединениям растительного происхождения, природным антиоксидантам, адаптогенам из лекарственного растительного сырья и витаминно-минеральным комплексам, ввиду изменения иммунного статуса пациентов [14, 19].
Патогенетическая терапия направлена на нормализацию функции иммунной системы организма, в том числе на активацию системы интерфероновой защиты, как правило, связанная с применением интерферонов (ИФН), индукторов ИФН и иммуномодуляторов. Специфическая иммунотерапия состоит в применении герпетической вакцины, хотя ряд исследователей считает, что надежды, возлагаемые на специфическую вакцинопрофилактику, не оправдали себя [11, 19]. Иммунотропные препараты, обладающие активностью против вируса герпеса, разнообразны и представлены в таблице.
Иммунотропные препараты, обладающие активностью против вируса герпеса
Использование противовирусной химиотерапии велико при лечении рецидивирующих форм простого герпеса с поражением кожи и слизистых оболочек. В лечении простого герпеса с применением противогерпетических химиопрепаратов можно выделить два принципиально отличающихся друг от друга подхода: 1) эпизодическое лечение – прием ациклических нуклеозидов (АН) в момент рецидива в терапевтических дозах при соблюдении кратности и длительности лечения; 2) супрессивная терапия – длительный, иногда многолетний, постоянный прием препаратов АН вне рецидива в более низких дозах [9, 25].
Согласно проведенным исследованиям, биодоступность (per os) противогерпетических препаратов из группы ациклических нуклеозидов возрастает следующим образом: ацикловир – 20 %, валацикловир – 54 % и фамцикловир – 77 % [24]. Тем не менее применение ацикловира по-прежнему остаётся востребованным среди врачей и пациентов в настоящее время, и одновременно ведутся исследования по увеличению растворимости ацикловира [5] и синтезу его производных [8].
В разные годы предпринимались многочисленные попытки повысить эффективность лечения ПГ путем комбинированной терапии. С этой целью использовались различные сочетания средств иммунного влияния, а также препаратов, отличающихся по этиопатогенетическому механизму действия [20].
Возможно сочетанное использование противовирусной терапии и глюкокортикостероидов. Выявлено, что такая комбинация эффективнее монотерапии противовирусными препаратами, особенно для лечения острой боли и коррекции различных аспектов качества жизни пациентов. Комбинация ацикловир + преднизолон значительно быстрее купирует острую боль и возвращает пациента к обычной жизнедеятельности в случае постгерпетической невралгии [2].
Наружные средства дополняют системную противовирусную терапию. Многочисленные наблюдения подтверждают, что в случае назначения таблетированных форм ациклических нуклеозидов на стадии предвестников в сочетании с наружной противовирусной терапией значительно чаще удается полностью прервать дальнейшее развитие рецидива или наблюдать его абортивное течение [20].
Местная терапия противовирусных лекарственных средств при герпесе кожи и слизистых оболочек требуется для уменьшения отёка, экссудации, боли и зуда, ускорения заживления язвочек и эрозий и сокращения длительности выделения вируса на участках поражения [22]. Применение данных лекарственных форм начинают при появлении первых признаков активации инфекции (чувство жжения, зуд и т.д.) и продолжают вплоть до эпителизации эрозий. Рано начатое местное лечение может предотвратить развитие везикул.
В комплексную терапию пациентов с простым герпесом необходимо включать местные противовирусные средства, способствующие стабилизации и разрешению процесса [12].
При анализе ассортимента противовирусных средств на российском рынке установлено, что большинство противовирусных препаратов выпускается в виде твёрдых лекарственных форм – 66 %, в виде мягких лекарственных форм – 22 %, а в форме жидких – 12 % [22], лидером же является ацикловир [6].
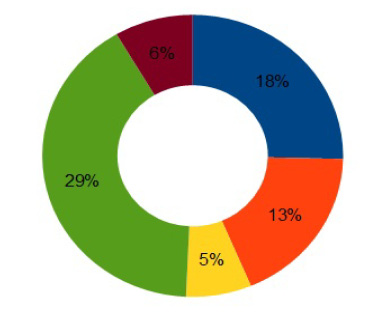

Ассортимент лекарственных форм, содержащих ацикловир
Следует отметить, что современная фармакотерапия герпеса эффективно уменьшает его клинические проявления, положительно влияет на психическое состояние пациентов и приобретает комплексный подход. Несмотря на различные достижения в лечении герпеса, ацикловир по-прежнему играет значительную роль в данном направлении и привлекает внимание исследователей по созданию комбинированных препаратов. В связи с чем актуальными являются исследования по разработке лекарственной формы комбинированного состава, обладающей противогерпесным эффектом – медицинские карандаши.
Рецензенты:
Степанова Э.Ф., д.фарм.н., профессор, профессор кафедры технологии лекарств ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск;
Хаджиева З.Д., д.фарм.н., профессор, профессор кафедры технологии лекарств ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Неизлечим и очень заразен
97 из 100 российских граждан носят в себе одну крайне неприятную и опасную болезнь. В случае активизации вируса последствия могут быть тяжелейшими — иммунодефицит, психические расстройства и слабоумие, многочисленные плохо поддающиеся лечению болезни внутренних органов. Болезнь эта называется герпес. По оценкам специалистов, ежегодно ей заболевают около двух миллионов россиян. С комментарием — медицинский обозреватель Ъ МИХАИЛ Ъ-КИРЦЕР.
Эту историю рассказывает один микропедиатр, опытный клиницист, когда впервые встречается с будущей матерью для предварительной беседы. Случай просто жуткий.
В одной вполне благополучной советской семье родилась девочка, доношенная и здоровенькая. Все было как полагается: папа пораньше убегал с работы купать дочку, мама читала книгу Спока; в положенное время девочка начала ходить и говорить; иногда болела, но ни разу ничего серьезного. В положенное время началась нервотрепка, предстояли выпускные и вступительные экзамены. Весна была ранняя и жаркая. Девочка простудилась и слегла, у нее начался сильнейший жар; дело осложнилось воспалением мозга, она попала в больницу, но ничего не помогло, и она умерла.
Расследование показало, что всему виной цитомегаловирусная инфекция, перенесенная, по всей видимости, ее матерью в период беременности. Сегодня из специальной медицинской литературы уже хорошо известно, что цитомегаловирус, относящийся к породе нашего сегодняшнего героя, герпеса, может, попав в организм еще во внутриутробный период, дремать полтора-два десятка лет, а потом внезапно проявиться и стать причиной тяжелой болезни. Впрочем, цитомегаловирус иногда дает и немедленные результаты — в виде врожденных уродств. Прочие же виды герпеса часто приводят к бесплодию, вызывая выкидыши на ранних стадиях беременности.
Герпетическая семья
Семейство герпеса до недавнего времени состояло из пяти вирусов. Первые два — так называемый простой вирус. Один из них поражает кожу и слизистые человека до линии сосков, другой — ниже этой линии и оттого называется генитальным. Правда, сейчас, с развитием орального секса, эти два вируса изрядно перемешались. Третий вирус — вирус ветряной оспы, он же вызывает заболевание "опоясывающий лишай". Те из нас, кто перенес ветрянку, имеет все шансы при ослаблении иммунитета переболеть еще и лишаем. Четвертый вирус — цитомегаловирус, о его особенностях уже сказано выше. Накожно он обычно никак не проявляется, но для беременных очень опасен. Пятый тип вируса вызывает инфекционный мононуклеоз и впоследствии может привести к назофарингиальной карциноме.
Уже открыты вирусы шестого, седьмого и восьмого типа. По данным американских специалистов, вирус герпеса шестого и седьмого типа вызывает экзонтему новорожденных — сыпь с температурой у младенцев. И одно из самых модных сейчас заболеваний, проявляющееся в виде синдрома хронической усталости. Вирусы восьмого типа до конца не изучены. Им приписывается пока определенная роль в развитии различных доброкачественных и злокачественных новообразований.
Герпес неизлечим
В некоторых развитых странах мира генитальный герпес в острой стадии законодательно определен как препятствие для вступления в брак, это заболевание считается венерическим и входит в группу тех, за заведомое заражение которыми наступает уголовная ответственность. В одном из романов известного автора детективов Рекса Стаута миллионер преследует свою бывшую любовницу и убивает ее только за то, что она заразила его генитальным герпесом.
Когда-то сифилис считался неизлечимым заболеванием, теперь есть мощные антибиотики, которые позволяют справиться с ним за считанные дни. К сожалению, полностью изгнать из организма вирус герпеса просто невозможно.
Герпес живет в большинстве из нас. По российской статистике, 97% шестилетних граждан страны уже заражены тем или иным видом герпеса. Пока иммунитет у человека находится в неплохом состоянии, вирус спит. Но как только иммунитет начинает снижаться (а к этому могут привести не только те или иные заболевания, но и просто стрессы, неблагоприятная внешняя среда), герпес проявляет себя с худшей стороны. Поэтому профилактика герпеса — это просто внимательное отношение к себе, по возможности здоровый образ жизни.
Особый путь России
С 1994 года в Москве стала развиваться диагностическая база по генитальному герпесу и, как всегда бывает в таких случаях, наблюдается стремительный рост числа заболевших. В целом по России, по оценкам — более двух миллионов вновь диагносцированных случаев в год. Поскольку, как уже сказано выше, герпес до конца неизлечим, в задачу врачей входит перевести его в более легкую фазу ремиссии, повысить качество жизни больного. На западе основа лечения — супрессивная, то есть подавляющая терапия. Пациенты годами принимают противовирусные препараты типа зовиракса. В России преобладает другой подход: лечить организм, а не болезнь, поддерживать высокий уровень иммунитета. Российские врачи предпочитают назначать своим пациентам индукторы интерферона, белка-убийцы. Это амиксин, полудан, алпизарин и другие.
ПРОТИВОВИРУСНЫЕ ХИМИОПРЕПАРАТЫ
Существует несколько групп противовирусных препаратов, различающихся по клинико-фармакологическим характеристикам и особенностям практического использования:
противогерпетические,
противоцитомегаловирусные,
противогриппозные,
препараты расширенного спектра,
антиретровирусные.
ПРОТИВОГЕРПЕТИЧЕСКИЕ ХИМИОПРЕПАРАТЫ
К основным противогерпетическим ЛС с эффективностью, доказанной в рандомизированных клинических исследованиях, относятся четыре близких по структуре препарата из группы аналогов нуклеозидов - ацикловир, валацикловир, пенцикловир и фамцикловир. Причем валацикловир и фамцикловир представляют собой исходно неактивные соединения, которые в организме человека превращаются в ацикловир и пенцикловир, соответственно. Все эти ЛС блокируют синтез ДНК у размножающихся вирусов герпеса, но не действуют на вирусы, находящиеся в латентном состоянии.
При резистентности ВПГ и вируса varicella-zoster применяют фоскарнет в/в*.
Для местного применения используются ацикловир, пенцикловир, идоксуридин, фоскарнет и тромантадин.
В России при офтальмогерпесе применяется отечественный препарат полудан, обладающий интерфероногенными и иммуномодулирующими свойствами, однако рандомизированных клинических испытаний этого препарата не проводилось.
Аналоги нуклеозидов
Механизм действия
Ацикловир является родоначальником противогерпетических препаратов – блокаторов синтеза вирусной ДНК. Противовирусное действие оказывает активный метаболит ацикловира - ацикловира трифосфат, который образуется в клетках, пораженных вирусом герпеса. Ингибируя вирусную ДНК-полимеразу, ацикловира трифосфат блокирует синтез вирусной ДНК. Препарат обладает очень низкой токсичностью, так как не действует на ДНК-полимеразу клеток человека и неактивен в здоровых клетках.
Пенцикловир в пораженных вирусом клетках человека активируется, превращаясь в пенцикловира трифосфат, который нарушает синтез вирусной ДНК. Пенцикловир имеет длительный внутриклеточный период полувыведения (7–20 ч), что значительно выше, чем у ацикловира (менее 1 ч). Но он обладает меньшим сродством к вирусной ДНК-полимеразе, чем фосфорилированный ацикловир.
В целом, все три препарата (ацикловир, валацикловир и фамцикловир) при приеме внутрь имеют сравнимую клиническую эффективность.
Фоскарнет образует неактивные комплексы с ДНК-полимеразой герпетических вирусов и ЦМВ.
Спектр активности
Наиболее чувствительны к ацикловиру ВПГ 1 и 2 типа. Вирус varicella-zoster более чем в 20 раз, а ЦМВ в 470 раз менее чувствителен к ацикловиру, чем ВПГ 1 типа. Пенцикловир очень близок к ацикловиру по активности в отношении к ВПГ 1 и 2 типа и вируса varicella-zoster.
Резистентность к противогерпетическим препаратам является редким явлением, особенно у пациентов с нормальным иммунитетом. Ацикловирорезистентные штаммы при умеренном иммунодефиците могут встречаться у 6–8% пациентов, а у пациентов, длительно получавших иммуносупрессивную терапию, и при СПИДе резистентность возрастает до 17%. Следует учитывать, что ацикловирорезистентные штаммы также устойчивы к валацикловиру и фамцикловиру. В этом случае препаратом выбора является фоскарнет * .
* Лекарственная форма для в/в введения не зарегистрирована в России
Фармакокинетика
Для перорального применения используются три препарата: ацикловир, валацикловир и фамцикловир, а в/в вводится только ацикловир. Наиболее низкую биодоступность при приеме внутрь имеет ацикловир (15–20%), но даже суточная доза 0,8–1,0 г достаточна для подавления ВПГ. Валацикловир является валиновым эфиром ацикловира, предназначенным для приема внутрь, и имеет значительно более высокую биодоступность (54%). В процессе всасывания в ЖКТ и в печени он превращается в ацикловир.
Биодоступность фамцикловира при приеме внутрь натощак - 70–80%. В ЖКТ превращается в пенцикловир, который затем фосфорилируется в клетках, пораженных вирусом.
Пенцикловир применяют только наружно, так как при приеме внутрь он имеет очень низкую биодоступность (5%).
Ацикловир хорошо распределяется в организме. Проникает в слюну, внутриглазную жидкость, вагинальный секрет, жидкость герпетических пузырьков. Проходит через ГЭБ. При местном применении незначительно всасывается через кожу и слизистые оболочки.
Как ацикловир, так и пенцикловир экскретируются преимущественно почками, на 60–90% в неизмененном виде. Ацикловир выводится путем клубочковой фильтрации и канальцевой секреции. Препараты имеют примерно сходный период полувыведения – 2–3 ч, у детей младшего возраста - до 4 ч. При почечной недостаточности (клиренс креатинина менее 30 мл/мин) период полувыведения значительно возрастает, что требует коррекции доз и режимов введения.
Фармакокинетика фоскарнета при местном применении не исследована.
Нежелательные реакции
Ацикловир, как правило, хорошо переносится пациентами, НР развиваются редко.
Местные
Жжение при нанесении на слизистые оболочки, особенно при вагинальном применении;
флебит при в/в введении.
Системные
ЖКТ: боль или дискомфорт в животе, тошнота, рвота, диарея.
ЦНС: у 1–4% пациентов при в/в введении ацикловира отмечаются заторможенность, тремор, судороги, галлюцинации, бред, экстрапирамидные расстройства. Симптомы обычно появляются в первые 3 сут лечения, связаны с высоким уровнем ацикловира в сыворотке крови (более 25 мкг/мл) и постепенно исчезают по мере его понижения. Факторы риска: почечная недостаточность, сопутствующее применение других нейротоксичных препаратов, интерферона, метотрексата.
Почки: вследствие кристаллизации препарата в почечных канальцах у 5% пациентов при в/в введении развивается обструктивная нефропатия, проявляющаяся тошнотой, рвотой, болью в пояснице, азотемией. Факторы риска: детский возраст, быстрое в/в введение, большие дозы, высокие концентрации ацикловира в плазме, обезвоживание, заболевания почек, сопутствующее применение других нефротоксичных препаратов (например, циклоспорина). Меры профилактики: обильное питье. Меры помощи: отмена препарата, инфузионная терапия.
Другие: головная боль, головокружение (чаще у пожилых людей).
Валацикловир по переносимости близок к ацикловиру для перорального приема. Особенностью являются редкие случаи развития тромботической микроангиопатии у пациентов с иммуносупрессией (больные СПИДом, онкологические пациенты), получающих множественную фармакотерапию.
По профилю безопасности у взрослых фамцикловир близок к ацикловиру. Наиболее частыми НР являются головная боль и тошнота.
Показания
Инфекции, вызванные ВПГ 1 и 2 типа:
инфекции кожи и слизистых оболочек;
офтальмогерпес (только ацикловир);
Инфекции, вызванные вирусом varicella-zoster:
Профилактика ЦМВ инфекции после трансплантации почек (ацикловир, валацикловир).
Местная терапия
Инфекции кожи и слизистых оболочек, вызванные ВПГ.
Противопоказания
Предупреждения
Беременность. Безопасность системной терапии ацикловиром, валацикловиром и фамцикловиром беременных полностью не доказана. Назначение ацикловира в I триместре беременности не увеличивает риска возникновения врожденных дефектов, по сравнению со средним уровнем в популяции. Результаты применения валацикловира и фамцикловира при беременности носят предварительный характер и не могут быть основанием для их регулярного применения. Однако ацикловир может с осторожностью применяться у беременных внутрь как во время первичного эпизода, так и при рецидивах герпеса.
Кормление грудью. Ацикловир проникает в грудное молоко, поэтому ацикловир и валацикловир следует применять с осторожностью женщинам, кормящим грудью.
Педиатрия. Основным препаратом для применения в педиатрии является ацикловир, так как он наиболее хорошо изучен у детей. Имеются рекомендации о возможности применения валацикловира и фамцикловира у детей старше 12 лет с иммунодефицитом. Однако валацикловир нельзя применять у детей с иммунодефицитом, вызванным ВИЧ. Дозу ацикловира у детей до 12 лет лучше рассчитывать на площадь поверхности тела: 0,25 г/м 2 , вместо 5 мг/кг; 0,5 г/м 2 , вместо 10 мг/кг.
Гериатрия. Учитывая возрастное понижение функции почек, перед началом терапии, особенно внутрь в больших дозах и при в/в введении, следует оценивать клубочковую фильтрацию. Может потребоваться коррекция режима дозирования.
Нарушение функции почек. Перед применением системных противогерпетических препаратов желательно определять клубочковую фильтрацию. Это обязательно следует делать при использовании внутрь в больших дозах и при в/в введении. У пациентов с нарушением функции почек дозу следует уменьшить. У пациентов, получающих гемодиализ, валацикловир применяют в дозе, рекомендуемой при клиренсе креатинина менее 15 мл/мин, причём препарат лучше принимать после сеанса гемодиализа.
Нарушение функции печени. У пациентов с печеночной недостаточностью коррекции дозы ацикловира и валацикловира не требуется, однако опыт применения этих препаратов у пациентов с тяжелым нарушением функции печени недостаточен. При печеночной недостаточности дозу фамцикловира следует уменьшить.
СПИД. При использовании валацикловира в больших дозах (0,8–3,2 г/сут) у пациентов со СПИДом отмечено повышение частоты развития тромботической микроангиопатии. При длительной супрессивной терапии валацикловиром в дозе 0,25–1 г/сут частота её развития не повышается.
Лекарственные взаимодействия
При сочетании ацикловира с аминогликозидами или другими нефротоксичными ЛС возрастает риск неблагоприятного воздействия на почки.
При сочетании ацикловира с зидовудином увеличивается риск развития нейротоксических реакций.
При сочетании валацикловира с циметидином увеличивается концентрация в крови ацикловира.
Информация для пациентов
Применение противогерпетических препаратов следует начинать как можно раньше, после появления первых симптомов заболевания. Внутрь можно принимать независимо от приема пищи.
Следует строго соблюдать предписанный режим назначений во время всего курса лечения, не прекращать лечение раньше положенного срока. В случае пропуска дозы принять ее как можно скорее. Не принимать ее, если почти наступило время приема следующей дозы (не удваивать дозу).
Необходимо проконсультироваться с врачом, если улучшение не наступает в течение нескольких дней или появляются новые симптомы.
Пораженные участки кожи следует содержать в чистоте и по возможности не носить плотно прилегающую к ним одежду. При герпетических высыпаниях на половых органах воздерживаться от половых контактов до полного заживления изъязвлений. Прием противогерпетических препаратов не предотвращает передачу генитального герпеса при половом контакте, поэтому рекомендуется пользоваться барьерными методами контрацепции (презерватив).
Применение противогерпетических препаратов не ведет к полному излечению, так как вирус герпеса сохраняется в организме в неактивном (латентном) состоянии.
Идоксуридин
Противогерпетический препарат, который применяется только в офтальмологии для лечения и профилактики инфекций, вызванных ВПГ.
Нежелательные реакции
Раздражение, боль, зуд краснота, отек, помутнение роговицы, появление пятен или точечных дефектов на эпителии роговицы.
Аллергические реакции в редких случаях.
Показания
Профилактика рецидивов герпетического кератита в раннем послеоперационном периоде после лечебной кератопластики.
Противопоказания
Повышенная чувствительность к препарату.
Предупреждения
Не применять при глубоких формах кератита.
Соблюдать осторожность при совместном применении с глюкокортикоидами.
Неэффективен при аденовирусных конъюнктивитах.
Тромантадин
Тромантадин является производным амантадина, применяющегося для терапии гриппа. Противовирусное действие обусловлено торможением репликации герпесвирусов.
В настоящее время вместо тромантадина применяют более активные препараты из группы ациклических нуклеозидов (ацикловир и др.).
Нежелательные реакции
Показания
Инфекции кожи и слизистых оболочек, вызванные ВПГ и varicella-zoster.
Противопоказания
Аллергические реакции на препарат.
Предупреждения
Данные о безопасности применения тромантадина при беременности и кормлении грудью отсутствуют.
Читайте также:


