Как протекает опоясывающий герпес в пожилом возрасте
Опоясывающий лишай (Herpes zoster) (син. — опоясывающий герпес) — заболевание вирусной природы, характеризующееся односторонними высыпаниями на коже с сильным болевым синдромом. Возбудитель — вирус ветряной оспы (Varicella zoster) семейства герпесвирусов, при первой встрече с организмом (чаще в молодом возрасте) вызывает типичную ветряную оспу.

Заболевают люди, ранее перенесшие ветряную оспу. Болеют преимущественно лица пожилого и старческого возраста, а так же люди с ослабленном иммунитетом: больные лейкозами, лимфогранулематозом, новообразованиями, получающие химиотерапию, длительно получающие кортикостероиды и иммуно-депрессанты. Особенно часто инфекция развивается у больных с синдромом приобретенного иммунодефицита
Доказано, что после перенесенной ветряной оспы вирус многие годы сохраняется в нервных волокнах человека, не нанося при этом никакого ущерба здоровью человека. При резком ослаблении местного и общего иммунитета может наступить активация вируса, и инфекция проявляется в виде высыпаний в тех кожных зонах, за которые ответственен пораженный нерв. Именно участие нервов в развитии болезни и обеспечивает выраженный болевой синдром. В большинстве случаев поражаются межреберные нервы или тройничный нерв.
Характерный признак опоясывающего герпеса — односторонность поражения.
В зависимости от локализации поражения нервов возможно развитие следующих состояний:
- Офтальмологический опоясывающий герпес – вирус проникает в глазную ветвь тройничного нерва, что опасно повреждением роговицы.
- Синдром Рамсея – Ханта – высыпания возникают в наружном слуховом проходе или ротоглотке и сопровождаются односторонним параличом мимических мышц. В некоторых случаях также развивается потеря слуха и системное головокружение.
- Двигательный опоясывающий герпес – слабость мышц в местах кожной сыпи.
Симптомы опоясывающего лишая
Для двигательного опоясывающего герпеса характерно острое начало, общее недомогание, лихорадка, небольшой зуд, чувство покалывания, резко выраженные жгучие боли в месте будущих высыпаний. Высыпания появляются по ходу отдельных чувствительных нервов в виде нечётких розоватых пятен (3—5 см), на фоне которых через 18—24 часов образуются группы болезненных пузырьков, заполненных прозрачным, а затем и мутным содержимым. Высыпания исчезают в течение 2—4 недель: пузырьки подсыхают, образуя жёлто-коричневые корочки, которые затем отпадают, оставляя незначительную пигментацию. Боли иногда становятся нестерпимыми, усиливаются при малейшем прикосновении к коже, при охлаждении, движении. Иногда болезнь характеризуется интоксикацией и невралгическими болями, сыпь отсутствует. При появлении кожных высыпаний боли становятся обычно менее интенсивными. Боль может сохраняться в течение недель и месяцев.

Офтальмологический опоясывающий лишай характеризуется особо тяжёлым течением, который может продолжаться в течение нескольких недель. При глазной форме наблюдаются специфический вирусный кератит, реже ирит, глаукома т.к. вирус проникает в глазную ветвь тройничного нерва.

Для синдрома Рамсея- Ханта характерна красная болезненная сыпь, в области ушей или во рту и лицевой паралич (например, века или рта) на одной стороне лица. Могут возникнуть такие симптомы такие как боль в ухе, головокружение, сухость глаз, изменения вкуса.

Лечение направленно на борьбу с интоксикацией, снятие болей и предупреждение генерализации инфекции. Как правило, больные опоясывающим лишаем не нуждаются в госпитализации и дальнейший прогноз благоприятен. Однако, для предотвращения осложнений при подозрении на опоясывающий лишай, необходимо срочно обратиться к врачу.
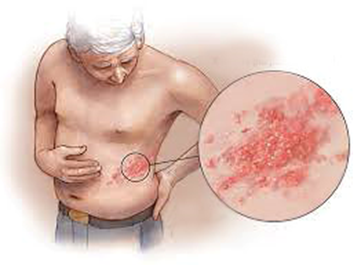
У пожилого мужчины в груди слева внезапно появилась сильная боль. Учитывая возраст и наличие сердечных проблем, близкие перепугались: инфаркт. Но врачи "скорой" подозрение не подтвердили. Миозит, решила врач, и назначила инъекцию анальгина. После укола боль почти прошла, но утром появилась снова, а на грудной клетке обозначилась цепочка мелких пузырьков.
Тогда пациент обратился к врачу-дерматологу в наш диспансер. Сгруппированные пузырьки по ходу межреберного нерва, боли в этой области дали врачу основание выставить диагноз: опоясывающий лишай. Учитывая возраст, а также выраженный болевой синдром, пациента госпитализировали в стационар.
Опоясывающий лишай, или герпес зостер, - это инфекционное заболевание, вызываемое специфическим вирусом. Попадая в организм человека, этот вирус может спровоцировать два заболевания: у одних - ветряную оспу, у других - опоясывающий лишай, а иногда у одного больного встречаются сразу оба заболевания.
Опоясывающий лишай возникает как вторичная инфекция, преимущественно у взрослых людей, обладающих частичным иммунитетом, который развился в результате прежнего контакта с вирусом.
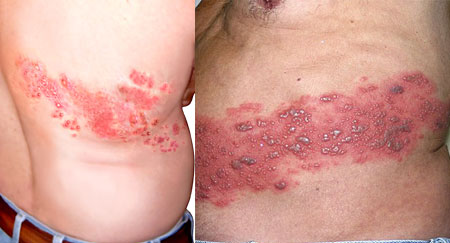
Типичными для опоясывающего лишая являются мелкопузырчатые высыпания, чаще всего расположенные по ходу ветвей пораженного чувствительного нерва. На любом участке тела -- чаще на туловище, на лице, а также на волосистой части головы (как правило, с одной стороны) появляются красные мелкие отечные пятнышки с пузырьками. Располагаются они неравномерно по линии пораженных нервов от позвоночника до средней линии живота, грудной клетки, лба. Пузырьки быстро становятся гнойничками и лопаются. В тяжелых случаях образуются язвочки, при заживании которых могут остаться рубцы.
Чаще поражаются вирусом межпозвоночные нервные узлы грудного отдела. Иногда в процесс воспаления вовлекаются нервные окончания солнечного сплетения, что приводит к нарушению функции желудочно-кишечного тракта (боли в животе, поносы, запоры), возможна также задержка мочеиспускания. При поражении веточек тройничного нерва высыпания располагаются на лбу, щеках, нижней челюсти, сопровождаются головной болью (чаще односторонней). В этом случае могут поражаться и глаза -- веки, глазные яблоки.
По ходу пораженных вирусом нервных окончаний нередко возникает внезапная, тупая или жгучая, иногда распространенная боль. Чаще всего боль держится долго после исчезновения высыпаний на коже, особенно если лечение было начато несвоевременно.
Несмотря на то что обычно опоясывающий лишай - местное локализованное заболевание, приблизительно у 5% больных наблюдаются общие явления - головная боль, тошнота, симптомы раздражения мозговых оболочек.
С возрастом заболеваемость опоясывающим лишаем возрастает и характеризуется более тяжелым течением.
ВАЖНО! При появлении болей в грудной клетке, пояснице, голове с последующим высыпанием пузырьков необходимо срочно обратиться к врачу (терапевту, невропатологу, дерматологу, инфекционисту). Больные опоясывающим лишаем с активными проявлениями на коже опасны - могут заразить ветряной оспой и опоясывающем лишаем как малолетних детей, так и ослабленных пожилых людей.
Заболевание женщины во время беременности, накануне родов может привести к внутриутробному заражению плода и гибели новорожденного.
В лечении опоясывающего лишая используются:
- противогерпетические антибиотики в виде таблеток, а в тяжелых случаях - в виде инъекций;
- для снятия воспаления и боли в нервных окончаниях назначаются витамины группы В (лучше в инъекциях), нестероидные противовоспалительные препараты, анальгетики.
В упорных случаях, когда интенсивная боль не проходит, применяется блокада новокаина в виде инъекций по ходу пораженных нервных окончаний. Для поднятия иммунитета показаны соответствующие иммуностимулирующие препараты.
Чтобы в лопнувшие пузырьки на коже не внедрилась гнойничковая инфекция, для местного лечения применяются: раствор зеленки, раствор фукарцина, мази с противомикробной активностью (гентамициновая, тетрациклиновая, эритромициновая), можно использовать также мазь бетатин, содержащую препараты йода.
Из физиотерапевтических процедур рекомендуются местное ультрафиолетовое облучение, сухое тепло после подсыхания пузырьков.
Матушевская Е.В., Негматов Б.И.
Российский государственный медицинский университет
Вирус герпеса третьего типа varicella zoster (VZV) вызывает два клинически обособленных заболевания - ветряную оспу и опоясывающий герпес (Баринский И.Ф. и др., 1986; Haanpaa M., 2001). Оба заболевания, прежде всего, характеризуются везикулярной сыпью. Первичная инфекция манифестирует в форме ветряной оспы (ветрянки), а реактивация латентного VZV обусловливает появление локализованных высыпаний - опоясывающего лишая (Хахалин Н.Н., 2002). Мысль о связи между ветрянкой оспой и опоясывающим лишаем впервые была высказана в 1888 венским врачом Яношом Бокеем (von Bokay J., 1909).
Эпизод ветряной оспы в детстве способствует формированию специфической клеточной и гуморальной иммунной защиты. Считается, что рецидив инфекции у таких пациентов может развиться только на фоне недостаточности иммунной защиты, вследствие снижения активности специфических натуральных киллеров, Т-киллеров и системы интерферонов (Fleming D.M. et al., 2004). После первичной инфекции излюбленным местом персистенции VZV являются ганглий тройничного нерва и спинномозговые ганглии чувствительных корешков грудного отдела спинного мозга, где VZV находится в латентном состоянии. В течение этого времени вирус не размножается и не проявляет патогенных свойств. По-видимому, время латентного состояния вируса определяется уровнем специфических антител к VZV. Снижение их количества ведет к реактивации вируса, вирусной репликации (размножению), что на клиническом уровне и проявляется в виде опоясывающего лишая (Arvin A., 2005). Данный вывод подтверждается высокой корреляцией между вероятностью возникновения опоясывающего лишая у людей пожилого возраста и возрастным ослаблением активности клеточного звена иммунитета (Gilden et al., 2000)., На это также указывают данные, свидетельствующие о более высокой заболеваемости опоясывающим герпесом среди лиц, инфицированных вирусом иммунодефицита человека (Gilson I.H. et al., 1989), однако точные механизмы, лежащие в основе перехода вируса из латентного состояния в активное неизвестны.
В случае реактивации VZV ганглии чувствительных нервов становятся местами репликации вируса, именно в них обнаруживаются наиболее выраженные дегенеративные повреждения нейронов (Zerboni L. et al., 2005; Reichelt M. et al., 2008). В результате развивается ганглионит, сопровождаемый распространением инфекции вниз по нервным аксонам к коже. Каким образом происходит транспортировка вируса в поврежденных аксонах неизвестно. Инфекция также может распространяться центрально, приводя к воспалению оболочек в области передних и задних рогов спинного мозга (Gray F. et al. 1994). Отдельные патолого-анатомические наблюдения также свидетельствуют о наличии воспалительных изменений и в контралатеральных спинномозговых ганглиях (Miller S. E. et al., 1997), отмечается снижение количества нейронов и наличие воспалительных инфильтратов в ганглиях, периферических нервах, и спинномозговых корешках (Gowrishankar K. et al., 2007). В некоторых случаях отмечается выраженные некротические изменения в спинномозговых ганглиях. Большинство изменений в периферическом нерве протекает по типу Валлериановской дегенерации, имеющей место, как в толстых, так и в тонких волокнах. (Denny-Brown et al., 1944).
Острая VZV инфекция клинически характеризуется стадией продрома и стадией везикулярных высыпаний (Arvin A., 2005).
В стадию продрома боль при опоясывающем лишае появляется на 48-72 ч. раньше специфических высыпаний на коже и постепенно усиливается в острую фазу инфекционного процесса (Ali N.M.K., 2000). Везикулы обычно формируются в течение первых 5-7 дней. Пустулы образуются в последующие 4-6 дней, когда везикулы прорываются и выпускают гной. Затем пустулы покрываются твердой коркой, после чего происходит заживление кожи, обычно в течение 2-4 недель после начала заболевания. Гистологические изменения в коже аналогичны таковым при ветряной оспе - выявляются гигантские многоядерные клетки с внутриядерными включениями (Johnson R.W., 2003).
Сыпь обычно локализуется в одном или нескольких смежных дерматомах и сопровождается развитием острой невропатической боли. У 50% больных сыпь встречается на туловище, у 20% - на голове, у 15% - на руках, и у 15% - на ногах (Arani R.B. et al., 2001).
Клинический диагноз опоясывающего лишая в типичных случаях достаточно прост. Однако иногда требуется проведение лабораторной диагностики с целью идентификации вируса. Наиболее быстрым и высокочувствительным методом является полимеразная цепная реакция.
В остром периоде болезни или после него возможно развитие осложнений, захватывающих различные системы организма. Наиболее серьезными считаются неврологические осложнения. В структуре неврологических расстройств ведущее место занимает поражение периферической нервной системы. При данном заболевании воспалительный процесс затрагивает региональные, чувствительные ганглии с развитием ганглиолитов. Наличие у больных корешковых болей, парастезий, сегментарных нарушений чувствительности отмечается практически у каждого больного (Stankus S. et al., 2000; Thyregod H. G. et al., 2007). Болевой синдром имеет выраженную вегетативную окраску в виде жгучих, приступообразных, резких болей, усиливающихся в ночное время. В головном мозге при опоясывающем герпесе могут быть обнаружены явления отека, выраженная диффузная инфильтрация подпаутинного пространства, геморрагии в белом веществе, базальных ганглиях (Sissoko D. et al., 1998). Следует заметить, что осложнения со стороны головного и спинного мозга в настоящее время встречаются редко. В случаях развития VZV-инфекции в области тройничного нерва часто наблюдаются осложнения со стороны глаз - кератит, ирит, ретинит, офтальмит. Ранее, при отсутствии специфической противогерпетической терапии, к частым осложнениям VZV-инфекции относились пневмонии, энцефалиты или гепатиты, иногда приводившие к летальному исходу.
Вместе с тем, из всех перечисленных осложнений VZV инфекции самым распространенным считается постгерпетическая невралгия (Dworkin R.H., Portenoy R.K., 1996).
Различают острую герпетическую невралгию (в течение 30 дней после начала заболевания) и постгерпетическую невралгию (Choo P. et al.,1997). К ПГН относят упорные боли в областях, затронутых герпесной инфекцией после заживления кожи (Dworkin R. et al. 2003). Наиболее хорошо установленными факторами риска для ПГН являются пожилой возраст, большая распространенность высыпаний на коже и выраженная боль перед везикулярной сыпью (Desmond R.A. et al., 2002; Fleming D.M. et al., 2004). Все эти факторы находятся во взаимосвязи, поэтому пациенты 50 лет и старше в большинстве случаев испытывают тяжелую, нестерпимую боль и значительные кожные высыпания, что гораздо чаще приводит к развитию ПГН. У пациентов со всеми этими факторами риск развития ПГН превышает 50-75 % (Gnann J., Whitley R. 2002; Jung B.F., 2004). Постгерпетическая невралгия может развиться в любом возрасте, однако для нее характерна прямая корреляция частоты встречаемости и длительности ПГН с возрастом. Более 50% всех пациентов с ПГН - старше 60 лет, 75% больных с указанной патологией приходится на возрастную группу старше 75 лет (Nurmikko T.J., 2001). Половина всех пациентов с ПГН старше 60 лет испытывает постоянную боль более 6 месяцев, в то время как в возрастной группе 30-50 лет ПГН более 6 месяцевь наблюдается у 10% больных (Whitley R. et al. 1996). В США ежегодно регистрируется 100-200 тыс. новых случаев ПГН (Nurmikko T.J., 2001). Однако, истинная распространенность ПГН не известна, не только потому, что эпидемиологические данные недостаточны, но также из-за отсутствия конценсусса по определению ПГН. Некоторые авторы относят к ПГН боли, возникающие в любой период герпесной инфекции, другие считают, что ПГН - это боль, сохраняющаяся спустя 3 месяца после заживления кожи. В первом случае определения ПГН ее распространенность составляет 8%, во втором - 4,5% (Choo P. et al. 1997). Постоянную боль в течение 1 мес после сыпи испытывают до 15% пациентов и около 4% пациентов от общего количества перенесших опоясывающий лишай отмечают сохранение боли в течение года (Lancaster T. et al. 1995).
Классическое проспективное исследование, проведенное Hope-Simpson (1975), продемонстрировало, что из 321 пациента с опоясывающим лишаем 10 % имеют выраженную боль спустя 3 месяца после острой герпетической инфекции, а 4 % - и через 12 месяцев. Подобные результаты были получены и в других проспективных исследованиях (Helgason S. et al. 1996; 2000; Scott F.T. et al., 2006), в которых также было показано, что наибольший риск пролонгации болевого синдрома после перенесенного опоясывающего лишая имеют пациенты в возрасте около 60 лет.
Постгерпетическая невралгия занимает третье место по частоте встречаемости среди различных типов невропатической боли и уступает только болям в нижней части спины и диабетической невропатии (Montero H.J. et al., 2005; Breivik H. et al, 2006; Torrance N. et al., 2006).
Локализация болевого синдрома практически всегда соответствует зоне кожных высыпаний. Интенсивность болевого синдрома как правило высокая. Кроме глубоких ноющих и стреляющих болей очень характерны поверхностные жгучие боли и наличие стимулозависимых болей - динамической гипералгезии и аллодинии (Baron R., 2004).
При клиническом осмотре в зоне болей выявляются нарушения поверхностной чувствительности. Качество боли в острый период опоясывающего лишая и при ПГН различно. Вместе с тем, несмотря на разный выбор дескрипторов из МакГилловского болевого вопросника, пациенты с опоясывающим лишаем и ПГН для описания своих болевых ощущений выбирают похожие по смыслу слова, например, горячая и жгучая боль или пронзающая и простреливающая боль (Bennett M., 2001).
Схожие проявления наблюдаются и при описании вызванной боли пациентами с опоясывающим лишаем и ПГН. И те, и другие отмечают наличие схожих типов гипералгезии и аллодинии (Haanpaa M. et al., 2000; Berry J.D., Rowbotham M.C., 2004).
У большинства пациентов боль, связанная с ПГН, уменьшается в течение первого года. Однако у части больных она может сохраняться годами и даже в течение всей оставшейся жизни, причиняя немалые страдания (Cunningham A.L., Dworkin R.H., 2000). Затяжной, тяжелый характер заболевания с длительным, выраженным болевым синдромом способствует формированию расстройств психики (Dworkin R.H., et al., 1992). У таких пациентов выявляются тревожно-депрессивные расстройства, когнитивные нарушения - снижение активного внимания, памяти, затруднения осмысления происходящего, отмечается некритичность, нетерпеливость, неряшливость, страх боли, неуверенность в завтрашнем дне, отмечается снижение социальной активности (Haythornthwaite J.A. et al., 2003). ПГН оказывает значительное отрицательное влияние на качество жизни и функциональный статус пациентов особенно пожилого возраста (Lydick E. et al., 1995). У пациентов с ПГН отмечается хроническая усталость, снижение массы тела, физической активности, нарушения сна (Morin C.M., Gibson D., Wade J., 1998).
В основе боли, связанной с ПГН, лежат воспалительные изменения или повреждения ганглиев задних корешков спинного мозга и периферических нервов в пораженных зонах тела. Такие боли относят к невропатическим болям, их выделяют в отдельную самостоятельную группу и определяют как боли, возникающие вследствие первичного повреждения соматосенсорной нервной системы (Treede R.D. et al., 2008).
Патофизиологической основой невропатических болевых синдромов являются нарушения генерации и проведения ноцицептивного сигнала в нервных волокнах, а также механизмов контроля возбудимости ноцицептивных нейронов в структурах спинного и головного мозга (Кукушкин М.Л., Хитров Н.К., 2004; Baron R. 2000).
Лечебная тактика при опоясывающем лишае включает два основных направления: противовирусная терапия и купирование невропатической боли, как в острый период заболевания, так и в стадии постгерпетической невралгии. Результаты нескольких рандомизированных контролируемых испытаний свидетельствуют о том, что раннее начало лечения простого герпеса может предотвратить развитие постгерпетической невралгии или способствовать ее скорейшему разрешению (Исаков В.А. и др., 2004; Helgason S. et al., 1996; Jackson J.L. et al., 1997 ; Volmink J. et al., 1996).
Наиболее широкое применение нашли такие специфические противогерпетические препараты, как ацикловир, фамцикловир и валацикловир, которые, являясь нуклеозидными аналогами, блокируют вирусную репликацию (Романцев М.Г., 1996; Beutner K. et al., 1995; Bruxelle J., 1995). Важно, что противовирусное лечение проявляет наивысшую активность, если назначено в течение 72 ч от начала герпетических высыпаний (Johnson R., 2001; Johnson R., Dworkin R.H., 2003). В ряде исследований доказана высокая эффективность ацикловира в уменьшении тяжести, продолжительности острой герпесной инфекции и профилактике ПГН, особенно при его раннем назначении. Оценка эффективности фамцикловира также продемонстрировала уменьшение времени до разрешения сыпи (Dworkin R.H. et al., 1998). В сравнительном исследовании ацикловира и валацикловира показана эквивалентная эффективность в сокращении продолжительности невропатической ПГН (Beutner K. et al. 1995). В другом клиническом испытании установлена терапевтическая эквивалентность фамцикловира и валацикловира для неосложненного герпеса (Tyring S. et al. 2000). Возможно также сочетанное использование противовирусной терапии и глюкокортикостероидов (Whitley R. et al. 1999). Выявлено, что такая комбинация эффективнее монотерапии противовирусными препаратами, особенно для лечения острой боли и коррекции различных аспектов качества жизни пациентов. Комбинация ацикловир+преднизолон значительно быстрее купирует острую невралгию и возвращает пациента к обычной жизнедеятельности, но существенно не влияет на течение ПГН, то есть она наиболее показана в остром периоде в старших возрастных группах для терапии острого болевого синдрома. Доказано, что хотя преднизолон является иммуносупрессором, его использование не увеличивает частоты развития ПГН и в этом смысле его действие сравнимо с влиянием плацебо, то есть данная комбинация может быть спокойно использована в старших возрастных группах. Для некупируемых тяжелых случаев ПГН некоторые исследователи рекомендуют интратекальное введение метилпреднизолона (Kost R., Straus S., 1996).
В настоящее время в США делается акцент на профилактику герпетической инфекции. С 1995 г. в США проводится всеобщая вакцинация от ветряной оспы, особенно пожилых лиц, и с 1999 г. отмечается резкое снижение заболеваемости (Hambleton S., Gershon A., 2005; Oxman M.N. et al., 2005).
При постгерпетической невралгии препаратами с доказанной эффективностью (класс А - терапия первой линии) являются: пластины с 5% лидокаином, габапентин, прегабалин, трициклические антидепрессанты, трамадол (Attal et al., 2006).
На сегодняшний день эффективность применения пластин с 5% лидокаином (Версатис, Grunenthal Gmbh) убедительно доказана при лечении ПГН. Так, в нескольких рандомизированных клинических исследованиях установлено, что применение пластин с 5% лидокаином статистически достоверно более значимо облегчает проявления болевого синдрома у пациентов с постгерпетической невралгией по сравнению с плацебо (Rowbotham M.C., 1996; Galer B.S., 1999, 2002). На основании полученных данных FDA одобрило применение данного препарата в качестве стартовой терапии у пациентов с постгерпетической невралгией. (Richard L. et al., 2004)
Версатис - это топический анальгетик, который действует непосредственно там, где болит. Он выпускается в виде мягких пластин размером 10х14 см, которые наклеиваются на неповрежденную кожу без признаков воспаления. Медленно высвобождающийся из пластины лидокаин создает более или менее значительную концентрацию лишь в поверхностных слоях кожи, где проходят тонкие волокна, обеспечивающие болевую и температурную чувствительность (Gammaitoni AR, Davis MW. 2002.). Лидокаин лишь в незначительной степени проникает в более глубокие слои кожи, где проходят кровеносные сосуды, поэтому его попадание в системный кровоток сведено к минимуму. У пациентов, использовавших пластины Версатис, не наблюдалось никаких известных системных эффектов лидокаина (влияние на деятельность ЦНС и сердечно-сосудистой системы). Таким образом, важнейшим преимуществом пластин Версатис служит отсутствие системного действия, что гарантирует безопасность лечения. Практически полное отсутствие системного эффекта позволяет назначать Версатис совместно с любыми другими препаратами для лечения нейропатической боли.
Механизм лечебного эффекта препарата Версатис не ограничивается только действием высвобождающегося из них лидокаина. Важное значение имеет также то, что пластина выполняет роль механического барьера, препятствуя раздражению участка кожи с измененной чувствительностью (аллодиния), а также оказывает не него легкое охлаждающее действие (Galer BS, Gammaitoni AR, Oleka N et al., 2004)
Пластины Версатис рекомендуется прикреплять на 12 ч в течение суток, затем следует 12-часовой перерыв. Обезболивающий эффект часто начинается в течение 30 мин после прикрепления пластины, но может проявляться и позже, нарастает в течение 4 ч и затем поддерживается в течение длительного времени, пока пластина прикреплена к коже. Более того, он может сохраняться и после ее удаления.
Для объективной оценки эффективности каждого из препаратов при лечении ПГН используется показатель NNT (number needed to treat - количество больных, которых нужно пролечить, чтобы получить у одного 50% снижение боли). Чем ниже NNT, тем более эффективен препарат при данной патологии. NNT для пластин с 5% лидокаином при лечении пациентов с ПГН составляет 2,0; для амитриптилина - 2,6; габапентина - 4,4; прегабалина - 4,6 (Wu C.L., Raja S.N., 2008); для трамадола - 3,9 (Kalso E., 2006).
Кроме того, в клинической практике очень важен показатель NNH (number needed to harm - число пациентов, которых необходимо пролечить данным препаратом, чтобы получить развитие 1 случая неблагоприятной побочной реакции, приводящей к отмене препарата). Он показывает, насколько безопасен данный препарат при его использовании. Величина NNH для трамадола, рассчитанная по результатам нескольких клинических исследований, составила 9.0, для ТЦА 14.7, для габапентина 26.1. Рассчитать показатель NNH для пластин с 5% лидокаином не представляется возможным в связи благоприятным профилем безопасности препарата, сравнимым с плацебо.
Таким образом, оценка препарата Версатис с позиций доказательной медицины делает его препаратом выбора при лечении постгерпетической невралгии, что подтверждено в соответствующих рекомендациях.
Постгерпетическая невралгия (ПГН) – часто встречающееся осложнение острого эпизода опоясывающего лишая, плохо поддающееся лечению и купированию состояния в связи с высокой степенью тяжести заболевания и его затяжной длительностью. Уровень специфических антител к вирусу Varicella zoster снижается с возрастом, что, вероятно, в значительной мере влияет на распространенность опоясывающего герпеса в старших возрастных группах. ПГН хорошо знакома специалистам в области иммунологии, поскольку они часто сталкиваются с ней в своей практике.
Опоясывающий лишай – одна из наиболее распространенных неврологических проблем; в США частота данного заболевания достигает до 1 млн новых случаев ежегодно (Oxman, 2005). Несмотря на то, что точные показатели встречаемости ПГН в США неизвестны, по данным исследований она предположительно составляет от 500 тыс. до 1 млн случаев в год (Bennett, 1997).
Основными факторами риска развития ПГН после эпизода опоясывающего герпеса являются следующие (Jung et al., 2004; Dworkin et al., 1998):
- пожилой возраст;
- сильная боль во время острого периода опоясывающего герпеса;
- тяжелая форма сыпи.
ПГН называют боль в зоне одного или нескольких дерматомов, которая сохраняется 120 и более дней от момента появления сыпи (Volpi, 2005). Эта боль может носить характер стимулзависимого постоянного жжения, пульсации или эпизодического острого, подобного удару током ощущения, а также характеризуется симптомами тактильной стимулзависимой аллодинии (возникновением боли после неболевого воздействия) и гипералгезии (возникновением сильной боли после воздействия слабого болевого раздражителя) (Dworkin, Portenoy, 1996). Кроме того, некоторые пациенты испытывают миофасциальную боль вследствие спазма мышц. Иногда наблюдается хронический зуд.
Более чем у 90% лиц с ПГН наблюдается аллодиния, встречающаяся в участках, где чувствительность относительно сохраняется (Bowsher, 1995). У пациентов также отмечается спонтанная боль в участках, где чувствительность потеряна или ухудшена. В данной статье рассмотрена доказательная база применения препаратов для лечения острого опоясывающего герпеса и ПГН, а также предложены стратегии профилактики опоясывающего герпеса.
Лечение острого опоясывающего герпеса: раннее начало терапии
Лечение острого опоясывающего лишая, основанное на доказательствах, включает противовирусные и аналгезирующие средства.
Противовирусные препараты подавляют репликацию вируса и оказывают положительное воздействие на острую и хроническую боль. Ацикловир (800 мг, 5 раз в день), валацикловир (1000 мг, каждые 8 часов) и фамцикловир (500 мг, каждые 8 часов) обычно применяют для лечения опоясывающего лишая. Все три препарата имеют сопоставимые профили эффективности и безопасности. Согласно метаанализу исследования пациентов в возрасте старше 50 лет, которым назначали ацикловир или плацебо, боль сохранялась в 15% случаев в группе ацикловира по сравнению с 35% группы плацебо (Dworkin, 2001). Также оценивали продолжительность болевого синдрома, сравнивая терапию фамцикловиром и плацебо. В результате у пациентов, принимавших плацебо, непроходящая боль отмечалась в течение 163 дней, тогда как у леченных фамцикловиром – 63 дней (Tyring, 1995).
На основании представленных фактов, антивирусные средства настоятельно рекомендуются для лечения опоясывающего лишая, особенно больным с повышенным риском развития ПГН. Противовирусную терапию необходимо начинать на протяжении 72 часов от начала высыпания. К сожалению, отсутствуют достоверные сведения, подтверждающие эффективность противовирусного лечения, примененного спустя трое суток после появления высыпания. Однако в неконтролируемом испытании была исследована эффективность ацикловира, который больные начали принимать до и по истечении 72 часов; различия в постоянстве боли между группами были незначительными, в связи с чем можно предположить, что эффект ацикловира проявляется даже при применении по прошествии трех дней (Kurokawa, 2002). В клинической практике диагноз опоясывающего лишая часто не ставится в течение 72 часов после возникновения симптомов. В связи с этим важно определять пациентов, для которых антивирусное лечение может быть эффективным, даже если оно начато относительно поздно, когда заболевание уже возникло. В особенности это имеет значение при глазном герпесе, поскольку в этом случае вирус может распространяться и по истечении трех дней (Zaal, 2001).
На практике для лечения боли, связанной с опоясывающим лишаем, применяют аналгезирующие средства, начиная с опиоидов короткого действия в сочетании с ацетаминофеном или нестероидными противовоспалительными препаратами. При неэффективности обычных аналгезирующих средств можно добавлять габапентин или прегабалин, а также трициклические антидепрессанты (ТЦА). Режим применения болеутоляющих препаратов должен быть скорректирован с учетом индивидуальных потребностей пациента. Если не удается контролировать боль, или побочные реакции невыносимы, рассматривают хирургические методы лечения, которые, однако, малоэффективны. К ним прибегают как к последнему варианту при отсутствии эффекта всех других мер. Адекватное купирование болевого синдрома в острой стадии заболевания может снижать риск развития стойкой ПГН.
Кортикостероиды обычно не рекомендуются в плановом порядке для лечения опоясывающего лишая. Однако иногда их применяют у пожилых пациентов с нормальным иммунитетом, в случае если антивирусная терапия и аналгезирующие средства не облегчают боль. В двух двойных слепых контролируемых исследованиях при приеме комбинации ацикловира и кортикостероидов в течение 21 дня уровень ПГН не снижался. Некоторая польза отмечалась с точки зрения возвращения пациентов к обычной повседневной активности и улучшения сна после отмены болеутоляющей терапии (Wood, 1994; Whitley, 1996).
Лечение ПГН, основанное на доказательствах
Медикаментозное лечение ПГН включает антиконвульсанты, ТЦА, опиоиды и средства местного применения. Инвазивные вмешательства имеют ограниченное, но важное значение в терапии боли при ПГН в клинической практике.
Блокаторы кальциевых каналов габапентин и прегабалин являются безопасными и относительно хорошо переносимыми препаратами. Они могут использоваться в качестве средств первой линии для лечения ПГН, начиная с минимальной дозы и повышая ее путем титрования. Габапентин одобрен Управлением по контролю над пищевыми продуктами и лекарственными средствами США (FDA) для терапии ПГН. Стартовая доза составляет 100-300 мг вечером, по мере необходимости доза увеличивается на 100-300 мг каждые 3-5 дней до максимальной, которая составляет 1800-3600 мг/сут. Суточная доза делится на 3-4 приема. В двух больших рандомизированных контролируемых исследованиях прием габапентина ассоциировался со статистически значимым уменьшением выраженности болевого синдрома, вследствие чего отмечалось улучшение сна и качества жизни (Rice, 2000). Побочные эффекты данного препарата включают сонливость, головокружение, периферические отеки, нарушение зрения и равновесия при ходьбе.
Поскольку габапентин экскретируется почками, необходимо с осторожностью использовать его у больных почечной недостаточностью. Уровень клиренса габапентина линейно связан с таковым креатинина и снижен у лиц пожилого возраста, а также у пациентов с нарушением функции почек. Следовательно, у таких больных необходимо корректно подбирать дозу габапентина и частоту приема препарата. У пациентов на гемодиализе уровень габапентина в плазме крови можно поддерживать на постоянном уровне путем приема 200-300 мг препарата спустя 4 часа после каждого сеанса диализа (Wong, 1995).
Не так давно FDA было разрешено применение габапентина пролонгированного действия при ПГН. Поводом для такого решения стали результаты 12-недельного основного исследования и двух дополнительных (2012).
В мультицентровом двойном слепом рандомизированном контролируемом плацебо исследовании в параллельных группах оценивали эффективность, безопасность и реакцию на габапентин пролонгированного высвобождения. Начальная рекомендованная доза составила 600 мг/сут в течение 3 дней, начиная с 4-го дня – 600 мг два раза в день, эффективной оказалась доза 1200 мг/сут. Согласно полученным данным, габапентин пролонгированного действия улучшает биодоступность активного вещества и поэтому снижает уровень отрицательных воздействий по сравнению с обычным габапентином.
В целом полученные доказательства весьма неоднозначны. В двух рандомизированных контролируемых исследованиях, посвященных габапентину пролонгированного действия, было показано преимущество препарата при применении дважды в день (600 мг утром и 1200 мг на ночь) по сравнению с однократным приемом дозы 1800 мг и плацебо для уменьшения интенсивности и специфического характера боли (Irving et al., 2009; Jensen et al., 2009). Однако в другом испытании габапентин замедленного высвобождения в дозе 1800 мг/сут не продемонстрировал превосходства по сравнению с плацебо (Wallace, 2010).
Прегабалин также утвержден FDA для лечения ПГН. Эффективный диапазон дозы составляет 150-600 мг/сут. По сравнению с плацебо прегабалин обеспечивал более высокий уровень облегчения боли и улучшал показатели сна у 776 пациентов с ПГН (Frampton, 2005). Нежелательные эффекты включают увеличение массы тела, головокружение и сонливость. Необходимо медленно титровать дозу препарата у лиц пожилого возраста.
Другие антиконвульсанты – блокаторы натриевых каналов, такие как топирамат, ламотриджин, карбамазепин, окскарабазепин, леветирацетам и вальпроевая кислота, не одобрены FDA при ПГН. Однако эти препараты могут быть вариантом выбора для пациентов с ПГН, у которых традиционная терапия оказалась неэффективной. В 8-недельном рандомизированном контролируемом исследовании пациенты в качестве лечения получали дивалпроекс натрия (вальпроевая кислота и вальпроат натрия) по 1000 мг/сут. В результате отмечалось значительное облегчение боли по сравнению с плацебо (Kochar et al., 2005). Среди побочных явлений могут иметь место головокружение, выпадение волос, головная боль, тошнота и диарея.
ТЦА, такие как амитриптилин, дезипрамин и нортриптилин ингибируют захват норадреналина и серотонина, а также блокируют натриевые каналы; возможно, существует другой, неизвестный пока, механизм их действия. Несмотря на то, что амитриптилин – наиболее изученный ТЦА при ПГН, имеющиеся доказательства и клинический опыт предполагают, что нортриптилин и дезипрамин обладают сопоставимой эффективностью и лучше переносятся (Watson, 1998; Dworkin et al., 2007).
Нортриптилин и дезипрамин рекомендуется принимать лицам с ослабленным иммунитетом и пожилым пациентам. Терапию целесообразно начинать с 10-25 мг/сут вечером, титруя в зависимости от переносимости каждые две недели до 75-150 мг/сут. Нежелательные эффекты включают сухость во рту, усталость, головокружение, седативное действие, задержку мочеиспускания, ортостатическую гипотензию, увеличение массы тела, нарушение зрения, удлинение интервала QT, запор и половую дисфункцию.
Что касается применения селективных ингибиторов обратного захвата серотонина и норадреналина (СИОЗСН), у пациентов с ПГН используют дулоксетин и венлафаксин в связи с их доказанной эффективностью в лечении диабетической нейропатии и других нейропатических болевых состояний. Дулоксентин назначают в дозе 60-120 мг/сут в два приема в случае отсутствия ответа на ТЦА или их непереносимости. В 12-недельных двойных слепых рандомизированных контролируемых плацебо исследованиях (2011) изучали прием дулоксетина по 60 мг/сут и 60 мг два раза в день для лечения диабетической периферической нейропатии. Были сделаны выводы, что доза 120 мг была безопасной и эффективной, однако не так хорошо переносилась, как 60 мг/сут.
Необходимо периодически исследовать функции печени у больных, применяющих дулоксетин. При назначении венлафаксина рекомендуемая доза составляет 75-225 мг/сут (Rowbotham et al., 2004).
Опиоидные анальгетики рекомендуются как препараты второй и третьей линии при ПГН. Побочные реакции включают тошноту, зуд, седативный эффект, спутанность сознания, запор, гипогонадизм, а также риск развития толерантности и привыкания.
В двойном слепом перекрестном исследовании оценивали болеутоляющую эффективность орального оксикодона. Лечение привело к значительному снижению аллодинии, стойкости болевого синдрома и спонтанной пароксизмальной боли. Использование оксикодона показало хорошие результаты в общей эффективности и снижении инвалидизации по сравнению с плацебо (Watson, Babul, 1998).
В рандомизированном перекрестном испытании комбинация габапентина и морфина превосходила любое из лекарственных средств относительно избавления от боли при ПГН (Gilron et al., 2005).
Атипичный опиоид трамадол обладает слабым эффектом агониста ?-опиоидных рецепторов и ингибирует обратный захват серотонина и норадреналина. Необходимо избегать его применения у больных с припадками судорог в анамнезе. Рекомендуемая максимальная доза составляет 400 мг/сут. Также можно использовать трамадол пролонгированного действия. В рандомизированном контролируемом плацебо исследовании трамадол обеспечивал превосходящее облегчение боли и улучшал качество жизни у пациентов с ПГН (Boureau et al., 2003).
Тапентадол – слабый агонист ?-опиоидных рецепторов; ингибирование обратного захвата норадреналина более выражено, чем ингибирование обратного захвата серотонина. Это лекарственное средство также доступно в форме замедленного высвобождения. Рекомендуемая максимальная доза составляет 600 мг/сут.
Местное лечение препаратами при ПГН связано с относительно меньшим количеством побочных явлений в сравнении со средствами, которые применяются перорально, поскольку их системная абсорбция минимальна.
Лидокаин доступен в виде трансдермального пластыря и местной гелеобразной мази. FDA одобрило применение пластыря с 5%-ным лидокаином для терапии ПГН. Лидокаин, блокатор натриевых каналов, можно использовать для лечения пациентов с клиническими признаками аллодинии. Пластырь можно разрезать, чтобы форма соответствовала зоне поражения; максимально возможно применять три пластыря одновременно в течение 12 часов, затем необходим 12-часовой перерыв. В случае эффективности пластырь можно оставить до 18 часов (Hermann et al., 2005).
В двух открытых нерандомизированных проспективных исследованиях у пациентов, которые применяли лидокаин в виде пластыря, уменьшилась интенсивность боли и улучшилось качество жизни.
Если по какой-то причине нет возможности приобрести пластырь лидокаина или есть трудности при его использовании, рекомендуется 5%-ный гель лидокаина.
Крем местного применения, содержащий капсаицин, выпускается в двух концентрациях: 0,025 и 0,075%. Активное вещество красного перца чили капсаицин действует как агонист ванилоидных рецепторов. Рекомендуемая дозировка – 3-4 раза в день. Начальное применение вызывает жжение, которое усиливается, однако повторное приводит к уменьшению боли и гипералгезии. В 6-недельном слепом параллельном исследовании, сопровождаемом 2-летним открытым последовательным испытанием, было показано, что при местном использовании крема с капсацином в концентрации 0,075% боль снижалась у 64% пациентов, тогда как при приеме плацебо – у 25% (таблица) (Watson et al., 1993).
 |
Исследователи рассмотрели несколько интервенционных методов терапии ПГН в случае резистентности к медикаментозному лечению. Ретроспективные испытания показали, что блокада симпатических узлов обеспечивает краткосрочное уменьшение боли у 40-50% пациентов с ПГН. Кроме того, межреберная нервная блокада обеспечивала длительное облегчение боли у лиц с грудной ПГН (Doi et al., 2002). Введение метилпреднизолона нейроаксиально интратекально оправдано у пациентов с тяжелой ПГН, поскольку представляет высокий риск неврологических осложнений. В клинической практике это вмешательство не рекомендуется (Kotani et al., 2000). Стимуляцию спинного мозга изучали проспективно в описании серии случаев 28 пациентов (Harke et al., 2002). Долгосрочное облегчение боли наблюдалось в 82% случаев. Стимуляцию спинного мозга у лиц с длительно сохраняющейся ПГН следует рассматривать при резистентности к обычному лечению. При применении криотерапии в случае лицевой боли при невралгии существенного эффекта не отмечено (Barnard, 1981). В других испытаниях наблюдалось краткосрочное действие метода у 11 из 14 пациентов, которые подверглись криотерапии межреберных нервов при грудной форме ПГН (Jones, 1987).
Результаты использования инъекций ботулинического токсина типа А представлены на собрании Американской академии лечения боли (2010). Было описано, что подкожная инъекция ботулинического токсина типа А уменьшала боль у лиц с ПГН по сравнению с инъекциями лидокаина и плацебо. Облегчение боли отмечалось через 1 неделю и сохранялось в течение 90 дней (Xiao, Hui, 2010).
Для лечения ПГН было описано и использовано множество хирургических вмешательств, однако ни один не рекомендуется применять в клинической практике.
Профилактика опоясывающего герпеса и ПГН
Очевидно, предотвращение ПГН связано с предупреждением опоясывающего лишая. Известно несколько способов предотвращения последнего:
- прививание детей вакциной против ветряной оспы, чтобы предотвратить первичную инфекцию (Marin et al., 2007);
- использование иммуноглобулинов Varicella zoster рекомендовано Консультативным комитетом по проблемам вакцинации (ACIP) у лиц с ослабленным иммунитетом, а также у серонегативных пациентов, которые недавно контактировали с больным ветрянкой или опоясывающим лишаем;
- назначение вакцины против опоясывающего лишая пациентам в возрасте старше 60 лет (Harpaz et al., 2008); FDA одобрило ее использование лицам в возрасте 50-59 лет, но ACIP не изменил свои рекомендации (Centers for Disease Control and Prevention, 2011).
На сегодняшний день есть возможность снизить заболеваемость опоясывающим лишаем и ПГН, так же как и более эффективно лечить постгерпетическую боль. Достижения последних лет включают разработку вакцины против опоясывающего лишая, а также консенсус о том, что противовирусная терапия и агрессивное лечение боли могут уменьшить тяжесть ПГН.
Помимо этого, важными являются идентификация эффективных методов лечения ПГН и признание ПГН в качестве модели для исследования нейропатической боли.
Подготовила Ярина Шутко
Читайте также:


