Ифа тест система корь

Иммуноферментный анализ (ИФА) — метод лабораторной диагностики, позволяющий обнаруживать специфические антитела и антигены при самых разных патологиях.
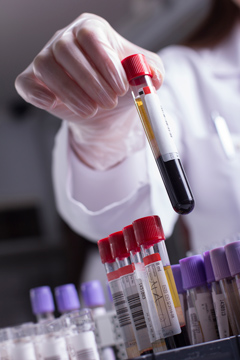
ИФА — один из самых распространенных и точных методов для выявления инфекций, передающихся половым путем, в частности ВИЧ, ВПЧ, гепатита В.

Для того чтобы результаты анализов были максимально достоверными, необходимо правильно подготовиться к их сдаче.

Спецпредложения, скидки и акции помогут существенно сэкономить на медицинском обследовании.
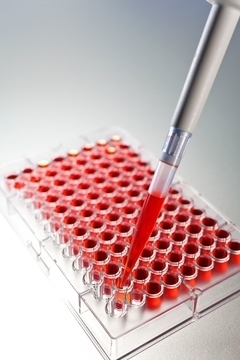
Контроль качества лабораторных исследований, осуществляемый по международным стандартам, — дополнительная гарантия точности результатов анализов.
Современная диагностика в медицине немыслима без высокочувствительных лабораторных анализов. Прежде для установления причин тех или иных симптомов врачи были вынуждены ориентироваться на косвенные признаки болезни, а также проводить многоступенчатые микроскопические исследования в попытке обнаружить возбудителя инфекции. Сегодня достаточно одного-единственного теста — такого как иммуноферментный анализ — чтобы подтвердить или опровергнуть первоначальный диагноз.
Основные понятия и принцип метода иммуноферментного анализа
Существует несколько разновидностей антител, каждая из которых вступает в действие на определенном этапе иммунного ответа. Так, первыми в ответ на проникновение антигена в организм синтезируются иммуноглобулины класса М (IgM). Содержание этих антител наиболее высоко в первые дни инфекционного процесса.
Следом за ними иммунная система выбрасывает в кровь иммуноглобулины класса G (IgG), которые помогают уничтожать антигены до полной победы над инфекцией, а также продолжают циркулировать по сосудам в дальнейшем, обеспечивая иммунитет к повторному заражению. На этом явлении основана вакцинация: благодаря прививкам, содержащим ослабленные антигены микробов и вирусов, в нашей крови появляется большое количество IgG, которые при контакте с реальной угрозой быстро подавляют инфекцию — до того, как она нанесет вред здоровью.
Как узнать, какие именно антигены или антитела присутствуют в организме человека? Когда врач предполагает, что причиной заболевания является определенная инфекция, или желает измерить концентрацию определенного гормона, он назначает пациенту иммуноферментный анализ.
ИФА бывает качественным и количественным. В первом случае подразумевается однозначный ответ: искомое вещество или найдено, или не найдено в образце. В случае с количественным анализом более сложная цепь реакций дает возможность оценить концентрацию антител в крови человека, что в сравнении с результатами предыдущих тестов даст ответ на вопрос о том, как развивается инфекционный процесс.
Бесспорные преимущества ИФА — высокая чувствительность и специфичность метода. Чувствительность — это возможность распознать искомое вещество, даже если его концентрация в образце невысока. Специфичность же подразумевает безошибочность диагностики: если результат положительный, значит, найдены именно те антитело или антиген, которые предполагались, а не какие-то другие.
Высокая степень технологичности проведения иммуноферментного анализа минимизирует влияние человеческого фактора, что снижает вероятность ошибки. Большинство используемых в современных лабораториях тест-систем и реактивов для ИФА выпускаются в промышленных условиях, что гарантирует точный результат.
В случае диагностики инфекционных заболеваний иммуноферментный анализ не может найти возбудителя и определить его специфичные свойства: он лишь указывает на наличие антител в крови у больного, косвенно свидетельствующих о присутствии чужеродного микроорганизма в теле человека.
ИФА — крайне точный, но не дешевый метод, поэтому обращаться к нему нужно с умом, а интерпретацией результатов должен заниматься квалифицированный врач.
Невозможно охватить полный список показаний к проведению ИФА. Вот наиболее распространенные цели анализа:
- Диагностика острых и хронических инфекционных заболеваний:
- IgM и IgG к вирусным гепатитам А, B, C, E, а также антигенов гепатитов В и С;
- IgG к ВИЧ;
- Ig M и IgG к цитомегаловирусной инфекции;
- Ig M и IgG к вирусу Эпштейна-Барр;
- Ig M и IgG к герпетическим инфекциям;
- Ig M и IgG к токсоплазмозу;
- Ig M и IgG к кори, краснухе, сальмонеллезу, дизентерии, клещевому энцефалиту и другим заболеваниям;
- IgG к паразитарным заболеваниям;
- Ig M и IgG к инфекциям, передающимся половым путем;
- IgG к хеликобактерной инфекции.
- Общая оценка показателей иммунитета человека и маркёров некоторых аутоиммунных заболеваний.
- Выявление онкологических маркёров (фактора некроза опухоли, простатспецифического антигена, раково-эмбрионального антигена и других).
- Определение содержания гормонов в сыворотке крови (прогестерона, пролактина, тестостерона, тиреотропного гормона и других).
Основной биоматериал для проведения ИФА — это сыворотка крови: в лаборатории у пациента берут образец крови из вены, из которого в дальнейшем удаляют форменные элементы, затрудняющие проведение анализа. В некоторых других случаях для анализа используется спинномозговая жидкость, околоплодные воды, мазки слизистых оболочек и т.д.
Для того чтобы избежать искажений в результатах, рекомендуется сдавать кровь натощак, а за две недели до исследования (если целью является диагностика хронических, скрыто протекающих инфекционных заболеваний) необходимо отказаться от приема антибиотиков и противовирусных препаратов.
При наличии необходимых реактивов и хорошей организации работы лаборатории результат анализа вы получите в течение 1–2 суток после забора крови. В некоторых случаях, при необходимости получения экстренного ответа, этот срок может быть сокращен до 2–3 часов.
- IgM — наличие этого класса иммуноглобулинов говорит об остром инфекционном процессе в организме. Отсутствие IgM может говорить как об отсутствии конкретного возбудителя в организме, так и о переходе инфекции в хроническую стадию.
- IgA при отрицательном результате теста на IgM чаще всего свидетельствует о хронической или скрыто протекающей инфекции.
- IgM и IgA (совместное присутствие) — два положительных результата говорят о разгаре острой фазы заболевания.
- IgG говорит либо о хронизации заболевания либо о выздоровлении и выработке иммунитета к инфекционному агенту.
В зависимости от содержания анализа в бланке могут быть представлены данные в виде таблицы с перечислением всех антител или антигенов с пометками об отрицательной или положительной реакции, либо будет указано количественное значение результата (отрицательный, слабоположительный, положительный или резко положительный). Последний вариант определяет, сколько антител содержится в анализируемом образце.
Еще один количественный показатель — индекс авидности антител, выраженный в процентах. Он указывает, сколько времени прошло от начала инфекционного процесса (чем выше индекс — тем больше).
Сегодня выпускаются тысячи видов тест-систем ИФА, позволяющих обнаруживать специфические антитела и антигены при самых разных патологиях. Поэтому этот анализ используется практически во всех медицинских отраслях. Диагноз, поставленный с помощью ИФА, — это гарантия назначения адекватной терапии и эффективного лечения заболевания.
Информативность ИФА делает этот анализ важным инструментом в работе многих медицинских центров. Но можно ли доверять такую диагностику государственным лабораториям или лучше самим выбрать, где провести такое исследование?
В последние годы обострилась эпидемиологическая обстановка, связанная с заболеваемостью корью. Это вызвано резким ростом числа заболевших в странах Европы, повлекшим за собой увеличение числа случаев завоза инфекции в Российскую Федерацию, а также наличием большой доли невакцинированных лиц или лиц с недостаточной иммунной защитой среди населения России, в первую очередь среди детей и молодежи. Заболеваемость корью в 2011 году в 5 раз превысила аналогичный показатель 2010 года. В 2011 году в РФ было зарегистрировано более 600 случаев заболевания, в январе 2012 года - еще 500 случаев. Число регионов, в которых выявлены новые случаи, постоянно растет. С января текущего года случаи заражения зарегистрированы в 47 субъектах РФ, в числе лидеров по распространению заболевания оказались Санкт-Петербург, Москва, Волгоградская, Белгородская и Московская области, Ставропольский край.
В соответствии с Санитарными правилами СП 3.1.2952-11 "Профилактика кори, краснухи и эпидемического паротита" для установления окончательного диагноза необходимо обязательное лабораторное подтверждение клинических данных. Для этого используют серологическое исследование: определение специфических антител классов IgM и IgG методом иммуноферментного анализа (ИФА). Наличие антител класса IgM является серологическим маркером острой инфекции. Согласно Санитарным правилам, положительный результат анализа на IgM должен быть подтвержден выявлением и увеличением концентрации (титра) антител класса IgG в парных образцах.
Быстрое распространение инфекции свидетельствует о недостаточном уровне защищенности населения и необходимости дополнительной вакцинации. Серологические исследования - определение антител класса IgG - необходимы как для выявления лиц, которым требуется вакцинация (отсутствие или низкий титр IgG), так и для оценки ее эффективности (концентрация IgG превышает определенный пороговый уровень).
ЗАО "Аналитика" предлагает применять ИФА-наборы производства компании "Euroimmun" (Германия) для выявления специфических антител класса IgG и IgM к вирусу кори. В наборе Anti-Measles Virus NP ELISA (IgM) в качестве антигена используется высокоочищенный рекомбинантный нуклеопротеин вируса, экспрессированный в клетках эукариот. Благодаря этой уникальной технологии достигается высокая специфичность определения IgM-антител, существенно превышающая специфичность наборов предыдущего поколения, основанных на использовании вирусного лизата. Набор Anti-Measles Virus ELISA (IgG) предназначен для количественного определения IgG-антител, необходимого как для диагностики заболевания, так и для оценки напряженности иммунной защиты. Результат анализа выражается в стандартизованных международных единицах, что позволяет достоверно определять содержание антител без дополнительной процедуры титрования исследуемых сывороток. Это экономит реагенты, время, снижает риск ошибок, более удобно при использовании автоматических анализаторов. ИФА-наборы компании "Euroimmun" особо отличаются стандартностью методики, взаимозаменяемостью реагентов, простотой и четкостью интерпретации результатов.
Набор Avidity: Anti-Measles Virus ELISA (IgG) предназначен для выявления низкоавидных IgG-антител, как правило, появляющихся в начальной стадии инфекции, и используется для дополнительного анализа, если определение антител класса IgM дало неоднозначный результат. Если необходимо, этот набор может использоваться и как обычный тест для определения IgG-антител. Среди тест-систем, применяемых в России, набор не имеет аналогов.
ЗАО "Аналитика" также предлагает уникальный ИФА-набор CSF: Anti-Measles Virus ELISA (IgG), предназначенный для выявления специфических IgG-антител в парных образцах сыворотки и спинномозговой жидкости. Этот набор позволяет оценить уровень внутричерепного синтеза специфических антител, сопровождающего проникновение вируса в ЦНС, что очень важно для диагностики коревых энцефалитов и других неврологических проявлений инфекции.
Все тест-системы зарегистрированы в Росздравнадзоре (РУ № ФСЗ 2010/07291 от 30.06.2010). Применение предлагаемых наборов возможно в иммунологических лабораториях больниц с инфекционными отделениями и профильных лабораториях системы Роспотребнадзора.
Информация для заказа:
[ EI2610-9601G ] Anti-Measles Virus ELISA (IgG), количественное определение IgG-антител, 96 тестов;
[ EI2610-9601-4M ] Anti-Measles Virus ELISA (IgM), полуколичественное определение IgM-антител, 96 тестов;
[ EI2610-9601-1G ] Avidity: Anti-Measles Virus ELISA (IgG), определение низкоавидных IgG-антител, 96 тестов;
[ EI2610-9601-LG ] CSF: Anti-Measles Virus ELISA (IgG), определение IgG-антител в ликворе, 96 тестов.

Корь — острое контагиозное заболевание, возбудитель которого — парамиксовирус рода Morbillivirus Polinosa morbillarum. Корь передаётся воздушным, воздушно-капельным и непрямым путём через предметы, контаминированные вирусом.
Заражаемость корью при контакте с заболевшим человеком или контаминированными предметами составляет около 100 %, поэтому самый эффективный способ профилактики — вакцинация.

Инфицированию подвержены люди всех возрастов, у которых нет стойкого иммунитета к вирусу. Они могут заболеть типичной или атипичной корью:
стёртой, митигированной — со слабо выраженными симптомами и нарушенным порядком их появления;
атипичной с аггравированными симптомами — гипертоксической (предельно выражена интоксикация), геморрагической (с экстравазатами в коже, содержащим кровь стулом, гематурией).
Инфекция опасна осложнениями (особенно у взрослых), развивающимися на её фоне и как следствие заболевания: отёком мозга (коревой энцефалит), менингитом (редко), слепотой, тяжёлой диареей с дегидратацией, ларингитом, отитом, крупом, пневмонией, лимфаденитом, гепатитом.
Именно они способны привести к летальному исходу, если не проводить эффективную сопутствующую терапию при первых признаках вторичного поражения. Осложнения чаще всего возникают у детей до 1—3 лет и взрослых старше 30 лет, в условиях недостаточной медицинской помощи, плохого питания, недостатка витамина А, ослабленного иммунитета, например, у ВИЧ-инфицированных.
После перенесённой кори часто наблюдается длительная астения, которая проходит без последствий при щадящем режиме учёбы, работы, полноценном питании, отдыхе.
Симптомы кори
Для течения болезни характерны общая интоксикация, лихорадка (гипертермия), сыпь на слизистых, макулопапулёзная сыпь (плоские и бугорковые высыпания на коже). Всё названное проявляется на разных стадиях заболевания, одновременно или последовательно.
Вирус атакует организм через слизистые глаз и дыхательных путей. В подслизистой, лимфоузлах происходит первичная репликация (создание копий вируса), после чего парамиксовирус попадает в кровь.
У кори довольно долгий период инкубации — до 14 (при стёртых формах до 27) суток. Он протекает бессимптомно. Первый признак заражения — высокая температура до 40 °C спустя 9—12 дней после заражения. Появляются насморк и кашель (сухой, иногда удушающий), глаза краснеют и слезятся, больно смотреть на свет (фотофобия, воспаление конъюнктивы), часто болит голова, а на слизистой щёк, напротив верхних маляров, выступают мелкие беловатые пятна с красным венчиком.

Затем, через 1—2 дня, лицо, заушные области, верхняя часть шеи покрывается сыпью — это стадия разгара. Примерно через 3 дня сыпь обнаруживается по всему телу и держится около недели. Коревая сыпь склонна к слиянию, чем отличается от краснушной сыпи.
При излечении сыпь исчезает через 6—7 дней, оставляя коричневые депигментированные участки — они исчезают ещё через 6—10 дней. Температура понижается до нормальной на 4—5-й день после появления высыпаний. Более долгий период лихорадки свидетельствует об осложнениях, потому нужно незамедлительно пройти новые исследования.
Источники инфекции, механизмы передачи
Заразиться корью воздушно-капельным путём от больного человека или предметов, с которыми он контактировал, можно с вероятностью до 100 %. Вирус мигрирует по воздуху в шахтах лифтов, в помещениях с кондиционерами, с иными источниками движения воздуха.
Вне носителя — в воздухе и на поверхностях — при комнатной температуре возбудитель активен в среднем 24 часа, при -20 °C — в течение 12 месяцев, при +37 °C — 2 часа, при +58 °C погибает мгновенно. От носителя он передаётся в период за 4 дня до кожных высыпаний и спустя 4 дня после того, как сыпь появилась.
Исследуемый материал для диагностики
Строгое доказательство поражения парамиксовирусом — серологическое подтверждение нахождения его в человеческом организме или собственно выделение парамиксовируса.
Серологическое подтверждение заключается в обнаружении специфических антител (класс М) или увеличении в сыворотке крови титра антител класса G (иммуноглобулины IgM и IgG).
Первым вырабатывается IgM, а через 3—4 недели после инфицирования — IgG, который сохраняется десятилетиями, надёжно защищая организм при новом заражении, и передаётся от матери к ребёнку через плаценту, сохраняясь у малыша до 6—7 месяцев.

Обычно корь довольно точно диагностируют по внешним клиническим признакам. Сложность вызывает диагноз митигированной кори — лёгкой формы заболевания, при который сыпь слабая, как и прочая симптоматика. Такая форма встречается у людей с активной или пассивной (перенесённое заболевание) иммунизацией, у грудничков, получивших антитела от матери плацентарно.
венозную кровь — в ней выявляют антитела;
назофарингиальные смывы, лимфоциты периферической крови (венозная кровь), мочу — для обнаружения собственно вируса кори;
мазки из носоглотки/ротоглотки — в них обнаруживают РНК (рибонуклеиновую кислоту) парамиксовируса.
Методы диагностики кори
РСК — реакция связывания комплемента: к исследуемой сыворотке крови добавляют антиген, затем к их иммунному комплексу (если он возникает) — стандартный комплемент, далее проводят инкубацию в течение 60 минут при температуре +37 °C. Далее определяют результаты с помощью индикаторной гемолитической системы. Если в сыворотке нет специфических антител, комплемент будет несвязанным.
РТГА — реакция торможения гемагглютинации: метод основан на подавлении антигенов вируса иммунной сывороткой, вследствие чего вирус не может агглютинировать (склеивать) эритроциты.
РИФ — реакция иммунофлюоресценции: метод основан на способности антигенов микробов светиться в ультрафиолетовых лучах, если микробы обработать иммунной сывороткой с антителами, которые мечены флюорохромами. Для реакции используют секрет дыхательных путей или мочу.

Все перечисленные методы имеют некоторые трудности в определении антител: это или большая доля ложноположительных реакций (что предусматривает повторные анализы и траты жизненно важного времени), или высокая стоимость технологии, или определённая неточность в анализе, вызванная визуальным учётом результатов.
Метод ИФА характеризуется высокой чувствительностью к антителам, стабильностью результатов и доступной стоимостью, потому используется в большинстве стран мира.
Ранняя ИФА-диагностика кори основана на выявлении антител IgM в сыворотке крови. Анализ особенно эффективен в период между 4-м и 28-м днём после того, как проявилась сыпь.
Примерно через 10—14 дней после первого анализа проводят второй — уже на присутствие и устойчивый рост титра антител IgG. Рост титра более чем в 4 раза — строгое основание для положительного диагноза кори.
Метод полимеразной цепной реакции с обратной транскрипцией относится к молекулярно-биологическим. Его ценность — в максимально раннем диагностировании кори, а условный недостаток — в необходимости дорогостоящего специального оборудования и обученного методу персонала.
ОТ-ПЦР основана на том, что вирус кори относится к РНК-содержащим. Реакция позволяет обнаружить молекулы РНК в биологическом образце. Метод относится к особо чувствительным, потому что обнаруживает даже минимальное количество молекул рибонуклеиновой кислоты.
Лечение и профилактика
Для кори нет специфической терапии. Выхаживание больных обычно проходит в домашних условиях и заключается в уходе, гигиенических процедурах, хорошем питании и устранении дегидратации приёмом оральных регидратационных растворов. Терапевтическая диета предусматривает молочно-растительный рацион в лихорадочный период и полноценное, богатое витаминами питание после нормализации температуры.

Детям с поставленным диагнозом назначают повышенные дозы витамина А. Хорошее питание и витамин А помогают снизить на 50 % вероятность слепоты и летальных исходов заболевания.
Сопутствующее лечение, госпитализация необходимы при тяжёлом течении болезни, при осложнениях. Вторичные инфекции — глазные, ушные — и пневмонию лечат антибиотиками. Специфической терапии для коревого энцефалита не существует, лечение заключается в назначении антигистаминных средств и глюкокортикоидных гормонов.
Если у больного выраженное психомоторное возбуждение, осторожно применяют психотропные препараты, при судорогах — противосудорожные.
Эффективная профилактика заключается только в иммунизации коревой вакциной. Чтобы предотвратить эпидемию или просто большое число заболевших, нужно своевременно выявлять и изолировать инфицированных.
Специальная дезинфекция помещений не является профилактическим средством, т. к. вирус крайне нестоек при обычной комнатной температуре.
Противокоревая иммунизация детей и взрослых

Вакцинация от кори чрезвычайно эффективна: 97 % вакцинированных не заболевают корью никогда. Настолько же, но с обратным результатом, эффективен отказ от вакцинации — при первом же контакте с заболевшим невакцинированный человек имеет почти 100-процентный шанс заразиться корью.
В 2017 году от кори умерли более 100 тысяч людей — детей и взрослых — во всём мире.
Всего за 10 лет — с 2000 по 2017 год — иммунизация снизила количество летальных исходов заболевания на 80 % и предотвратила более 20 миллионов смертей.
Противокоревая вакцина очень эффективна, безопасна. Часто её объединяют с вакцинами от краснухи, свинки (паротита), ветряной оспы, что нисколько не снижает эффективность и безопасность прививок.
Национальный календарь вакцинации предусматривает 2 этапа иммунизации детей:
· в 12 месяцев — когда иммунитет, переданный младенцу от матери, исчезает;
· в 6 лет — когда ребёнок идёт в школу.
Если по каким-то причинам прививки не были сделаны, вакцинируют подростков в 15—17 лет и взрослых до 35 лет. Вакцинация проводится также в 2 этапа с перерывом в 3 месяца.
После 35 лет человек может вакцинироваться по собственному желанию и уже за свой счёт. Это ограничение не действует для тех, кто в детстве не прошёл иммунизацию (лил вакцинировался однократно), никогда не болел корью или проконтактировал с инфицированным.
Противопоказания к иммунизации
Временные:
· заболевания в острой форме (инфекции и не-инфекции), в том числе — хронические. При хронических заболеваниях прививку о кори делают в период ремиссии;
Постоянные:
тяжёлая аллергия на аминогликозиды;
злокачественные новообразования и злокачественные патологии крови;
выраженная реакция на противокоревую вакцину: повышение температуры до 40 градусов и выше, отёк диаметром более 8 см в месте инъекции.
Людям с ВИЧ-инфекцией вакцинация не противопоказана.
Не рассматривают врачи всего мира как противопоказание и аллергию на куриный/перепелиный белок, если аллергия не приводит к анафилактическому шоку, отёку Квинке, генерализованной крапивнице.
В таком случае вакцинацию рекомендуют провести в любом возрасте.
Если прививка делалась, но о ней забыли, повторная иммунизация не нанесёт никакого вреда здоровью, зато обеспечит безопасность и душевный покой.
Лабораторная диагностика кори в Северо-Западном центре доказательной медицины
В наших лабораториях анализы выполняются на современном оборудовании специалистами, прошедшими специальную подготовку для проведения сложных исследований.
Вы получите точный результат быстро и сможете своевременно начать лечение, что значительно повысит его эффективность.
Будьте здоровы и берегите себя!
Лаборатория АО "СЗЦДМ" предлагает услуги, обеспечивающие комплексное и преемственное лабораторное обследование пациента
Диагностика В медицинских центрах АО "СЗЦДМ" проводят качественные диагностические исследования всего организма
Лечение Наши медицинские центры ориентированы на обслуживание пациентов в амбулаторном режиме и объединены единым подходом к обследованию и лечению пациентов.
Реабилитация Реабилитация - это действия, направленные на всестороннюю помощь больному человеку или инвалиду для достижения им максимально возможной полноценности, в том числе и социальной или экономической.
Выезд на дом Внимание! Действует акция "Выезд на дом - 0 рублей"
Профосмотры АО "СЗЦДМ" проводит профилактические осмотры работников, которые включают в себя - комплексы лечебных и профилактических мероприятий, проводимых для выявления отклонений в состоянии здоровья, профилактики развития и распространения заболеваний.
| Классы МПК: | A61K39/165 вирус свинки или вирус кори C12N7/00 Вирусы, например бактериофаги; их композиции; приготовление или очистка их G01N33/535 с ферментными метками | ||||||||||||||||||||||||||||||||||||||||||||||||
| Автор(ы): | Пьянков Степан Александрович (RU) , Агафонов Александр Петрович (RU) , Лебедев Леонид Рудольфович (RU) , Шиков Андрей Николаевич (RU) , Демина Ольга Константиновна (RU) , Дроздов Илья Геннадиевич (RU) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Патентообладатель(и): | Федеральное государственное учреждение науки "Государственный научный центр вирусологии и биотехнологии "Вектор" Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФГУН ГНЦ ВБ "Вектор" Роспотребнадзора) (RU) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Приоритеты: |
| Таблица 3 | |||
| Результаты ИФА при постановке положительного и отрицательного образцов с применением иммуносорбента, изготовленного на основе разных фракций хроматографической очистки комплексного антигена | |||
| Концентрация NaCl для элюции фракции антигена с колонки | О.П. положительного образца | О.П. отрицательного образца | ОП(+)/ОП(-) |
| Несорбирующаяся фракция (проскок) | 0,117 | 0,256 | 0,5 |
| 0,1 М NaCl | 0,075 | 0,179 | 0,4 |
| 0,2 М NaCl | 0,187 | 0,120 | 1,6 |
| 0,3 М NaCl | 1,459 | 0,121 | 12,1 |
| 0,4 М NaCl | 2,453 | 0,163 | 16.2 |
| 0,5 М NaCl | 1,469 | 0,204 | 7,2 |
| 0,7 М NaCl | 0,552 | 0,192 | 2,9 |
| 1 М NaCl | 0,340 | 0,184 | 1,8 |
Выход высокоочищенного комплексного антигена с 3 л КВЖ и лизата клеток составляет 15-20 мг.
Пример 4. Изготовление иммуносорбента
Иммуносорбент готовят добавлением 0,20±0,06 мл комплексного антигена вируса кори после очистки на колонке (см. Пример 3) к 1,00±0,01 л р-ра для сорбции. Состав р-ра для сорбции: 2,00±0,01 г натрия углекислого, 0,50±0,01 г натрия азида, 0,400±0,012 мл 2% фенолфталеина, вода очищенная - до 1 литра. Иммуносорбент перемешивают на магнитной мешалке в течение 1 ч при температуре от 18°С до 24°С.
Пример 5. Методика применения набора реагентов для одностадийного ИФА "Анти-корь Ig Трисорбент"
Для проведения анализа используется сыворотка или плазма крови человека. Для проведения анализа достаточно 10 мкл образца. Для выявления антител класса G к вирусу кори можно использовать сыворотку (плазму) крови человека как свежеприготовленную, так и хранившуюся не более 7 суток при температуре от 2°С до 8°С при условии отсутствия микробной контаминации либо не более 12 месяцев при температуре минус 20°С. Допускается замораживание сыворотки (плазмы) до температуры минус 20°С не более двух раз.
Для проведения реакции во все лунки планшета вносят по 90 мкл р-ра для разведения образца (состав: 2,00±0,01 г натрия углекислого, 0,50±0,01 г натрия азида, 0,400±0,012 мл 2% фенолфталеина, вода очищенная - до 1 литра). В лунку планшета А1 вносят 10 мкл К1+, в лунки В1 и С1 вносят по 10 мкл К2+. В лунку D1 вносят 10 мкл К-. В остальные лунки планшета вносят по 10 мкл исследуемых сывороток (конечное разведение контрольных и исследуемых образцов - 10 раз). Раствор перемешивают пипетированием и инкубируют в течение 40 мин при температуре 37°С. По окончании инкубации содержимое лунок удаляют и планшет промывают семь раз рабочим раствором ФСБ-Т. В каждую лунку вносят по 100 мкл р-ра хромагена и планшет помещают на 15 мин в защищенное от света место при температуре 37°С. Реакцию останавливают внесением в каждую лунку планшета по 50 мкл стоп-реагента.
Величину ОП растворов в лунках иммуносорбента измеряют на спектрофотометре в двухволновом режиме: основной фильтр - 450 нм, референс-фильтр - в диапазоне от 620 до 700 нм. Результаты теста считают положительными, если ОП исследуемой сыворотки больше ОПК2+ср. (нижняя граница положительных значений соответствует 0,28 МЕ/мл). Результаты теста считают отрицательными, если ОП исследуемой сыворотки меньше ОПК2+ср. - 20% (верхняя граница отрицательных значений соответствует 0,12 МЕ/мл).
Псыв. рассчитывают по формуле:
где ОПсыв. - значение ОП исследуемой сыворотки.
Асыв. (титр антител в МЕ) рассчитывают по формуле:
где а и b - константы, специфичные для каждой серии (указаны в Инструкции, которая сопровождает каждый набор).
Пример расчета полученных данных приведен в таблице 4.
| Таблица 4 | |
| Пример расчета титра антител к вирусу кори в исследуемой сыворотке | |
| (ОПК1+ср.) - среднее значение ОП в лунках А1 и В1 | 2,919 - в диапазоне Приложения |
| (ОПК2+ср.) - среднее значение ОП в лунках С1 и D1 | (0,273+0,275):2=0,274 - в диапазоне Приложения |
| Нижняя граница положительных значений | >(ОПК2+ср.)=0,274 |
| Верхняя граница отрицательных значений | 0,168 =1,47 |
| Ответ: специфическая активность сыворотки 1,47 МЕ/мл |
В образцах больных методом ПЦР был обнаружен генетический материал (РНК) вируса кори. Секвенирование показало принадлежность вируса, вызвавшего вспышку, к генотипу Н.
ФОРМУЛА ИЗОБРЕТЕНИЯ
1. Комплексный антиген вируса кори, используемый в качестве компонента иммуноферментной тест-системы для диагностики антител к вирусу кори, полученный из культуральной жидкости, содержащей штаммы вируса кори Ленинград 16 с титром не менее 10 5.0 ТЦД 50 /мл, Эдмонстон - не менее 10 6.0 ТЦД 50 /мл, NovO/96 - не менее 10 8.0 ТЦД 50 /мл путем инактивации ее инфекционной активности детергентом и выделением белка из клеточного лизата хроматографической очисткой в количестве не менее 2 мкг/мл с чистотой не менее 70%.
2. Комплексный антиген по п.1, отличающийся тем, что культуральная вируссодержащая жидкость получена при раздельном культивировании указанных в п.1 штаммов вируса кори на монослое культуры клеток Vero с последующим смешением культуральных вируссодержащих жидкостей в соотношении 1:1:1 по объему.
Читайте также:
- Ингаляции при герпетической ангине у детей
- Секс не лишая девственности в месячные
- Что лучше от лабиального герпеса
- Эминем и кори тейлор
- Корь ребенок ничего не ест
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции

