Гризеофульвин лечение лишая у детей
Действующее вещество
Фармакологическая группа
Нозологическая классификация (МКБ-10)
Состав и форма выпуска
| Таблетки | 1 табл. |
| гризеофульвин | 125 мг |
в контурной ячейковой упаковке 10 шт.; в пачке картонной 2 упаковки
Описание лекарственной формы
Таблетки белого цвета с кремоватым оттенком, горьковатого вкуса, без запаха.
Фармакологическое действие
Противогрибковый антибиотик, эффективен в отношении грибов рода Trichophyton, Microsporum, Epidermophyton. Вызывает нарушение структуры митотического веретена и синтеза клеточной стенки у хитинсодержащих грибов, подавляет деление грибковых клеток в метафазе и синтез белка из-за нарушения связи с матричной РНК . Накапливается в клетках кожи, волос, ногтей. По мере отделения инфицированного кератина происходит замена его здоровой тканью.
Фармакокинетика
Абсорбция — высокая. Сmax — 0,5–5 мг/л, Тmax после приема внутрь — 4–5 ч. Связь с белками плазмы — 80%. Избирательно накапливается в роговом слое кожи и ее придатках, а также в печени, жировой клетчатке, скелетной мускулатуре. Незначительное количество распределяется в жидкостях и тканях организма. Проникает через плаценту. Метаболизируется в печени с образованием неактивных метаболитов (6-метилгризеофульвина и глюкуронидного производного). Т1/2 — 24 ч. Выводится почками ( в т.ч. 1% — в неизмененном виде) и через кишечник (36% — в неизмененном виде).
Показания препарата Гризеофульвин
Микозы кожи, волос, ногтей: трихофития, фавус, микроспория волосистой части головы, гладкой кожи, дерматомикоз бороды и усов, эпидермофития гладкой кожи, эпидермофития стоп, паховая эпидермофития, онихомикозы.
Противопоказания
Гиперчувствительность, порфирия, системная красная волчанка, волчаночноподобный синдром, системные заболевания крови, лейкопения, острые и подострые заболевания печени и почек с нарушением их функций, печеночная недостаточность, злокачественные новообразования, нарушения мозгового кровообращения, состояние после инсульта, маточные кровотечения, беременность, период грудного вскармливания, детский возраст (до 2 лет — эффективность и безопасность не изучены).
Применение при беременности и кормлении грудью
Побочные действия
Со стороны ЦНС : головная боль, головокружение, дезориентация, необычная утомляемость или слабость, бессонница, периферическая нейропатия, нарушение координации движений, парестезии конечностей, спутанность сознания.
Со стороны ЖКТ : тошнота, рвота, диарея, гастралгия, кандидозный стоматит, гепатит.
Со стороны органов кроветворения: гранулоцитопения, агранулоцитоз, лейкопения.
Аллергические реакции: крапивница, кожная сыпь, зуд, ангионевротический отек, фотосенсибилизация, волчаночноподобный синдром, мультиформная экссудативная эритема, синдром Лайелла.
Взаимодействие
Усиливает действие этанола. Снижает активность эстрогенсодержащих пероральных контрацептивов, антикоагулянтов непрямого действия (вследствие индукции микросомальных ферментов печени). Барбитураты и примидон уменьшают противогрибковую активность.
Способ применения и дозы
Внутрь, во время или после еды с растительным маслом. При микроспории детям назначают из расчета 21–22 мг на 1 кг массы тела больного в сутки, взрослым — от 500 до 1000 мг (8 табл. в сутки). Препарат принимают ежедневно до первого отрицательного анализа на грибы, затем в той же дозе через день в течение 2 нед и затем 2 раза в нед в течение 2 нед .
При трихофитии (поверхностная и инфильтративно-нагноительная формы) и фавусе детям — из расчета 18 мг/кг массы тела по той же схеме, что и при микроспории.
При онихомикозах, трихофитии и фавусе волосистой части головы суточная доза для взрослых массой тела до 50 кг составляет 625 мг (5 табл.) Максимальная суточная доза — 1 г (8 табл.). Суточная доза у детей и подростков — 16 мг/кг массы тела.
При онихомикозах препарат в течение первого мес назначают ежедневно, второго мес — через день, далее 2 раза в нед в той же суточной дозе до полного отрастания ногтей. Общая продолжительность лечения — не менее 8 мес.
Меры предосторожности
С осторожностью применять во время работы водителям транспортных средств и людям, профессия которых связана с повышенной концентрацией внимания.
Особые указания
Лечение проводят под контролем морфологического состава крови (1 раз в 10–15 дней).
В процессе лечения у больных микозами волосистой части головы необходимо еженедельно сбривать волосы, а голову мыть теплой водой с мылом 2 раза в нед . Рекомендуется втирать в кожу головы противогрибковые мази и смазывать очаги 2–3% настойкой йода.
При онихомикозах рекомендуется комбинировать назначение препарата с удалением пораженных ногтей с помощью кератолитических пластинок и местной противогрибковой терапии.
Производитель
Условия хранения препарата Гризеофульвин
Хранить в недоступном для детей месте.
Срок годности препарата Гризеофульвин
Не применять по истечении срока годности, указанного на упаковке.
- КЛЮЧЕВЫЕ СЛОВА: дерматомицеты, пробиотики, микоз, элиминация, гризеофульвин
Считается, что наиболее часто микроспорией страдают дети от шести до 14 лет, однако патология нередко встречается и у детей до года. У пациентов старше 15 лет доля поражения волосистой части головы снижается, но увеличивается процент поражения других волосистых зон. Речь, в частности, идет о пограничной зоне роста волос – зоне офиаза, зонах подбородка и лобка [1].
Системная терапия микозов волосистых участков кожи – одно из обязательных условий эффективности лечения, основной целью которого является быстрое и надежное купирование инфекционного процесса. Подавление размножения патогенного гриба и его своевременная элиминация позволяют избежать необратимых поражений аппарата волоса и восстановить его к моменту полного излечения [1, 3]. При микроспории продолжительность системной терапии обычно составляет шесть – восемь недель, при трихофитии – четыре – шесть (без учета времени на определение излеченности) [3–5].
На сегодняшний день для системной терапии микозов волосистой части головы показаны четыре основных вещества (молекулы). Первые два – ксенобиотики, искусственно синтезированные вещества. К таковым относятся флуконазол и итраконазол – соединения группы имидазола [3, 4, 6]. Два вторых представляют собой природные соединения, либо соединения, используемые в неизмененном виде (гризеофульвин), либо соединения, имеющие природные аналоги (тербинафин) [4].
Гризеофульвин – вещество, синтезируемое грибом Penicillium griseofulvum (P. nigricans). Гризеофульвин относится к группе гризанов. Его молекула имеет определенное сходство с молекулой пенициллина [3, 7].
Вещество было обнаружено в культуре гриба в 1938 г., однако только 20 лет назад начато его применение в медицинских целях.
Гризеофульвин является фунгистатиком. Его активность проявляется только в отношении дерматомицетов (дерматофитов).
Механизм действия указанного препарата связан с нарушением синтеза нуклеиновых кислот. Проникая в ядро клетки через микротубулярные структуры, гризеофульвин связывается с белками внутри ядерных канальцев и вызывает нарушение их проводящих функций. В результате нарушения транспорта различных метаболитов прекращается рост гриба и спорообразование, митоз останавливается на стадии метафазы, образуются многоядерные клетки. Изменения в клеточной стенке являются вторичными – в результате нарушения синтеза белка [7, 8].
Минимальная ингибирующая концентрация гризеофульвина для дерматомицетов – 0,1–0,5 мкг/мл [7, 8].
Помимо противогрибкового действия гризеофульвин обладает противовоспалительным, сосудорасширяющим и иммуносупрессивным свойствами, способен улучшать трофическую функцию периферических нервов.
Необходимо отметить, что в настоящее время область применения гризеофульвина постепенно сужается. Однако препарат по-прежнему занимает свою нишу в терапии микозов волосистых участков кожи у детей и подростков.
Схема применения препарата обусловлена его фармакокинетикой: концентрация вещества медленно снижается в течение 48 часов после приема и уже через 72 часа не определяется в роговом слое. Поэтому была рекомендована трехэтапная схема терапии. На первом (основном) этапе гризеофульвин принимают в дозе 21–22 мг/кг/сут. Суточную дозу делят на три приема с равными интервалами – по восемь часов [1]. Длительность первого этапа лечения в среднем составляет две-три недели (пока не прекратится свечение волос в лучах лампы Вуда и не перестанут обнаруживаться грибы в растворе КОН). На втором этапе гризеофульвин назначают через день, при этом суточная доза не меняется. Продолжительность этого этапа – две недели. Если грибы не обнаруживают при микроскопическом исследовании, пациента переводят на прием гризеофульвина два раза в неделю, то есть через 48 часов, суточная доза остается прежней. Продолжительность третьего этапа, как правило, составляет две недели [3, 9].
Следует подчеркнуть, что на данный момент времени гризеофульвин используется исключительно для лечения микроспории волосистой зоны кожи. Поэтому рассматриваются терапевтические дозы из расчета 21–22 мг/кг/сут. Это расчетные дозы для микродисперсного гризеофульвина с размером частиц около 4 мкм. Использование ультрамикродисперсного гризеофульвина с размером частиц менее 4 мкм позволяет снизить суточную дозу до 15–16 мг/кг, что достигается благодаря повышению биодоступности. Как показывает практика, применение препарата в дозе 15 мг/кг/сут приводит к формированию устойчивости даже у грибов рода Microsporum [3, 10].
Снижение суточной дозы препарата позволяет снизить нежелательные реакции терапии, которые, как правило, носят дозозависимый характер.
Как отмечалось ранее, гризеофульвин обладает довольно выраженным иммуносупрессивным действием. На фоне его приема обостряются хронические инфекции (как правило, ЛОР-органов). Поэтому, если во время терапии гризеофульвином пациент заболевает острой респираторной вирусной инфекцией или гриппом, лечение следует прервать во избежание развития осложнений [3, 5].
Гризеофульвин также обладает нефротоксичностью, гепатотоксичностью, коканцерогенным (усиление роста уже имеющейся опухоли), эмбриотоксическим, тератогенным и фотосенсибилизирующим эффектами. Данная терапия также ассоциируется с ортостатическим коллапсом вследствие сосудорасширяющего действия, различными неврологическими нарушениями – от снижения быстроты реакции до токсического энцефалита [7, 8].
Частота возникновения указанных нежелательных явлений не менее 15%, что не отвечает стандартам Надлежащей производственной практики (Good Manufacturing Practic – GMP) [2, 9].
Существенным побочным эффектом гризеофульвина является нарушение всасывания в кишечнике витаминов, преимущественно группы В. Этот эффект также носит дозозависимый характер. Однако степень его выраженности зависит от индивидуальных особенностей пациента – от незначительного гиповитаминоза в виде слабых проявлений хейлоза (заеды на фоне гиповитаминоза В2) до выраженных пеллагроподобных высыпаний (гиповитаминоз РР) или неврологических нарушений (гиповитаминоз В1). Несколько реже на фоне терапии гризеофульвином у детей встречается гиповитаминоз В6 и В12. Очевидно, что индивидуальны не только количественные показатели гиповитаминоза, но и качественные. Патологическое снижение концентрации витаминов может отмечаться как по одному веществу, так и по нескольким, доходя до пангиповитаминоза [7, 11].
Количественные и качественные показатели снижения биодоступности витаминов обусловлены активностью ряда кишечных ферментов. Активность и устойчивость ферментативных систем – наследуемые признаки. В норме врожденные нарушения ферментативной активности могут не проявляться, триггером могут стать те или иные вещества, попавшие в организм. Примером может служить фавизм – врожденное снижение активности (или количества) фермента глюкозо-6-фосфатдегидрогеназы. Данное состояние характеризуется возникновением токсических реакций (острая гемолитическая анемия) при приеме ацетилсалициловой кислоты, сульфаниламидных препаратов, садовых бобов. Аналогичная реакция наблюдается на фоне лечения гризеофульвином, с одной лишь разницей – нарушение может быть поливалентным [7, 12].
Каков же выход из этой ситуации? Во-первых, можно провести мониторинг концентрации витаминов в организме. Во-вторых, назначить адъювантные препараты. Последний способ является менее затратным.
Адъювантные препараты – средства, применяемые для нивелирования побочных эффектов основного лечения. При лечении микоза гризеофульвином в качестве адъювантных средств используют поливитаминные комплексы. Они позволяют компенсировать дефицит витаминов, вызванный препаратом.
Однако обычный поливитаминный комплекс не способен повлиять на состояние иммунной системы. Назначение нескольких адъювантных препаратов может привести к неоправданной полипрагмазии [8, 13].
Сказанное выше обусловливает целесообразность использования в качестве адъювантного средства препаратов, которые сочетали бы свойства поливитаминного комплекса и иммунного регулятора [14], например пробиотик-поливитаминных комплексов.
Известно, что препараты, содержащие кишечные бактерии человека, способны оказывать мощное системное иммунорегулирующее воздействие, очевидно за счет стимуляции кишечной микробиоты [11].
Все средства, нормализующие кишечную флору, можно разделить на четыре группы [14]:
- пробиотики (живые микроорганизмы): жидкие (на молочной сыворотке) и сухие (лиофилизированные);
- пребиотики (субстраты для поддержания жизнедеятельности нормальных микроорганизмов);
- синбиотики (комбинация пре- и пробиотика);
- симбиотики (сочетание различных пробиотических культур).
История применения пробиотиков в хозяйственной жизнедеятельности насчитывает не одно тысячелетие. Формирование научного подхода началось лишь со второй половины ХХ в.
Положительные свойства современных пробиотических препаратов обусловлены органичным сочетанием свойств указанных выше классов препаратов. Это позволяет не увеличивать до бесконечности количество микробных тел в одном грамме препарата, в то же время обеспечить оптимальное их количество – в пределах 10 7 –10 8 КОЕ/г. Данной концентрации бактериям достаточно для создания колонии и биопленки [11].
Необходимо отметить, что механизм нарушения обмена витаминов зависит от антибактериального вещества. Так, натуральные и полусинтетические антибиотики воздействуют по типу синдрома мальабсорбции. Сульфаниламиды (полностью синтетические соединения – ксенобиотики) сами способны нарушать обмен витаминов, прежде всего фолиевой кислоты, за счет чего и обеспечивается их антибактериальное действие. Фторхинолоны нарушают синтез белка, как следствие, снижается ферментативная активность слизистой кишечника и развивается синдром наподобие мальабсорбции [14]. Гризеофульвин относится к натуральным пенициллинподобным антибиотикам [15].
По сути, пробиотик-поливитаминный комплекс – это адаптоген, позволяющий проводить последовательные и длительные курсы терапии антибактериальными препаратами без ущерба для кишечного биоценоза.
В настоящее время на российский фармацевтический рынок выведено четыре таких комплекса.
В нашем исследовании использован пробиотик-поливитаминный комплекс, содержащий пробиотические культуры Lactobacillus gasseri PA 16/8, Bifidobacterium bifidum MF 20/5, Bifidobacterium longum SP 07/3 – 10 7 КОЕ/г каждого вида [16, 17].
Данный препарат отличается удобством применения – один раз в сутки. Этого достаточно для достижения терапевтического эффекта. Длительность курса должна составлять не менее двух-трех месяцев. Продолжительность лечения влияет на устойчивость эффекта [17].
Целью нашего исследования стало сравнение эффективности пробиотик-поливитаминного комплекса и поливитаминного комплекса.
Материал и методы
Под наблюдением находилось 44 пациента с микроспорией волосистых участков кожи. Лиц мужского пола – 17, женского – 27. Возраст больных – от 11 до 18 лет. С микроспорией волосистой части головы – 32 человека, микроспорией иной локализации – 12. Поражение кожи бровей зафиксировано у шести пациентов, лобка – у трех, подбородка – у двух, век – у одного больного.
Критерии включения в исследование:
- грибковое поражение волосистых участков кожи;
- показания к лечению гризеофульвином по стандартным схемам;
- отсутствие системных противопоказаний (в том числе аллергии на препараты пенициллинового ряда);
- отсутствие противопоказаний к приему гризеофульвина.
- наличие показаний для проведения короткого курса терапии гризеофульвином, без соблюдения стандартной схемы (например, микроспория гладкой кожи с поражением пушковых волос);
- наличие противопоказаний к применению гризеофульвина;
- аллергия или иная непереносимость препаратов из группы пенициллинов;
- аллергия или иная непереносимость поливитаминных препаратов;
- обнаружение в очагах поражения спор грибов в отсутствие мицелия (диагноз не подтвержден).
Только у шести пациентов не фиксировалось свечение пораженных волос в лучах лампы Вуда. В четырех случаях пациенты обращались на второй – четвертый день заболевания, когда свечение отсутствует. В двух случаях свечение не отмечалось в течение всего срока наблюдения.
Посев на патогенные грибы выполнен в 26 случаях. Рост грибов обнаружен в 22: в 15 – Microsporum canis, в пяти – M. audouinii, в одном – M. ferrugineum, в одном – M. gallinae.
Строгими показаниями для выполнения посева считали отсутствие свечения волос в лучах лампы Вуда, выраженный воспалительный компонент в очагах с везикуляцией, наличие волос, обломанных на разном уровне.
В большинстве случаев очаги поражения на волосистых участках кожи были единичными.
Два и три очага поражения на волосистой части головы обнаружены у четырех пациентов (по два на каждый случай). Необходимо отметить, что большинство очагов микроспории на волосистой части головы достигали от 1 до 3 см и имели четкие границы.
При микроспории других локализаций единичные очаги выявлены в четырех случаях: в одном – в области лобка, в двух – в области подбородка и еще в одном – в области век. У восьми пациентов очаги были множественными – от двух до четырех.
Во всех случаях воспаление проявлялось в виде эритемы от розового до ярко-красного цвета (рис. 1). Мелкие (милиарные) папулезные высыпания наблюдались как в центральной, так и в периферической зоне поражения. У пяти пациентов на этих участках отмечалась везикуляция. Шелушение в большинстве случаев было необильным, мелкопластинчатым.
В семи случаях волосы в пределах очагов поражения были обломаны над поверхностью кожи на разном уровне – от 3 до 12 мм.
Участники исследования были разделены на две группы. Первая группа (n = 20) получала в качестве адъювантного средства поливитаминный комплекс. Поливитаминный комплекс принимали по одной таблетке три раза в день. Вторая группа (n = 24) в качестве адъювантного средства использовала пробиотик-поливитаминный комплекс. Схема применения – по одной капсуле один раз в день.
Оба препарата пациенты применяли в течение всего периода системной терапии гризеофульвином. Продолжительность последней – от 33 до 58 дней.
Перед началом лечения все больные прошли обследование, включавшее общеклинический анализ крови с определением лейкоцитарной формулы и скорости оседания эритроцитов, общеклинический анализ мочи, биохимический анализ крови с оценкой аланинаминотрансферазы, аспартатаминотрансферазы, щелочной фосфатазы, мочевины, креатинина, билирубина, глюкозы.
Терапию гризеофульвином проводили в соответствии с клиническими рекомендациями Российского общества дерматовенерологов и косметологов 2015 г. На первом этапе препарат назначали в дозе 22 мг/мг/сут (обычно три недели), на втором – в той же суточной дозе через день (две недели), на третьем этапе – в той же суточной дозе два раза в неделю (как правило, две недели). Основанием для перехода от одного этапа к другому служило отсутствие мицелия гриба в контрольных исследованиях и свечения волос в очагах поражения.
Все пациенты получали одинаковую топическую терапию:
- утром – на очаги поражения 5%-ный раствор повидон-йода;
- вечером – противогрибковый крем.
При значительной везикуляции в течение первой недели вместо повидон-йода назначали фукорцин.
Раз в неделю пациентам с микроспорией волосистой части головы сбривали волосы в очагах поражения. В случае микроспории другой локализации применяли как бритье, так и депиляцию.
В качестве основного критерия эффективности комбинированной терапии выбран период времени до негативации свечения волос в пораженных зонах (рис. 2), дополнительного, служившего основанием для очередного взятия материала на наличие грибов в очаге поражения, – отсутствие новых папуло-везикулезных высыпаний, отрастание клинически неизмененных волос [18]. Важно отметить, что данный критерий является условным, так как пациенты в основном применяли цветные растворы для лечения (повидон-йод, фукорцин).
Клинический эффект отмечен у пациентов обеих групп. Это выражалось в уменьшении интенсивности свечения волос и шелушения в очагах поражения, а также в постепенном отрастании здоровых волос. Светящаяся часть волос была приподнята над уровнем кожи и легко удалялась при сбривании.
В первой группе время до негативации свечения в среднем составило 24,55 ± 0,61 дня, во второй – 22,79 ± 0,56 дня (p

Как лечили лишай на голове гризеофульвином. А подруга – тербинафеном. (…) И потом все равно – гризеофульвином.
Если засекли у себя эту штуку – рекомендую сразу же в поликлинику обратиться, не заниматься самолечением.
ИМЕННО ПОЭТОМУ при возникновении стригучего лишая на голове врачи уговаривают мам положить детей в стационар (что не даст гарантию полного излечения, опыт знакомых…) и в обязательном порядке прописывают токсичный противогрибковый препарат гризеовульфин в довольно большой (в сравнении с инструкцией) дозировке.

Нам прописали 4,5 таблетки. Весил ребенок на тот момент около 30 кг. В инструкции сказано:
Внутрь, во время или после еды, за один или несколько приемов. Взрослым – в суточной дозе 500 мг. При тяжелых микозах дозу увеличивают. Детям – в суточной дозе 10 мг/кг. Продолжительность лечения при тяжелых микозах – до 12 месяцев. Курс лечения при поражении кожи тела – 2-4 недели, волосистой части головы - 4-6 недель, стоп – 4-8 недель, пальцев рук – не менее 4 месяцев, пальцев ног – не менее 6 месяцев. Высшая суточная доза – 1 г.
Получается, что нам положено около 2,5 табл. в день. На самом деле при лечении стригучего лишая дозировка рассчитывается иначе - из расчета 21-22 мг/кг в сутки (в 2 раза больше!). То есть, наш врач оказался прав.

Что еще.
-голову обрить на лысо. И так после каждого анализа.
-наносить ежедневно утром йод – сочненько, на полголовы. В обед и вечером мазь на всю голову целиком.

-носить банданы и платочки каждый день чистые – пропаренные утюгом. Наволочки менять каждый день. Да, я каждый день стирала и пропаривала платочки, наволочки, нательную одежду, шапки и капюшоны, простыни.
-вообще не мыть голову. Только при очередном бритье.
А как. А вот так. Чтоб заразу не разносить . Мазь на мазь… Но я иногда протирала салициловым спиртом. И снимала корочки и пленочки крема.
Важно: не забывайте про витаминизацию и белковые продукты. Например, творог.
У нас хорошим был анализ уже спустя 9 дней после начала лечения. И все, плохих с тех пор не было.
Важно: споры – в луковицах. Именно поэтому волосы желательно не просто брить, а вытаскивать испорченные, пустые волосы. Они уже мертвы и вытаскиваются легко. Выше я упомянула специальный фонарик. У меня вот такой, за 150 рублей в ларьке на вокзале взяла.


Лампа вуда стоит от 2000 руб. Но если не смотря на хорошие контрольные (раз в месяц) анализы вы вдруг обнаружили лампой плохой волос – не переживайте раньше времени. Я, конечно, сразу же продолжила мазать, сменила противогрибковую мазь на другую (тербинафен) и ждала худшего. В итоге следующие контрольные анализы оказались тоже нормальные. И следующие.
И вот звонит мне подруга. После получасового девичьего бла-бла-релакса, она как про между прочим рассказывает про странное пятнышко на головке у сына. Ну вы поняли, да? Распросила и отправила ее к врачу – срочно. Оба сына оказались заражены. Пришлось брать отпуск на месяц. Ей прописали довольно массивный наружный курс (круче и дороже, чем у нас), а внутрь – тербинафин, как менее токсичные таблетки. Недели 3 они им безрезультатно пролечились и перешли таки на старый проверенный гризеовульфин. Успешно.
Состав:
Активное вещество: гризеофульвин (в пересчете на активное вещество) - 125 мг.
Вспомогательные вещества: лактозы моногидрат (сахар молочный), кальция стеарат, повидон (поливинилпироллидон низкомолекулярный медицинский 12600 ± 2700), крахмал картофельный.
Побочные эффекты:
Со стороны нервной системы: головная боль, головокружение, слабость, усталость, бессонница, периферическая нейропатия, нарушение координации движений, дезориентация, парестезии конечностей, спутанность сознания.
Со стороны пищеварительной системы: тошнота, рвота, диарея, гастралгия, кандидозный стоматит, гепатит.
Со стороны органов кроветворения: гранулоцитопения, агранулоцитоз, лейкопения.
Аллергические реакции: крапивница, кожная сыпь, зуд, отек Квинке, фотосенсибилизация, волчаночноподобный синдром, мультиформная экссудативная эритема, токсический эпидермальный некролиз (синдром Лайелла).
При распространенных высыпаниях проводят десенсибилизирующую терапию. Если высыпания будут нарастать гризеофульвин следует отменить на 3 – 4 дня. После исчезновения высыпаний антибиотик назначают вновь, но начинают с 1/2 таблетки в день, а затем дозу постепенно повышают до первоначальной в течение 3 – 4 дней.
Единственное, что я помню – ребенок в какой-то период начал жаловаться на сердечко, уже после приема таблеток. На самом деле, покалывание в этой области можно связать с чем угодно – с активным ростом, например. И все же есть смысл об этом упомянуть.
Не помню, чтобы подруга упоминала о каких-то проблемах, связанных с приемом гризеовульфина.
Важно: мы параллельно принимали хофитол для поддержки печени.
Особые указания:
Вследствие отрицательного влияния на репродуктивную функцию (как у мужчин, так и у женщин) необходимо использовать эффективные негормональные методы контрацепции.
Гризеофульвин системного действия не применяют для лечения инфекций легкой степени тяжести, при которых достаточно назначение только противогрибковых средств для наружного применения.
Влияние на способность управлять транспортными средствами, механизмами
Следует принимать во внимание потенциальную возможность развития таких побочных эффектов, как головокружение, сонливость, нарушения координации движений, дезориентация, спутанность сознания. При появлении описанных нежелательных явлений следует воздержаться от выполнения указанных видов деятельности.
Я начиталась немало ужастиков про гризеофульвин и могу их порекомендовать только при условии, если врач прописал. Еще лучше - сдать анализы на "печеночные пробы" (кажется так он называется). Добавлю, в этот период ребенку выпало еще и гипс на плечах носить, месяц не снимал. Риск обнаружить лишай под гипсом был очень велик, сами понимаете. Но таблетки свое дело сделали - тело оказалось чистым.
Вкус и запах я принципиально комментировать не буду - не уместно.
Стоимость таблеток относительно не большая - 150-180 рублей за 20 штук.

Микроспория – высококонтагиозная дерматофития, вызываемая грибами рода Microsporum [6]. Эпидемиологическая ситуация по заболеваемости микроспорией детей в Российской Федерации неблагоприятная, интенсивный показатель варьирует от 10 до 600 случаев на 100 тыс. детского населения. Автором отмечено, что в Саратовской области в 2013 г. участились случаи регистрации грибковых инфекций на 6,9?%, из них 77?% приходится на больных микроспорией [7]. Заболеваемость микроспорией детского населения в Свердловской области сохраняется на стабильно высоком уровне, в 2014 году составила 218,5 на 100 тыс. населения [5].
Основным возбудителем микоза в России является Microsporum canis [4]. Заражение, как правило, происходит при контакте с больными кошками или через предметы, инфицированные их шерстью. Заражение от человека наблюдается крайне редко, в среднем в 2% случаев.
Классификация микоза определяется локализацией очагов поражения, различают микроспорию волосистой части головы; микроспорию гладкой кожи туловища и конечностей, обращая внимание на вовлечение в патологический процесс не только пушковых волос, но и жестких волос ресниц, бровей, верхней губы подбородка, лобка, половых губ. Отдельно выделяют микроспорийные онихомикозы, которые встречаются редко [3].
Помимо типичной клинической картины зооантропонозной микроспории описаны атипичные варианты, удельный вес которых увеличился [1; 9; 10]. Исследователи указывают, что высыпания при атипичных вариантах микроспории могут сопровождаться выраженной эритемой, отеком, слабым шелушением. В таких случаях ошибочно диагностируется синдром Свита, центробежная эритема Дарье, многоформная экссудативная эритема, эритема Афцелиуса-Липшютца [1; 11; 16].
Авторами описаны атипичные, в том числе глубокие, формы микроспории, клинически проявляющиеся инфильтрацией, нагноением. При локализации на волосистой части головы высыпания имитируют инфильтративно-нагноительную трихофитию типа kerion Celsii и глубокие формы пиодермии [8; 15].
Кerion Сelsii (от греч. kerion – медовые соты; Aulus Cornelius Celsus – римский философ и врач, впервые описал клиническую картину данной формы tinea capitis) характеризуется образованием глубоких фолликулярных абсцессов, обычно в очаге округлой формы. Чаще очаги располагаются на волосистой части головы, кожи лица, шеи, открытых участках тела, где имеются пушковые волосы. Элементы отграничены от прилегающих тканей, поверхность их покрыта корками, после снятия которых из зияющих отверстий волосяных фолликулов выделяется гной светло-желтого цвета, напоминающий мед. Основными возбудителями Кerion Сelsii являются дерматофиты рода Trichophyton и Microsporum [13; 15].
Глубокие формы микроспории возникают на фоне реакции гиперчувствительности к компонентам грибковой клетки или продуктам жизнедеятельности гриба. Кerion Сelsii обычно наблюдается на коже головы, возможна нетипичная локализация в паховой области, области наружных половых органов [14]. Наиболее частым осложнением данной формы микоза является формирование рубцовой алопеции.
По данным авторов, глубокие формы микроспории регистрируются у 4,8-6,3% больных. M.Scerlev et al. (2010) наблюдали 58 больных глубокими формами микоза волосистой части головы в течение восьми лет, вызванные Microsporum spp. При культуральном исследовании был выделен М. canis в 52 cлучаях и М. gypseum – в 6 cлучаях [15]. G. Ginter-Hanselmayer et al. (2007) указывают, что в странах Средиземноморья и приграничных странах, таких как Австрия, Венгрия, Германия и Польша, M. сanis является основным возбудителем tinea capitis и наиболее распространенным патогеном, вызывающим кerion у человека [12].
Формированию инфильтративно-нагноительных форм микроспории способствуют нерациональная терапия, наличие сопутствующих заболеваний, позднее обращение к врачу [2]. При инфильтративно-нагноительной микроспории за счет резорбции продуктов жизнедеятельности грибов и нередко присоединяющейся вторичной бактериальной инфекции, а также лизиса тканей наблюдается общая интоксикация, которая проявляется недомоганием, головной болью, лихорадкой.
По данным исследователей, инфильтративно-нагноительная форма волосистой части головы относится к редким формам, в связи с эти приводим наши наблюдения.
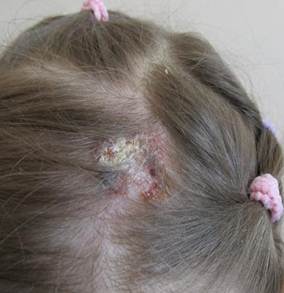
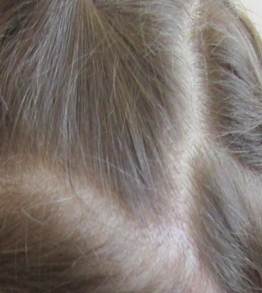
Рис. 1. Больная Н., 7 лет, с инфильтративно-нагноительной формой микроспории волосистой части головы до (А) и после лечения (Б)
Status specialis. На коже волосистой части головы, в теменной области слева определяется ограниченный, опухолевидно возвышающийся, умеренной плотности очаг диаметром 2х3 см, покрытый гнойными корками. Волосы из очага легко удаляются, из отверстий опустевших фолликулов обильно выделяется гной.
Поднижнечелюстные, передние шейные лимфатические узлы до 1,5 см в диаметре, умеренно болезненные, не спаяны с подлежащими тканями. При осмотре - температура тела 36,5 °С (рис. 1А). Общеклинические исследования: в общем анализе крови отмечен лимфоцитоз 60%, биохимические показатели и общий анализ мочи в переделах нормы.
При сборе эпидемиологического анамнеза установлено, что ребенок контактировал с бродячими кошками, находясь на каникулах в деревне у бабушки. Проведена люминесцентная диагностика, микроскопическое исследование чешуек кожи и волос, взят биоматериал для культурального исследования волос и чешуек из очага с целью определения типа возбудителя. Свечения в лампе Вуда не наблюдалось. При микроскопии чешуек кожи обнаружены нити мицелия, волос – поражение волоса по типу ectothrix megasporon. При бактериологическом исследовании волос и чешуек выявлен М. canis.
В соответствии с федеральными клиническими рекомендациями по ведению больных микроспорией (РОДК, 2015 г.) ребенку была назначена системная антимикотическая терапия гризеофульвином перорально с чайной ложкой растительного масла из расчета 22 мг на кг массы тела в сутки в 3 приема ежедневно до первого отрицательного микроскопического исследования на наличие грибов, затем через день в течение 2 недель, далее 2 недели 1 раз в 3 дня. Проводилось наружное лечение: Unguentum Ichthyoli 10% 2 раза в сутки с противовоспалительной целью в начале курса терапии, затем Сream Ketoconazoli 2% 2 раза в сутки. Длительность лечения составила 2 месяца, критериями излеченности явились трехкратные отрицательные результаты микроскопического исследования на грибы. После проведенного лечения наблюдалось разрешение очага на коже волосистой части головы, воспалительные явления в очагах регрессировали, рост волоса в местах поражения восстановился, что связано с небольшим диагностическим периодом, рациональным лечением микоза, в результате чего разрушения волосяного фолликула не произошло и рубцовая алопеция не сформировалась (рис. 1Б).
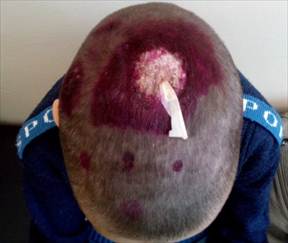
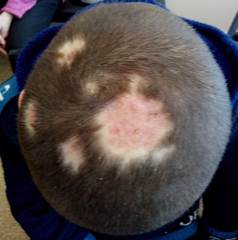
Рис. 2. Пациент Б., 9 лет, с инфильтративно-нагноительной формой микроспории волосистой части головы до (А) и после лечения (Б)
Status specialis. На коже волосистой части головы, в области макушки определяется крупный очаг в диаметре 5 см, покрытый гнойными корками, в центре очага хирургический дренаж. По периферии крупного очага в теменной области справа и слева имеются мелкие, диаметром 2х3 см, очаги, возвышающиеся над уровнем кожи, покрыты гнойными корками. Волосы из мелких очагов также легко эпилировались, из отверстий волосяных фолликулов выделялся гной.
Регионарный лимфаденит не определялся. При осмотре - температура тела 36,6 °С (рис. 2А). Общеклинические исследования: в общем анализе крови отмечен лейкоцитоз (12,5 х 1012), сдвиг лейкоцитарной формулы влево (баз. 1%, эоз. 2%, сегм. 75%, лимф. 20%, мон. 3%), биохимические показатели и общий анализ мочи в переделах нормы.
При сборе эпидемиологического анамнеза установлено, что ребенок посещал парикмахерскую за 2 недели до начала заболевания, контакт с животными отрицает. При проведении люминесцентной диагностики специфического свечения в лампе Вуда не было. При микроскопическом исследовании кожных чешуек выявлены нити мицелия, определялось поражение волоса по типу endothrix. При бактериологическом исследовании волос и чешуек выявлен М. canis.
На фоне системной антимикотической терапии гризеофульвином, адекватного наружного лечения (противовоспалительные и антимикотические препараты) через 2,5 месяца наблюдалось клиническое и микологическое излечение. Критерием излеченности явились трехкратные отрицательные результаты микроскопического исследования на грибы. У данного пацинта в результате запоздалой диагностики и длительного неадекватного наружного лечения впоследствии сфомировалась вторичная рубцовая алопеция (рис. 2Б).
Наружное лечение направлено на устранение воспаления, с этой целью назначаются местные препараты, содержащие ихтиол. После стихания острого воспаления показана местная противогрибковая терапия в виде крема, шампуня, содержащего кетоконазол, для уменьшения распространения спор грибковой инфекции и сокращения продолжительности лечения.

Читайте также:


