Генферон или кипферон что лучше в гинекологии от герпеса
Действующее вещество
Фармакологическая группа
Нозологическая классификация (МКБ-10)
Состав и форма выпуска
| Суппозитории | 1 супп. |
| интерферон человеческий рекомбинантный альфа-2 | не менее 500000 МЕ |
| комплексный иммуноглобулиновый препарат сухой (КПИ) | 60 мг |
| вспомогательные вещества: жир; парафин; эмульгатор Т-2 |
в контурной ячейковой упаковке 10 шт.; в пачке картонной 1 упаковка.
Характеристика
Комбинация рекомбинантного человеческого интерферона альфа-2 и комплексного иммунобиологического препарата (КИП), содержащего иммуноглобулины основных трех классов G, A, M.
Фармакологическое действие
Препарат сочетает антихламидийное действие специфических антител, содержащихся в КИП, и антибактериальное, противовирусное, противовоспалительное и иммуномодулирующее действие рекомбинантного интерферона альфа-2. Эффект проявляется как во внутриклеточной, так и во внеклеточной среде организма за счет прямого действия на возбудителей заболевания и стимуляции механизмов местного и общего иммунитета. Повышенное содержание белка в данной лекарственной форме обеспечивает бóльшую стабильность интерферона в присутствии агрессивных факторов секретов слизистых и отделяемого в очагах поражения кожи и слизистых оболочек.
Показания препарата Кипферон ®
Урогенитальный хламидиоз (лечение) у женщин ( в т.ч. с проявлениями дисбактериоза влагалища, вульвовагинита, цервицита шейки матки, эрозии шейки матки) на фоне общепринятой антибиотикотерапии.
Неспецифические воспалительные заболевания, герпес, вирусные (ретровирусные) и бактериальные (сальмонеллез, дизентерия, колли-инфекция) кишечные инфекции у взрослых и детей; частые воспалительные заболевания респираторного тракта, рецидивирующий бронхит, пневмония; дисбактериоз влагалища и кишечника различного происхождения; вирусные гепатиты B, C и А у детей; при подготовке к плановым гинекологическим и другим операциям (для профилактики инфекционных осложнений.)
Противопоказания
Побочные действия
Способ применения и дозы
Ректально, интравагинально (до контакта с задним сводом влагалища и шейкой матки). По 1–2 супп. (в зависимости от выраженности заболевания), 2 раза в день. Курс лечения составляет, в среднем, 10 дней; при наличии эрозии шейки матки применение продолжают до ее эпителизации. По показаниям курс лечения может быть повторен. Лечение следует начинать в первые дни после окончания менструации. Перед введением рекомендуется удалить слизь со слизистых оболочек влагалища и шейки матки.
Схемы назначения препарата Кипферон ® , суппозитории
Детям — 1 супп. 1 раз в сутки, в течение 10 дней. У девочек со стертыми клиническими формами хламидийного вульвовагинита и без клинических проявлений воспалительного процесса матки и ее придатков, хламидийной инфекции мочевыводящих путей, респираторного хламидиоза лечение проводят только на фоне вагинального и перорального приема эубиотиков, в остальных случаях лечение хламидиоза у детей Кипфероном ® сочетают с назначением антибиотиков и эубиотиков.
Взрослым — в суточной дозе 1–2 млн МЕ (2–4 супп.) в 2 приема, курс лечения — 10–14 дней; дополнительно проводят антибиотикотерапию и назначают вагинально и перорально эубиотики. Если после лечения сохраняются клинические признаки хламидиоза или инфицирование хламидиями, проводят повторный курс терапии Кипфероном ® .
При вирусных гепатитах B, C и A у детей
Ректально. Детям до 7 лет Кипферон ® назначают в разовой дозе 50000 МЕ/кг массы тела в 2 приема, но не более 1 млн МЕ/сут (2 супп.); 8–11 лет — 1,5 млн МЕ/сут (3 супп.); старше 12 лет — 2 млн МЕ/сут (4 супп.). Длительность курса лечения при остром течении вирусных гепатитов составляет 14 дней. Первые 7 дней препарат применяют ежедневно, затем — 2 раза в неделю. При затяжном течении заболевания длительность курса достигает 3–4 нед .
При частых воспалительных заболеваниях респираторного тракта, рецидивирующих бронхитах ( в т.ч. с обструктивным синдромом), пневмониях у детей
Ректально. В суточной дозе 1 млн МЕ (2 супп.) в 2 приема ежедневно в течение первых 5 дней, затем — 2 раза в неделю в течение 3 нед . Возможно применение в виде монотерапии или в комплексном лечении, на фоне базисной антибактериальной терапии.
При генитальном герпесе
Взрослым по 1–2 млн МЕ (2–4 супп.) в течение 10–14 дней; возможно проведение повторного курса лечения; детям — в суточной дозе 500000 МЕ (1 супп.) в 1 прием, курс лечения — 10 дней.
Антибиотикотерапия при генитальном герпесе проводится только при наличии сопутствующей бактериальной инфекции. У женщин и девочек-подростков лечение препаратом рекомендуется начинать в первые дни после окончания менструации. Перед вагинальным введением целесообразно удалить слизь тампоном со слизистых оболочек влагалища и шейки матки.
При кишечных инфекциях у детей
Ректально (после очистительной клизмы или акта дефекации). Детям до 12 лет — в средней разовой дозе 50000 МЕ/кг массы тела, но не более 1 млн МЕ/сут (2 супп.), старше 12 лет — не более 2 млн МЕ (4 супп.). Наиболее целесообразно применять препарат в первые 3 дня заболевания, т.е. в острый период. Курс лечения вирусной диареи среднетяжелой формы — 3–5 дней; тяжелой формы — 7 дней.
Кипферон ® может быть единственным этиопатогенетическим средством лечения (без антибактериальных препаратов) на фоне общепринятой базисной терапии (пероральная регидратация, дозированное лечебной питание, при необходимости — инфузионная терапия). При тяжелых формах в комплекс терапии целесообразно включать антибиотики.
При подготовке к плановым гинекологическим и другим операциям с целью профилактики инфекционных осложнений
Ректально. Кипферон ® используют в суточной дозе 1 млн МЕ (2 супп.), в 2 приема, за 3–5 дней до и во время операции, а также в послеоперационном периоде. Курс лечения — 10–15 дней. Интервал между приемами — 12 ч.

Чтобы приостановить размножение вирусов и ускорить процесс выздоровления назначают противовирусные препараты Кипферон и Генферон.
Генферон описание
Этот препарат считается противовирусным средством. В состав входит рекомбинантный человеческий интерферон. Также содержит таурин и бензокаин.
Выпускается в суппозиториях для ректального и вагинального введения. Характеризуется иммуномодулирующим, антипролиферативным, противомикробным, местноанестезирующим и регенерирующим эффектами. Этот медикамент обладает местным и системным воздействием.
Лекарство включается в состав комплексной терапии во время лечения неосложненных болезней у детей и взрослых.
В инструкции по применению указано, что препарат показан при:
- хламидиозе;
- генитальном герпесе;
- микоплазмозе;
- уреаплазмозе;
- гарднереллезе;
- папилломавирусной инфекции;
- трихомониазе;
- эрозии шейки матки;
- бактериальном вагинозе;
- вульвовагините;
- цервиците;
- аднексите;
- уретрите;
- баланите;
- простатите.
Нередко Генферон назначается женщинам при развитии молочницы.
Медикамент запрещено использовать женщинам до 12-13 недель беременности. С осторожностью свечи назначаются пациентам в период обострения патологий иммунной системы.
Во время применения суппозиториев может проявиться побочная симптоматика. Такой процесс сопровождается:
- головной болью;
- лейкопенией или тромбоцитопенией;
- гипертермией, повышенным потоотделением;
- утомляемостью, болезненным чувством в мышечных тканях;
- ухудшением аппетита.

Нередко Генферон назначается женщинам при развитии молочницы.
При возникновении заболеваний мочеполовой системы назначается по 1 свече дважды в день. Лечебный курс длится 10 суток.
Кипферон описание
Включен в категорию противовирусных средств. В качестве действующих компонентов выступают сухой иммуноглобулин и человеческий интерферон. Выпускается в свечах. Характеризуется иммуномодулирующим, противоопухолевым, противомикробным, противовирусным и противовоспалительным свойствами.
В инструкции по применению указано, что Кипферон назначается:
- при урогенитальной хламидийной инфекции у женщин;
- при осложненном дисбактериозе влагалища;
- при воспалении или эрозии шейки матки;
- при герпесной инфекции;
- при дизентерии, сальмонеллезе, коли-инфекции;
- при острых вирусных инфекциях пищеварительного тракта у ребенка и взрослого;
- при частой пневмонии и рецидивирующем бронхите;
- при вирусном гепатите у детей.
Используется в качестве профилактики перед проведением оперативного вмешательства.
Побочные реакции при применении медикамента выявлены не были.
Суппозитории вводятся ректально или вагинально. Суточная дозировка составляет 2-4 свечи в зависимости от тяжести болезни. Продолжительность лечебного курса составляет 1-1,5 недели.

Суточная дозировка Кипферона при лечении вирусных инфекций составляет 2-4 свечи.
В чем разница между Кипфероном и Генфероном
Одним из главных отличий считается состав. Генферон, кроме человеческого интерферона, состоит из таурина и бензокаина. Таким образом, медикамент проявляет местный обезболивающий и ранозаживляющий эффекты.
Кипферон содержит комплексный иммуноглобулин. Этот компонент состоит из специфических антител к ротавирусу, герпесвирусу, стафилококкам, хламидии, энтеробактериям.
Первый тип медикамента часто применяется для лечения мочеполовых инфекций. Кипферон показан для лечения детей и взрослых при различных заболеваниях вирусного и бактериального характера.
Оба лекарства выпускаются в свечах. Но отличаются схемой применения. Генферон вводится по 1 суппозиторию 2 раза в сутки. Суточная дозировка Кипферона составляет 2-4 свечи.
При назначении лекарственного средства учитываются противопоказания. Кипферон не применяется у тех пациентов, у которых есть повышенная восприимчивость к составляющим медикамента.
Генферон отличается списком противопоказаний. Препарат не назначается женщинам до 12-13 недель беременности, а также больным в период обострения заболеваний иммунной системы.
Оба лекарства предназначены для лечения вирусных инфекций и выпускаются в России, но отличаются ценой. Кипферон обойдется в 660-753 руб. Генферон стоит от 337 до 960 руб.
Кипферон и Генферон: что лучше
Медикаменты обладают противовирусным эффектом. Но В состав Кипферона входят активные вещества на основе антител, что делает препарат эффективнее. Второй тип лекарства чаще используется для лечения болезней мочеполовой системы у взрослых пациентов. Но имеет больше противопоказаний и вызывает побочные реакции.
Оба медикамента безопасны для лечения детей.
Но если вирусная инфекция привела к бактериальным осложнениям, то тогда лучше использовать Кипферон.
Отзывы
Эдуард Владимирович, гинеколог, 46 лет, Курск
Все чаще у женщин стали диагностироваться эрозия шейки матки и молочница. Поэтому в состав комплексного лечения включаю свечи Генферон. Препарат эффективно борется с возбудителями болезней и повышает местный иммунитет. Также оказывает местный обезболивающий эффект, способствует быстрому заживлению ранок.
Елена Анатольевна, педиатр, 39 лет, Волгоград
Дети чаще взрослых страдают вирусными инфекциями. Виной тому ослабленный иммунитет. Чтобы быстро снять симптомы заболевания и повысить сопротивляемость организма, назначаю свечи Кипферон. Стоит препарат дорого, но в его состав входят антитела не только к вирусам, но и к некоторым бактериям.
Анна, 27 лет, Томск
Во время беременности заболела ОРВИ. Знаю, что многие лекарства принимать нельзя, поэтому боялась, что возникнут осложнения. Врач назначил Кипферон. Сказал ставить по 2 суппозитория в сутки. Симптомы исчезли через 3 дня. Полностью поправилась через неделю. Осложнений не было, на ребенке никак не отразилось. Но стоимость у медикамента высокая.
Виталий, 35 лет, Астрахань
У жены выявили хламидиоз. Лечение проводили в амбулаторных условиях. В состав комплексной терапии входили свечи Генферон. Лечилась 1,5 недели. После этого сдала повторно анализ, все было чисто. Но во время лечения жаловалась на головную боль. Доктор сказал, что так проявляется побочная реакция, при которой не требуется отмена препарата.
- КЛЮЧЕВЫЕ СЛОВА: урогенитальные инфекции, кондиломатоз, герпес, вагиноз, Генферон, Циклоферон
Больные с данной вирусной патологией входят в группу риска хронических воспалительных заболеваний половых органов, осложнений после инвазивных манипуляций, онкологических заболеваний половых органов. Тяжелое течение, частые рецидивы наносят серьезный психологический ущерб, вызывая снижение эмоциональной и физической активности больных, а также нарушение их социальной адаптации. Генитальный кондиломатоз и генитальный герпес нередко способствуют развитию диспластических изменений в эпителии гениталий с последующим перерождением в рак (5, 8, 16).
Герпетическая инфекция, связанная с присутствием в организме вируса простого герпеса I или II серотипов, является наиболее распространенной латентно протекающей вирусной инфекцией человека. Она характеризуется многообразием клинических проявлений с поражением кожи, слизистых оболочек, ЦНС, глаз. Герпетическая инфекция нередко вызывает патологию беременности, родов, гибель плода и генерализованную инфекцию новорожденных детей (4, 6).
Папилломовирусная инфекция (ПВИ) поражает поверхностный слой кожи и слизистых оболочек. В конце инкубационного периода ДНК вируса размножается в ядре клетки, что сопровождается появлением экзофитных разрастаний. Пусковым моментом является микротравма кожи и слизистых оболочек, чаще всего – во время половых контактов. Большинство случаев рака шейки матки связаны с ПВИ (имеет значение тип ВПЧ, продолжительность инфекционного процесса) (11, 14).
Инфицирование возбудителями генитального герпеса и ПВИ и последующее развитие заболевания тесно связаны с иммунным статусом организма. В свою очередь, вирусы сами инициируют формирование иммунодефицита, в результате чего снижается противовирусный иммунитет. Это приводит к длительной персистенции возбудителя в организме больного и рецидивам заболевания (8, 10).
Раннее начало половой жизни, частая смена половых партнеров, а также партнер, имеющий множественные половые связи, являются значимыми факторами риска заражения.
Изменение среды влагалища и аномального состояния поверхностного слоя эпителия способствует проникновению вируса в клетки. Снижение защитных сил организма ведет к заражению и проявлению вирусных урогенитальных инфекций (1, 4, 12).
Учитывая сложный этиопатогенез урогенитальных инфекций, терапия должна способствовать ускорению регенерации, нормализации микрофлоры влагалища, профилактике рецидивов заболевания. Лекарственный препарат должен хорошо переноситься пациентками, и быть удобен в применении.
В настоящее время одним из приоритетных и наиболее эффективных методов терапии герпес- и папилломавирусной инфекции является иммунотерапия. Кроме того, наличие выраженной симптоматики делает необходимым проведение симптоматической терапии (7, 8, 10).
В последние годы в лечении генитального герпеса и генитального кондиломатоза нашли широкое применение иммуномодуляторы, препараты α-, β- и γ-интерферона, обладающие противовирусным, иммуномодулирующим и антипролиферативным действиями, а также индукторы эндогенных интерферонов (2, 3, 9, 15).
Применение препаратов интерферона в комплексной терапии больных рецидивирующим генитальным герпесом приводит не только к улучшению клинического состояния больных, но также и к восстановлению иммунного статуса. При этом следует отметить обратимый характер изменений иммунной реактивности, показатели которой нормализуются после лечения, что сочетается с обратным развитием клинических признаков заболевания. Заместительное применение препаратов α-ИФН приводит к уменьшению продолжительности и остроты рецидивов. Однако при парентеральном введении препаратов α-ИФН могут возникать существенные побочные реакции (артралгии, депрессии, кожный зуд, гриппоподобный синдром и др.) (3).
Существенно меньшими побочными эффектами экзогенной интерферонизации обладают лекарственные формы интерферона для местного применения (10), в связи с чем область их применения в клинической практике быстро расширяется. Одним из препаратов данной группы является Генферон, нашедший свое применение в терапии инфекционно-воспалительных заболеваний урогенитального тракта, в том числе генитального герпеса, папилломовирусной инфекции, хламидиоза, уреаплазмоза, микоплазмоза, рецидивирующего вагинального кандидоза, бактериального вагиноза, трихомониаза и др.
Генферон − комбинированный препарат, действие которого обусловлено лечебными свойствами компонентов (ИФН α-2; таурин, анестезин), входящих в его состав. Интерферон α-2 повышает активность естественных киллеров, Т-хелперов, фагоцитов, а также интенсивность дифференцировки В-лимфоцитов, непосредственно ингибирует репликацию и транскрипцию вирусов, хламидий. Таурин обладает регенерирующими, репаративными, мембрано- и гепатопротективными, антиоксидантными и противовоспалительными свойствами. Анестезин − местный анестетик, препятствует возникновению болевых ощущений. Данное сочетание компонентов весьма рационально для лечения герпес- и папилломовирусной инфекции в связи с наличием при обострении герпетической инфекции и после местной деструктивной терапии кондилом выраженного болевого синдрома и изменений в микрофлоре влагалища. В связи с этим большой интерес представляет сравнение эффективности Генферона и суппозиториев с интерфероном-альфа, имеющих другой компонентный состав. Кроме того, остается неизученным вопрос о сравнительной эффективности препаратов интерферона и индукторов эндогенного интерферона, а также их комбинации.
Целью нашего исследования явилось сравнительное изучение клинической эффективности препаратов Генферон, Виферон и индуктора интерферона – Циклоферон при лечении больных генитальным герпесом и генитальным кондиломатозом. Критериями излеченности в соответствии с общепринятыми стандартами лечения, являлись устранение клинических проявлений заболевания, прекращение или снижение остроты воспалительных реакций и элиминация инфекционного агента.
Пациенты и методы
Препарат Генферон назначался в течение 10 дней параллельно с проведением комплексной терапии – женщинам в дозе 500 000 МЕ 2 раза в сутки вагинально, мужчинам – в дозе 1 000 000 МЕ
2 раза в сутки ректально. Виферон применялся в дозе 1 000 000 МЕ
2 раза в сутки ректально в течение 10 дней параллельно стандартной терапии. Циклоферон вводился внутримышечно в дозе 250 мг 1 раз в день на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23-й дни лечения.
Помимо исследуемых препаратов больные генитальным герпесом получали традиционную базовую терапию ацикловиром 400 мг 3 раза в день в течение 7 дней. У больных генитальным кондиломатозом в первый день лечения проводилась местная деструкция очагов поражения: диатермокоагуляция при поражении шейки матки или солкодерм при поражении аногенитальной области. Все пациентки имели сопутствующие воспалительные заболевания влагалища. При бактериальном вагинозе назначался орнидазол 500 мг 2 раза в день в течение 3 дней, при вагинальном кандидозе − микосист 150 мг
2 раза с интервалом 7 дней. На протяжении всего исследования пациенты пользовались методами барьерной контрацепции. В течение 40 дней с момента включения в исследование, не разрешалось применение других иммуномодулирующих препаратов, помимо исследуемых.
В общей сложности в исследование было включено 120 пациентов, находящихся на амбулаторном лечении (60 мужчин и 60 женщин). У 94 пациентов поставлен диагноз генитального герпеса, у 26 – диагноз генитального кондиломатоза. Распределение пациентов по группам проводилось рандомизированно – методом случайной выборки. В процессе рандомизации проводилась стратификация больных по полу, природе и тяжести заболевания. Было сформировано 3 группы пациентов, каждая из которых включала 40 больных (20 мужчин и 20 женщин).
В первой группе из 40 пациентов в дополнение к стандартной терапии применялся препарат Генферон, во второй – Виферон, в третьей – Циклоферон.
В процессе исследования проводилось физикальное обследование, ПЦР-диагностика вирусов простого герпеса I и II типов, а также вирусов папилломы человека, микроскопия мазков, окрашенных по Граму, цитологическое исследование мазков, окрашенных по Папаниколау, кольпоскопия и изучение качества жизни с помощью опросника
SF-36. Обследование проводилось до начала лечения, повторно – через 10 дней (кроме ПЦР-диагностики) и через 40 дней после начала лечения.
Результаты контрольного исследования методом ПЦР (PCR Amp/Cycle Graf for FAM-490) продемонстрировали высокую эффективность проведенного лечения (таблица 1, рисунок 1).
В группе пациентов, в комплексном лечении которых применялся Генферон, была достигнута более высокая частота элиминации инфекционного агента, чем при применении других иммунотропных лекарственных препаратов. Повторное выявление возбудителя через 40 дней после начала лечения Генфероном наблюдалось лишь у одного мужчины с генитальным герпесом и одной женщины с генитальным кондиломатозом. При этом у данных пациентов отсутствовали какие-либо клинические проявления заболевания.
В то же время при применении Виферона положительный результат ПЦР через 40 дней после начала лечения наблюдался у 6 из 40 больных, при применении Циклоферона – у 12 из 40 пациентов.
У 19 из 20 женщин, имевших проявления неспецифического вульвовагинита и бактериального вагиноза, через 40 дней после начала применения Генферона полностью исчезали указанные состояния, в то время как после использования Виферона клинические проявления этих заболеваний сохранялись у 2 женщин, а после курса Циклоферона – у 5 пациенток (рисунок 2).
При наблюдении за течением раневого процесса после процедуры деструкции кондилом у больных урогенитальным кондиломатозом отмечено также противовоспалительное действие Генферона – региональный отек и признаки воспаления были менее выраженными по сравнению с соответствующими проявлениями у пациентов других групп.
Анализ динамики самочувствия пациентов обоего пола показал, что наибольшее количество случаев значительного улучшения в ранние сроки после начала лечения было зарегистрировано у пациентов, применявших Генферон, что, вероятно, связано со снижением остроты болевых ощущений под влиянием входящего в состав препарата анестезина.
Несмотря на наличие обширного спектра противовирусных и иммуномодулирующих препаратов, проблема рецидивирующих урогенитальных инфекций вирусной этиологии актуальна до сих пор.
Анализ результатов данного исследования свидетельствует о том, что комплексная терапия урогенитальных инфекций вирусной этиологии с использованием препарата Генферон имеет наибольшую эффективность. Применение Генферона позволило достичь негативного результата ПЦР у 95% пациентов. Большая доля ВПГ- и ВПЧ-негативных результатов в группе пациентов, принимавших Генферон, по сравнению с препаратами Виферон и Циклоферон, является показателем более высокой антивирусной и иммуномодулирующей активности Генферона.
Применение препарата Генферон в комбинации со средствами стандартной терапии хорошо переносится пациентами, не вызывает местных и системных реакций, уменьшает болевой синдром, способствует элиминации возбудителя и быстрому заживлению пораженных тканей, а также снижает вероятность рецидивов заболевания.
Результаты исследования позволяют сформулировать следующие рекомендации для применения препарата Генферон при генитальном герпесе и генитальном кондиломатозе:
- Комплексная терапия женщин с генитальным герпесом: Генферон в дозе 500 000 МЕ 2 раза в сутки вагинально в течение 10 дней параллельно с назначением ацикловира 400 мг 3 раза в день в течение 7 дней или фамвира 250 мг 3 раза в день в течение 7 дней.
- Комплексная терапия женщин с папилломовирусной инфекцией: Генферон в дозе 500 000 МЕ 2 раза в сутки вагинально в течение 10 дней параллельно с проведением диатермокоагуляции, применением солкодерма или аналогов.
- Комплексная терапия мужчин с аналогичными заболеваниями включает в себя назначение Генферона ректально в дозе 1 000 000 МЕ 2 раза в сутки в течение 10 дней параллельно с проведением этиотропной терапии или деструктивных методов.
- При возникновении рецидива заболевания возможно проведение повторного курса лечения Генфероном по описанной выше схеме или в виде монотерапии.
- Для профилактики рецидивов заболевания при неполной элиминации вирусов (положительный тест ПЦР в контроле после проведенного лечения) рекомендуется проведение повторного курса лечения Генфероном по описанной выше схеме в виде монотерапии через 25-30 дней после окончания предыдущего курса.

В своей практической деятельности врачи многих специальностей встречаются с заболеваниями, вызванными вирусами семейства Herpesviridae, которые широко распространены в человеческой популяции. Они способны поражать практически все органы и системы организма хозяина, вызывая латентную, острую и хроническую формы инфекции при этом, спектр клинических проявлений, развитие которых они обусловливают, чрезвычайно широк [7]. Особого внимания заслуживает рецидивирующая форма герпетической инфекции (ГИ), относящаяся к числу наиболее распространенных психосоматических кожных заболеваний. Хроническое течение, зуд, частая локализация и характер высыпаний на лице или интимно значимых участках кожного покрова сопровождаются изменениями эмоциональной сферы. В свою очередь, состояния стресса, восприятие самим пациентом проявлений болезни оказывает влияние на интенсивность и частоту рецидивов простого герпеса (ПГ) [24].
Многочисленные исследования в области проблемы ГИ, особенно вызванные вирусами простого герпеса (ВПГ) 1 и 2 типов, не теряют своей актуальности в настоящее время [21, 16].
Серьёзной проблемой является высокая инфицированность здорового населения, преимущественно молодого, трудоспособного возраста. В мире ежегодно заражаются от 16 до 800, а в России – от 40 до 80 человек на 100 тыс. населения. В настоящее время заболеваемость ПГ крайне высока, по статистике ВОЗ, она занимает второе место среди вирусных поражений, уступая лишь гриппу. ВПГ-1 инфицировано около 90 % взрослого населения планеты, распространенность ВПГ-2 колеблется от 7 до 40 %. В США ежегодно регистрируется до 98 млн случаев лабиального герпеса и 20 млн случаев рецидивирующего герпеса гениталий, 500 тыс. случаев офтальмогерпеса и более 5 тыс. случаев герпетического энцефалита, около 1 тыс. случаев герпеса новорожденных. По мнению ведущих специалистов, в нашей стране ежегодная заболеваемость герпесом губ составляет 10 млн, герпесом кожи – 1 млн, офтальмогерпесом – 250 тыс. случаев. Рецидивирующими формами герпеса страдают от 10 до 20 % населения, а ежегодный прирост увеличивается на 15–17 % [3, 13, 23].
Литературные данные свидетельствуют, что большинство населения Земли инфицировано ВПГ-1, ВПГ-2 или тем и другим вирусом одновременно. Первичная инфекция, ассоциированная с ВПГ-1 или ВПГ-2, может протекать в клинически выраженной форме в очаге инфицирования (например, в орофациальной или генитальной области) либо как бессимптомная или нераспознанная инфекция. Генитальная форма простого герпеса может быть связана с ВПГ-1, так же как и лабиальная форма – с ВПГ-2. После первичного инфицирования у 50–75 % больных отмечается рецидивирующее течение простого герпеса. В течение первых 12 месяцев после инфицирования ВПГ-2 рецидив возникает у 80 % пациентов, ВПГ-1 – у 55 % [15, 26].
Современная медицина не располагает методами лечения, позволяющими элиминировать ВПГ из организма человека. Целью лечения герпеса является: 1) подавление репродукции ВПГ в период обострения (купирование рецидива); 2) снижение частоты и длительности рецидивов заболевания, тяжести их течения; 3) формирование адекватного иммунного ответа и его длительное сохранение с целью блокирования реактивации ВПГ в очагах персистенции.
Всё разнообразие методов терапии и профилактики обострения герпесвирусных инфекций можно сгруппировать в направления этиотропного, патогенетического и симптоматического лечения с применением химиотерапии, иммунотерапии и комплексного лечения [1, 7, 11].
Большое внимание уделяется антигерпетическим соединениям растительного происхождения, природным антиоксидантам, адаптогенам из лекарственного растительного сырья и витаминно-минеральным комплексам, ввиду изменения иммунного статуса пациентов [14, 19].
Патогенетическая терапия направлена на нормализацию функции иммунной системы организма, в том числе на активацию системы интерфероновой защиты, как правило, связанная с применением интерферонов (ИФН), индукторов ИФН и иммуномодуляторов. Специфическая иммунотерапия состоит в применении герпетической вакцины, хотя ряд исследователей считает, что надежды, возлагаемые на специфическую вакцинопрофилактику, не оправдали себя [11, 19]. Иммунотропные препараты, обладающие активностью против вируса герпеса, разнообразны и представлены в таблице.
Иммунотропные препараты, обладающие активностью против вируса герпеса
Использование противовирусной химиотерапии велико при лечении рецидивирующих форм простого герпеса с поражением кожи и слизистых оболочек. В лечении простого герпеса с применением противогерпетических химиопрепаратов можно выделить два принципиально отличающихся друг от друга подхода: 1) эпизодическое лечение – прием ациклических нуклеозидов (АН) в момент рецидива в терапевтических дозах при соблюдении кратности и длительности лечения; 2) супрессивная терапия – длительный, иногда многолетний, постоянный прием препаратов АН вне рецидива в более низких дозах [9, 25].
Согласно проведенным исследованиям, биодоступность (per os) противогерпетических препаратов из группы ациклических нуклеозидов возрастает следующим образом: ацикловир – 20 %, валацикловир – 54 % и фамцикловир – 77 % [24]. Тем не менее применение ацикловира по-прежнему остаётся востребованным среди врачей и пациентов в настоящее время, и одновременно ведутся исследования по увеличению растворимости ацикловира [5] и синтезу его производных [8].
В разные годы предпринимались многочисленные попытки повысить эффективность лечения ПГ путем комбинированной терапии. С этой целью использовались различные сочетания средств иммунного влияния, а также препаратов, отличающихся по этиопатогенетическому механизму действия [20].
Возможно сочетанное использование противовирусной терапии и глюкокортикостероидов. Выявлено, что такая комбинация эффективнее монотерапии противовирусными препаратами, особенно для лечения острой боли и коррекции различных аспектов качества жизни пациентов. Комбинация ацикловир + преднизолон значительно быстрее купирует острую боль и возвращает пациента к обычной жизнедеятельности в случае постгерпетической невралгии [2].
Наружные средства дополняют системную противовирусную терапию. Многочисленные наблюдения подтверждают, что в случае назначения таблетированных форм ациклических нуклеозидов на стадии предвестников в сочетании с наружной противовирусной терапией значительно чаще удается полностью прервать дальнейшее развитие рецидива или наблюдать его абортивное течение [20].
Местная терапия противовирусных лекарственных средств при герпесе кожи и слизистых оболочек требуется для уменьшения отёка, экссудации, боли и зуда, ускорения заживления язвочек и эрозий и сокращения длительности выделения вируса на участках поражения [22]. Применение данных лекарственных форм начинают при появлении первых признаков активации инфекции (чувство жжения, зуд и т.д.) и продолжают вплоть до эпителизации эрозий. Рано начатое местное лечение может предотвратить развитие везикул.
В комплексную терапию пациентов с простым герпесом необходимо включать местные противовирусные средства, способствующие стабилизации и разрешению процесса [12].
При анализе ассортимента противовирусных средств на российском рынке установлено, что большинство противовирусных препаратов выпускается в виде твёрдых лекарственных форм – 66 %, в виде мягких лекарственных форм – 22 %, а в форме жидких – 12 % [22], лидером же является ацикловир [6].
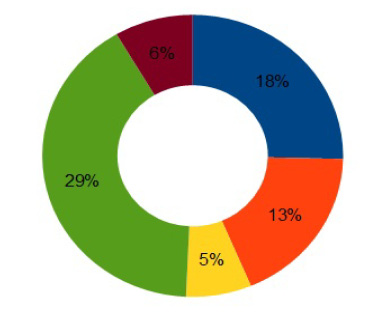

Ассортимент лекарственных форм, содержащих ацикловир
Следует отметить, что современная фармакотерапия герпеса эффективно уменьшает его клинические проявления, положительно влияет на психическое состояние пациентов и приобретает комплексный подход. Несмотря на различные достижения в лечении герпеса, ацикловир по-прежнему играет значительную роль в данном направлении и привлекает внимание исследователей по созданию комбинированных препаратов. В связи с чем актуальными являются исследования по разработке лекарственной формы комбинированного состава, обладающей противогерпесным эффектом – медицинские карандаши.
Рецензенты:
Степанова Э.Ф., д.фарм.н., профессор, профессор кафедры технологии лекарств ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск;
Хаджиева З.Д., д.фарм.н., профессор, профессор кафедры технологии лекарств ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Читайте также:


