Физиотерапия при герпетическом кератите
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
В странах умеренного пояса вирусные кератиты доминируют среди различных проявлений патологии роговицы. Наиболее часто это заболевание роговицы вызывает вирус простого герпеса. Герпес-вирусный кератит (ГК) прочно занимает первое место среди причин корнеальной слепоты. Клиническая тяжесть заболевания, высокая функциональная ценность глаза и социальные последствия во многом объясняют тот факт, что ГК человека, как правило, был первой мишенью для испытания новейших противовирусных средств, включая ИДУ (5-йод-2-дезоксиуридин), человеческий интерферон, и вирусный индуктор интерферона интерфероноген [1–3]. За прошедшие 30 лет сформировались три основных направления противовирусной терапии ГК:
1) химиотерапия;
2) неспецифическая (индукторы интерферона, иммуномодуляторы, интерфероны);
3) специфическая (герпетическая вакцина, противогерпетический иммуно- глобулин).
Исследования, проводившиеся в ряде научных центров нашей страны (Клиника глазных болезней ММА им.
И.М. Сеченова, НИИ глазных болезней, НИИ вирусологии им.Д.И. Ивановского, НИИ полиомиелита и вирусных энцефалитов, МНИИ глазных болезней им.Гельмгольца Минздрава РФ), впервые привели к разработке и внедрению в клиническую практику трех новых эффективных направлений в лечении ГК [4–10].
1. Метод неспецифической противовирусной терапии, высокоэффективный в лечении различных проявлений офтальмогерпеса, основан на местном и системном введении индукторов интерферона интерфероногенов, обладающих широким спектром противовирусного иммуномодулирующего действия. Налажен производственный выпуск первого отечественного высокоактивного интерфероногена полудана (комплекс поли А: поли У). В настоящее время полудан выпускается в виде ампул и флаконов-капельниц.
2. В основу не существовавшей ранее эффективной методики противорецидивной терапии положен принцип специфической иммунокоррекции посредством системного курсового введения герпетической вакцины в сочетании с кратковременными инстилляциями интерферонoгeнов. Организован производственный выпуск вакцины в Одессе и Санкт-Петербурге. Предложена очаговая аллергическая проба с герпетической вакциной, впервые открывшая возможность неинвазивной этиологической диагностики внутриглазного герпеса. На Международной конференции по глазным инфекциям (Иерусалим, 1995 г.) [5] указанные методики получили название “Русский метод иммунодиагностики и иммунотерапии” (J. Gordon).
3. Система щадящих микрохирургических методик, адаптированных к лечению активного ГК и его исходов (аргонлазеркоагуляция, микродиатермокоагуляция, внутриглазная инфузия полудана, бесшовный метод кератопластики, эксцентричная неперфорирующая миникератопластика, полная стромэктомия + кератопластика, тройная процедура и др.). Разработаны рациональные методы послеоперационной терапии, микродиатермокоагулятор для лечения язв роговицы и набор инструментария для лечебной кератопластики (совместно с Казанским медико-инструментальным заводом).
Учитывая характер данного офтальмологического издания, представляется целесообразным сделать акцент на практических аспектах лечения ГК. Лечение типичной формы ГК – эпителиального древовидного кератита – мы начинаем с частых инстилляций (6–8 раз в день) одного или двух из нижеследующих противовирусных средств: полудана, пирогенала в концентрации 20 мг в 1 мл дистиллированной воды, рекомбинантного интерферона реаферона либо 3–5 разовых аппликаций 3% мази ацикловира.
Рандомизированные исследования, проведенные в группах больных древовидным кератитом (общая численность 700 человек), показали, что большая часть приведенных противовирусных препаратов, включая 0,25–0,5% мази флореналь и теброфен, обладает примерно одинаковым терапевтическим потенциалом с Офтан ИДУ (0,1% 5-йод-2-дезоксиуридин). Первое противовирусное средство Офтан ИДУ приводит к выздоровлению 2/3 больных древовидным кератитом, и при использовании его в сроки до 3 нед дает меньше побочных реакций, чем мази флореналь, теброфен и бонафтон. Определенными преимуществами перед Офтаном ИДУ обладают полудан и ацикловир. Они заключаются в лучшей переносимости, возможности более длительного применения, а также использования других путей введения (периокулярные инъекции для полудана и пероральное применение для ацикловира), что особенно показано в случаях сочетанного поражения эпителия, стромы и наличия сопутствующего иридоциклита у больных древовидным кератитом.
Целесообразно комбинированное применение интерферона или интерфероногенов с химиотерапевтическими препаратами (Офтан ИДУ, ацикловир), обеспечивающее синергидный эффект. При этом число местных аппликаций каждого из препаратов снижают вдвое (см. таблицу).
Согласно данным Центра по офтальмогерпесу, работающему на базе НИИ глазных болезней РАМН, наилучшим образом отвечают современным требованиям, предъявляемым к лечению активных проявлений герпетической болезни глаз, два химиотерапевтических противовирусных препарата: полудан и ацикловир. Характерно, что оба препарата наряду с выраженным ингибирующим воздействием на вирус простого герпеса обладают минимальным побочным действием (токсико-аллергические реакции). Это позволяет применять их достаточно длительно не только местно в виде инстилляций и аппликаций, но и системно, что является основной предпосылкой для успешной терапии тяжелых проявлений офтальмогерпеса.
Полудан – биосинтетический полирибонуклеотидный комплекс, обеспечивающий при субконъюнктивальном введении выработку интерферона не только в тканях глаза, но и в крови (рис. 1, 2). Ацикловир – ациклический аналог дезоксигуанозина. В эксперименте на модели экспериментального герпетического кератита кроликов, а также в клинике установлено возрастание терапевтического эффекта при комбинированном применении этих двух базовых препаратов, обладающих различным механизмом ингибирующего воздействия на внутриклеточный вирус. Это выразилось в достоверном сокращении сроков лечения и увеличении числа вылеченных больных при снижении дозы каждого из препаратов. Сравнительные контрольные исследования показали, что совместное применение этих двух базовых препаратов представляется наиболее эффективным.
Третий базовый препарат – это герпетическая вакцина, ставшая основой впервые разработанной противорецидивной терапии офтальмогерпеса. Препарат создан в Институте вирусологии им. Д.И. Ивановского РАМН, а новые его возможности раскрыты в НИИ глазных болезней РАМН.
Препарат используют у больных, страдающих частыми обострениями офтальмогерпеса, применяя в межрецидивный период в виде повторяющихся каждые полгода курсов внутрикожных инъекций. Противорецидивный эффект вакцинации, заключающийся в активации клеточного иммунитета, усиливается при сочетании с местным применением индуктора интерферона полудана и системным использованием средств неспецифической иммунотерапии (тималин, тактивин и др.).
При отсутствии четких признаков ремиссии процесса при лечении противовирусными медикаментами в течение первых 3–5 дней, а нередко и в первый день обращения мы прибегаем к микродиатермокоагуляции – соскобу. Комбинированное лечение способствует существенному сокращению среднего срока лечения. Процедуру проводят с использованием специально созданного для роговицы электрохирургического высокочастотного аппарата АХВЧ-5-1-O (НПО “Экран”), обладающего плавной регулировкой, звуковой и световой сигнализацией, набором микроэлектродов. Данная методика эффективна в лечении вирусных и гнойных язв роговицы, обладает рядом преимуществ перед другими микрохирургическими приемами (механический соскоб, криопексия, лазеркоагуляция и др.), учитывая доступность прибора по цене, а также возможность использования в глазном кабинете поликлиники. Использование эксимерного лазера не решает проблему излечения активных стромальных кератитов, однако является весьма успешным в устранении поверхностных помутнений в центральной зоне роговицы после вирусных кератитов.
Лечение стромального ГК требует не только местного (инстилляции, аппликации), но и системного введения противовирусных средств. К ним в первую очередь могут быть отнесены обладающие противовирусной и иммуномодулирующей активностью полудан и реаферон, а из химиотерапевтических средств – ацикловир и его производное вальтрекс в таблетках. Следует отметить широту противовирусного спектра полудана, реаферона, оказавшихся эффективными в лечении аденовирусных кератоконъюнктивитов [9, 11].
Полудан в течение последних 10 лет зарекомендовал себя как эффективное и нетоксичное противовирусное средство. Препарат, применяемый для лечения герпетических кератоиридоциклитов в виде повторных периокулярных и внутриглазных инъекций, позволяет получить выраженный терапевтический эффект у 50–60% больных. По своей эффективности полудан не уступает ацикловиру, при этом стоимость курсовой дозы полудана (20 ампул по 10 ед.) в 2–3 раза ниже таковой при использовании ацикловира перорально (40–50 таблеток по 200 мг). Комбинированное применение обоих препаратов позволяет добиться успеха у 70% больных с признаками герпетического кератоиридоциклита (увеакератита). Исследования, проведенные НИИ глазных болезней РАМН совместно с кафедрой иммунологии РГМУ (Л.В. Ковальчук, А.С. Павлюк, Т.Ю. Ульянова), показали, что введение полудана приводило к значительному усилению активности естественных киллеров, исходно сниженной у больных офтальмогерпесом. Исследования влияния полудана на иммунологические показатели в системе in vitro показывают, что препарат стимулирует не только естественную цитотоксичность (рис. 3), но и функционирование других иммунокомпетентных клеток, в регуляции активности которых существенную роль играет интерферон [7, 9]. Впервые установлено антиапоптозное влияние полудана на культуру лимфоцитов [12]. На основе соединения полудана с аутокровью больного разработана (совместно с Е.А. Каспаровой) экспресс-аутоцитокинотерапия, позволившая повысить эффективность лечебных мероприятий при тяжелых формах герпес-вирусного кератоиридоциклита [8] (рис. 4).
Методика применения реаферона сходна с таковой при использовании полудана, терапевтическая эффективность ее несколько ниже, однако побочные аллергические реакции встречаются чаще.
В комплексном лечении стромальных форм ГК с определенным успехом используют иммуномодуляторы – тималин, тактивин, левамизол, ликопид, нуклеинат натрия и др.
В процессе изучения находятся следующие отечественные интерфероногены и иммуномодуляторы: ридостин, циклоферон, амиксин, ларифан, xeлeпин, актимол и дp. [5]. Клинические испытания первого отечественного химиопрепарата для перорального применения бонафтона не подтвердили его терапевтическую эффективность, но свидетельствовали о токсичности препарата [7].
Наш опыт подтверждает необходимость использования при лечении ГК минимума лекарственных средств помимо противовирусных препаратов: инстилляций мидриатиков, растворов антибиотиков или антисептиков при наличии патогенной микрофлоры в мазке с конъюнктивы или профилактически при обширных язвенных дефектах. Опыт показывает, что медикаментозная аллергия развивается как вследствие индивидуальной непереносимости противовирусных средств, так и при перегруженности лечения антибиотиками, витаминными препаратами и т.д. В этих случаях необходимо определить минимум хорошо переносимых противовирусных средств (растворы пирогенала или полудана), внутрь назначить антигистаминные препараты, местно – примочки с раствором борной кислоты и инстилляции кромогликата натрия (лекролина). Применение кортикостероидов противопоказано при язвенных формах ГК. В то же время, учитывая, что герпес-вирусная инфекция роговицы сопровождается целым рядом местных иммунных реакций, применение кортикостероидов показано в качестве патогенетической терапии при стромальных формах, протекающих без изъязвления. Мы предпочитаем в таких случаях применять инстилляции 0,01% дексаметазона “под зонтиком” противовирусной терапии через 1–2 нед после ее начала. Использование больших доз кортикостероидов (субконъюнктивальные инъекции) без должного противовирусного прикрытия способно привести к тяжелейшим последствиям вплоть до гибели глаза (перфорация роговицы, вторичная глаукома, гнойный иридоциклит, эндофтальмит).
При всех успехах противовирусной терапии у 30–35% больных с герпетическими кератоиридоциклитами не удается добиться излечения медикаментозным путем. В этих случаях лечение необходимо дополнять микрохирургическими методами. Наш опыт, включающий свыше 1000 операций при активном ГК и его исходах, свидетельствует о высокой эффективности ранней послойной лечебной кератопластики. Успех операции во многом определяется использованием щадящих методик операции, радикальным иссечением зоны воспаления с помощью усовершенствованного инструментария и рациональной послеоперационной терапией (интерфероногены, ацикловир, противогерпетическая вакцинация). Купирование процесса удается у 92% больных, повышение остроты зрения в пределах 0,2–1,0 с переносимой коррекцией – у 60% больных (рис. 5).
Основой противорецидивного лечения является противогерпетическая вакцинация, показанная двум группам риска: 1) больным с наличием частых обострении ГС (1 раз и более в год); 2) больным, перенесшим лечебную кератопластику. Для вакцинации используют культуральную инактивированную герпетическую вакцину, выпускаемую Санкт-Петербургским НИИ вакцин и сывороток. Схемы вакцинации подробно описаны в нашей монографии “Офтальмогерпес”. В сочетании с вакциной местно и системно применяют интерфероногены и иммуномодуляторы. Комплексное противорецидивное лечение проводится в течение 3–5 лет, способствует прекращению (60%) рецидивов или их урежению (26% больных). Лишь у 10–11% больных частота рецидивов не изменялась.
В последние годы с целью профилактики рецидивов генитального герпеса и офтальмогерпеса предпринимаются попытки длительного лечения (свыше 1 года) ацикловиром перорально. Применение такого рода лечения при ГК нам представляется весьма проблематичным как с медицинской, так и с экономической точки зрения.
В заключение хотелось отметить, что дифференцированное и своевременное использование представленных методов и средств лечения ГК во многом решеют проблему успешного контроля и управляемости герпес-вирусной инфекции роговицы.

Герпетический кератит глаза лечение которого зависит от стадии заболевания, представляет собой воспаление роговицы, спровоцированное вирусом герпеса. Данная форма кератита наиболее сложна, и встречается чаще других.
При отсутствии медицинской помощи герпетический кератит грозит потерей зрения и другими серьезными осложнениями. Развиться данное заболевание может после активизации вируса герпеса под влиянием таких факторов:
- сильный стресс, депрессия;
- длительная болезнь, повлекшая за собой ослабление иммунитета;
- переохлаждение;
- злоупотребление алкоголем.
Женщины заболевают герпетическим кератитом под влиянием гормональных перестроек организма: при беременности, в период менопаузы, при длительных и сильных моральных потрясениях, при истощении от сильных физических нагрузок и жестких диет.
Как узнать, что это именно кератит
Герпетическая форма характеризуется следующей клинической картиной:
- сильная боль в пораженном глазу;
- покраснение и дискомфорт кожи в зоне вокруг глаз;
- покраснение глазного белка;
- чувство, как будто в глаз попал песок;
- высокая светочувствительность, невозможность полноценно открыть глаза на солнечном свету;
- жжение и зуд в глазах и вокруг глаз;
- помутнение роговицы, потеря блеска;
- ухудшение самочувствия;
- лихорадка, температура;
- обостренная чувствительность кожного покрова у пораженного глаза;
- ухудшение остроты зрения.
Заболевание классифицируется на первичный и постпервичный кератит. Первый возникает после первого заражения вирусом герпеса, постпервичный – при снижении иммунитета и вирусе, уже локализующемся в организме, чаще это рецидив.
Герпетический кератит глаза лечение патологии
Терапия чаще всего проводится в стационаре под непрерывным наблюдением. Длится лечение от двух недель до одного месяца. Заключается оно в комплексном подходе, когда одновременно устраняется причина – вирус герпеса, и следствие.
В ходе терапии в зависимости от степени поражения тканей применяются:
- капли с противовирусным действием;
- стероидные противовоспалительные средства;
- физиотерапевтические методы;
- методики хирургического вмешательства.

Последнее актуально в особо запущенных случаях, когда классическая терапия не способна дать какие-либо результаты.
Допускается лечение по методам народной медицины. Однако эти способы подходят только в качестве вспомогательных мер, и их действие также нуждается в постоянном врачебном контроле.
При поверхностном поражении кератитом врачи назначают средства местного действия: мази Зовиракс, Ацикловир. Их закладывают в конъюнктивный мешок – под нижнее веко три раза в день. Мази пресекают жизнедеятельность вирусов, в результате чего отек и воспаление быстро уменьшаются.
Многим пациентам с поверхностным герпетическим кератитом показаны закапывания глаз раствором Идоксиуридина 0,1%. Курс лечения длится до двух недель, количество закапываний – 5-8 раз в сутки.
Также для закапываний назначаются:
- Интерлок. 10 000 МЕ на 0,1 мл буфера фосфатного. Курс и дозировки подбираются врачом индивидуально.
- Реаферон. 5 000 МЕ на 1 мл. дистиллированной воды. Курс – 6 дней по несколько процедур в день.
- Фрон. Разбавлять не нужно. Закапывать 6 раз в день по 2 капли в течение недели. Внутримышечно назначают витамины B1 и B2. Внутрь – витамин C.
При глубоком поражении глаз кератитом лечение более сложное. Показаны такие препараты:
- Мази Зовиракс, Ацикловир или Виролекс. Закладывать в конъюнктивный мешок 5 раз в сутки.
- Для инстилляций препарат Реаферон. Дозировка и длительность курса определяется врачом на основании состояния пациента.
- Витамин B2 и различные иммуномодуляторы для усиления сопротивляемости организма.
- Инъекции Лидокаина для устранения боли.
Если течение болезни затягивается, назначаются нестероидные противовоспалительные медикаменты. Их выбор тоже осуществляется индивидуально.
Физиотерапия при кератите

Из всех современных методик физиотерапии при кератите наиболее эффективен электрофорез. Эта процедура подавляет активность вирусов и заметно тормозит воспалительный процесс. Электрофорез делают с использованием препаратов для глаз с противовирусным действием. В них смачивают ватные тампоны и накладывают на больной глаз непосредственно перед процедурой.
Народные рецепты от герпетического кератита
Против боли и воспаления помогают домашние средства:
- Облепиховое масло. Закапывать по 1 капле каждый час во время бодрствования на протяжении двух дней, затем каждые 2-4 часа еще несколько дней. Масло снижает светобоязнь и обезболивает.
- Сок чистотела. Отлично помогает при гнойных очагах. Сок нужно смешать с раствором прополиса 1:3 и закапывать в больной глаз перед сном по две капли.
- Глиняный компресс. Глину развести водой, чтобы она стала пластичной и густой. Сделать лепешку толщиной 3 см. и приложить ко лбу на 1,5-2 часа. Делать так утром и вечером.
Операция герпетического кератита
Тип операции подбирается, исходя из тяжести случая. Если кератит поразил только верхние слои, проводится соскабливание эпителия, пораженного вирусом. При особо сложной клинической картине назначается резекция тканей. Ход операции тоже всегда планируется индивидуально, так как область патологии локализуется на разных местах и в различных масштабах.
В заключение
Герпетический кератит сложно вылечить раз и навсегда. Рецидивы возможны при каждом снижении иммунитета независимо от причины. Поэтому пациентам следует внимательно следить за своим здоровьем:
- поддерживать организм правильным питанием и физкультурой;
- отказаться от вредных привычек;
- избегать стрессов и тяжелой работы.
При правильном образе жизни герпетический кератит глаза лечение и дальнейший прогноз не будут вас волновать. Думать об этом не придется.
Понравилось? Поделитесь в социальных сетях!
Не нашли ответ на свой вопрос?
Оставьте заявку и наши специалисты
проконсультируют Вас.
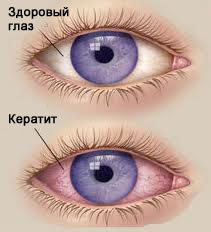
Кератит — заболевание роговой оболочки глаза воспалительного характера, проявляющееся преимущественно болью и покраснением глаза, помутнением и изъязвлением роговицы.
Причинами кератита могут стать повреждения глаза (механическое, химическое, термическое и др.), различные инфекции (бактериальные, вирусные, грибковые), а также хронические заболевания, нарушения обмена веществ, аллергии и т.д..
Наиболее часто встречаются вирусные и бактериальные кератиты. Основными возбудителями вирусных кератитов являются вирусы простого герпеса (герпетический кератит) и аденовирусы, они возникают также при таких вирусных заболеваниях, как ветряная оспа, корь. Бактериальные кератиты чаще всего вызываются кокковой флорой, синегнойной палочкой, возбудителями туберкулеза, сифилиса.
Часто заболеванию предшествует микротравма роговицы, эрозия эпителия роговицы, царапина роговицы. Важную роль играет состояние общего и местного иммунитета; оно же в значительной степени определяет характер течения кератита и тяжесть патологического процесса.
Особо выделяют кератиты, развившиеся после ношения контактных линз. Причиной развития кератита может быть и предшествующая внутриглазная операция.
Кератиты являются серьезным заболеванием и требуют оказания скорой медицинской помощи. При отсутствии должного лечения кератит может стать причиной помутнения роговицы и образования бельма, спаек в области значка, что в свою очередь приводит к снижению остроты зрения. При проникновении инфекции вглубь глаза может развиться гнойная язва роговицы, исходом которой будет гибель глаза как органа. В особо тяжелых ситуациях больного госпитализируют, для проведения комплексной противовоспалительной терапии.
Если у Вас наблюдаются подобные симптомы, советуем записаться на прием к врачу. Своевременная консультация предупредит негативные последствия для вашего здоровья. Телефон для записи +7 (495) 292-39-72
Диагноз кератита и его этиологические формы устанавливают на основании особенностей клинической картины и данных анамнеза.
Кератит клинически выглядит как нарушение прозрачности роговицы. В основе воспалительного помутнения лежит инфильтрат – скопление в ткани роговицы клеточных элементов типа лейкоцитов, лимфоцитов, гистиоцитов, плазматических и других клеток.
Основной метод исследования при кератите — биомикроскопия глаза, позволяющая достаточно точно определить размеры и характер поражения, а также обнаружить признаки кератита на ранних стадиях заболевания.
Важную роль в диагностике воспалительного заболевания играет глубина расположения инфильтрата, которая может быть установлена как биомикроскопически, так и с помощью метода бокового освещения.
При подозрении на гнойное поражение роговицы, о чем свидетельствует желтоватый оттенок инфильтрата, проводят срочное бактериоскопическое исследование и определяют проходимость слезных путей.
При кератите применяются:
- бактериологическое и цитологическое исследование эпителия конъюнктивы и роговицы,
- иммунологические методы исследования,
- аллергические диагностические пробы с различными антигенами,
Основным методом лечения кератитов является применение глазных капель, инстилляций, мазей и лекарственных пленок, содержащих современные антибактериальные, противовоспалительные и другие препараты (противогерпетические средства, иммуномодуляторы, и т.д.) в зависимости от вида кератита. При тяжелых поражениях роговицы препараты вводят субконъюнктивально (производятся инъекции в нижнюю конъюнктиву глазного яблока или наружный угол глаза).
Наряду со специфическими средствами при кератитах различной этиологии местно назначают мидриатики, новокаиновые блокады по ходу поверхностной височной артерии, растворы антисептиков, средства, способствующие эпителизации язв.
При снижении остроты зрения назначают физиотерапевтическое лечение электрофорез и фонофорез с ферментами, биогенные стимуляторы. Также при лечении кератита применяются озонотерапия, внутривенное лазерное облучение крови (ВЛОК).
При отсутствии эффекта от консервативной терапии в течение 1 месяца и резком снижении остроты зрения больным назначают хирургическое лечение.
Прогноз лечения во многом определяется причиной кератита, локализацией и характером инфильтрата, сопутствующими осложнениями. При своевременном и рациональном лечении поверхностные инфильтраты полностью рассасываются либо остаются легкие помутнения типа облачка. Глубокие кератиты, протекающие как с изъязвлением, так и без него, способны приводить к значительному снижению остроты зрения, астигматизму.
Аннотация научной статьи по клинической медицине, автор научной работы — Егоров В.В., Смолякова Г.П., Гохуа Т.И., Борисова Т.В.
Clinical evaluation of new physiotherapeutic technology in the complex treatment of bacterial inflammation of the cornea
В.В. ЕГОРОВ12, Г.П. СМОЛЯКОВА12, Т.И. ГОХУА1, Т.В. БОРИСОВА1
Институт повышения квалификации специалистов здравоохранения МЗ ХК, 680009, г. Хабаровск, ул. Краснодарская, д. 9
Клиническая оценка новой физиотерапевтической технологии в комплексном лечении бактериального воспаления роговицы
Егоров Виктор Васильевич — доктор медицинских наук, профессор, директор, заведующий кафедрой офтальмологии ИПК, тел. (4212) 22-51-21, e-mail: naukakhvmntk@mail.ru
Смолякова Галина Петровна — доктор медицинских наук, профессор, врач-офтальмолог клинико-экспертного отдела, профессор кафедры офтальмологии ИПК, тел. (4212) 22-51-21, e-mail: naukakhvmntk@mail.ru
Гохуа Татьяна Ивановна — врач-физиотерапевт, тел. (4212) 72-27-92, e-mail: naukakhvmntk@mail.ru
Борисова Татьяна Владиславовна — заведующая кабинетом физиотерапии, тел. (4212) 72-27-92, e-mail: naukakhvmntk@mail.ru
Лонгидаза получила широкое распространение в разных областях клинической медицины при воспалениях, травмах и хирургических вмешательствах [18].
Экспериментальная стадия изучения влияния этого препарата при субконъюнктивальном введении на репаративный процесс в зоне хирургической травмы при антиглаукоматозных операциях показала высокий лечебный эффект и отсутствие токсического и аллергического воздействия на роговицу, склеру и другие ткани глаза [19, 20]. Данное обстоятельство и высокий уровень безопасности позволили авторам рекомендовать лонгидазу для клинического применения в офтальмологии. В связи с этим особый интерес в практическом плане прежде всего представляет выбор оптимальных и атравматических способов топического введения лонгидазы.
Согласно данным литературы, для увеличения биодоступности лекарственных препаратов наибо-
лее перспективными в настоящее время являются физиотерапевтические технологии, преимущества которых основываются на суммации лечебного эффекта лекарственного препарата и физического фактора [21, 22].
Несмотря на явные преимущества использования магнитофотофореза лонгидазы при БК, данная медицинская технология пока не получила должного применения.
Цель работы — улучшить результаты лечения пациентов с БК путем включения магнитофотофо-реза лонгидазы в их комплексную терапию.
Материал и методы
В клиническом исследовании участвовали 28 пациентов с БК в возрасте от 28 до 57 лет. В соответствии с Федеральными клиническими рекомендациями [25] среди них преобладали пациенты БК средней степени тяжести (19 чел.), реже — с тяжелой степенью тяжести (9 чел.). Клиническая картина БК характеризовалась: острым началом, следующими клиническими проявлениями заболевания: отеком век, роговичным синдромом, отделяемым из конъюнктивальной полости, смешанной инъекцией, снижением остроты зрения до 0,01-0,09 отн. ед. На роговице, чаще в центре либо парацен-трально, диагностировали инфильтрат размером от 4 до 9 мм с изъязвлением от 1/3 до половины толщины роговичной стромы с выраженным пери-фокальным отеком. У части пациентов (12 чел.) в передней камере (ПК) имел место фибринозный (8 чел.) либо гнойный (4 чел.) экссудат.
Возбудителем заболевания по результатам бактериологических исследований конъюнкти-вального секрета явились S.aureus (16 чел.), реже Pseudomonas aeruginosa (8 чел.) и смешанная микрофлора, представленная ассоциацией S.epidermidis и Escherichia coli (4 чел.). В большинстве случаев инфицированию предшествовали микротравмы роговицы (22 чел.) и нарушение режима обработки и ношения контактных линз (6 чел.).
Всем пациентам при поступлении на стационарное лечение проводили промывание антисептиками слезно-носовых путей и назначали стандартную системную и местную антибактериальную терапию. После купирования инфекции лечение БК дополняли стимуляторами репаративных процессов (баларпан, корнерегель, витА-ПОС). С первого дня пребывания в стационаре 16 пациентам (основная группа наблюдения) проводили магнитофотофорез лонгидазы; 12 пациентам (контрольная группа наблюдения) — магнитофототерапию без лонгидазы. Сформированные группы пациентов были сопоста-
вимы по полу, возрасту, клиническим проявлениям и степени тяжести БК (р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Сравнительная характеристика клинического течения БК в основной и контрольной группах
Клинические признаки Группы наблюдения р — достоверность межгрупповых различий
Контрольная п = 12 чел. Основная п = 16 чел.
Длительность воспаления (М±т, сут) 19,2±1,1 13±0,5 0,05
Контрольная 95,0±2,0 78,7±22 5,0±0,1
В динамике лечения — 3 сут.
Основная 51,2±0,9 25,9±1,05 19,0±0,9 17,0±0,5 5,0±0,3
Контрольная 81,4±2,3 47,9±1,9 12,5±1,0 5,0±0,2 1,1±0,1 р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
1. В клиническом исследовании получены доказательства о достоверных различиях в течении БК у пациентов основной группы, получивших в составе комплексной терапии магнитофотофорез лонгидазы, по сравнению с контрольной группой, комплексное лечение которой включало магнито-фототерапию без лонгидазы.
2. Установлено, что под влиянием магнитофото-фореза лонгидазы у пациентов с БК исчезновение таких клинических признаков воспаления, как ро-говичный синдром, смешанная инъекция глазного яблока, рассасывание перифокального отека и инфильтрата роговицы, наступает на 4-5 дней раньше, чем у пациентов в контрольной группе наблюдения.
3. При изучении лечебного эффекта магнитофотофореза лонгидазы по составу мигрирующих клеток в очаг воспаления выявлено сокращение продолжительности воспалительно-дегенеративной
фазы, более быстрое развитие регенераторных реакций, уменьшение плотности фибробластов, которые ограничивают вероятность развития в исходе БК грубых рубцовых помутнений роговицы.
4. Результаты исследования функционального состояния оптической системы по показателю восстановления остроты зрения указывают на ее возрастание в 2 раза у пациентов основной группы (после завершения магнитофотофореза лон-гидазы) в сравнении с пациентами контрольной группы, которая сочетается с положительной динамикой КДК, отображающего выраженность субъективных симптомов дискомфорта.
5. Полученные в клиническом исследовании результаты, обобщающие первый опыт использования магнитофотофореза лонгидазы, при лечении БК открывают новые возможности для профилактики грубых воспалительных рубцовых помутнений роговицы и восстановления зрения.
1. Сидиков З.У., Мираюбова O.A. Эффективность лечебной кератопластики при гнойных поражениях роговицы // Вопросы клинической офтальмологии: Сб. тезисов. — Куйбышев, 1980. — С. 40-42.
2. Волкович Т.К., Королькова Н.К., Хорошенькая Н.В. Бактериальный кератит: этиология, патогенез // Вестник Витебско-
го государственного медицинского университета. — 2011. — Т. 10, №3. — С. 6-11.
3. Шаимова В.А. Бактериальный кератит. Клинико-иммуноло-гические особенности течения, прогноза, лечения разных форм заболевания: автореф дис. . д.м.н. — Челябинск, 2007. — 44 с.
4. Майчук Ю.Ф. Глазные инфекции // Русский медицинский журнал. — 1999. — №1. — С. 7.
5. Шаимова В.А. Перекисное окисление липидов и антиокси-дантная защита при заболевании глаз // Вестник офтальмологии. — 2002. — Т. 118, №3. — С. 56-57.
6. Каспарова Е.А. Гнойные язвы роговицы: клиника, диагностика, консервативное лечение // Вестник офтальмологии. — 2015. — №6. — С. 106-119.
7. Каспаров. А.А. Офтальмогерпес. — М.: Медицина, 1994. — С. 106-108.
8. Майчук Д.Ю., Васильева О.А., Руссу Л.И., Мезенцева М.В. Сравнительная клинико-иммунологическая оценка вариантов терапии инфильтративного поражения роговицы после перенесенного аденовирусного кератоконъюнктивита // Вестник офтальмологии. — 2015. — №4. — С. 49-55.
9. Улащик В.С. Физико-фармакологические методы лечения и профилактики. — Минск: Беларусь, 1979. — 223 с.
10. Чеснокова Н.Б. Роль протеолитических ферментов и их ингибиторов в патологии роговицы: автореф. дис. . д.м.н. — М., 1991. — 34 с.
11. Сосин И.Н., Буявых А.Г. Физическая терапия глазных болезней. — Симферополь: Таврия, 1998. — 248 с.
12. Назаренко К.А., Хороших Ю.И., Запускалов И.В. Энзимо-терапия в офтальмологии // Вестник офтальмологии. — 2006. — №3. — С. 36-42.
13. Доценко В.Л., Нахикян Н.И., Соловьева Н.И. и др. Протео-литические ферменты слезной жидкости как факторы патогенеза хронических язв роговой оболочки // Вопросы медицинский химии. — 1990. — №3. — С. 73-76.
14. Орехова Э.М., Конгурова Т.В., Лукьянова Т.В. и др. Применение препарата Лонгидаза 3000 Ме при заболеваниях, сопровождающихся патологией соединительной ткани / Пособие для врачей. — М., 2008. — 26 с.
15. Круглова Л.С., Дворников А.С. Опыт применения фотофоре-за и фонофореза с лонгидазой у пациентов с ограниченной склеродермией и вульгарными угрями // Российский журнал кожных и венерических заболеваний. — 2010. — №6. — С. 8-10.
16. Дворников А.С., Круглова Л.С., Минкина О.В. Фотофорез Лонгидазы у пациентов с ограниченной склеродермией // Физиология и патология иммунной системы. — 2007. — Т. 11, №6. — С. 10-19.
17. Макарова А.С. Экспериментальное изучение протеолитиче-ской профилактики избыточного рубцевания в хирургии глауком: автореф. дис. . к.м.н. — М, 2013. — 24 с.
18. Ходырева Л.А, Дударева А.А., Карпов В.А. Лонгидаза в комплексной терапии хронического простатита // Эффективная фармакотерапия. Урология и нефрология. — 2014. — №3(32). — С. 10-14.
19. Шмырева В.Ф., Иванова А.С., Федоров А.А. и др. Экспериментальное исследование ферментного препарата Лонгидаза как средства профилактики избыточного рубцевания после анти-глаукомных операций // Всероссийская школа офтальмолога, 11-я: Сборник научных трудов. — М., 2012. — С. 274-281.
20. Шмырева В.Ф., Иванова А.С., Федоров А.А. и др. Медико-биологическое исследование лонгидазы. Часть 2 // Глаукома. — 2012. — №1. — С. 3-7.
21. Ванштейн Е.С., Зобина Л.В. Физиотерапия в офтальмологии / В кн. Курортология и физиотерапия. — М.: Медицина, 1985. — С. 566-590.
22. Егоров В.В., Смолякова Г.П., Гохуа Т.И., Борисова Т.В. Магнитофорез кудесана в комбинации с деринатом в лечении язвенных поражений роговицы // Новые технологии диагностики и лечения заболеваний органа зрения в Дальневосточном регионе: Сборник научных работ. — Хабаровск, 2012. — С. 184-187.
23. Каменских Т.Г., Райгородский Ю.М. Магнитотерапия и ее сочетание с другими физическими факторами // Окулист. — 2004. — №12. — С. 10-12.
24. Скрипкин Ю.К., Богуш П.Г., Круглова Л.С., Дворников А.С. Опыт применения Лонгидазы методом фотофореза у пациентов с ограниченной склеродермией // Вестник дерматологии и венерологии. — 2007. — №5. — С. 57-59.
25. Арестова Н.Н., Бржеский В.В., Вахова Е.В., Яни Е.В. Клиника, диагностика и консервативная терапия бактериальных язв роговицы / Федеральные клинические рекомендации. — М., 2014. — 16 с.
26. Воспаление. Руководство для врачей / Под ред. В.В. Серова, В.С. Паукова. — М.: Медицина, 1995. — 640 с.
Читайте также:


