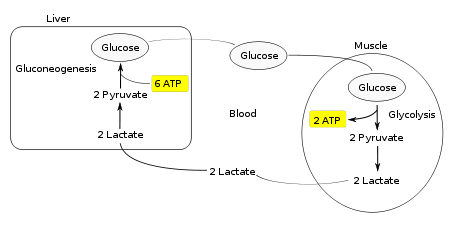
Цикл кори это глюконеогенез
Ткани и органы. Мышцы
Метаболическая регуляция мышечного сокращения
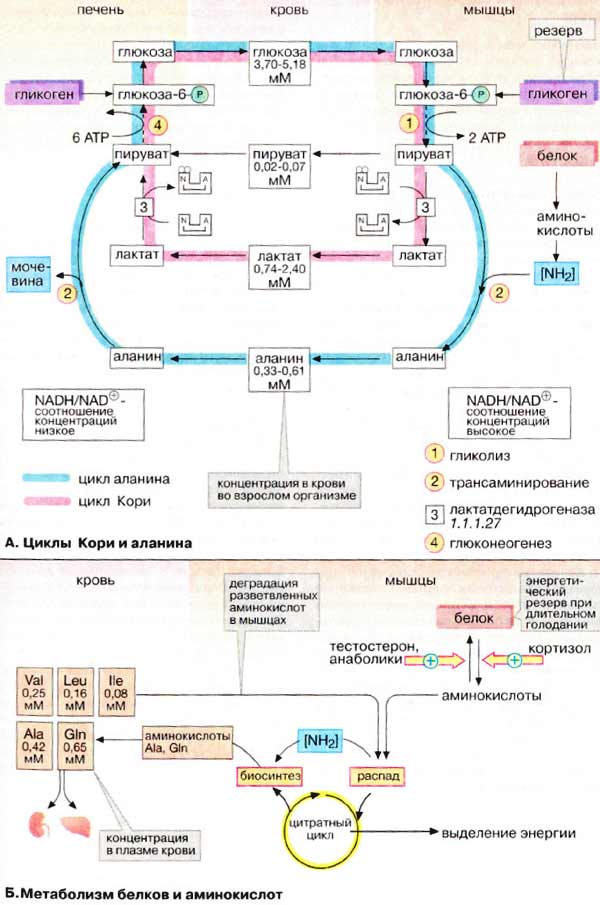
А. Циклы Кори и аланина
В клетках, не содержащих митохондрий (например, в эритроцитах), или в тканях при недостаточном снабжении кислородом (например, в активно работающих мышцах) АТФ (АТР) синтезируется за счет процесса превращений глюкозы в лактат, т. е. за счет процесса брожения (= анаэробного гликолиза , см. рис. 153). Лактат переносится кровью в печень, где в процессе глюконеогенеза с затратой АТФ (см. рис. 157) вновь конвертируется в глюкозу ( цикл Кори ).
При интенсивной работе мышцы максимально активируется гликолиз. Продукт гликолиза, пировиноградная кислота (пируват) накапливается в цитоплазме и недостаточно быстро поступает в митохондрии, если они из-за недостатка кислорода не готовы к окислению пирувата. В анаэробных условиях пируват в реакции, катализируемой лактатдегидрогеназой (см. рис. 103) (заключительный этап гликолиза) восстанавливается до лактата. Одновременно НАДН (NADH), кофермент лактатдегидрогеназы, окисляется до НАД + (NAD + ), который вновь используется на окислительном этапе гликолитического пути. Этой реакции способствует относительно высокое отношение НАДН/НАД + в мышечной ткани. Лактат диффундирует в кровь и поступает в печень, где конвертируется в глюкозу. Таким образом, образование лактата временно заменяет аэробный метаболизм глюкозы и частично переносит этот процесс из мышц в печень.
Обратная связь, подобная циклу Кори, существует в цикле аланина , в котором также участвует пируват . Цикл аланина берет начало с протеолиза белков. Образующиеся аминокислоты в результате трансаминирования в присутствии ферментов превращаются в α-кетокислоты (на схеме не приведено, см. рис. 181), которые в основном включаются в цикл трикарбоновых кислот (цитратный цикл) (см. рис. 183).Одновременно в реакции, катализируемой аланинтрансаминазой, аминогруппы из разных аминокислот переносятся на имеющийся субстрат, пируват. Образующийся аланин поступает в кровь и переносится в печень. Таким образом, цикл аланина служит каналом передачи азота и предшественников глюкозы в печень, которая является местом синтеза конечных продуктов азотистого обмена, например мочевины (см. рис. 185).
Следует напомнить, что при анаэробном гликолизе образуются кислоты, которые, не принимая участие в последующем обмене, существуют в форме анионов. Поэтому при интенсивном анаэробном гликолизе рН мышечной клетки может понизиться настолько, что сокращение станет невозможным. Обычно этого не происходит благодаря быстрому выходу кислых метаболитов (лактата и пирувата) в кровь, которая также может оказаться закисленной (метаболический ацидоз).
Б. Метаболизм белков и аминокислот
Скелетные мышцы активно участвуют в метаболизме аминокислот. Это наиболее важный участок деградации разветвленных аминокислот (Val и Ile, см. с. 402). Ряд других аминокислот также деградируются преимущественно в мышцах. Одновременно идет ресинтез и высвобождение в кровь аланина и глутамина . Эти аминокислоты служат переносчиками азота, образующегося при расщеплении белков, в печень (цикл аланина) и почки (см. рис. 319).
При голодании мышечные белки служат энергетическим резервом организма. Они гидролизуются до аминокислот, которые поступают в печень. Здесь углеродный скелет аминокислот конвертируется в промежуточные продукты цитратного цикла, в том числе в ацетоацетил-КоА и ацетил-КоА (см. рис. 183). Эти амфиболические соединения окисляются в цикле трикарбоновых кислот или включаются в процесс глюконеогенеза.
Синтез и расщепление мышечных белков контролируются гормонами. Тестостерон и синтетические анаболики стимулируют биосинтез белка; напротив, кортизол подавляет образование мышечных белков.
Белки актин и миозин содержат остатки гистидина, метилированного на стадии посттрансляционной модификации. При расщеплении этих белков образуется 3-метилгистидин, который дальше не разрушается. Количество метилгистидина в моче служит мерой деградации мышечных белков.
Глюконеогенез – синтез глюкозы из неуглеводных продуктов de novo. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Протекает в основном в печени и менее интенс. в корковом в-ве почек, в слиз. об-ке кишеч.Большинство р-ций глюконеогенеза протекает за счёт обратимых р-ций гликолиза и катализируется теми же ферментами. Однако 3 реакции необратимы. На этих стадиях р-ции глюконеогенеза протекают другими путями.

ПВК включ. в глюконеогенез, а образ-я глюкоза поступает в кровь и поглощ. скелет. м-цами - "глюкозо-лактатным циклом", или "циклом Кори", -обесп. утилизацию лактата; предотвращает его накопление- опасное снижение рН (лактоацидоз). Часть ПВК, обр. из лактата, окисляется печенью. Энергия ок. может исп. для синтеза АТФ, необхо. для р-ций глюконеогенеза. Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Аланин из мышц переносится кровью в печень, где преобразуется в ПВК, который частич. окисляется и частично включ. в глюкозонеогенез.
99.Глюконеогенез.см.выше и в метаболизме*
100-102. Аэробное окисление глюкозы(см.85).
103-104. Челночные механизмы транспорта. 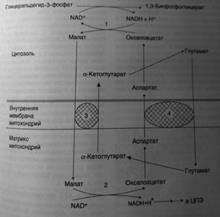
*малат-аспартатный челнок. Перенос водорода из цитозоля НАДН в митохондрии происходит при участии специальных механизмов, называющихся челночными. Суть этих механизмов сводится к тому, что НАДН в цитозоле восстанавливает некоторое соединение, способное проникать в митохондрию; в митохондрии это соединение окисляется, восстанавливая внутримитохондриальный НАД+, и вновь переходит в цитозоль. Самая активная малат-аспартатная система, действующая в митохондриях печени, почек и сердца. На каждую пару электронов цитозольной НАДН, переданную на кислород по этой системе, образуется 3 молекулы АТФ.
В скелетных мышцах и мозге перенос восстановительных эквивалентов от цитозольной НАДН осуществляет глицеролфосфатная система. При этом восстановительные эквиваленты передаются в цепь переноса электронов через комплекс II, и поэтому синтезируется только 2 молекулы АТФ.
Глицеро-фосфатный челнок: 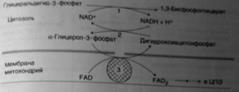
105. Роль инсулина и глюкагона в регуляции энергетического метаболизма при нормальном питании и при голодании.Инсулин и глюкагон играют главную роль в регуляции метаболизма при смене абсорбтивного и постабсорбтивного периодов и при голодании.Абсорбтивный период: Увеличение отношения инсулин/глюкагон вызывает ускорение использования метаболитов для запасания энергоносителей: происходит синтез гликогена, жиров и белков. Режим запасания включается после приёма пищи и сменяется режимом мобилизации запасов после завершения пищеварения.
Голодание: В отсутствие пищи в крови снижается уровень глюкозы, ам-к и ТАГ. инсулинглюкагоновый индекс снижается, и повышается концентрация контринсулярных гормонов, в первую очередь кортизола. Сущ.2 наиболее встречающиеся формы нарушения переваривания дисахари-дов в кишечнике – дефект лактазы(β-гликози-дазного комплекса) и сахаразы (сахаразо-изомальтазного комплекса непереноси-мостьлактозы и сахарозы. Отсутствие гидролиза соответствующих дисахаридов приводит к осмотическому эффекту и задержке воды в просвете кишечника.
Кроме этого, сахара активно потребляются микрофлорой толстого кишечника и метаболизируют с образованием органических кислот (масляная, молочная) и газов. Из-за этого симптомами лактазной или сахаразной недостаточности являются диарея, срыгивания, метеоризм, вспучивание живота, его спазмы и боли, атопический дерматит.
Сахарный диабет - заболевание, возникающее вследствие абсолютного или относительного дефицита инсулина. При сахарном диабете, как правило, соотношение инсулин/глюкагон снижено. При этом ослабевает стимуляция процессов депонирования гликогена и жиров, и усиливается мобилизация запасов энергоносителей. Печень, мышцы и жировая ткань даже после приёма пищи функционируют в режиме постабсорбтивного состояния.
Читайте также:
|
| Рубрика | Химия |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 10.07.2015 |
| Размер файла | 238,7 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Министерство образования и науки Российской Федерации
бюджетное образовательное учреждение
Высшего профессионального образования
Воронежский Государственный Педагогический Университет
Глюконеогенемз -- метаболический путь, приводящий к образованию глюкозы из неуглеводных соединений (в частности, пирувата). Наряду с гликогенолизом, этот путь поддерживает в крови уровень глюкозы, необходимый для работы многих тканей и органов, в первую очередь, нервной ткани и эритроцитов. Он служит важным источником глюкозы в условиях недостаточного количества гликогена, например, после длительного голодания или тяжёлой физической работы. Глюконеогенез является обязательной частью цикла Кори (совокупность биохимических ферментативных процессов транспорта лактата из мышц в печень, и дальнейшего синтеза глюкозы из лактата, катализируемое ферментами глюконеогенеза), кроме того, этот процесс может быть использован для превращения пирувата, образованного при дезаминировании аминокислот аланина и серина.
Глюконеогенез происходит у животных, растений, грибов и микроорганизмов. Его реакции одинаковы для всех тканей и биологических видов. Важными предшественниками глюкозы у животных выступают трёхуглеродные соединения, такие как лактат, пируват, глицерол, а также некоторые аминокислоты. У млекопитающих глюконеогенез происходит главным образом в печени, в меньшей степени -- в корковом слое почек и эпителиальных клетках, выстилающих тонкую кишку. Образованная в ходе глюконеогенеза глюкоза уходит в кровь, откуда доставляется к другим тканям. После интенсивной физической работы лактат, образовавшийся при анаэробном гликолизе в скелетных мышцах, возвращается в печень и превращается там в глюкозу, которая снова поступает в мышцы или превращается в гликоген (этот круговорот известен как цикл Кори). У проростков растений запасённые в семени жиры и белки превращаются, в том числе и через глюконеогенез, в дисахарид сахарозу, который транспортируется по всему развивающемуся растению. Глюкоза и её производные служат предшественниками для синтеза растительной клеточной стенки, нуклеотидов, коферментов и многих других жизненно важных метаболитов. У многих микроорганизмов глюконеогенез начинается с простых органических соединений, содержащих два или три атома углерода, например, ацетата, лактата и пропионата, которые содержатся в питательной среде.
Хотя реакции глюконеогенеза одинаковы у всех организмов, соседние метаболические пути и регуляторные пути глюконеогенеза отличаются у различных видов и в различных тканях. Рассмотрим подробнее особенности глюконеогенеза млекопитающих.
Глава 1. Особенности глюконеогенеза млекопитающих
1.1 Понятие глюконеогенеза
Глюконеогенез - синтез глюкозы из неуглеводных продуктов. Такими продуктами или метаболитами являются в первую очередь молочная и пировиноградная кислоты, так называемые гликогенные аминокислоты, глицерол и ряд других соединений. Иными словами, предшественниками глюкозы в глюконеогенезе может быть пируват или любое соединение, превращающееся в процессе катаболизма в пируват или один из промежуточных продуктов цикла трикарбоновых кислот.
Основные стадии гликолиза:
1.2 Обходные реакции глюконеогенеза
Образование фосфоенолпирувата из пирувата. Синтез фосфоенолпирувата осуществляется в несколько этапов. Первоначально пируват под влиянием пируваткарбоксилазы и при участии СО2 и АТФ карбоксилируется с образованием оксалоацетата:
Затем оксалоацетат в результате декарбоксилирования и фосфорилирования под влиянием фермента фосфоенолпируваткарбоксилазы превращается в фосфоенолпируват. Донором фосфатного остатка в реакции служит гуанозинтрифосфат (ГТФ):
Установлено, что в процессе образования фосфоенолпирувата участвуют ферменты цитозоля и митохондрий.
Первый этап синтеза протекает в митохондриях. Пируват-карбоксилаза, которая катализирует эту реакцию, является аллостери-ческим митохондриальным ферментом. В качестве аллостерического активатора данного фермента необходим ацетил-КоА. Мембрана митохондрий непроницаема для образовавшегося оксалоацетата. Последний здесь же, в митохондриях, восстанавливается в малат:
Реакция протекает при участии митохондриальной НАД-зависимой малатдегидрогеназы. В митохондриях отношение НАДН/НАД+ относительно велико, в связи с чем внутримитохондриальный оксалоацетат легко восстанавливается в малат, который легко выходит из митохондрии через митохондриальную мембрану. В цитозоле отношение НАДН/НАД+ очень мало, и малат вновь окисляется при участии цитоплазматической НАД-зависимой малатдегидрогеназы:
Дальнейшее превращение оксалоацетата в фосфоенолпируват происходит в цитозоле клетки.
Превращение фруктозо-1,6-бифосфата во фруктозо-6-фосфат. Фосфо-енолпируват, образовавшийся из пирувата, в результате ряда обратимых реакций гликолиза превращается во фруктозо-1,6-бифосфат. Далее следует фосфофруктокиназная реакция, которая необратима. Глюконеогенез идет в обход этой эндергонической реакции. Превращение фруктозо-1,6-бифосфата во фруктозо-6-фосфат катализируется специфической фосфатазой:
Образование глюкозы из глюкозо-6-фосфата. В последующей обратимой стадии биосинтеза глюкозы фруктозо-6-фосфат превращается в глюкозо-6-фосфат. Последний может дефосфорилироваться (т.е. реакция идет в обход гексокиназной реакции) под влиянием фермента глюкозо-6-фосфатазы:
1.3 Другие предшественники глюкозы
Описанный выше биосинтетический путь образования глюкозы относится к синтезу глюкозы не только из пирувата, но также 4-, 5- и 6-углеродных промежуточных соединений цикла трикарбоновых кислот. Цитрат, изоцитрат, б-кетоглутарат, сукцинил-СоА, сукцинат, фумарат и малат -- все промежуточные продукты цикла трикарбоновых кислот могут окисляться до оксалоацетата. Некоторые или все атомы углерода большей части аминокислот могут быть катаболизированы в пируват или промежуточные соединения цикла трикарбоновых кислот. Поэтому эти аминокислоты могут подвергнуться превращению в глюкозу и называются глюкогенными. Аланин и глутамин -- важнейшие молекулы, переносящие аминогруппы в печень из других тканей -- служат особенно важными глюкогенными аминокислотами у млекопитающих. После того, как эти аминокислоты отдают свои аминогруппы в митохондриях печени, их углеродные скелеты (пируват и б-кетоглутарат соответственно) вовлекаются в глюконеогенез. Аминокислоты образуются при распаде белков мышц и соединительной ткани, их включение в глюконеогенез происходит при продолжительном голодании или длительной физической нагрузке.
У растений, дрожжей и многих бактерий имеется путь, позволяющий получать углеводы из жирных кислот -- глиоксилатный цикл. У животных ключевых ферментов этого цикла нет, и, ввиду необратимости пируватдегидрогеназной реакции, они не могут получать пируват из ацетил-СоА, а значит, образовывать углеводы из жирных кислот (следовательно, и из липидов). Тем не менее, они могут использовать для глюконеогенеза те небольшие количества глицерола, который образуется при распаде жиров. При этом глицерол фосфорилируется глицеролкиназой, далее следует окисление центрального атома углерода с образованием дигидроксиацетонфосфата, который является промежуточным соединением глюконеогенеза.
Глицеролфосфат является необходимым промежуточным соединением при синтезе жиров (триглицеридов) в адипоцитах, однако эти клетки лишены глицеролкиназы и поэтому не могут осуществлять фосфорилирование глицерола. Вместо этого адипоциты могут осуществлять сокращённый вариант глюконеогенеза, известный как глицеронеогенез: преобразование пирувата в дигидроксиацетонфосфат через первые реакции глюконеогенеза, вслед за которым следует восстановление дигидроксиацетонфосфата до глицеролфосфата.
1.4 Регуляция глюконеогенеза
В целом можно выделить два способа регуляции глюконеогенеза: гормональная при участии гормонов и метаболическая, т.е. при помощи промежуточных или конечных продуктов обмена глюкозы.
Гормональная активация глюконеогенеза осуществляется глюкокортикоидами, которые увеличивают синтез пируваткарбоксилазы, фосфоенолпируват-карбоксикиназы, фруктозо-1,6-дифосфатазы. Глюкагон стимулирует те же самые ферменты через аденилатциклазный механизм путем фосфорилирования.
Также имеется метаболическая регуляция, при которой аллостерически активируется пируваткарбоксилаза при помощи ацетил-SКоА, фруктозо-1,6-дифосфатаза при участии АТФ.
Гормональные и метаболические факторы, регулирующие глюконеогенез:
1.5 Клиническое значение
При снижении использования лактата в качестве субстрата для глюконеогенеза, которое может вызываться дефектом ферментов глюконеогенеза, концентрация лактата в крови повышается, что приводит к понижению pH крови и развитию лактатацидоза.
Лактамтацидомз (лактамтацидотимческая комма, молочнокимслая комма, гимперлактамтацидемимя) -- редкое крайне тяжёлое состояние, летальность при котором от 50 до 90% -- неспецифический синдром, развивающийся в ряде тяжёлых патологических состояний (в том числе, сахарный диабет), когда создаются предпосылки для повышенного образования и накопления в крови и периферических тканях молочной кислоты.
Обычно развивается остро (в течение нескольких часов), предвестники, как правило, отсутствуют или не характерны. Пациенты могут отмечать мышечную боль, боль за грудиной, диспептические явления, учащение дыхания, апатию, сонливость или бессонницу. Однако превалирующими симптомами клинической картины лактатацидоза являются проявления сердечно-сосудистой недостаточности, усугубляющиеся тяжёлым ацидозом, на фоне которого наступают изменения сократительной способности миокарда. В динамике состояние пациентов прогрессивно ухудшается: по мере нарастания ацидоза может появиться боль в животе, рвота. Выявляется разнообразная неврологическая симптоматика от арефлексии до спастических парезов и гиперкинезов. Перед развитием комы (потери сознания), несмотря на отсутствие запаха ацетона в выдыхаемом воздухе (нет кетонемии), наблюдается шумное дыхание Куссмауля, обычно сопровождающее выраженный метаболический ацидоз. Развивается коллапс с олиго-, а затем и анурией, гипотермией. На этом фоне развивается ДВС-синдром (синдром внутрисосудистого свёртывания крови), нередки внутрисосудистые тромбозы с геморрагическими некрозами пальцев рук и ног. Быстрое развитие лактатацидоза (несколько часов) не способствует выявлению признаков, характерных для диабетической комы (сухость кожи, слизистых оболочек и языка). У 10--30% пациентов с диабетической и гиперосмолярной комой присутствуют элементы лактатацидоза
Стоит отметить, что кратковременный лактатацидоз встречается и у здоровых людей при интенсивной мышечной работе, в этом случае он компенсируется путём гипервентиляции лёгких и ускоренным выведением углекислого газа.
биохимический глюкоза фермент
Так как синтез и окисление глюкозы являются крайне важными для существования клетки (гликолиз) и всего организма (глюконеогенез), то регуляция этих процессов отвечает запросам органов и тканей при различных условиях существования.
Глюконеогенез, как образование глюкозы из неуглеводных компонентов, необходим:
1) При гипогликемии во время мышечной нагрузки - синтез из молочной кислоты, поступающей из мышц, из глицерола, образующегося при мобилизации жиров;
2) При гипогликемии при голодании - синтез из аминокислот, образующихся при катаболизме белков.
Таким образом, при голодании или физической нагрузке глюконеогенез, идущий в печени, обеспечивает глюкозой все остальные органы (эритроциты, нервная ткань, мышцы и др.), в которых активен гликолиз и другие процессы, производящие энергию. Наличие глюкозы в указанных клетках необходимо, чтобы поддержать концентрацию оксалоацетата и обеспечить сгорание ацетил-SКоА (получаемого также из жирных кислот или кетоновых тел) в цикле трикарбоновых кислот.
Список использованной литературы
1. Биохимия: Учеб. для вузов, Под ред. Е.С. Северина. - Москва: Аспект пресс, - 2004. - 779 с.
2. Ефимов А.С. Клиническая диабетология. /А.С. Ефимов, Н.А. Скробонская /Киев: Здоровье, 2008.. -- 320 с.
3. Кольман Я. Наглядная биохимия./ Я. Кольман, К. Рём/ -- 4-е изд. -- Москва: БИНОМ. Лаборатория знаний, 2012. -- 469 с.
Размещено на Allbest.ru
Общая характеристика глюконеогенеза. Изучение роли глиоксилатного цикла в глюконеогенезе. Характеристика структуры гена и белка. Определение активности изоцитратлиазы. Выделение суммарной клеточной популяции РНК. Проведение полимеразной цепной реакции.
дипломная работа [760,2 K], добавлен 01.05.2015
Определение и строение глюкозы - моносахарида и шестиатомного сахара. Изомеры. Фруктоза. Физические и химические свойства. Особенности получения - гидролиз крахмала, фотосинтез. Сферы применения. Распространение в природе. Значение глюкозы для человека.
презентация [6,1 M], добавлен 11.09.2016
Разработка урока по расширению знаний об углеводах, изучению строения и свойств глюкозы. Проведение химического эксперимента по взаимодействию раствора глюкозы с гидроксидом меди и аммиачным раствором оксида серебра. Тестовые упражнения, задание на дом.
презентация [440,8 K], добавлен 31.10.2009
Строение углеводов. Механизм трансмембранного переноса глюкозы и других моносахаридов в клетке. Моносахариды и олигосахариды. Механизм всасывания моносахаридов в кишечнике. Фософорилирование глюкозы. Дефосфорилирование глюкозо-6-фосфата. Синтез гликогена.
презентация [1,3 M], добавлен 22.12.2014
Определение содержания глюкозы в вине методом обратного титрования с помощью йодометрического метода, который заключается в окислении альдоз щелочным раствором йода. Химический состав вина: протеины, углеводы, липиды, волокна, минеральные соли, вода.
дипломная работа [605,0 K], добавлен 19.12.2007
Виды и способы получения глюкозы, ее физико-химические свойства. Характеристика продуктов глюкозного производства. Получение глюкозно-фруктозного сиропа из крахмала с помощью ферментного или кислотного осахаривания. Свойства глюкозно-фруктозного сиропа.
реферат [102,7 K], добавлен 10.10.2014
Обзор методов получения глюкозы. Анализ основной реакции: физические, химические свойства и электронная структура целлюлозы, глюкозы и воды. Механизм и кинетическая модель реакции, расчет материального и теплового баланса, расчет объема реактора.
дипломная работа [2,7 M], добавлен 14.05.2011
Общая характеристика, классификация и номенклатура моносахаридов, строение их молекул, стереоизомерия и конформации. Физические и химические свойства, окисление и восстановление глюкозы и фруктозы. Образование оксимов, гликозидов и хелатных комплексов.
курсовая работа [1,6 M], добавлен 24.08.2014
Белки и углеводы: классификация, свойства, функции. Структурно-пространственная организация белковых молекул. Обменные процессы биомолекул в живом организме. Метаболические пути глюконеогенеза. Действие концентрированных кислот на белки и углеводы.
курсовая работа [637,6 K], добавлен 07.04.2016
Сахароза C12H22O11, (свекловичный, тростниковый сахар) — дисахарид, состоящий из двух моносахаридов — альфа-глюкозы и бета-фруктозы. Определение ее физико-химических свойств; Природные и антропогенные источники бесцветных моноклинных кристаллов.
презентация [383,5 K], добавлен 16.12.2010
Читайте также:
- Удаление папиллом лазером в истре
- Герпес шейки матки цитология
- Генферон свечи отзывы в гинекологии при герпесе
- Можно ли использовать фенистил гель при ветрянке у детей
- Как лечить герпесную ангину и стоматит у ребенка
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции