Коронавирус днк или рнк содержащий вирус
Сейчас известно 39 видов коронавирусов, в каждый вид могут входить десятки и сотни штаммов. Кроме того, есть еще 10 видов — кандидатов в коронавирусы. Специалисты пока только проверяют, можно ли их считать настоящими коронавирусами. У них широкий спектр хозяев среди птиц и зверей, у которых они вызывают заболевания дыхательной системы и желудочно-кишечного тракта. К людям коронавирусы приходят от животных: вирус атипичной пневмонии 2002—2003 годов SARS-CoV пришел от подковоносых летучих мышей, от которых он перескочил в мусанга, или малайскую пальмовую куницу, а из мусанга — уже в человека. (Любителям кофе малайская пальмовая куница должна быть знакома — это тот самый зверек, без которого не было бы кофе копи-лювак: мусангам скармливают кофейные зерна, которые определенным образом ферментируются в кишечнике, изменяя вкусовые свойства; кофе из зерен, которые прогнали через мусангов, считается особо изысканным и стоит весьма немалых денег.)
Еще один человеческий коронавирус известен по вспышке ближневосточного респираторного синдрома, первые случаи которого были зарегистрированы в 2012 году в Саудовской Аравии, — он получил название MERS-CoV. Этот вирус также пришел к людям от летучих мышей с промежуточной остановкой в одногорбых верблюдах (оттого его еще называют верблюжьим гриппом, что неправильно, — коронавирусы от вирусов гриппа отличаются). Умирают от него более трети заразившихся, однако заразиться им сложно: с момента появления вируса и до начала этого года в мире зарегистрировано лишь около двух с половиной тысяч случаев.
Подозревают, что и новый вирус SARS-CoV-2 тоже пришел к нам от летучих мышей.
Наконец, есть еще четыре человеческих коронавируса, два из которых, HCoV-229E и HCoV-OC43, были известны еще до атипичной пневмонии от SARS-CoV, а два других, HCoV-NL63 и HCoV-HKU1, открыли в 2004 и 2005 годах. Все четыре не вызывают ничего серьезнее мягкой простуды; хотя коронавирусная простуда встречается довольно часто — на ее счет относят 15—30% всей простуды в мире.
Но об эпидемиологии коронавирусов мы рассказывать не будем, а вместо этого поговорим о том, как они устроены и как на них реагируют наши клетки.
Обладатели белковой короны
И белок S, и белок HE сидят в мембранной липидной оболочке. Откуда она берется? Как мы помним, наши клетки окружены мембраной и внутри них существует много мембранных органелл — клеточных органов, выполняющих разные функции и ради правильной работы отделенных от остальной клетки двуслойной липидной мембраной. Ее-то вирус и заимствует, выходя из клетки, а как именно, скажем чуть ниже. Кроме S и HE в ней сидит очень много белка М, который поддерживает и структурирует мембрану, и еще немного белка E. Под липидной оболочкой с белками мы найдем геном вируса — нить молекулы РНК, которая усажена белком N: он упаковывает вирусную РНК в компактную свернутую спираль. (Белковая оболочка вирусов, непосредственно взаимодействующая с нуклеиновой кислотой, называется капсидом.) Когда РНК попадает в клетку, то на ней сразу можно синтезировать белки, и такую РНК у вирусов обозначают плюсом.
По этим признакам коронавирусы относят к РНК-содержащим вирусам, чей геном представляет собой одну-единственную плюс-цепь РНК. Так же выглядит геном у множества других вирусов, среди которых есть риновирусы (одна из самых частых причин простуды) и вирус гепатита С. В то же время коронавирусы относят к оболочечным вирусам, у которых кроме нуклеиновой кислоты и связанного с ней структурно-защитного белка (у коронавирусов это белок N) есть еще мембранная оболочка. К оболочечным вирусам еще относятся, например, вирусы герпеса, у которых наследственная информация хранится в ДНК, и ВИЧ. Как видим, по отдельности разные молекулярные черты можно найти у множества вирусов и лишь по их сочетанию отделить одну группу вирусов от другой.
Кстати, геном в виде РНК — это, можно сказать, слабость коронавирусов. В нуклеиновых кислотах время от времени появляются мутации либо из-за внешних факторов, вроде фоновой радиации, либо из-за стандартных ошибок белков, которые эти нуклеиновые кислоты копируют. Но в клеточной ДНК мутации могут быть исправлены специальными ремонтными белками. Этим же ремонтом способны воспользоваться вирусы с геномом в виде ДНК или же те, которые геномную РНК на время копируют в ДНК (такие вирусы называются ретровирусами). А в коронавирусной РНК ошибки никак не исправляются. Мутации помогают вирусам сменить хозяина, но среди мутаций есть очень много вредных, и если вирус не может никак корректировать дефекты в ДНК, они в какой-то момент могут сделать его просто нежизнеспособным.
Любые вирусы — это, грубо говоря, лишь комок молекул, пусть и сложно устроенный. Собственного обмена веществ у вирусов нет, и размножаться за пределами клетки они не могут. Вирусам с мембранной оболочкой проникнуть в клетку проще как из-за самой мембраны, так и благодаря сидящим на ней белкам: они хорошо подходят к клеточным рецепторам. Кроме того, белки мембранной оболочки, как собственно вирусные, так и те, которые вирус прихватил у клетки вместе с куском мембраны, помогают вирусу уходить от иммунной атаки. Но из-за мембраны такие вирусы более чувствительны к разным неблагоприятным факторам, вроде обезвоживания или моющих детергентов, мембрану разрушающих. Поэтому вирусы с мембранной оболочкой лучше всего передаются от хозяина к хозяину, а сидеть на какой-то поверхности и ждать, когда их оттуда снимет потенциальный хозяин, они долго не могут. Этим они отличаются от вирусов без мембраны, которые представляют собой нуклеиновую кислоту, заключенную в белковый капсид, — они более устойчивы в окружающей среде, но проникнуть в клетку для них зачастую сложнее.
Внедрение в клетку
Разные вирусы пользуются разными клеточными белками для входа. Так, вирус атипичной пневмонии SARS-CoV и относительно безобидный HCoV-NL63 связываются с ангиотензинпревращающим ферментом 2, который помогает регулировать кровяное давление, участвует в управлении иммунитетом и играет роль еще в целом ряде процессов. Но белка одного вида для входа бывает недостаточно, поэтому, например, SARS-CoV нужен еще белок TMPRSS2 — одна из сериновых протеаз, участвующая в разных биохимических реакциях. Вирус сначала связывается с одним белком на поверхности клетки, а потом второй белок на поверхности клетки режет вирусный белок S, после чего мембраны вируса и клетки соединяются.
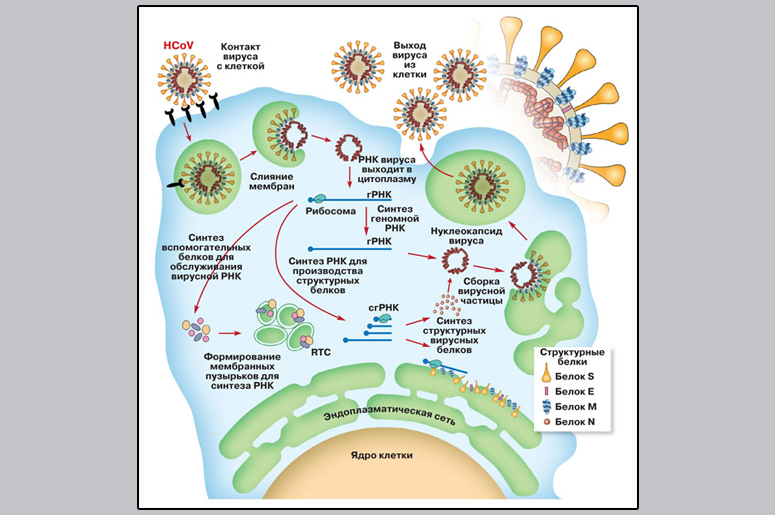
Схема жизненного цикла коронавируса. Проникнув в клетку, вирус высвобождает свою РНК, на которой рибосомы — клеточные машины для белкового синтеза — собирают вирусные белки, необходимые для формирования мембранных пузырьков и для синтеза плюс-цепи геномной РНК — гРНК. На вспомогательных мембранных пузырьках появляются вирусные белки, образующие RTC — replication transcription complex, этот комплекс выполняет репликацию (удвоение генома вируса) и транскрипцию — синтез коротких субгеномных РНК (сгРНК), предназначенных для сборки структурных вирусных белков. Структурный белок N соединяется с геномной РНК и образует нуклеокапсид вируса (геном плюс капсидный белок). На эндоплазматической сети синтезируются другие структурные белки, которые организуют вирусу липидную мембрану.
Вирус проник в клетку, и теперь он начинает копировать свой геном, то есть молекулу РНК, и синтезировать белки, нужные для копирования РНК и для формирования вирусных частиц. Кроме полных геномных РНК коронавирусы создают еще набор более коротких РНК — они синтезируются на больших геномных РНК и нужны только для синтеза белков; в вирусные частицы эти короткие РНК не попадают (точно так же ведут себя некоторые другие вирусы, которые вместе с коронавирусами объединяют в группу Nidovirales). Все вирусные РНК синтезируются в особых белковых комплексах, которые, в свою очередь, закреплены в небольших мембранных пузырьках. Эти пузырьки создает сам вирус: его белки вторгаются во внутриклеточные мембраны и фрагментируют их, создавая пузырьки-везикулы, чтобы РНК-синтезирующим комплексам было к чему пришвартоваться.
Часть насинтезированной РНК остается плавать в цитоплазме клетки — на ней синтезируется белок N, который будет упаковывать геномную вирусную РНК в спираль. Другие структурные белки, те, что потом окажутся в мембранной оболочке вируса (S, M и пр.), синтезируются на РНК, осевшей на особой внутриклеточной структуре — эндоплазматической сети, или эндоплазматическом ретикулуме (ЭР). Эндоплазматическая сеть — это огромная система мембранных канальцев, цистерн и пузырьков, на которых сидят белоксинтезирующие молекулярные машины рибосомы и собирают белки в соответствии с информацией в РНК. Готовые белки погружаются внутрь полостей ЭР, где приобретают правильную пространственную форму и потом либо переходят в клеточную цитоплазму, либо отправляются на экспорт, наружу из клетки, будучи заключены в транспортный мембранный пузырек.
Особенности внутриклеточной борьбы
О том, что у нее внутри орудует вирус, клетка может догадаться по неполадкам с внутренними мембранами — мы помним, что коронавирусы фрагментируют мембраны, чтобы дать опору своим белкам, синтезирующим РНК, и сами вирусные частицы прихватывают себе куски мембран. Кроме того, вирусные белки накапливаются в эндоплазматической сети и вызывают так называемый ЭР-стресс, то есть стресс эндоплазматического ретикулума. ЭР-стресс заставляет клетку остановить синтез белков (что, несомненно, бьет по вирусу — ведь он зависит от клеточной белоксинтезирующей машины) и активирует сигнальные молекулярные пути, которые включают программы клеточного суицида. Наконец, клетка может понять по вирусной РНК, что внутри у нее поселилась инфекция, и в ответ начать синтез интерферона первого типа. Это сигнальный белок, который выходит из клетки и оповещает всех об инфекции, в результате здоровые клетки готовятся защищаться от своей соседки, а иммунные клетки стремятся уничтожить зараженную клетку.
Вместе со специалистом профилактической медицины Екатериной Степановой Sputnik выяснил, как вирусам удается обманывать наш организм и почему ученые считают их в некотором роде полезными.
Информационными носителями биологической жизни являются гены (белковые структуры), которые определенным образом собраны в цепочки (ДНК и РНК).

Принято считать, что гены находятся в клетках живых организмов, бактерий, растений, которые потребляют питательные вещества, производят энергию, делятся (размножаются) и погибают.
Но существуют и другие формы существования генных цепочек ДНК и РНК – это вирусы. Точное их количество на сегодняшний день доподлинно не известно.
Вирусы не имеют клеточного строения, это генетическая программа (фрагмент ДНК или чаще РНК), покрытая белковой оболочкой – капсидом.
Они не могут жить самостоятельно, у них нет для этого ничего, никаких механизмов поддержания жизни. Поэтому вирусы паразитируют на живых клетках организмов и используют их для своего репродуцирования (воспроизводства того, что сохранилось в памяти генов).

Такое соседство почти всегда заканчивается гибелью живой клетки. Все виды живых клеток на Земле имеют свой набор вирусов: человек, мыши, клещи, растения, бактерии. Как правило, вирус опасен для одних видов и безопасен для других (растение – человек).
Попав в организм, вирус ищет именно свою клетку, свой орган.
В научном мире до сих пор идут споры о том, что такое вирус. Он производит себе подобных, но непонятно, зачем, ведь у него отсутствует механизм размножения (для этого ему нужен носитель-хозяин) он просто реплицирует (копирует свои данные из одной клетки в другую).
Но, безусловно, вирус влияет на жизнь людей. И не лучшим образом.
Размер вируса невероятно мал и определяется наукой в нанометрах. Вирус настолько мал относительно человека, как человек мал относительно размеров земного шара.
Он не виден в обычном световом микроскопе, для его изучения используют электронный, с выведением изображения на экран монитора.

Вирусы не могут отнести ни к какой эволюционной системе.
Вирус состоит из белковой оболочки, которая помогает ему сохраниться во внешних условиях и защититься от физических факторов (уфо-лучи, ферменты, химические агенты). Она же помогает найти по белку в организме именно свою клетку. Но эта же оболочка может представлять и угрозу для вируса – на ее поверхности содержится антиген, благодаря которому наша иммунная система его распознает. Поэтому иногда сложный вирус бывает покрыт дополнительной липидной оболочной – она называется суперкапсидом.
Внутренняя структура вируса называется сердцевиной – это одна или две генные цепочки РНК, реже ДНК. Цепочки могут иметь свой заряд (+ или -).
Геном вируса содержит самую важную для него информацию: как регулировать и запускать процесс заражения клетки, как размножить саму генную цепочку, как сформировать (синтезировать) белковые оболочки, в которые нужно упаковать новые генные цепочки. Они синтезируются по отдельности с оболочкой в разных частях пораженной клетки, и только потом идет окончательный сбор.
С момента появления вирус эволюционирует и в этот период ведет себя агрессивно. После того, как он доходит до пика развития, агрессия спадает, вирус всячески старается сосуществовать со своим хозяином, иначе погибнет и он сам. А иногда он уничтожает хозяина еще до пика развития.
Известно несколько механизмов проникновения в клетку.
- Вирус прикрепляется к клетке. Если у клетки гибкая мембрана, вирус накрывает ее своей оболочкой. Похожие белковые структуры сливаются вместе, и вирус проникает вглубь клетки. Поэтому каждый вирус в организме ищет свою "родственную" белковую оболочку.
- Благодаря белковым рецепторам на своей поверхности вирус убеждает клетку, что он не чужак. И, как троянский конь, попадает в нее.
- Использует механизм фагоцитоза клетки: она поглощает его как что-то чужеродное в надежде переварить и заражается.
Как только вирус проник в клетку, он высвобождает свой генный материал и замещает ДНК клетки на свою. С этого момента зараженная клетка уже начинает производить вирусные фрагменты (работает на вирус).

Иногда клетка довольно длительное время производит аналогичный вирус, и вирусные образования (верионы) постоянно выходят в межклеточное пространство, поражая другие клетки. А иной раз клетка реплицирует вирус в себе до того момента, пока ее ресурс не исчерпается. Тогда в определенный момент клетка разрывается под действием фермента вируса, в этот момент огромное число верионов выходит в межклеточное пространство и массово поражает соседние здоровые клетки.
От механизма распространения вируса зависит и общее состояние организма. Нюанс в том, что иногда, выходя из клетки, верион (вирусное образование) может забирать с собой фрагмент или часть оболочки или ядра клетки, поэтому наша иммунная система не сразу может распознать "чужака".
В 1971 году Дэвиду Балтимору удалось разделить известные вирусы на 7 классов по форме, размеру, содержимому сердцевины. Но в природе их, безусловно, неисчислимое количество, они постоянно мутируют.
Поэтому нельзя создать универсальную таблетку или вакцину просто от вируса.
Как это ни странно, но ученые утверждают, что и для человека, и для природы есть определенная польза.
Попадая в организм, вирус тренирует нашу иммунную систему. Она совершенствуется. Переходя от клетки к клетке, из организма в организм, вирус частично в момент клеточного синтеза обменивается генами с клеткой. И они не всегда "плохие", бывают и положительные мутации для организма.

Выжившие клетки начинают свой обновленный цикл развития, что сказывается и на эволюции человека – следы столкновения с вирусами оседают в наших генах. Положительные мутации открывают нашему организму новые возможности. Например, на поверхности трехдневного эмбриона уже сидит много вирусных белков от древнего вируса, которые защищают сам эмбрион от враждебных "чужаков". Вирусы широко используют в генной инженерии, а для природы вирусы – часть контроля популяции.
Коронавирус для науки тоже частично известен, и он имеет свои особенности и штаммы.
Получил он такое название за схожесть по форме с короной. В 70% случаев он приходит из природы и от животных.
Полностью победить вирус трудно – можно вылечить всех людей, но невозможно вылечить всех мышей или, например, клещей. История знает множество подобных примеров.
При любом вирусном поражении стоит вопрос не в самом принципе заражения, а в уязвимости определенных групп населения и их систем организма.

Коронавирус поражает дыхательные пути – легкие, вернее, альвеолы – клетки, где происходит непосредственно газообмен. Смертность в основном наступает не от самого вируса, а от реакции организма на него, так как мутация для нас новая.
Наша иммунная система, имеющая комплекс механизмов, отвечает разнообразными процессами, часть из которых формирует воспаление (формирование интерферонов), а часть противостоит воспалению, формируя другие механизмы борьбы. Пока сохраняется баланс – большой угрозы для жизни нет.
Но такой баланс может быть сохранен при нормальном здоровом функционировании всех систем в организме: детокс-органов (печень, почки, кишечник), сосудов (их проходимость без бляшек) и т.д.
Воспаление – это всегда отек, и если воды много, в частности в альвеолах легких, функция дыхания затрудняется, человек может погибнуть. Процесс борьбы и реакции развивается от 6 до 10 дней – в этот период человеку нужна сторонняя помощь, к примеру, искусственная вентиляция легких. Потом воспалительные реакции идут на спад. Правда, при этом и сама иммунная система истощается, поэтому в такой период необходимо уберечься уже от бактериальных инфекций как факта осложнения.
Вирулентность (злобность) вируса определяется количеством вирусных частиц, которые попадают на слизистые. Поэтому принципы личной гигиены и самоизоляция всегда первостепенны, как и образ жизни.
А в питании должны присутствовать белки животного происхождения, потому что из них синтезируются клетки иммунной системы, а также железо, цинк, животные жиры (сливочное масло), масло какао, омега-3, щелочные продукты.
В любом случае, наше здоровье заслуживает большего внимания, чем мы иногда ему оказываем: кто-то уверен, что четыре часа сна в сутки – достаточно, кто-то отказывает от мяса, другие живут в постоянном стрессе. А между тем все это факторы, угнетающие иммунитет.
Мы – человеческая популяция, и от ответственности каждого из нас зависит здоровье и выживаемость человечества вообще.
Без кризиса нет развития, любой пережитый вирус делает наш организм совершеннее.


Об этом "РГ" беседует с молекулярным вирусологом, и.о. директора Института биомедицинских систем и биотехнологий Санкт-Петербургского политехнического университета Петра Великого, доктором биологических наук Андреем Васиным.
Андрей Владимирович, пандемия COVID-19 открыла нам глаза на то, что мир вирусов способен преподнести людям немало сюрпризов, хотя мы сталкиваемся с ними постоянно. Почему, на ваш взгляд, новый вирус оказался таким шоком для человечества?
Андрей Васин: Подавляющее большинство людей просто недооценивало опасность, которую представляют вирусы. Почти все слышали такие слова, как "Эбола", "птичий грипп", "вирус Зика", "атипичная пневмония". Но все это было в заголовках новостей и где-то далеко - в Африке, Юго-Восточной Азии, Южной Америке - и не касалось непосредственно нас. Не случайно, наверное, что страны Юго-Восточной Азии, которые сталкивались с некоторыми из перечисленных вирусов, оказались более подготовленными к реагированию на COVID-19, чем, например, страны Европы.
Охвативший весь мир "свиной грипп" (т.е. вирус гриппа A/H1N1), объявленный пандемией, воспринимался просто как осложненный грипп. Плюс к этому было много разговоров про то, что это все обман с целью отвлечения внимания людей от каких-то более важных проблем, "заговор фармкомпаний, чтобы продавать больше препаратов", и т.п. А сейчас оказалось, что угроза пандемии реальна и может затронуть всех. К такому повороту событий общество многих стран, мне кажется, не было готово.
Известно, что вирусы крайне изменчивы. Чем объясняется эта их способность?
Андрей Васин: В основе всей жизни на земле лежит процесс репликации, то есть копирования генома, который у всех клеточных форм жизни представлен молекулой ДНК. За этот процесс в клетках отвечают специальные ферменты, которые называются полимеразы. В процессе репликации ДНК (у человека размер генома, например, составляет 10 в девятой степени!) неизбежно возникают ошибки. Поэтому в процессе эволюции появились специальные ферменты, которые отвечают за репарацию, то есть за устранение этих ошибок. У вирусов геном может быть представлен молекулой как ДНК, так и РНК. При этом РНК-содержащие вирусы являются более изменчивыми и патогенными, чем ДНК-содержащие. В частности, к РНК-содержащим вирусам человека относятся ВИЧ, вирус Эбола, вирус Зика, вирусы гриппа и коронавирусы, в том числе COVID-19. Изменчивость РНК-содержащих вирусов связана с тем, что у них, как правило, нет систем репарации. В результате вирусная полимераза совершает ошибки довольно часто. Размер генома вируса гораздо меньше, поэтому у них на каждый цикл репликации приходится в среднем одна мутация. С учетом скорости размножения вируса и скорости его распространения в популяции число мутаций будет довольно велико, что и объясняет такую изменчивость.
А помимо постепенного накопления мутаций в геноме РНК-содержащих вирусов возможны и более резкие изменения, например, в процессе реассортации и рекомбинации. Реассортация - это перемешивание сегментов генома разных вирусов. Если эти сегменты были от вирусов разных хозяев (например, человека и птицы), такой новый вирус чаще всего бывает нежизнеспособным. Однако в редких случаях он все же получает возможность эффективно размножаться и передаваться от человека к человеку. Именно таким образом возникали все известные пандемии гриппа. Для некоторых вирусов с монолитным геномом возможна рекомбинация, то есть обмен фрагментами генома между разными штаммами.
В частности, такие механизмы встречаются у коронавирусов. Реассортация и рекомбинация приводят не к плавным, а к резким изменениям биологических свойств вируса. Такая изменчивость и является одним из ключевых факторов их способности ускользнуть от иммунитета человека.

В состоянии ли наука предсказать появление более опасных штаммов тех вирусов, которые давно циркулируют среди людей?
Андрей Васин: Наука в состоянии предположить, что может сделать уже известные вирусы более опасными, изучая их молекулярно-генетические механизмы. Мы можем предполагать, на какие вирусы стоит обратить особое внимание с точки зрения их пандемического потенциала. Но сказать, какое именно событие усилит патогенность вируса в реальности и тем более когда оно произойдет, к сожалению, пока невозможно.
Известно, что существует около 250 вирусов, вызывающих ОРВИ. Однако для них не создано ни тест-систем, ни вакцин. С чем это связано? И оправдано ли такое спокойствие человечества?


Андрей Васин: Сложно дать однозначный ответ. С одной стороны, обычные люди и даже многие медики считают, что вызванные вирусами респираторные заболевания в целом схожи друг с другом, и подход к их лечению примерно одинаковый. Единственное исключение составляет грипп, при этом многие люди гриппом называют все ОРВИ. Зачем тогда тратить время и деньги на их дифференциальную диагностику? Считается, что важно определить, вирус или бактерия вызвали заболевание, а если вирус, то грипп это или нет, а остальное неважно. Ведь специфических противовирусных препаратов для других респираторных вирусов нет - в отличие от множества антибиотиков против бактериальных инфекций. Но каждый вирус имеет свою собственную программу репликации в организме, поэтому и течение инфекции тоже будет отличаться, а значит, и схема лечения тоже должна иметь отличия. Как молекулярный вирусолог, я считаю, что ставить диагноз ОРВИ и не обращать внимания на то, какой вирус ее вызвал, неправильно. Возможно, медицинские вирусологи и инфекционисты не будут столь категоричны. Но я уверен, что по мере изучения респираторных вирусов нас ждет еще много сюрпризов, в том числе в механизмах их патогенеза и развития осложнений.
Но тест-системы на определение ОРВИ есть, они широко используются в системе надзора за гриппом и другими ОРВИ, осуществляемой, в частности, Национальным центром ВОЗ на базе НИИ гриппа им. Смородинцева Минздрава России. Что касается вакцин, то ОРВИ преимущественно вызваны РНК-содержащими, то есть сильно изменчивыми вирусами, и создать эффективную вакцину от них не так просто. Мы это видим на примере вакцины от гриппа, состав которой меняется ежегодно, и прививаемся мы ею не единожды в жизни, а практически каждый год. Попытки создать вакцины и против других ОРВИ предпринимались в 1960-е годы, но они оказались безуспешными. Ярким примером является респираторно-синцитиальная инфекция, вызывающая тяжелые заболевания нижних дыхательных путей, особенно у младенцев и детей младшего возраста. Была получена инактивированная вакцина, но на стадии клинических испытаний она не только не позволила защитить от инфекции, но и существенно утяжелила заболевание. После этого работы по вакцине против РС-инфекции были надолго закрыты. Только в наше время вновь вернулись к активной разработке этих вакцин, когда открыли молекулярные механизмы усиления инфекции, возникавшего при использовании вакцины в те годы, но уже с использованием новых технологий. Сейчас на стадии доклинических и клинических исследований находится несколько десятков вакцинных препаратов. Мы также проводим доклинические исследования нашего варианта вакцины против РС-инфекции в НИИ гриппа, работа финансируется Центром стратегического планирования и управления медико-биологическими рисками здоровью Минздрава России.
А были ли попытки создать вакцины от коронавирусов?
Андрей Васин: Среди сезонных респираторных вирусов встречается 4 типа коронавирусов: OC43, HKU1, NL63 и 229E. И если про коронавирусы SARS (атипичной пневмонии) и MERS (ближневосточного респираторного синдрома) люди еще слышали, то про эти четыре коронавируса ничего не знают. Против них не было разработано ни лекарств, ни вакцин. Если бы они были, мы чувствовали бы себя сейчас намного уверенней и смогли бы гораздо быстрее создать вакцину или лекарственный препарат от COVID-19.
На нашей памяти - эпидемия Эбола в Африке, вспышки других опасных вирусных лихорадок. Какие уроки были извлечены из них?


Андрей Васин: Вирус Эбола был хорошо известен специалистам и до эпидемии. Локальные вспышки заболевания фиксировались, но при чрезвычайно высокой летальности число заболевших было невелико. Эпидемия столь опасного вируса особенно в условиях бедных стран Африки - это событие чрезвычайное, требующее неотложных мер, что в конечном итоге и было сделано. На момент начала эпидемии различными лабораториями разрабатывался целый ряд препаратов против вируса Эбола, в том числе с использованием новых технологий. Был определенный задел и по вакцинам, который позволил оперативно инициировать их разработку. Эпидемия Эбола позволила апробировать целый ряд новых биотехнологических решений, которые можно применять в дальнейшем для борьбы и с другими вирусными инфекциями.
Как вы полагаете, какие изменения в нашей жизни, в организации санэпиднадзора и системы здравоохранения должны будут произойти после нынешней пандемии?
Андрей Васин: Основные изменения будут связаны скорее всего с экономическими последствиями пандемии. ВОЗ постоянно говорит о необходимости подготовки к пандемиям, разработаны соответствующие "дорожные карты". После пандемии COVID-19 эта работа будет усилена как на глобальном уровне, так и на уровне отдельных стран. А в обычной жизни, надеюсь, люди будут уделять гораздо больше внимания правилам личной гигиены, более ответственно относиться к респираторным заболеваниям и не приходить, например, на работу или в места скопления людей с ОРВИ, заражая окружающих. По крайней мере, хотя бы в первое время.
Многие годы нам рекомендовали в качестве профилактики вирусных инфекций то витамины, то модуляторы интерферонов. Теперь об этом что-то молчат. Установки изменились?
Андрей Васин: Возможно, появилась ответственность за то, что предлагаешь, так как спрос на эти предложения будет действительно серьезный. Надеюсь, что одним из положительных последствий ситуации будет и более серьезное отношение к тому, чем предлагается лечить ОРВИ. А также то, что число сторонников антипрививочного движения сократится. Ведь вакцины - это одно из величайших достижений человечества, позволившее спасти миллиарды человеческих жизней.
Как вы считаете, нужно ли все же выделить средства на изучение вроде бы не очень опасных респираторных вирусов, разработку тест-систем, доступную диагностику, вакцинопрофилактику и терапию?


Андрей Васин: Несомненно! В "мирное" время кажется, что есть более важные задачи, но вирусы - это реальная угроза человечеству. Мы живем в условиях постоянной биологической войны, только не рукотворной, а природной, которая длится миллиарды лет. Мы никогда не сможем полностью исключить вирусную угрозу, но должны быть максимально готовы ее предотвратить. Биологическая наука развивается семимильными шагами. Например, всего за несколько дней после идентификации вируса COVID-19 его геном был секвенирован и депонирован в общедоступные базы данных, что позволило оперативно начать разработку тест-систем и вакцин. В 2009 году, во время пандемии гриппа, вызванного вирусом А/H1N1, этот процесс занял гораздо больше времени. Нам нужно более подробно изучать вирусы человека и животных. Не надо забывать, что основной путь появления новых инфекций - зоонозный, поэтому крайне важно знать, что происходит с вирусами в естественных животных резервуарах. Нужно развивать новые технологии создания вакцин и препаратов. В этом смысле многообещающе выглядят РНК-вакцины, неслучайно им сейчас уделяют столько внимания. Именно это направление мы выбрали в СПбГПУ как основное.
Не знаю, насколько уместно будет такое сравнение, но инвестиции в вирусологию - это как страховой полис на автомобиль. Пока с автомобилем все в порядке, кажется: зачем я заплатил за полис, лучше бы потратил на что-то более насущное. Но если с автомобилем что-то случилось, начинаешь понимать, что без страхового полиса ты остался бы ни с чем. Думаю, что даже небольшой части суммы экономических потерь от нынешней пандемии хватило бы на поддержание и оснащение вирусологических лабораторий по всему миру на многие годы.
Читайте также:


