Задняя обратимая лейкоэнцефалопатия богданов статья
Аннотация научной статьи по клинической медицине, автор научной работы — Богданов Э. И., Хасанов И. А., Мамедов Х. И., Хасанова Д. М.
В статье представлены современные сведения об этиологии, патогенезе, клинической картине и МР-характеристиках синдрома задней обратимой лейкоэнцефалопатии, а также его дифференциальная диагностика с инфарктами в бассейне задних мозговых артерий . Кроме того приведено собственное наблюдение случая синдрома задней обратимой лейкоэнце-фалопатии.
Похожие темы научных работ по клинической медицине , автор научной работы — Богданов Э. И., Хасанов И. А., Мамедов Х. И., Хасанова Д. М.
Differential diagnosis of posterior reversible leukoencephalopathy syndrome and infarcts in the pool posterior cerebral arteries
The paper presents contemporary data on etiology, pathogenesis, clinical features and MR characteristics of posterior reversible leukoencephalopathy syndrome and its differential diagnosis with infarcts in the pool posterior cerebral arteries. Besides the own observation case of reversible posterior leukoencephalopathy syndrome is introduced here.
Э.И. БОГДАНОВ, И.А. ХАСАНОВ, Х.И. МАМЕДОВ, Д.М. ХАСАНОВА УДК 616.831-005-036.i-07
Республиканская клиническая больница М3 РТ, г. Казань Казанский государственный медицинский университет
Дифференциальная диагностика синдрома задней обратимой лейкоэнцефалопатии и инфарктов в бассейне задних мозговых артерий
I Богданов Энвер Ибрагимович
доктор медицинских наук, профессор, заведующий кафедрой неврологии и реабилитации 420012, г. Казань, ул. Бутлерова, д. 49, тел. (843) 261-84-35, e-mail: enver_bogdanov@mail.ru
В статье представлены современные сведения об этиологии, патогенезе, клинической картине и МР-характеристиках синдрома задней обратимой лейкоэнцефалопатии, а также его дифференциальная диагностика с инфарктами в бассейне задних мозговых артерий. Кроме того приведено собственное наблюдение случая синдрома задней обратимой лейкоэнце-фалопатии.
Ключевые слова: синдром задней обратимой лейкоэнцефалопатии, инфаркты в бассейне задних мозговых артерий, вазогенный отек головного мозга, инфаркт мозга.
E.I. BOGDANOV, I.A. KHASANOV, H.I. MAMEDOV, D.M. KHASANOVA
Republican Clinical Hospital of Ministry of Health Care of the Republic of Tatarstan, Kazan Kazan State Medical University
Differential diagnosis of posterior reversible leukoencephalopathy syndrome and infarcts in the pool posterior cerebral arteries
The paper presents contemporary data on etiology, pathogenesis, clinical features and MR characteristics of posterior reversible leukoencephalopathy syndrome and its differential diagnosis with infarcts in the pool posterior cerebral arteries. Besides the own observation case of reversible posterior leukoencephalopathy syndrome is introduced here.
Keywords: posterior reversible leukoencephalopathy syndrome, posterior circulation infarcts, vasogenic edema of brain, brain infarcts.
В последние десятилетия с развитием методов нейровизуализации выделился ряд патологических состояний, часто имитирующих острые нарушения мозгового кровообращения, среди которых особое место занимает синдром задней обратимой лейкоэнцефалопатии (СЗОЛ), впервые описанный и. НтсИеу и соавт. в 1996 г [11]. Данный синдром нередко ошибочно расценивается как билатеральный инфаркт в бассейне задних мозговых артерий вследствие эмболической окклюзии дистального отдела основной артерии, что влечет за собой неадекватное лечение и, соответственно, неблагоприятный прогноз для больного. В связи с этим представляется полезным
провести анализ современных данных литературы по данной проблеме и представить описание наблюдения СЗОЛ из собственной практики.
СЗОЛ представляет собой состояние, характеризующееся острым потенциально обратимым вазогенным отеком субкортикального белого вещества, преимущественно захватывающим затылочные и теменные доли головного мозга [1, 10, 12, 15]. Патологический процесс также может распространяться на височные и лобные доли, базальные ганглии, ствол мозга и мозжечок [10, 11]. Иногда наряду с белым поражается и прилежащее серое вещество [12].
Патогенетические механизмы, лежащие в основе СЗОЛ, в настоящее время изучены не достаточно полно. На сегодняшний день существуют две теории, призванные объяснить формирование вазогенного отека белого вещества при артериальной гипертензии. Согласно первой теории, получившей наибольшее распространение, внезапное значительное повышение артериального давления вызывает нарушения в системе ауторегуляции мозгового кровообращения, что приводит к дилатации церебральных артериол, открытию эндотелиальных клеточных соединений с последующим выходом плазмы и форменных элементов во внеклеточное пространство. Преимущественное вовлечение задних отделов головного мозга объясняется тем, что симпатическая иннервация в сосудах вертебро-базилярного бассейна представлена не столь выраженно, как в каротидном бассейне, соответственно, физиологический адренергический дефицит в данной области делает ее более чувствительной к резким подъемам АД и приводит к преждевременной потере вазоконстрикторных свойств в ответ на действие повреждающего фактора [4, 7,
13, 17]. Другая теория развивает гипотезу компенсаторного усиления церебральной ауторегуляции в ответ на острую значительную гипертензию, что ведет к вазоспазму, уменьшению церебрального кровотока (преимущественно в зонах смежного кровоснабжения) и ишемическому цитотоксическому, а затем и к вазогенному отеку мозга [7, 12].
Имеются также данные о том, что при использовании ряда иммуносупрессантов имеет место прямое токсическое воздействие на сосудистый эндотелий, которое может вести за собой формирование вазогенного отека и СЗОЛ [5, 10, 11]. Аналогичное поражение эндотелиальных клеток развивается и при некоторых метаболических нарушениях (в том числе при уремической энцефалопатии) [10].
СЗОЛ наблюдается у пациентов различных возрастных групп (от 4 до 90 лет), несколько чаще у женщин, чем у мужчин [4, 7, 8].
Наиболее часто СЗОЛ ассоциирован с артериальной гипертензией, преэклампсией и эклампсией, применением ци-тотоксических и иммуносупрессивных препаратов и нарушением функции почек различной этиологии (в первую очередь гломерулонефрит, люпус-нефрит и острая почечная недостаточность) [10]. Существуют и другие причины, способные спровоцировать развитие синдрома, хотя встречаются они гораздо реже: системные заболевания (в том числе системная красная волчанка, узелковый полиартериит и синдром Бехче-та), тромбоцитопеническая пурпура, порфирия, массивные гемотрансфузии, сепсис, несахарный диабет, лекарственно-индуцированный гепаторенальный синдром, внутривенное введение иммуноглобулина, высокие дозы стероидов, передозировка парацетамола, гиповолемический шок и тяжелые нарушения водно-элеткролитного баланса [10, 15].
Несмотря на то, что в подавляющем большинстве случаев развитию СЗОЛ предшествует значительный подъем артериального давления, описаны пациенты с нормальным или умеренно повышенным АД, но почти все они имели тяжелые метаболические нарушения (ишемическая болезнь кишечника, септическое состояние, лихорадка, лейкоцитоз, электролитные расстройства и др.) [4, 7].
Основными клиническими проявлениями СЗОЛ являются головная боль, головокружение, тошнота, рвота, эпилептические припадки, поведенческие расстройства, расстройства сознания (от сомнолентности до комы) и зрительные нарушения в виде гемианопсии, скотом, корковой слепоты, синдрома Антона. Эпилептические припадки нередко развиваются в дебюте заболевания и почти всегда представляют собой вторично генерализованные тонико-клонические судороги, которым зачастую
предшествует аура в виде зрительных галлюцинаций. Сухожильные рефлексы обычно повышены. В ряде случаев могут иметь место очаговые неврологические симптомы вплоть до развития глубоких парезов, грубых чувствительных нарушений и дискоординаторных расстройств. При осмотре глазного дна патологии обычно не выявляется. При адекватном лечении регресс неврологических нарушений происходит обычно в течение нескольких недель (описаны случаи восстановления пациентов от нескольких дней до года и более) [3, 11, 12]. Повторные эпизоды СЗОЛ отмечаются редко [13].
Нейровизуализационные изменения на МРТ при СЗОЛ обычно ассоциированы с повышением интенсивности сигнала на Т2-взвешенных изображениях, преимущественно в задних областях головного мозга, что связано с субкортикальным вазогенным отеком белого вещества [2, 14]. Лучше всего нарушения визуализируются в режиме FLAIR, при котором происходит подавление сигнала от цереброспинальной жидкости и выявляются даже малозаметные изменения, характерные для СЗОЛ [6]. Дополнительные МРТ-режимы - DWI и ADC-картирование выявляют микроскопическое движению (диффузию) молекулярной воды в клетках. Они позволяют различить вазогенный отек, имеющий место при СЗОЛ, от цитотоксического отека, характерного для ишемии и инфарктов в бассейне задних мозговых артерий. В зоне острого инфаркта происходит разрыв макроэргичных фосфатных связей, что ведет к угнетению активности Na-K-АТФазы. Вода депонируется внутриклеточно и ее движение ограничивается, что выявляется значительной гиперинтенсивностью на DWI и гипоинтенсивностью на ADC. При СЗОЛ же, наоборот, нарастает область вазогенного отека, это характеризуется гипо- или изоинтенсивными очагами на МРТ DWI и повышением интенсивности сигнала при ADC-картировании (участки поражения выглядят ярче интактных областей) [4, 10, 14, 15]. Большинство нарушений при СЗОЛ не отражаются на Т1-взвешенных изображениях [12].
Определяющей характеристикой СЗОЛ является полная ее обратимость. Время проведения повторной нейровизуализации для определения выздоровления пациента точно не установлено. Согласно данным некоторых авторов, разрешение отека по данным МРТ может происходить от нескольких дней до нескольких недель [12].
Высокоинтенсивный сигнал пораженных областей в Т2-режиме может выходить за пределы типичных областей, захватывая лобные доли, базальные ганглии, таламус и мозговой ствол. Поражения при СЗОЛ не всегда строго ограничиваются белым веществом. Вовлечение серого вещества происходит более чем в 40% случаев и даже чаще, согласно различным отчетам [13]. Обычно нейровизуализационные нарушения на МРТ симметричны, хотя унилатеральное поражение встречается не так уж редко [2, 6, 10].
Хотя процесс обычно обратим, в ряде случаев, особенно при несвоевременном и/или неадекватном лечении, состояние может прогрессировать вплоть до возникновения необратимых изменений в головном мозге и даже лейкомаляции [4, 16]. Приблизительно у % больных после перенесенного СЗОЛ на МРТ визуализируются небольшие резидуальные инфаркты. Вероятно, данные находки отражают преобразование вазогенного отека в цитотоксический (по другой версии - наличие пред-существующей ишемической болезни мозга) [12]. Другими потенциальными осложнениями при СЗОЛ, особенно у пациентов с коагулопатиями, являются внутримозговые кровоизлияния (по типу гематомы или геморрагического пропитывания очагов, реже - субарахноидальные кровоизлияния). Они имеют место примерно в 15% случаев СЗОЛ [3, 13].
При СЗОЛ, в отличие от ишемического инсульта, в патологический процесс практически никогда не вовлекаются шпорные
борозды и парамедианные извилины [7]. У пациентов с инфарктом затылочных долей часто обнаруживается одновременное ишемическое поражение таламуса и среднего мозга [9].
Своевременный дифференциальный диагноз данных состояний позволяет определить верную тактику ведения пациентов: при ишемическом инсульте в начале лечения рекомендуется поддерживать умеренную гипертензию и, при отсутствии противопоказаний, ставить вопрос о проведении тромболитической терапии, а при СЗОЛ, наоборот, чтобы обратить патологический процесс и упредить возникновение необратимых изменений в головном мозге, необходимо своевременное и адекватное снижение артериального давления, тромболизис противопоказан.
Клинический пример. Пациентка А., 18 лет, 29.01.2010 г. поступила на стационарное лечение в отделение патологии беременных. Установлен диагноз — беременность 32-33 недели. Гестоз средней степени тяжести. Хроническая фетоплацентарная недостаточность. Асимметричная форма синдрома задержки развития плода I степени. Маловодие.
При поступлении субъективных жалоб не предъявляла. Объективно отмечались отеки стоп и голеней, АД -160/110 мм рт. ст., протеинурия -0,4 г/л, гемоглобин -106 г/л, Н1- 34 %, СОЭ -46 мм/ч.
На фоне проводимой терапии с 29.01.2010 г. по 10.02.2010 г. АД стабилизировалось до цифр 120-130/70-80 мм рт. ст., отеки регрессировали, отмечалось незначительное увеличение про-теинурии до 0,6 г/л.
Утром 11.02.2010 г. возникли жалобы на интенсивные давящие головные боли. Объективно АД повысилось до 160/100 мм рт. ст., появилась пастозность голеней, лица. Белок в моче увеличился до 1,7 г/л. Учитывая прогрессирование гестоза, появление клиники преэклампсии, отсутствие эффекта от проводимой терапии, принято решение завершить беременность путем операции кесарева сечения в экстренном порядке. Операция проведена под эпидуральной анестезией. Кровопотеря во время операции составила 600 мл. Через 3 ч. 15 мин. после окончания операции у больной развились генерализованные тонико-клонические судороги с потерей сознания. Приступ купирован в/в введением диазепама, через 15 минут больная пришла в сознание, о случившемся не помнила. Через час приступ повторился вновь, больная введена в медикаментозный сон путем введения дроперидола 2,0 в/в + реланиума 10 мг в/в + про-медола 1,0 в/м. Объективно после второго припадка: больная в медикаментозном сне, на болевые раздражители реагирует. Лицо симметричное, язык по средней линии. Сухожильные рефлексы вызываются, с расширенных зон, симметричные. Аналог Россолимо с 2-х сторон, патологических стопных рефлексов нет. Ригидность мышц затылка на 1,5-2 см, симптом Кернига 160° с обеих сторон. Умеренные отеки в дистальных отделах нижних конечностей. АД 160/100 мм рт. ст. С целью создания охранительного режима состояние медикаментозного сна поддерживалось у больной до утра 12.02.2010 г.
Утром 12.02.2010 г. больная в сознании, оглушена, на вопросы отвечает не сразу, команды выполняет после нескольких повторений. Предъявляет жалобы на тяжесть в голове, умеренные диффузные головные боли. Появились зрительные нарушения - мерцающая скотома, не исчезающая при закрытии глаз. Зрачки равные, фотореакции сохранены. Глазные движения в полном объеме, нистагмоидные подергивания в крайних отведениях. Лицо симметричное, язык по средней линии. Сухожильные рефлексы с конечностей вызываются, без разницы сторон, с расширенных зон. Аналог Россолимо с 2-х сторон. Ригидность мышц затылка и симптом Кернига 160° с обеих сторон сохраняются. АД 135/90, ЧСС 96 в минуту.
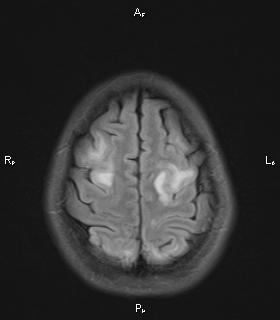
На проведенной 13.02.2010 г. МРТ головного мозга выявляются признаки вазогенного отека серого и белого вещества конвекситальных отделов теменно-затылочных долей, ножек мозга, моста, а также подкорковых ядер слева.
На фоне проводимой терапии (магния сульфат 25%, дек-саметазон, фуросемид, эналаприл) к 18.02.2010 г. состояние больной полностью стабилизировалось, жалоб нет, зрительных нарушений нет, АД 120/80 мм рт. ст., лабораторные показатели в пределах нормальных значений, в неврологическом статусе -без особенностей.
1. Скворцова В.И., Губский Л.В., Мельникова Е.А. Синдром задней обратимой энцефалопатии // Журнал неврологии и психиатрии им. Корсакова. — 2010. — № 5. — С. 104-109.
2. Ahn K.J., You W.J., Jeong S.L. et. al. Atypical manifestations of reversible posterior leukoencephalopathy syndrome // AJNR Am. J. Neuroradiol. — 2004. — Vol. 46, № 12. — P. 978-983.
3. Aranas R.M., Prabhakaran S., Lee V.H. Posterior Reversible Encephalopathy Syndrome associated with Hemorrage // Neurocrit. Care. — 2009. — № 3. — P. 306-312.
4. Ay H., Buonanno F.S., Schaefer P.W. et. al. Posterior leukoencephalopathy without severe hypertension: utility of diffusion-weighted MRI // J. Neurol. — 1998. — №. 51. — P. 1369-1376.
5. Bhatt A., Farooq M.U., Majid A. et. al. Chemotherapy-related Posterior reversible encephalopathy syndrome // Nature Cinical. Practice.
— 2009. — Vol. 5, № 3. — P. 163-169.
6. Casey S.O., Sampaio R.C., Michel E. et. al. Posterior reversible leukoencephalopathy syndrome // AJNR Am. J. Neuroradiol. — 2000.
— Vol. 21, № 7. — P. 1199-1206.
7. Chou S.O., Lai P.H., Yeh L.R. et. al. Posterior reversible leukoencephalopathy syndrome: magnetic resonance imaging and diffusion-weighted imaging in 12 cases // Kaohsiung J. Med. Sci. — 2004. — Vol. 20, № 8. — P. 381-388.
8. Covarrubias D.J., Leutmer P.H., Caumpeau N.G. Posterior reversible leukoencephalopathy syndrome: prognostic utility of quantitative diffusion-weighted MR image // AJNR Am. J. Neuroradiol. — 2002. — Vol. 23, № 6. — P.1038-1048.
9. Dineen R. Imaging of acute neurological conditions in pregnancy and the puerperium // Clinical radiology. — 2005. — № 60. — P. 11561170.
10. Garg R.K. Posterior leukoencephalopathy syndrome // Postgrad. Med. J. — 2001. Vol. 77, № 903. — P. 24-28.
11. Hinchey J., Chaves C., Appignani B. et al. A reversible posterior leukoencephalopathy syndrome // N. Engl. J. Med. — 1996. — Vol. 22, 334, № 8. — P. 494-500.
12. Lee V.H., Wijdicks E.F.M., Manno E.M. et. al. Clinical Spectrum of reversible posterior leukoencephalopathy syndrome // ARCH. NEUROL. — 2008. — Vol. 65, № 2. — P. 205-210.
13. Perloff D. Hypertension and pregnancy-related hypertension // Cardiol. Clin. — 1998. — № 16. — P. 79-101.
Похожие темы научных работ по клинической медицине , автор научной работы — Савицкая И.Б., Иевлева В.И., Гетманенко А.В., Карпенко В.Г., Супрун С.Н.
САВИЦКАЯ И.Б., ИЕВЛЕВА В.И., ГЕТМАНЕНКО A.B., КАРПЕНКО В.Г., СУПРУН С.Н., КУРСОВ С.Н. Харьковская медицинская академия последипломного образования Харьковская больница скорой и неотложной медицинской помощи Харьковская городская клиническая больница № 7
СИНДРОМ ОБРАТИМОЙ ЗАДНЕЙ ЭНЦЕФАЛОПАТИИ У БЕРЕМЕННОЙ ПАЦИЕНТКИ (КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ)
Больная Л., 28 лет, находилась на стационарном лечении в Харьковской городской клинической больнице скорой и неотложной медицинской помощи (ХГКБСНМП).
При поступлении — жалобы на выраженную головную боль диффузного характера, сопровождающуюся тошнотой, рвотой, на общую слабость.
Заболела остро утром, когда появилась вышеописанная симптоматика. Обратилась за медицинской помощью в роддом по месту жительства, где после клинико-лабораторного обследования установлен диагноз: III беременность, 23 недели, преэклампсия I степени. Хронический инфекционно-аллергический энцефалит с частыми вегетативно-сосудистыми пароксизмами, эписиндромом. Хронический бронхит. Хронический фарингит. Миопия средней степени. Ангиопатия сетчатки средней степени. ВСД по смешанному типу. Однако на фоне проводимой терапии (инфузионная, противо-судорожная терапия) у больной наросла головная боль, сопровождающаяся тошнотой, рвотой, отмечалось колебание цифр АД от 130/80 до 90/60 мм рт.ст., возобновились и участились судорожные приступы в виде petit mal. После расширенного консилиума в связи с наличием тяжелой сопутствующей неврологической патологии беременная переведена в ОИТ многопрофильной больницы (ХГКБСНМП).
Из анамнеза жизни известно, что болеет в течение 10 лет, когда остро на 23-25-й неделе первой беременности появилась головная боль, развился приступ с потерей сознания, судорогами в конечностях. Лечилась стационарно в неврологическом отделении с диагнозом: острый вирусный стволовой энцефалит с судорожным синдромом. Беременность прервана по жизненным показаниям (усугубление церебральной симптоматики на фоне беременности), судорожный синдром в послеоперационном периоде не возобновлялся.
Повторные курсы лечения проводились ам-булаторно и стационарно с диагнозом: стойкие последствия перенесенного инфекционно-ал-лергического арахноэнцефалита с выраженным ликворно-гипертензионным синдромом, лик-ворно-венозной дистензией, вестибулоатакти-ческим синдромом, левосторонней пирамидной недостаточностью, частыми вегетативно-сосудистыми пароксизмами, синкопальными состояниями, эписиндромом (в анамнезе), астеническим синдромом. Признана инвалидом III группы.
Болезнь Боткина, сахарный диабет, туберкулез, венерические и кожные заболевания отрицает. Аллергологический анамнез не отягощен. Со слов больной, инфекционных заболеваний в семье нет.
Status praesens objectivus communis: нормо-стеник. Кожные покровы и видимые слизистые бледно-розовые, чистые, свободные от высыпаний. Периферические лимфоузлы не увеличены. Аускультативно в легких везикулярное дыхание, хрипов нет. Тоны сердца приглушены, ритмичные. АД 140/80 мм рт.ст., пульс 76 ударов в 1 минуту. Живот мягкий, безболезненный, патологические образования на всем протяжении не пальпируются. Стул и диурез в норме. Пастоз-ность голеней.
Status neurologicus: сознание ясное. Менин-геальные знаки отрицательные. Глазные щели D = S. Зрачки D = S. Фотореакции средней живости D = S. Корнеальные рефлексы D = S. Нистагма, диплопии нет. Лицо симметричное. Положительный симптом Манна. Язык по средней линии. Глоточные рефлексы сохранены. Фонация достаточная. Сухожильные рефлексы с рук, ног оживлены слева. Левосторонний гемипарез
до 4,5 балла. Мышечный тонус снижен в левых конечностях. Левосторонняя гемигипестезия. Брюшные рефлексы не вызываются. Патологические стопные рефлексы не вызываются. Коорди-наторные пробы выполняет удовлетворительно. Речь не нарушена.
Во время осмотра (в течение 10 минут) дважды отмечались приступы потери сознания по типу petit mal, сопровождающиеся отведением глазных яблок влево с ротаторным нистагмом, отсутствием фотореакций, продуктивного контакта в течение 10—12 секунд.
Дополнительные методы исследования: клинические анализы крови, мочи, биохимии крови, коагулограммы — без особенностей.
Данные ЭЭГ свидетельствуют о повышении пароксизмальной активности на фоне дисфункции срединно-стволовых структур головного мозга.
На серии МР-томограмм (в день поступления), взвешенных по Т1 и Т2, в трех проекциях визуализированы суб- и супратенториальные структуры. Между теменными и затылочными долями симметрично в обеих гемисферах определяются углубления борозд с формированием расщелин, которые окружены мозговой тканью по МР-сигналу, идентичной корковому веществу (корковая дисплазия). Боковые желудочки мозга несколько сужены, симметричны. Третий и четвертый желудочки не изменены. Хиазмальная область без особенностей, ткань гипофиза имеет обычный сигнал. Субарахноидальные конвек-ситальные пространства несколько расширены, больше в задних отделах. Срединные структуры не смещены. Краниовертебральный переход без изменений. Изменений очагового и диффузного характера не выявлено. Заключение: признаки внутричерепной гипертензии, врожденной дис-плазии.
Окулист: ангиопатия сетчатки, застойные явления на глазном дне. Миопия обоих глаз.
УЗИ органов брюшной полости, почек: хронический калькулезный холецистит.
Несмотря на проводимую противоотечную, противосудорожную терапию, нейровегетатив-ные блокады, состояние беременной пациентки прогрессивно ухудшалось. Динамическое наблюдение за больной в течение суток позволило констатировать усугубление церебральной недостаточности с судорожным синдромом — учащение и удлинение судорожных приступов (развернутых генерализованных и бессудорожных по типу petit mal).
Таким образом, у пациентки на 23-й неделе беременности развилась клиника, свидетельствующая о внутричерепной гипертензии, проявляющаяся выраженной цефалгией, судорожным синдромом, подтвердившаяся параклиническими методами (ЭЭГ, МРТ головного мозга, застойные явления на глазном дне). Симптоматика развивалась остро и стремительно нарастала в течение 48
часов (около суток в роддоме до перевода и сутки в ХГКБСНМП). Все вышеизложенное позволило заподозрить у больной синдром обратимой задней энцефалопатии (СОЗЭ) с органическим поражением ЦНС, выраженным судорожным синдромом. Расширенным консилиумом по медицинским показаниям (усугубление церебральной симптоматики на фоне беременности) принято решение о прерывании беременности путем кесарева сечения.
В послеоперационном периоде сознание ясное, пациентка адекватна, несколько заторможена вследствие продолжающейся усиленной противосудорожной терапии. Под контролем ЭЭГ, МРТ-динамики (без очаговой патологии, признаков внутричерепной гипертензии) доза противосудорожной терапии снижена до 2 табл. карбамазепина в сутки. Судорожный синдром не возобновлялся, кардиореспираторная система компенсирована, цефалгии не возобновлялись. В неврологическом статусе сохранялась левосторонняя сенсопирамидная недостаточность. Выписана из клиники на 7-е сутки после операции под наблюдение гинеколога, невролога; рекомендован контроль ЭЭГ, прием противосудорожных препаратов (карбамазепин по 200 мг 2 раза в день, вальпроком по 300 мг 2 раза в день).
Синдром обратимой задней энцефалопатии является редкой неврологической патологией, проявляющейся судорогами, головной болью, нарушением психического состояния, нарушением зрения, корковой слепотой, при наличии или без наличия гипертензии. Клиника развивается остро и стремительно нарастает в течение 12—48 часов. Развитие СОЗЭ может быть ассоциировано со следующими патологическими состояниями: острой артериальной гипертензией, преэкламп-сией и эклампсией, заболеваниями почек (гломе-рулонефрит, люпус-нефрит), сепсисом, а также с приемом иммуносупрессантов (циклоспорин, интерферон), внутривенным введением больших доз стероидов и другими состояниями [1, 2, 6, 7]. Отмечается тесная патофизиологическая связь беременности и СОЗЭ, так как гормональные изменения (повышенный уровень эстрогенов, прогестерона) при беременности приводят к стимуляции выработки факторов свертывания крови, повышению проницаемости сосудов капилляров и развитию вазогенного отека мозга.
Клинические проявления синдрома обратимой задней энцефалопатии часто являются неспецифическими, поэтому подтвердить диагноз можно с помощью МРТ (является предпочтительным методом) [6], желательно с контрастным усилением [7]. При СОЗЭ развивается обратимый вазогенный отек преимущественно в задних от-
Медицина неотложных состояний, ISSN 2224-0586
делах полушарий мозга, хотя она может осложниться и необратимым цитотоксическим отеком и инфарктом мозга. Отек захватывает преимущественно белое вещество мозга [1]. У нашей больной проявления вазогенного отека также носили обратимый характер.
При развитии данного синдрома следует проводить неотложную терапию, включая контроль артериальной гипертензии (при наличии тяжелой неконтролируемой гипертензии), противо-отечную и противосудорожную терапию, что приводит к полному обратимому развитию клинической и нейровизуализационной картины. Симптомы обычно исчезают или выраженность их уменьшается в течение нескольких дней после прекращения лечения, хотя у некоторых пациентов возможны некоторые неврологические последствия [1, 4, 5]. Таким образом, только своевременное распознавание данного состояния и немедленное начало адекватной терапии могут предотвратить более тяжелые последствия церебральной недостаточности.
1. Скворцова В.И., Губский Л.В., Мельникова Е.А. Синдром задней обратимой энцефалопатии //Журнал неврологии и психиатрии. — 2010. — № 5. — С. 104-109.
2. Богданов Э.И., Хасанов И.А., Мамедов Х.И. и др. // Неврологический журнал. — 2011. — № 5. — С. 48-56.
3. Богданов Э.И., Хасанов И.А., Мамедов Х.И. и др. //Дифференциальная диагностика синдрома задней обратимой лей-коэнцефалопатии и инфарктов в бассейне задних мозговых артерий //Практическая медицина. — 2012. — Т. 1. — С. 32-36.
4. Casey S.O., Sampaio R.C., Michel E. et al. Posterior reversibleleukoencephalopathysyndrome//Am. J. Neuroradiol. — 2000. — Vol. 21, № 7. — P. 1199-1206.
5. Chou M.C., Lai P.H., Yeh L.R. et al. Posterior reversible encephalopathy syndrome: magnetic resonance imaging and diffusion — weighted in 12 cases // Kaohsiung J. Med. Sci. — 2004. — Vol. 20(8). — P. 381-388.
6. Hinchey J., Chaves C., Appignani B. et al. A reversible posterior leukoencephalopathy syndrome // N. Engl. J. Med. — 1996. — Vol. 334, № 8. — P. 494-500.
7. Jonathan A. Edlow, Louis R. Caplan, Karen O'Brien et al. Diagnosis of acute neurological emergencies in pregnant and postpartum women // The Lancet Neurology. — 2013. — Vol. 12. — P. 175-85.
Синдром задней обратимой энцефалопатии (англ. сокращенно - PRES) - это нейротоксическое состояние возникающее вторично в ответ на неспособность системы задней циркуляции реагировать на острые изменения артериального давления. Гиперперфузия ведет к нарушению гемато-энцефалического барьера, приводя в итоге к развитию вазогенного отека, без инфаркта, чаще в теменно-затылочной области.
Синдром задней обратимой энцефалопатии так же известен под терминами острая гипертензивная энцефалопатия или задняя обратимая лейкоэнцефалопатия. Термин является неточным, поскольку при данном синдроме изменения могут распространяться за пределы задних отделов мозга. Кроме того, хотя в большинстве случаев при адекватном лечении большинство изменений полностью регрессирует, у некоторых пациентов состояние может прогрессировать приводя к постоянному повреждению паренхимы головного мозга с остаточным неврологическим дефицитом. Необходимо отличать данное состояние от хронической гипертензионной (гипертонической) энцефалопатии, также известной как гипертензивная микроангиопатия, которая приводит к микрокровоизлияниям в базальные ганглии, мост и мозжечок.
Клинические проявления включают головную боль, судороги, энцефалопатию и нарушения зрения.
К развитию данного синдрома могут предрасполагать различные клинические состояния. Хотя механизм изучен не до конца, считается что изменения связаны с нарушением целостности гемато-энцефалического барьера. Основные теории:
- повышенное артериальное давление ведет к нарушению саморегуляции, гиперперфузии, повреждению эндотелия и развитию вазогенного отека
- эндотелиальная дисфункция ведет к вазоконстрикции, гипоперфузии, развитию ишемии головного мозга с последующим формированием вазогенного отека
Однако у 25% пациентов артериальное давление не повышено или не достигает верхней границы системы саморегуляции (150-160 мм рт. ст.).
- выраженная гипертензия
- послеродовая
- эклампсия/преэклампсия
- острый гломерулонефрит
- гемолитически-уремический синдром
- тромбоцитопеническая пурпура (болезнь Верльгофа)
- системная красная волчанка
- за счет лекарственной токсичности таких препаратов как
- цисплатин
- интерферон
- эритропоэтин
- такролимус
- циклоспорин
- азатиоприн
- L-аспаргиназа
- пересадка костного мозга или стволовых клеток
- сепсис
- гипераммониемия
В большинстве случаев синдром задней обратимой энцефалопатии проявляется вазогенным отеком в теменных и затылочных долях (наблюдается в
98% случаев), что возможно связано с нарушением в системе задней циркуляции. Отек обычно симметричный. Несмотря на термин “задняя”, отек может локализоваться не только в задних отделах, но обычно ограничен сосудистым бассейном, например лобным, нижневисочным, мозжечковым и стволовым сосудистым бассейном [2]. Отек распространяется как кору так и подкорковые зоны. Основные виды (паттерны отека головного мозга):
- распространение на всю гемисферу в пределах бассейна (дословно зоны водораздела)
- вовлечение верхних лобных извилин
- преобладание в теменно-затылочных областях [2]
Проявления встречающиеся менее чем в 5% случаев синдрома задней обратимой энцефалопатии включают: ограниченный односторонний отек, центральный отек (отек ствола мозга или базальных ганглиев без вовлечения коры и подкоркового белого вещества).
Инфаркты паренхимы и кровоизлияния сочетанные с синдром задней обратимой энцефалопатии встречаются в 10-25% и 15% случаев. Наличие контрастного усиления, не зависимо от типа, не изменяет прогноз.
Затронутые области имеют пониженную, относительно неизмененной паренхимы, плотность.
Сигнальные характеристики в затронутых областях:
- T1: гипоинтенсивный МР сигнал
- T1 с парамагнетиками: пятнистое контрастное усиление встречается примерно у
35% пациентов, в остальных случая обычно имеет лептоменингеальный или кортикальный характер усиления.
Основные нозологические единицы схожие при визуализации:
- прогрессирующая мультифокальная лейкоэнцефалопатия
- поражение перивентрикулярных и подкорковых отделов, щадящее кору
- менее выраженные или отсутствующие масс-эффект и контрастное усиление
- выраженная гипогликемия
- инсульт в бассейне задней циркуляции
- включает поражение теменных долей и мозжечка
- глиоматоз головного мозга
- более асимметричный
- тромбоз сагиттального синуса
- гипоксически-ишемическая энцефалопатия
Читайте также:


