Стафилококк с конститутивным mlsb фенотипом что это
Глава из монографии "Макролиды"
Под редакцией Попковой А.М. Верткина А.Л. Колобова С.В.
При анализе резистентности к макролидам нельзя не учитывать наличие изначально резистентных (мутантных) штаммов некоторых грамположительных кокков, что в ряде случаев может ограничивать применение некоторых препаратов данной группы. Резистентность к макролидам может быть приобретена с помощью 3 различных механизмов: модификацией клетки-мишени (рибосомальной субъединицы 50 S), инактивацией и активным выведением препарата. Резистентность к макролидам в результате мутации очень редко наблюдается в клинических культурах. Наиболее часто встречающимся механизмом является посттранскрипционная модификация рибосомальной РНК 23S путем моно/диметилирования остатка аденина [24, 49, 103, 131]. В результате нарушается комплиментарность антибиотика-макролида к рибосоме, и препарат не может оказывать свое действие. Данная резистетность является перекрестной с 14- и 15-членными макролидами, стрептограминами, линкосамидами и хлорамфениколом и не является перекрестной с 16-членными макролидами. При этом гены метилаз (ферменты, индуцирующие метилирование) могут наследоваться бактериальными клетками или передаваться через плазмиды [24, 103]. Гены, кодирующие различные метилазы, определяют как эрм (эритромицин резистентная метилаза). Выялено по меньшей мере 8 классов эрм генов [63, 66, 117].
У стафилококков синтез метилаз РНК может быть конструктивным или индуцируемым 14 - членными макролидами или азалидами. 16-членные макролиды являются слабыми индукторами резистентности, и бактерии с индуцируемой резистентностью сохраняют чувствительность к 16-членным макролидам. Однако при индуцировании в присутствии эритромицина бактерии с индуцированной резистентностью нечувствительны и к 16 - членным макролидам. Бактерии, конструктивно резистентные к эритромицину, также резистентны к 16-членным макролидам [66, 152].
Большинство мутантных штаммов микроорганизмов, обладающих приобретенной резистентностью к эритромицину, обладают резистентностью и к кларитромицину [180]. Есть данные, что резистентность к кларитромицину может передаваться за счет плазмиды, кодирующей метилазу. Такие штаммы нечувствительны и к эритромицину [143].
Другие механизмы резистентности включают инактивацию эритромицин-эстеразами и макролидной фосфотрансферазой (E. coli) или неопределенными ферментами (Staphylococcus hominis, S. haemolyticus, S. saprophyticus). Штаммы S. epidermidis обнаружили резистентность к эритромицину из-за непроницаемости для препарата. Такой механизм резистентности, как активный выброс антибиотика, был отмечен для S. epidermidis, в штаммах которого связанный с АТФ белок выполнял функцию откачивающего насоса. В работе Peters и соавт. (1992) было показано, что микроорганизмы, продуцирующие b -лактамазу невосприимчивы к эритромицину и к азитромицину [179]. Возможно, что данная резистентность является приобретенной, а ген, кодирующий b -лактамазу может передаваться между различными штаммами микроорганизмов через плазмиды. Не исключено включение данного гена в микроорганизмы нормальной микрофлоры и сохранение его длительное время у микроорганизмов-сапрофитов. Поэтому, если в анамнезе было установлено наличие инфекционного заболевания, вызванного эритромицин-резистентными микроорганизмами, то применение данного препарата в дальнейшем может быть неэффективным. Возможно, что синтез b -лактамазы является одним из механизмов приобретенной резистентности к эритромицину. Однако данный вопрос требует дальнейшего изучения; в настоящее время имеющиеся литературные данные не достаточно полно охватывают эту проблему и во многом противоречивы.
Аминогликозид-резистентные штаммы S. aureus невосприимчивы и к азитромицину, и к метициллину и его производным [144]. Азитромицин неэффективен против некоторых штаммов S. pneumoniae, обладающих резистентностью к пенициллину [152], при этом есть данные, что чувствительность S. pneumoniaе к азитромицину, кларитромицину и пенициллину одинакова [141, 143].
Рис. 1.4.
Фармакокинетика азитромицина и кларитромии-цина после недельной терапии 10 мг/кг per os [123, 143]. МАК- минимальная активная концентрация. Если концентрация антибиотика больше МАК, но меньше МИК, то возможно развитие резистентности к препа-рату (закрашенная область). Видно, что закрашенная область для азитромицина существенно больше, чем для кларитромицина.
Интересно отметить тот факт, что из-за того, что время полувыведения кларитромицина составляет 5-6 часов, а азитромицина - 35-76 часов (см также гл. 2), частота развития резистености к кларитромицину существенно ниже, чем к азитромицину [127, 143]. Это обусловлено длительной персистенцией азитромицина в организме в низких концентрациях, которые не способны подавлять рост микроорганизмов, но тем не менее могут вызвать мутации, способствующие развитию резистентности (рис. 1.4).
Поэтому, так как спектр антибактериального действия препаратов во многом сходен, обычно кларитромицин предпочтительней азитромицина.
Резистентность к макролидам варьирует во всем мире в зависимости от клинического применения, видов бактерий и других факторов, таких как источник штаммов (больница/общество). Первые резистентные к эритромицину штаммы были обнаружены еще в 1956 г. у стафилококков (фенотип МЛСb) и с тех пор распространились на многие роды бактерий [7, 8].
Во Франции распространенность резистентности фенотипа МЛСb у стафилококков возросла с 1954 г. до 1962 г. и стабилизовалась на уровне около 40% (больница) и 10% (общество). Последующая эволюция резистентного фенотипа МЛСb в больнице развивалась параллельно с эволюцией резистентности к метициллину и отражает появление мультирезистентных форм в больнице. Отмечены большие межбольничные и межпалатные различия. В 1988 г. общая резистентность во Франции составила около 30% (больница) и 20% (общество). В многоцентровом международном эпидемиологическом исследовании более 1000 штаммов S. aureus в Англии 14% штаммов оказались резистентными к эритромицину, против 1,7% одновременно к спирамицину и эритромицину. Применение неиндукторных макролидов вызвало появление структурного фенотипа, который увеличил с 30 до 60% общее число штаммов S. aureus, резистентных к МЛСb. Что касается стрептококков, наблюдаемые различия зависят от штамма. У энтерококков резистентность очень высока (50 - 60%); с 1989 г. отмечалось увеличение процентного содержания эритромицин-резистентных культур у стрептококков группы А с 4% (1981 г.) до 24% (1990 г.) Возникает проблема среди пневмококков; первые резистентные штаммы были обнаружены в 1976 г., а в 1990 г. их частота возрастала до 29% во Франции, до 6,5% в Англии, 60% и 23 % в Испании у детей младшего возраста и у взрослых соответственно. У Bacteroides общая резистентность к МЛСb низкая [59, 74, 83, 92, 102, 125, 141, 144, 152, 164, 167, 194, 198, 208].
Согласно статистическому исследованию, проведенному в США, приблизительно 30% бактериальных инфекций, вызванных S. aureus в этой стране обладает одновременно резистентностью как к атибитикам-макролидам, так и к метициллину и аминогликозидам [144].
Однако появление препаратов нового поколения в значительной степени решило проблему резистентности: штаммы грамположительных кокков, обладающих резистентностью к макролидам первого поколения, чаще всего не обладают резистентностью к препаратам второй генерации [24, 49]. Резистентность к натамицину в клинической практике не отмечена [58, 73, 77, 129, 175].
Частота встречаемости резистентных штаммов при длительном назначении антибиотиков-макролидов in vivo представлена в таблице 1.4.
Таблица 1.4.
Частота встречаемости резистентных штаммов при длительном назначении антибиотиков-макролидов in vivo ( в %) [117].
Механизмы резистентности к макролидам принято делить на три типа: на уровне внутриклеточной мишени - проникший в клетку антибиотик не реагирует с рибосомой; на уровне защитных ферментов - проникший в клетку антибиотик инактивируется тем или иным путем; на уровне клеточной мембраны - за счет усиления функций системы активного выброса ксенобиотиков .
Комплексная проблема резистентности к макролидам оказывается при ее подробном рассмотрении связанной не только с проблемой целенаправленного создания их новых структур, проблемами эпидемиологии и экологии, но и с проблемами биотехнологии, учитывая наличие в кластере у продуцентов этих антибиотиков генов биосинтеза и генов, колирующих системы защиты от аутогенных антибиотиков.
Наиболее ранние данные (50-60-х годов) касаются механизма резистентности к макролидам, а точнее - к эритромицину у грамположительных кокков. Было отмечено, что рибосомы резистентных штаммов не связывают меченный радиоизотопами эритромицин; соответственно, активность бесклеточных систем белкового синтеза с рибосомами из резистентных штаммов не подавлялась эритромицином, в отличие от активности систем из чувствительных штаммов.
Поскольку уже было известно, что эритромицин связывается с пептидилтрансферазным центром рибосом, последовал вывод, что у резистентных штаммов изменена конформация этого центра, причем таким образом, что связывание эритромицина предотвращается. При этом было отмечено, что с измененным пептидилтрансферазнам центром не связывается и второй известный в те годы макролидный антибиотик - олеандомицин (имеющий, подобно эритромицину, 14-членное лактонное кольцо), а также антибиотики другой структуры - линкозамиды ( линкомицин , клиндамицин ) и стрептограмины . Перекрестная резистентность к трем группам антибиотиков - макролидам, линкозамидам и стрептограминам получила наименование MLS-резистентности. Работы, связанные с ее обнаружением и изучением механизмов, обобщены в ряде ранних обзоров и монографий.
Выяснено, что изменение конформации пептидилтрансферазного центра обусловлено метилированием в 23 S рибосомной РНК одного из остатков аденина специфической метилазой (кофактор S-аденозилметионин). Ген, кодирующий этот фермент, получил обозначение erm. Локализация гена может быть как в хромосоме, так и в плазмиде. В целом работы в этой области проводились по нескольким направлениям: исследование наличия конститутивной или индуцированной MLS-резистентности у тех или иных организмов; исследование этого типа резистентности на молекулярно-генетическом и молекулярно-биологическом уровне; исследование сочетания в одной клетке MLS-резистентности с другими типами резистентности к макролидам.
Значительное внимание уделялось проблеме индукции резистентности к макролидам, в частности, выяснению связи между индуцирующей активностью и реагированием антибиотика с местом его связывания на рибосоме. Для индукции резистентности у Staphylococcus aureus (в случае резистентных штаммов) достаточно их экспозиции с субингибиторными концентрациями макролидов. Учитывая многочисленность структур, перекрывающих место связывания эритромицина на большой рибосомной субъединице, к наличию индукции или ее отсутствию привлечено внимание с позиции структурно-функциональных исследований. В результатах работ уже 70-х годов оказалось немало противоречий. В одних случаях индуцирующей активностью обладал широкий круг антибиотиков, принадлежащих к структурно разнообразной MLS-группе, в других - только 14-членные макролиды [7]. Был сделан вывод, что не только особенности структуры представителя MLS-группы антибиотиков, но и свойства штамма определяют возможность индукции. Описан, в частности, мутант, у которого индукция была связана с высокой температурой [8]. По данным некоторых сообщений 10, различия в индуцирующей активности отдельных макролидов отчасти связаны со структурой и местом связи с макроциклическим кольцом их 6-дезоксисахаров. Работа с 18 макролидными производными эритромицина показала, что индуцирующая активность наблюдается при присоединении сахара (кладинозы) именно к С-3 лактонного кольца. Замещение кладинозы по С-4 вело к исчезновению индуцирующей, но не антибиотической активности. Это свидетельствует о том, что два вида биологической активности - подавление функций рибосомы и индукция резистентности могут быть разобщены [7].

Стафилококк признан одним из наиболее распространенных возбудителей различных инфекций человека. Устойчивость к антимикробным препаратам среди стафилококков является растущей проблемой. Это привело к возобновлению интереса к использованию макролидов, линкозамидов и стрептограминов [6, 7]. Макролиды, линкозамиды и стрептограмины были объединены в одну группу (МЛС), это связано с общностью их механизмов действия и резистентности к ним микроорганизмов. Устойчивость к препаратам группы МЛС может быть связана с модификацией мишени действия, их активным выведением и быстрой инактивацией [4].
Наиболее распространенным и клинически важным механизмом резистентности стафилококков является метилирование. Известны два основных типа экспрессии устойчивости, связанной с метилированием: конститутивный и индуцибельный. При конститутивном типе синтез фермента метилазы (соответственно модификация мишени) происходит постоянно и не зависит от внешних условий, и бактерии проявляют перекрестную устойчивость ко всем макролидам, линкозамидам и стрептограминам. При индуцибельном – фермент синтезируется только в ответ на появление в окружающей среде антибиотиков. Штаммы с индуцибельным характером экспрессии метилаз, устойчивые к 14- и 15-членным макролидам, сохраняют чувствительность к 16 -членным макролидам и стрептограминам [4].
В последнее время, клиндамицин из-за его активного проникновения в ткани, является одним из наиболее эффективных антибиотиков в лечении инфекций, вызванных Staphylococcus aureus, особенно кожи и мягких тканей и остеомиелита [8].
Тем не менее выявленные чувствительные к клиндамицину стафилококки могут проявить индуцибельную резистентность во время проводимого лечения. На основании проведенных исследований было сделано заключение, что резистентные к эритромицину и чувствительные к клиндамицину стафилококки в ходе антибиотикотерапии могут приобретать резистентность, что и приводит к неэффективности проводимого лечения. Исходя из этого, возникает необходимость определения индуцибельного типа резистентности к клиндамицину с помощью постановки диско-диффузионого D-теста, для выявления антагонизма между клиндамицином и эритромицином [9, 10].
Материалы и методы исследования
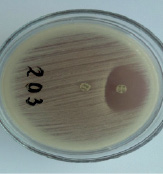
Рис. 1. Д-зона ингибирования вокруг диска с клиндамицином указывает на индуцибельный тип резистентности
Методика постановки D-теста и интерпритация результатов осуществлялась следующим образом: суспензию Staphylococcus spp. мутностью 0,5 McFarland наносили на поверхность Мюллера-Хинтон агара в чашке Петри, затем помещали диски с эритромицином (15 мкг) и клиндамицином (2 мкг) на расстоянии между ними 15 мм. После инкубации при 37°C в течение 18–24 часов уплощение зоны (D-образные) вокруг клиндамицина указывало на индуцибельный тип резистентности к клиндамицину (рис. 1). Если D-тест положительный (D+), то изолят следует считать устойчивым к клиндамицину, если отрицательный (D-), то чувствительным.
Результаты исследования и их обсуждение
По результатам идентификации установлено, что видовой состав выявленных стафилококков включал: коагулазоположительный вид S. aureus – 174 шамма и ряд коагулазонегативных видов (S. epidermidis, S. hyicus, S. auricularis, S. haemolyticus, S. hominis, S. capitis, S. saprophyticus) – 56 штаммов. Среди выявленных стафилококков S. aureus встречался в три раза чаще (рис. 2).
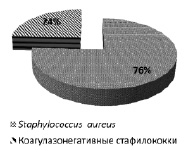
Рис. 2. Частота выявления Staphylococcus aureus и коагулазонегативных стафилококков из ран и свищей у больных хроническим остеомиелитом
Проведена сравнительная характеристика восприимчивости стафилококков к эритромицину и клиндамицину (рис. 3). Было установлено, что чаще встречаются штаммы, резистентные к эритромицину, причем у метициллинрезистентных коагулазонегативных стафилококков (MRCNS) эта разница составляла 36,4 %.
Среди метициллинрезистентных штаммов устойчивых к клиндамицину и эритромицину лидирующее положение занимает S. aureus, среди метициллинчувствительных – коагулазонегативные стафилококки (CNS).
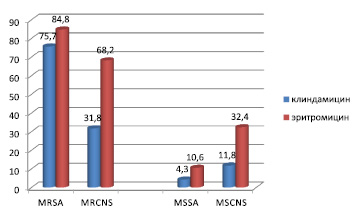
Рис. 3. Сравнительная характеристика резистентности эритромицина и клиндамицина к стафилококкам. Примечание. MRSA – метициллинрезистентные Staphylococcus aureus, MRCNS – метициллинрезистентные коагулазонегативные стафилококки, MSSA – метициллинчувствительные Staphylococcus aureus, MSCNS – метициллинчувствительные коагулазонегативные стафилококки
Сравнение различных типов восприимчивости стафилококка к клиндамицину и эритромицину
Антибиотики прямо под нашим носом
Немецкие ученые обнаружили новое оружие для борьбы с больничным монстром – мультирезистентным золотистым стафилококком. Долгие годы оно скрывалось не в вечной мерзлоте или Марианской впадине, а прямо под нашим носом. Вернее – в нём.
В последние годы во всем мире увеличилось количество инфекционных заболеваний, вызванных устойчивыми к антибиотикам бактериями. Организмы с множественной лекарственной резистентностью (multidrug-resistant organisms, MDRO), такие как метициллин-резистентный золотистый стафилококк, нечувствительные к ванкомицину энтерококки или резистентные к цефалоспоринам третьего поколения грамотрицательные бактерии, в ближайшие десятилетия могут стать более частыми причинами смерти, чем рак [1].
Несколько лет назад удалось обнаружить, что представители человеческой микробиоты способны производить бактериоцины, поражающие близкородственных бактерий [2]. Например, в 2014 году из человеческого комменсала Lactobacillus gasseri выделили и описали новый синтезируемый рибосомами тиопептидный антибиотик – лактоциллин [3].
Немецкий исследователь Александр Ципперер со своими сотрудниками в июле 2016 года сообщил о том, что обнаружил в человеческом носу бактерию Staphylococcus lugdunensis IVK28, которая подавляет рост метициллин-резистентного золотистого стафилококка (methicillin-resistant Staphylococcus aureus, MRSA) [1].
Стафилококки относятся к типичным бактериям-комменсалам, колонизирующим кожу и поверхности слизистых оболочек. Staphylococcus aureus – шаровидные грамположительные бактерии, вырабатывающие каротиноидный пигмент, который придает их клеткам золотистый цвет (рис. 1). Эти микроорганизмы чрезвычайно устойчивы к внешним воздействиям и выживают в воздухе, пыли, почве, продуктах питания, на оборудовании пищевых производств и предметах быта [6, 7].

Рисунок 1. Staphylococcus aureus и лейкоциты. Рисунок с сайта relatedscience.blogspot.ru.
Staphylococcus aureus – бактерия условно-патогенная, проявляющая свои патологические свойства только в благоприятных условиях, а создает их, как правило, ослабление иммунитета носителя. Активная жизнедеятельность стафилококка может привести к разнообразным заболеваниям [5, 7, 8]:
- кожи (прыщи, фурункулы, синдром ошпаренной кожи);
- органов дыхания (плеврит, пневмония);
- костной и соединительной тканей (артрит, остеомиелит);
- нервной системы и органов чувств (отит, менингит);
- сердечно-сосудистой системы (эндокардит, флебит, стафилококковая бактериемия).
Факторы патогенности S.aureus – это микрокапсула, компоненты клеточной стенки, ферменты агрессии и токсины. Микрокапсулы защищают клетки бактерий от фагоцитоза, способствуют их адгезии и распространению по организму хозяина. Составляющие клеточной стенки (например пептидогликан, тейхоевые кислоты и белок А) вызывают развитие воспаления, обездвиживают фагоциты и нейтрализуют иммуноглобулины. Коагулаза, главный фермент агрессии, вызывает свертывание плазмы крови [7, 9].
Наиболее опасны метициллин-резистентные стафилококки (methicillin-resistant S.aureus, MRSA) (рис. 2). Метициллин – это модифицированный пенициллин, с помощью которого еще недавно успешно боролись со стафилококковой инфекцией. MRSA устойчивы не только к метициллину, но и к другим антибиотикам пенициллиновой группы (диклоксациллину, оксациллину, нафциллину и др.), а также к цефалоспоринам.

Рисунок 2 (с сайта thinglink.com). Метициллин-резистентные золотистые стафилококки.
В последнее время выявлены штаммы и с более широким спектром устойчивости: ванкомицин-резистентные (VRSA) и гликопептид-резистентные (GISA) [6, 9, 10].
Штамм S.lugdunensis IVK28 эффективно боролся со своим вредоносным родственником лишь в условиях недостатка железа и только на твердых агаризованных средах (рис. 3, слева). Механизм противостояния был неясен, а потому Ципперер провел транспозонный мутагенез клеток выделенного штамма – чтобы выявить ген, ответственный за синтез смертельного для S.aureus вещества.

В итоге удалось получить мутанта IVK28, который не мог подавлять рост MRSA. Анализ места встройки транспозона показал, что тот нарушил структуру гена предполагаемой нерибосомной пептидсинтетазы (НРПС). Оказалось, что этот ген вместе с другими последовательностями, связанными с биосинтезом антибиотиков, входит в состав оперона размером 30 т.п.н. Это указывало на то, что предполагаемая молекула ингибитора может быть комплексом нерибосомных пептидов.
Оперон методом ПЦР обнаружили во всех культурах S.lugdunensis, а значит, он характерен для всего вида, а не только для штамма IVK28. Однако GC-состав оперона (26,9%) отличался от GC-состава остального генома S.lugdunensis (33,8%), что свидетельствовало о возможном заимствовании этого полезного генетического кластера у других видов бактерий – путем горизонтального переноса.
Оперон состоит из генов lugA, B, C и D, кодирующих пептидсинтетазные белки (см. врезку ниже), а также из других генов, чьи продукты необходимы для синтеза и транспорта нерибосомного пептида.
Чтобы окончательно вменить оперону участие в антибактериальной деятельности S.lugdunensis, наименьший ген (lugD) удалили. Мутант ΔlugD, как и ожидалось, не мог подавлять рост золотистого стафилококка, но когда в него ввели плазмиду с работающим геном lugD, агрессивный фенотип восстановился (рис. 3, в центре и справа).
Выделенный Ципперером продукт lug-оперона оказался нерибосомным циклическим пептидом, состоящим из пяти аминокислот (двух D-валинов, L-валина, D-лейцина и L-триптофана) и тиазолидинового гетероцикла (рис. 4). Назвали антибиотик лугдунином.

Химическим синтезом удалось получить продукт с идентичными природному лугдунину химическими свойствами и антибактериальным эффектом. Ученые предположили, что этот антибиотик ингибирует синтез бактериальных биополимеров – белков, ДНК и пептидогликанов [5].
Этот класс пептидов синтезируется в клетках низших грибов и бактерий без участия рибосом. Нерибосомные пептиды (НРП) также встречаются и у высших организмов, которые имеют бактерий-комменсалов [12].
НРП подразделяются на несколько функциональных групп [13]:
- антибиотики (ванкомицин);
- предшественники антибиотиков (ACV-трипептид – предшественник пенициллина и цефалоспорина);
- иммуносупрессоры (циклоспорин);
- противоопухолевые пептиды (блеомицин);
- сидерофоры (пиовердин);
- токсины (HC-токсин);
- сурфактанты (сурфактин).
Каждый модуль состоит как минимум из трех доменов:
- конденсирующего (принимающего пептидную цепь из предыдущего модуля);
- аденилирующего (выбирающего нужную аминокислоту);
- пептидильного (образующего пептидную связь).
Нередко модули включают и другие домены, в том числе эпимеризующий, который преобразует L-аминокислоты в D-формы [14].
По аналогии с триплетным рибосомным кодом для синтеза белка существует и нерибосомный, код НРПС, определяемый 10 остатками аминокислот в субстрат-связывающем кармане аденилирующего домена. От комбинации этих остатков зависит то, какая аминокислота будет встроена в пептид конкретным модулем НРПС. Зная этот код, можно предсказывать субстратную специфичность аденилирующих доменов и даже произвольно изменять ее посредством замены аминокислот в домене [14].
В экспериментах немецких ученых лугдунин действовал не только на метициллин-резистентных стафилококков, но и на гликопротеин-резистентных, и даже на других грамположительных бактерий типа листерии и ванкомицин-резистентного энтерококка (табл. 1). Минимальная ингибирующая концентрация (МИК) нового бактериоцина – 1,5–12 мкг × мл −1 , что говорит о высокой активности вещества. При этом такие концентрации никак не влияли на человеческую сыворотку, не вызывали лизис нейтрофилов или эритроцитов и не ингибировали метаболическую активность моноцитов. Бактериальные же клетки под действием лугдунина в концентрации даже ниже МИК прекращали синтезировать ДНК, РНК, белки и компоненты клеточной стенки. В этом отношении лугдунин напоминает даптомицин, дающий такой же эффект, но способ действия которого пока не изучен. Не было отмечено возникновения резистентности клеток S.aureus к лугдунину даже после их месячного выращивания на малых концентрациях.
| Виды и штаммы | Резистентность | МИК лугдунина (мкг × мл −1 ) | |||||
| Staphylococcus aureus USA300 (LAC) | MRSA | 1,5 | |||||
| + 50% человеческой сыворотки крови | 1,5 | ||||||
| Staphylococcus aureus USA300 (NRS384) | MRSA | 1,5 | |||||
| Staphylococcus aureus Mu50 | GISA | 3 | |||||
| Staphylococcus aureus SA113 | 3 | ||||||
| Staphylococcus aureus RN4220 | 3 | ||||||
| Enterococcus faecium BK463 | VRE | 3 | |||||
| Enterococcus faecalis VRE366 | VRE | 12 | |||||
| Listeria monocytogenes ATCC19118 | 6 | ||||||
| Streptococcus pneumoniae ATCC49619 | 1,5 | ||||||
| Bacillus subtilis 168 (trpC2) | 4 | ||||||
| Pseudomonas aeruginosa PAO1 | >50 | ||||||
| Escherichia coli DH5α | >50 | ||||||
| Условные обозначения: MRSA — метициллин-резистентные S. aureus; GISA — устойчивые к гликопротеинам S. aureus; VRE — ванкомицин-резистентные Enterococcus. Таблица из [1]. | |||||||
Испытания в боевых условиях
Как и полагается, способность лугдунина лечить стафилококковые инфекции продемонстрировали in vivo на мышиной модели (рис. 5). У шести мышей сбрили шерсть на спине и, повредив кожу многократным приклеиванием/отклеиванием пластыря, нанесли на это место золотистого стафилококка. Затем кожу обработали мазью, содержащей 1,5 мкг лугдунина, и спустя шесть часов оценили результат. Обработка новым антибиотиком сильно сокращала или даже полностью уничтожала популяцию S.aureus. Причем не только на поверхности кожи, но и в более глубоких ее слоях.

Рисунок 5. Общая схема подхода к идентификации природного антибиотика. Из бактериальных популяций человеческого тела отбирают представителей, которые не могут сосуществовать с интересующими патогенными бактериями. Этих возможных конкурентов тестируют по отдельности на средах с инфекционным агентом. Из культуры, успешно подавляющей рост патогенов, выделяют антибиотик, действие которого проверяют на животных моделях. Рисунок из [5], модифицирован и адаптирован.
Чтобы понять, может ли S.lugdunensis помешать колонизации носовой полости позвоночных животных золотистым стафилококком в естественных условиях, ученые провели следующий эксперимент. В носы хлопковых хомяков ввели два вида смешанных культур (S.aureus + S.lugdunensis IVK28 и S.aureus + S.lugdunensis IVK28ΔlugD) и каждую по отдельности. В контрольных случаях, когда вводили по одному штамму, все три культуры стабильно колонизировали носовую полость. Однако при введении смеси S.aureus + S.lugdunensis IVK28 количество золотистого стафилококка через 5 дней значительно уменьшилось по сравнению со смесью S.aureus + S.lugdunensis IVK28ΔlugD. Этот эксперимент показал, что продукция лугдунина позволяет штамму IVK28 эффективно конкурировать с золотистым стафилококком in vivo.
Оставалось разобраться, предотвращает ли присутствие S.lugdunensis в носу человека колонизацию бактериями S.aureus. Ципперер и его коллеги исследовали мазки из носовых ходов 187 госпитализированных больных. Из них у 60 человек (32,1%) обнаружили золотистого стафилококка и у 17 человек (9,1%) – S.lugdunensis. И только у одного пациента с S.lugdunensis в носу обитал S.aureus. У всех выделенных штаммов S.lugdunensis ПЦР-анализ продемонстрировал наличие lug-оперона, а все обнаруженные штаммы S.aureus оказались восприимчивы к лугдунину.
Лугдунин оказался первым обнаруженным бактериоцином нового класса – макроциклических тиазолидиновых пептидных антибиотиков. Все проверенные штаммы S.aureus (как природные, так и лабораторные) не смогли выработать резистентности к нему. Это дает надежду на то, что лугдунин в будущем станет коммерческим препаратом для борьбы с золотистым стафилококком.
И наконец, сам факт обнаружения нового антибиотика у представителя человеческой микробиоты должен послужить стимулом для активизации поиска других продуцентов бактериоцинов в составе именно таких сообществ. В дальнейшем это поможет медикам успешнее сдерживать наступление мультирезистентных патогенов.
Читайте также:


