Прогрессирующая мультифокальная лейкоэнцефалопатия что это такое
• ЧТО ТАКОЕ ПМЛ?
• КАК ОБНАРУЖИТЬ ПМЛ?
• КАК ЛЕЧИТЬ ПМЛ?
• ГДЕ Я МОГУ ПОЛУЧИТЬ БОЛЬШЕ ИНФОРМАЦИИ?
• ОСНОВНЫЕ МОМЕНТЫ
ЧТО ТАКОЕ ПМЛ?
"Энцефало" означает мозг, а "патия" означает заболевание. Энцефалопатия - это болезнь мозга. "Лейко-" означает белый. Лейкоэнцефалопатия – заболевание белого вещества мозга. "Прогрессивная" означает, что эта болезнь ухудшается в течение короткого времени. "Многоочаговая" означает, что инфекция проявляется в нескольких местах одновременно.
По оценкам исследователей ПМЛ развивается примерно у 6% людей со СПИДом. В большинстве случаев ПМЛ встречается у людей с количеством CD4 клеток ниже 100. Точный уровень распространенности трудно узнать, потому что ПМЛ сложно диагностировать.
В большинстве случаев ПМЛ заканчивается смертельным исходом. Люди с диагнозом ПМЛ жили в среднем 6 месяцев, и большинство из них умерли в течение 2 лет. Однако если люди начинают прием сильных антиретровирусных препаратов (АРВ) для контроля за ВИЧ-инфекцией, они живут намного дольше. Сейчас лишь около половины всех людей, живущих с ВИЧ и ПМЛ, умирают от ПМЛ.
ПМЛ вызывает вирус " JC ". Во всем мире около 80-85% всего взрослого населения подвергаются воздействию этого вируса. У людей с ослабленной иммунной системой вирус JC может активизироваться.
КАК ОБНАРУЖИТЬ ПМЛ?
Симптомы ПМЛ начинаются со слабости или проблем координации в руках или ногах. Возможны сложности с мышлением или речью. Могут иметь место проблемы со зрением и памятью, припадки и головные боли.
Эти симптомы могут также возникнуть при других оппортунистических инфекциях, в том числе токсоплазмозе, лимфоме, инфекциях внутреннего уха, или криптококовом менингите. Важно исключить эти заболевания.
ПМЛ можно обнаружить с помощью сканирования головного мозга путем магнитно-резонансной томографии (МРТ). Другой способ провериться на ПМЛ – анализ спинномозговой жидкости. Образец забирается с помощью иглы из спинного канала, процедура называется спинномозговая пункция.
КАК ЛЕЧИТЬ ПМЛ?
Одной из основных проблем при лечении любой инфекции мозга является "гематоэнцефалический барьер". Кровеносные сосуды вокруг мозга отличаются от остальной части тела. Они представляют собой "плотную ткань" для защиты мозга от токсичных веществ. Химические вещества, которые растворяются в жире, могут проникнуть через него. Те, которые растворяются в воде, - не могут. К сожалению, к последним относится большинство антибиотиков и многие другие лекарства.
На сегодняшний день не существует проверенного лечения ПМЛ. Научные исследования имели противоречивые результаты, а другие возможности лечения не были тщательно изучены. Вместе с тем, у некоторых пациентов, принимающих сильные препараты для борьбы с ВИЧ, ПМЛ замедляется или исчезает.
Ара-C (Цитозин арабинозид или цитарабин) проходил испытания против ПМЛ. Его вводили внутривенно, а также непосредственно в мозг. Казалось, это работало в одном небольшом исследовании, но не в тех, которые проводились позже. Ара-С очень токсичный и повреждает костный мозг.
Большие дозы АЗТ испытывались для лечения ПМЛ, потому что АЗТ может пересечь гематоэнцефалический барьер. Другие вещества, которые были опробованы с разной степенью успеха, включают ацикловир, гепарин, пептид-T-, бета-интерферон, дексаметазон, и н-ацетилцистеин, топотекан и цидофовир. Некоторые исследования показывают, что внутривенно цидофовира может улучшить работу мозга у людей с ПМЛ.
В связи с тем, что ПМЛ может быстро прогрессировать, важно быстро начать лечение.
ГДЕ Я МОГУ ПОЛУЧИТЬ БОЛЬШЕ ИНФОРМАЦИИ?
Прекрасным источником информации является книга "Прогрессивная многоочаговая лейкоэнцефлопатия (ПМЛ): Исследования и возможности лечения". Петр и Лиза Броснан написали книгу в 1993 году. Они не являются врачами-специалистами, брат Лизы получил диагноз ПМЛ, и Броснаны начали поиск возможного лечения. Брат Лизы умер, но они продолжили поиски и опубликовали свою работу.
Вы можете получить их книгу, написав по адресу: Питер Броснан, 1709 Н. Фуллер пр. # 25, Лос-Анджелес, штат Калифорния, 90046. Для покрытия расходов он просит врачей и учреждения направить 30 долларов, больных СПИДом 20 долларов, а в случае сложной ситуации он отправит книгу бесплатно.
ОСНОВНЫЕ МОМЕНТЫ
ПМЛ - это вирусная инфекция головного мозга. В 50% случаев она заканчивается смертельным исходом. Ее можно перепутать с другими заболеваниями.
Подтвержденного лечения ПМЛ не существует, хотя некоторые виды лечения могут быть полезными. Любое лечение должно быть начато как можно скорее. Комбинированная антиретровирусная терапия (АРТ) может замедлить течение ПМЛ.
Полный текст:
При лечении ревматоидного артрита (РА) ритуксимабом (РТМ) возможны различные неблагоприятные реакции, среди которых особое место занимает прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ). Заболевание обусловлено активацией оппортунистической вирусной (JC-вирус) инфекции на фоне ослабления клеточного иммунитета, что приводит к массивной демиелинизации структур головного мозга. В статье описан клинический случай применения РТМ у пациентки с РА с системными проявлениями. Это лечение было эффективно в течение двух лет, но после последнего (четвертого) курса инфузий наблюдалось развитие многоочагового поражения головного мозга, характерного для ПМЛ. Дифференциальная диагностика с другими заболеваниями, которые сопровождаются сходными изменениями головного мозга, позволила авторам рассматривать ПМЛ как наиболее вероятный диагноз у данной пациентки, несмотря на отрицательный результат определения в ликворе и крови ДНК JC-вируса. Выбранная лечебная тактика с учетом предполагаемой у пациентки ПМЛ (снижение дозы глюкокортикоидов, прием ингибитора обратного захвата серотонина, антидепрессанта миртазапина, лечебный плазмаферез) себя оправдала и обеспечила умеренную позитивную динамику.
1. Насонов ЕЛ, редактор. Генно-инженерные биологические препараты в лечении ревматоидного артрита. Москва: ИМА-ПРЕСС; 2013. С. 200-21
2. Насонов ЕЛ, редактор. Ревматоидный артрит. В кн.: Российские клинические рекомендации. Ревматология. Москва: ГЭОТАР-Медиа; 2017. С. 17-57
3. Муравьев ЮВ. Нежелательные реакции при применении ритуксимаба. В кн.: Насонов ЕЛ, редактор. Анти-В-клеточная терапия в ревматологии: фокус на ритуксимаб. Москва: ИМА-ПРЕСС; 2012. С. 258-95
4. Yusof MY, Vital EM, Buch MH. B cell therapies, approved and emerging: a review of infectious risk and prevention during use. Curr Rheumatol Rep. 2015;17(10):65. doi: 10.1007/s11926-015-0539-7
5. Белов БС. Прогрессирующая мультифокальная лейкоэнцефалопатия: ревматологические аспекты. Современная ревматология. 2015;9(3):4-9. doi: 10.14412/1996-7012-2015-3-4-9
6. Белов БС, Наумцева МС, Тарасова ГМ, Буханова ДВ. Таргетная терапия и инфекции при ревматических заболеваниях. Современная ревматология. 2016;10(4):4-15 doi: 10.14412/1996-7012-2016-4-4-15
7. Захарова МН. Прогрессирующая мультифокальная лейкоэнцефалопатия (обзор литературы). Журнал неврологии и психиатрии. 2012;9(2):29-33
8. Palazzo E, Yahia SA. Progressive multifocal leukoencephalopathy in autoimmune diseases. Joint Bone Spine. 2012;79(4):351-5. doi: 10.1016/j.jbspin.2011.11.002
9. Molloy ES, Calabrese CM, Calabrese LH. The risk of progressive multifocal leukoencephalopathy in the biologic era: prevention and management. Rheum Dis Clin North Am. 2017;43(1):95-109. doi: 10.1016/j.rdc.2016.09.009
10. Molloy ES, Calabrese LH. Progressive multifocal leukoencephalopathy: a national estimate of frequency in systemic lupus erythematosus and other rheumatic diseases. Arthritis Rheum. 2009;60(12):3761-5. doi: 10.1002/art.24966
11. Harris HE. Progressive multifocal leucoencephalopathy in a patient with systemic lupus erythematosus treated with rituximab. Rheumatology (Oxford). 2008;47:224-5. doi: 10.1093/rheumatology/kem299
12. Clavel G, Moulignier A, Semerano L. Progressive multifocal leukoencephalopathy and rheumatoid arthritis treatments. Joint Bone Spine. 2017;84(6):671-5. doi: 10.1016/j.jbspin.2017.03.002
13. Molloy ES, Calabrese LH. Progressive multifocal leukoencephalopathy associated with immunosuppressive therapy in rheumatic diseases: evolving role of biologic therapies. Arthritis Rheum. 2012;64(9):3043-51. doi: 10.1002/art.34468
14. Arkema EV, van Vollenhoven RF, Askling J; ARTIS Study Group. Incidence of progressive multifocal leukoencephalopathy in patients with rheumatoid arthritis: a national population-based study. Ann Rheum Dis. 2012;71(11):1865-7. doi: 10.1136/annrheumdis-2012-201638
15. Clifford DB, Ances B, Costello C, et al. Rituximab-associated progressive multifocal leukoencephalopathy in rheumatoid arthritis. Arch Neurol. 2011;68(9):1156-64. doi: 10.1001/archneurol.2011.103
16. Fleischmann RM. Progressive multifocal leukoencephalopathy following rituximab treatment in a patient with rheumatoid arthritis. Arthritis Rheum. 2009;60(11):3225-8. doi: 10.1002/art.24906
17. Molloy ES, Calabrese LH. Progressive multifocal leukoencephalopathy associated with biologic therapy in rheumatic diseases: strengthening association with rituximab. Arthritis Rheum. 2014;66(Suppl 10):369.
18. Шмидт ТЕ. Прогрессирующая мультифокальная лейкоэнцефалопатия и другие неврологические проявления реактивации вируса JC. Неврологический журнал. 2014;(4):4-10
19. Berger JR, Aksamit AJ, Clifford DB, et al. PML diagnostic criteria: consensus statement from the AAN Neuroinfectious Disease Section. Neurology. 2013;80(15):1430-8. doi: 10.1212/WNL.0b013e31828c2fa1
20. Steiner I, Berger JR. Update on progressive multifocal leucoencephalopathy. Curr Neurol Neurosci Rep. 2012;12(6):680-6. doi: 10.1007/s11910-012-0313-4

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
, MD, University of Utah School of Medicine
Last full review/revision January 2019 by John E. Greenlee, MD

Этиология
Прогрессируящая мультифокальная лейкоэнцефалопатия развивается вследствие реактивации повсеместно распространенного JC-вируса из семейства паповавирусов, который обычно попадает в организм в детстве и пребывает в латентном состоянии в почках и других органах и тканях (например, в мононуклеарных клетках, ЦНС). Реактивированный вирус тропен к олигодендроцитам.
Большинство пациентов с развивающейся ПМЛ, имеют ослабление клеточного иммунитета, вызванное:
СПИД (наиболее распространенный фактор риска)
Расстройства ретикулоэндотелиальной системы (например,, лейкемия, лимфома)
Риск развития ПМЛ у больных СПИДом возрастает с увеличением вирусной нагрузки; в настоящее время распространенность ПМЛ уменьшилась в связи с широким применением более эффективных антиретровирусных препаратов.
В то же время возрастает количество случаев ПМЛ, таких как осложнения иммуномодулирующей терапии (например, моноклональными антителами, такими как натализумаб и ритуксимаб). Измерение сывороточных антител к вирусу JC (индекс вируса JC) может помочь оценить риск ПМЛ у пациентов, принимающих натализумаб.
Клинические проявления
Первым проявлением заболевания может быть неловкость и неповоротливость при движениях. Очень часто при обследовании выявляется гемипарез. Также часто наблюдаются афазия, дизартрия и гемианопсия. У двух третей больных многоочаговое поражение коры больших полушарий приводит к развитию когнитивных нарушений. Могут наблюдаться поражения сенсорных структур, мозжечка и ствола головного мозга.
Головные боли и судорожные припадки редки и встречаются чаще всего у больных СПИДом.
Неуклонное прогрессирование заболевания приводит к смерти, как правило, спустя 1–9 мес. после появления симптомов заболевания.
Диагностика
Исследование ЦСЖ на ДНК JC-вируса
Наличие прогрессирующей мультифокальной лейкоэнцефалопатии следует подозревать у пациентов с необъяснимыми прогрессирующими признаками поражения головного мозга, особенно у больных с иммунодефицитными состояниями.
Предварительный диагноз ПМЛ ставится на основании данных МРТ с контрастом, выявившей единичные или множественные очаги поражения белого вещества на Т2-взвешенных изображениях. Контрастное вещество слабо накапливается, как правило, по периферии в 5–15% очагов. При КТ могут определяться очаги пониженной плотности, не накапливающие контраст, однако этот метод является менее чувствительным по сравнению с МРТ.

ЦСЖ исследуется на ДНК JC-вируса с использованием ПЦР; положительные результаты этого анализа в сочетании с характерными изменениями при нейровизуализации подтверждают диагноз ПМЛ. Общий анализ ЦСЖ, как правило, не изменен.
Серологические исследования неинформативны. Иногда с целью дифференциальной диагностики выполняют стереотактическую биопсию мозга, которая, впрочем, редко себя оправдывает.
Лечение
Лечение прогрессивной многоочаговой лейкодистрофи, в основном, поддерживающее.
Экспериментальное применение цидофовира и других противовирусных препаратов не подтвердило своей эффективности. Антиретровирусная терапия (АРТ) улучшает прогноз заболевания у ВИЧ-инфицированных пациентов с ПМЛ, увеличивая уровень годовой выживаемости с 10 до 50%. В то же время, агрессивная антиретровирусная терапия может приводить к развитию у пациентов воспалительного синдрома восстановления иммунной системы (ВСВИС). При ВСВИС восстанавление иммунной системы вызывает интенсивную воспалительную реакцию на вирус JC, тем самым ухудшая симптоматику. При проведении нейровизуализации на фоне ВСВИС выявляются значительное усиление накопления контрастного вещества очагами и иногда – отек головного мозга. Эффективной может быть терапия кортикостероидами. В зависимости от тяжести течения ВСВИС и СПИДа возможно рассматривать вопрос о прекращении антиретровирусной терапии.
Отмена иммуносупрессантов может привести к улучшению самочувствия пациентов. В то же время у этих пациентов повышается риск развития ВСВИС.
При развитии ПМЛ у пациентов, получающих лечение натализумабом, иным иммуномодулирующим лекарственным средством или иммуносупрессантами, прием указанных лекарственных средств необходимо прекратить, с последующим проведением плазмафереза для удаления остатков препарата в циркулирующей крови.
Ключевые моменты
ПМЛ развивается вследствие реактивации повсеместно распространенного JC-вируса, как правило, на фоне снижения клеточного иммунитета.
При ПМЛ чаще всего наблюдаются нарушение координации движений, гемипарезы, афазия, дизартрия, гемианопсия и когнитивные нарушения.
У пациентов со снижением клеточного иммунитета и необъяснимыми прогрессирующими признаками поражения головного мозга необходимы проведение МРТ головного мозга и исследование ЦСЖ на ДНК JC-вируса.
Проводите поддерживающую терапию пациентов и лечите основные заболевания согласно показаниям (например, прекратив прием натализумаба, другого иммуномодулирующего лекарственного средства или иммунодепрессантов, или инициируя антиретровирусную терапию и со всесторонним контролем за развитием воспалительного синдрома восстановления иммунитета).

Дата публикации: 24.11.2018 2018-11-24
Статья просмотрена: 1002 раза
Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) — редкое демиелинизирующее заболевание головного мозга, вызываемое полиомавирусом человека 2 (JC-вирус) на фоне иммунодефицита. Впервые вирус был обнаружен и описан в 1971 году. На данный момент заболевание встречается у 5 % пациентов больных СПИДом. Кроме того, заболевание может возникать после применения иммунносупрессивных препаратов, трансплантации органов и тканей, при опухолях системы крови — таких как болезнь Ходжкина, хронический лимфолейкоз, у больных рассеянным склерозом, находящихся на лечении натализумабом, при аутоиммунных воспалительных процессах.
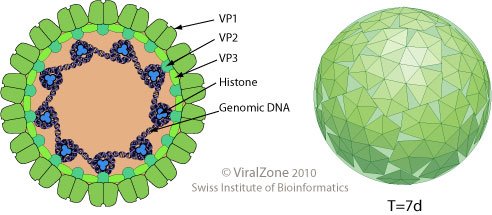
Рис. 1: JC-вирус. Строение.
ПМЛ — оппортунистическая инфекция, которая встречается в равной степени как у мужчин, так и у женщин, как правило, старше 50 лет. Предполагается, что около 80 % людей являются носителями JC-вируса. Вирус JC попадает в организм человека как воздушно-капельным, так и фекально-оральным путем. Первичное инфицирование не проявляется никакой симптоматикой, в дальнейшем вирус продолжает находится в организме в латентном состоянии. Персистенция вируса наблюдается в стволовых клетках костного мозга, эпителиальных клетках почек, а также в лимфоидных органах. Человек может в течение всей жизни являться носителем JC-вируса и не знать об этом. Если никакие иммуносупрессорные факторы не оказывают влияние на организм, то заболевание может и не проявиться. Однако в условиях иммунодефицита вирус реактивируется, при этом основная роль принадлежит состоянию Т-клеточного иммунитета. Происходит генетическая перестройка вирусного генома, после чего вирус способен проникать в центральную нервную систему, инфицировать олигодендроциты, вызывая их гибель. Патоморфологическим проявлением этого процесса являются множественные очаги демиелинизации без признаков воспаления, выявляемые на МРТ головного мозга. Их наибольшее количество наблюдается в полушариях ГМ, стволе и мозжечке.
Клиническая картина может иметь подострое (несколько дней) и затяжное развитие (несколько недель). Как правило, отсутствуют признаки инфекции, а также общемозговые и менингеальные симптомы. Типичный вариант течения болезни характеризуется следующим симптомокомплексом:
- Психопатические нарушения: отмечаются изменения характера, поведения, лабильность эмоциональной сферы, больные агрессивны, вспыльчивы, для них характерна подозрительность, настороженность, определяется ослабление памяти, внимания, мышления.
- Пирамидные нарушения– чаще всего проявляются в виде центрального гемипареза.
- Соматосенсорные расстройства — в виде парестезии.
- Мозжечковые нарушения — атаксия, дисметрия.
- Нарушения зрения — гемианопсия.
- Нарушения высших мозговых функций — апраксия, афазия.
- Эпилептические припадки.
Сочетание вышеперечисленных симптомов зависит от локализации очагов поражения, в связи с чем заболевание имеет вариабельное течение.
Летальный исход, как правило, наступает в течение 10–12 месяцев от начала появления клинических симптомов.
ПМЛ необходимо дифференцировать с оппортунистическими инфекциями ЦНС. Главным образом — с церебральным токсоплазмозом. По статистике, токсоплазмоз чаще встречается у мужчин, средний возраст — 30–40 лет. Частота встречаемости токсоплазмоза у пациентов больных СПИДом составляет 25–80 %, что выше по сравнению с частотой встречаемости ПМЛ при СПИДе. Общим признаком с ПМЛ является то, что заражение происходит алиментарным путем, после чего возбудитель находится в организме в латентном состоянии и реактивируется при наличии выраженной иммуносупрессии. Как правило, токсоплазмоз начинается постепенно, с общеинфекционных признаков, таких как слабость, недомогание, повышение температуры тела до 38–40°С, озноб, которые присутствуют в течение 1–2 месяцев. После этого появляются психические нарушения, очаговые неврологические симптомы схожие с таковыми при ПМЛ. Однако, для клинической картины церебрального токсоплазмоза также характерно наличие общемозговых и менингиальных симптомов. Заболевание может протекать и с молниеносным развитием очаговой неврологической симптоматики — в течение нескольких недель. При проведении КТ и МРТ также обнаруживаются некоторые отличия: при ПМЛ выявляются множественные ассиметричные очаги, без отека и смещения прилежащих структур; при церебральном токсоплазмозе — одиночные или множественные очаги с кольцевидной тенью, накапливающие контраст на периферии, со смещением прилежащих структур.
Также необходимо проведение дифференциальной диагностики ПМЛ со стадией обострения рассеянного склероза. Основываться исключительно на клиническую картину не представляется возможным, так как многие симптомы могут наблюдаться как при обострении РС, так и при ПМЛ. Для постановки диагноза необходимо провести МРТ головного мозга с контрастным усилением водорастворимыми парамагнитными веществами на основе гадолиния. В случае развития ПМЛ на МРТ выявляются гиперинтенсивные очаги в лобных, затылочных и реже в теменных и височных долях. Также может поражаться вещество ствола головного мозга и мозжечка, очень редко-таламус и спинной мозг. В 40 % случаев при ПМЛ в очагах поражения может гетерогенно накапливаться контрастное вещество, при этом масс-эффект отсутствует. В отличие от ПМЛ, при обострении рассеянного склероза очаги будут накапливать контрастное вещество. Очаги будут иметь преимущественно вытянутую форму и располагаться перивентрикулярно, образуя пальца Доусона.
Также существуют дополнительные методы исследования, позволяющие более достоверно верифицировать диагноз и проводить дифференциальную диагностику:
‒ Иммунохимическая методика определения активности интратекального синтеза IgG которая присутствует примерно у 95 % пациентов с РС.
‒ ПЦР исследование спиномозговой жидкости которое выявляет ДНК вируса JC, однако антиретровирусная терапия у больных СПИДом снижает достоверность анализа до 58 %.
‒ Специфический анализ крови на наличие антител к JC-вирусу.
На сегодняшний день специфического лечения ПМЛ не разработано. Применяется исключительно симптоматическая и поддерживающая терапия. Используют следующие группы лекарственных препаратов: противовирусные, цитостатики, антагонисты серотониновых рецепторов, а также трансплантацию стволовых клеток костного мозга.
Возможность возникновения ПМЛ необходимо учитывать при назначении иммуносупрессивной терапии. Так, например, согласно стандарту оказания медицинской помощи больным с рассеянным склерозом, перед назначением препаратов типа натализумаб необходим контроль уровня антител к JC-вирусу, с повторным исследованием этого показателя каждые 6 месяцев.
Войти через uID
| Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) — это тяжелое демиелинизирующее заболевание ЦНС. Возбудитель — вирус JC из группы ДНК-содержащих полиомавирусов. Свое название вирус получил по инициалам больного, у которого был впервые выделен в 1971 г. Вопреки распространенному заблуждению вирус JC никак не связан с синдромом Крейтцфельдта-Якоба. Доля серопозитивных среди населения достигает 80%, предполагается возможность латентной персистирующей инфекции. Реактивация вируса и клинически выраженное заболевание развиваются только при нарушении клеточного иммунитета. Полагают, что вирус достигает ЦНС посредством лейкоцитов и поражает в основном олигодендроциты, образующие миелиновую оболочку. Разрушение миелиновых оболочек макроскопически проявляется мультифокальной демиелинизацией. В наибольшей степени страдает белое вещество полушарий головного мозга, но возможно также поражение мозжечка и серого вещества. Нередко наблюдается тяжелый иммунодефицит, однако для развития ПМЛ он не обязателен. В отличие от ЦМВ-инфекции и инфекции, вызванной атипичными микобактериями, ПМЛ не всегда указывает на терминальную стадию ВИЧ-инфекции. Хотя обычно ПМЛ развивается при числе лимфоцитов менее 100 мкл 1 , она возможна и при числе лимфоцитов более 200 мкл 1 . Снижение заболеваемости ПМЛ не столь заметно, как заболеваемости другими ОИ. После церебрального токсоплазмоза ПМЛ сегодня занимает второе место среди ОИ по частоте поражения нервной системы. |
Пока не было ВААРТ прогноз при ПМЛ был плохим. После появления симптомов продолжительность жизни обычно составляла 3 6 мес. Обычно смерть наступала от вторичных осложнений, типичных для лежачих больных. У больных с числом лимфоцитов более 200 мкл 1 прогноз немного лучше. На фоне ВААРТ болезнь прогрессирует гораздо медленнее, иногда даже наступает полная ремиссия. Однако положительное влияние ВААРТ не столь значительно как при других ОИ: в испанском исследовании, в которое вошли 118 больных с ПМЛ, получающих ВААРТ, 64% больных были живы спустя 2,2 года после постановки диагноза. Даже при эффективной ВААРТ полная ремиссия достигается не всегда. Большинство случаев полной ремиссии достигается при воспалительной ПМЛ, развивающейся на фоне синдрома восстановления иммунитета.
Несмотря на разнообразие симптомов ПМЛ, обусловленное различной локализацией очагов демиелинизации, можно выделить и ряд общих черт клинической картины. Помимо когнитивных нарушений (от легких нарушений концентрации внимания до деменции) для ПМЛ очень характерны очаговые неврологические симптомы. Чаще наблюдаются моно- и гемипарез, а также нарушения речи и зрения. Мы наблюдали нескольких больных, у которых ПМЛ привела к слепоте. Поражение ЦНС поначалу иногда проявляется отдельными нарушениями координации движений, но при этом может быстро привести к тяжелой инвалидности. У некоторых больных развиваются эпилептические припадки. Выпадение чувствительности, лихорадка и головная боль встречаются редко и более характерны для церебрального токсоплазмоза.
Во многих случаях МРТ позволяет дифференцировать ПМЛ с токсоплазмозом и лимфомой. Однако классические поражения, которые обычно приводятся в учебниках, — обширные, затрагивающие все полушарие — обнаруживаются не всегда. ПМЛ всегда начинается с маленького очага, поэтому маленькие и единичные очаги не исключают диагноза. ПМЛ может развиться в любой части головного мозга, типичной локализации нет. Очаги нередко обнаруживаются в теменной и затылочной областях или перивентрикулярно, однако может страдать и мозжечок. Важно, чтобы заключение по результатам МРТ давал специалист по лучевой диагностике или врач, имеющий опыт по ПМЛ. Но даже в этом случае ПМЛ бывает трудно отличить от инфекции, вызванной вирусом герпеса человека типа 6 и ВИЧ-лейкоэнцефалопатии.
Таким образом диагноз, поставленный по клинической картине и данным МРТ, не является бесспорным. Важное значение имеет исследование СМЖ. Как правило, если нет сопутствующих инфекций, то признаков неспецифического воспаления в СМЖ не бывает, а общий уровень белка немного повышен. Цитоз обнаруживается редко, если он достигает 100 мкл 1 , диагноз ПМЛ маловероятен. У всех больных нужно исследовать СМЖ на вирус JC. Чувствительность новых исследований на основе ПЦР составляет около 80%, специфичность — более 90%. Образец СМЖ для исследования нужно направить в лабораторию, имеющую опыт выявления вируса JC.
При характерных клинической картине и данных МРТ в сочетании с положительным результатом ПЦР на вирус JC диагноз ПМЛ можно поставить с достаточной степенью вероятности. В этих случаях выполнять биопсию головного мозга сегодня не рекомендуется. Тем не менее отрицательный результат ПЦР не исключает ПМЛ. Количество вируса в крови может колебаться в значительной степени и не коррелировать с размером поражений. К сожалению, после появления ВААРТ ПЦР на вирус JC стала менее информативной, так как на фоне ВААРТ его концентрация в крови зачастую падает. У некоторых больных может потребоваться стереотаксическая биопсия головного мозга.
Специфического лечения ПМЛ не существует. Фоскарнет, интерферон, иммуностимуляторы и глюкокортикоиды дают лишь небольшой эффект и не применяются. Цитарабин в рандомизированном испытании показал плохие результаты и больше не рекомендуется. Сегодня надежды возлагаются на два новых препарата — цидофовир и камптотецин. Однако есть опасения, что этих препаратов постигнет та же судьба. Камптотецин - алкалоидный цитостатик, который ингибирует топоизомеразу I — ядерный фермент, который необходим для синтеза ДНК и, следовательно, для репликации вируса JC. Пока данных о применении этого препарата недостаточно. В небольших, в основном неконтролируемых испытаниях, имеющихся на сегодня, в ряде случаев цидофовир оказывал положительный эффект. Наш собственный опыт применения этого препарата в целом был неудачным, при ретроспективном анализе 35 случаев при лечении цидофовиром прогноз оказался даже хуже. Однако это может объясняется тем, что цидофовир применялся у более тяжелых больных. В целом, цидофовир следует применять только в крайнем случае — когда оптимизация ВААРТ не возможна или когда состояние больного ухудшается несмотря на эффективную ВААРТ.
Мы считаем, что абсолютный приоритет в лечении ПМЛ имеет оптимизация АРТ. В 1998 г. нами было показано, что ВААРТ значительно улучшает прогноз. Данные других исследователей подтвердили это наблюдение. In vitro продемонстрирован синергизм между ВИЧ и вирусом JC, поэтому нужно добиваться максимального подавления вирусной нагрузки. Хотя описаны случаи прогрессирования ПМЛ на фоне правильной антиретровирусной терапии, сегодня ВААРТ нередко остается единственным шансом для больных.
Профилактика
Профилактики не существует. Предотвратить заражение вирусом также не возможно.
Таблица 13. Лечение и профилактика прогрессирующей мультифокальнойлейкоэнцефалопатии
1 Прогрессирующая мультифокальная лейкоэнцефалопатия (обзор литературы) М.Н. ЗАХАРОВА Научный центр неврологии РАМН, Москва Progressive multifocal leukoencephalopathy (review) M.N. ZAKHAROVA Research Center of the Neurology Russian Academy of Medical Sciences, Moscow Статья посвящена проблеме прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ), которая является в большинстве случаев фатальным прогрессирующим демиелинизирующим заболеванием ЦНС. ПМЛ представляет собой оппортунистическую инфекцию, которая развивается в условиях иммуносупрессии, вызываемой как хроническими заболеваниями, так и агрессивной терапией. Рассматриваются возможные механизмы развития ПМЛ, диагностика заболевания и современные подходы к лечению. Ключевые слова: демиелинизация, ПМЛ, рассеянный склероз, JC-вирус. The study is devoted to the problem of progressive multifocal leukoencephalopathy (PME) which in most cases is a fatal progressive demyelinating disease of the CNS. PME is an opportunity infection that develops during immunosupression caused by chronic diseases or aggressive therapy. The authors consider possible mechanisms of the PME development, diagnosis of this disease and current approaches to treatment. Key words: demyelination, PML, multiple sclerosis, JC-virus. Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) это редкое прогрессирующее демиелинизирующее заболевание центральной нервной системы (ЦНС), вызванное реактивацией существующего в латентном состоянии папова вируса (JC-вируса) при иммунодефицитных состояниях [8]. Первое описание двух случаев, похожих на ПМЛ, было сделано в 1930 г. J. Halervorden. Термин ПМЛ был введен в 1958 г. K. Astrom и соавт. [2], которые выделили ПМЛ в самостоятельное заболевание. Первые случаи ПМЛ были описаны ими при лимфопролиферативных заболеваниях хроническом лимфолейкозе, ходжкинской лимфоме. Предположение о вирусной этиологии заболевания впервые было высказано в работах [23] после идентификации внутриядерных включений в олигодендроглиоцитах. Вирусная этиология ПМЛ была установлена в 1971 г., когда из мозга больного J. Cunningham был выделен вирус, получивший название по имени этого исследователя JC-вирус [21]. В 1984 г. было установлено, что JC-вирус является ДНКсодержащим вирусом семейства папова вирусов [10]. М.Н. Захарова, 2012 В развитии эпидемиологических исследований при ПМЛ можно выделить 4 этапа. До 80-х годов ПМЛ являлась редким заболеванием; заболеваемость составляла 1: человек. С 1958 по 1984 г. всего описано 230 случаев ПМЛ. До эпидемии СПИДа 80% случаев ПМЛ было связано с лимфопролиферативными заболеваниями, ходжкинской лимфомой, тяжелыми формами туберкулеза. С начала 90-х годов ( ), в связи с ростом ВИЧинфекции, заболеваемость ПМЛ выросла в 5 раз и в настоящее время составляет 1: человек в популяции [22]. При этом среди ВИЧ-инфицированных встречаемость ПМЛ до применения высокоактивной антиретровирусной терапии (ВААРТ) составляет 3,3:1000. С внедрением ВААРТ заболеваемость ПМЛ снизилась в 2,5 раза и составила 1,3 на 1000 ВИЧ-инфицированных [9]. С 2005 г. все чаще стали регистрировать случаи ПМЛ у не ВИЧинфици рованных больных с аутоиммунными заболеваниями, после трансплантации органов, с рассеянным склерозом в результате применения новых методов агрессивной иммуносупрессии (глюкокортикостероиды, пуриновые аналоги флударибин, кладрибин, азатиоприн, алкилирующие соединения циклофосфамид, кармустин, декарбазин, моно- 29
3 Основными патоморфологическими признаками ПМЛ являются множественные очаги демиелинизации, вызванные гибелью олигодендроцитов, наибольшее число их встречается в полушариях большого мозга, мозговом стволе и мозжечке. Воспалительные изменения в головном мозге практически отсутствуют. Гистологически при ПМЛ выявляются следующие изменения: измененные олигодендроциты с увеличенными ядрами и внутриядерными вирусными включениями; пролиферация астроцитов с образованием гигантских причудливой формы клеток с гиперхроматическими ядрами; множественные очаги демиелинизации с образованием полостей в них; иногда наблюдаются также изменения в нервных клетках мозжечка с вирусными внутриядерными включениями. Заболевание характеризуется подострым (несколько дней) или постепенным (несколько недель) развитием неврологической и психопатологической симптоматики. Характерно отсутствие общеинфекционных, общемозговых и менингеальных симптомов. Наиболее часто при дебюте заболевания появляются двигательные нарушения (гемипарезы, мозжечковая атаксия), нарушения зрения (гемианопсии), нарушения высших корковых функций (афазия), психические расстройства. В конечной стадии заболевания наблюдаются глубокая деменция, кома и гибель больного. Течение вариабельно, летальный исход наступает в течение 6 12 мес. Клиническая картина заболевания, появление и прогрессирование неврологической и психической симптоматики у иммунодефицитного больного заставляют заподозрить ПМЛ. Наибольшие диагностические трудности возникают при СПИДе, когда клиника и МРТ-признаки сходны при ПМЛ и ВИЧассоциированной энцефалопатии [17]. МРТ головного мозга является необходимым методом диагностики при подозрении на ПМЛ. МРТ-картина при подозрении на ПМЛ характеризуется мультифокальными очагами высокой интенсивности сигнала с нечеткими границами на Т2- взвешенных изображениях в подкорковом белом веществе. Чаще поражается белое вещество теменных и затылочных долей, однако очаги могут наблюдаться в любых отдела мозга, включая мозжечок и ствол [1]. В начале заболевания выявляется несколько очагов, по мере прогрессирования процесса отмечается нарастание количества сливных очагов. Очень редко наблюдается незначительный масс-эффект, и в этих случаях их трудно отличить от глиомы. Контрастное усиление отсутствует в результате малой выраженности воспаления. Однако у 5 15% больных отмечается контрастирование по периферии очагов. У 50% больных поражается также и серое вещество [6]. Задняя черепная ямка поражается у 48% больных. Спинной мозг вовлекается крайне редко. Поражение зрительных нервов при ПМЛ не наблюдается. JC-вирус не вызывает общевоспалительной реакции, в связи с чем изменения в крови и ЦСЖ неспецифичны и не коррелируют с наличием в ЦСЖ JC-вируса. Состав ЦСЖ при ПМЛ у 71% больных не отличается от нормы. У 29% имеется легкое повышение белка (40 80 мг/мл), у 6% небольшой плейоцитоз (до 16 клеток в 1 мл). Диагностика ПМЛ в настоящее время основывается на клинических проявлениях заболевания, данных МРТ и результатах исследования ЦСЖ и мозга больных на наличие JC-вируса. Согласно современной классификации, вероятный диагноз может быть выставлен при наличии характерных клинических и нейровизуализационных проявлений при отсутствии JC-вируса в ЦСЖ и мозговой ткани. Лабораторно подтвержденный диагноз устанавливается при наличии ДНК JC-вируса в ЦСЖ больного по данным ПЦР. Гистологически подтвержденный диагноз ПМЛ устанавливается в случае определения JC-вируса методом ПЦР в биопсийном материале мозга больного. Дифференциальный диагноз ПМЛ должен проводиться со СПИД-деменцией или ВИЧ-энцефалопатией, с оппортунистическими инфекциями ЦНС (энцефалиты цитомегаловирусной, токсоплазменной и грибковой этиологии), а также лимфомой головного мозга. Наибольшие трудности вызывает дифференциальная диагностика с ВИЧ-энцефалопатией, которая может не отличаться ни по клиническим, ни по нейровизуализационным признакам от ПМЛ. В данных случаях только выявление JCвируса в ЦСЖ и биоптатах головного мозга позволяет установить диагноз [18]. Развитие ПМЛ у больных с аутоиммунными заболеваниями и рассеянным склерозом, получавших терапию моноклональными антителами (ритуксимаб, натализумаб), делает необходимым учитывать возможность развития ПМЛ у этих больных. Появление нехарактерных клинических симптомов (когнитивные нарушения, афазия, гемианопсия, психические расстройства), прогрессирующее течение ранее ремиттирующего заболевания, появление новых очагов на МРТ, не накапливающих контрастное вещество, являются основаниями предположить наличие ПМЛ у этих пациентов. Основным подтверждением является наличие JCвируса в ЦСЖ. При отрицательном результате необходимо повторять исследование ЦСЖ каждые 4 нед. Биопсия головного мозга проводится в редких случаях при отсутствии JC-вируса в ЦСЖ при повторных исследованиях. Дифференциальный диагноз должен проводиться также с токсической лейкоэнцефалопатией, 31
4 вызванной действием цитостатиков, и различными инфекциями ЦНС (herpes simplex, вирус CMV, varicella zoster, criptocoсcus, aspergillus). В отличие от вышеназванных инфекций, при ПМЛ не встречается общеинфекционных и менингеальных симптомов в связи с отсутствием воспалительной реакции как в ЦНС, так и на периферии. Исследования последних лет показали, что использование специфических моноклональных антител при рассеянном склерозе, аутоиммунных и лимфопролиферативных заболеваниях повышает риск развития ПМЛ среди пациентов, которые получают эти препараты. К моноклональным антителам относятся такие препараты, как ритуксимаб, натализумаб, инфликсимаб, этанерцепт и др. Ритуксимаб является препаратом моноклональных антител против CD20 предшественников В-лимфо цитов и зрелых В-лимфоцитов. Разрешен к применению при клеточной неходжкинской лимфоме, резистентном ревматоидном артрите. В 2006 г. одобрен FDA для лечения системной краской волчанки. В настоящее время для контроля за действием ритуксимаба и выявления побочных эффектов препарата действует специальный проект (RADAR Research on Advers Drag Events and Report) при участии вирусологов, онкологов, неврологов и других специалистов [3]. Риск развития ПМЛ у больных, получающих ритуксимаб, составляет 1:8000 [16]. На сегодняшний день отмечено 270 случаев развития ПМЛ при применении ритуксимаба; смертность среди этих больных составляет 90%. Натализумаб препарат моноклональных антител к α-4 субъединице α-4β1 и α-4β7 интегринов, экспрессирующихся лейкоцитами и являющихся молекулами адгезии; используется в клинической практике с 1999 г. при рассеянном склерозе, ревматоидном артрите, болезни Крона. В связи с развитием 3 случаев ПМЛ у 2 больных рассеянным склерозом и 1 больного болезнью Крона с 28 февраля 2005 г. было приостановлено его применение. Предполагают несколько механизмов развития ПМЛ при лечении натализумабом: снижение иммунного лейкоцитарного ответа и реактивация JCвируса; стимуляция высвобождения JC-вируса из костного мозга и незрелых лейкоцитов [14, 26]. Была разработана и утверждена специальная программа для уменьшения риска развития ПМЛ у больных, получающих натализумаб (Risk Minimization Action Plan Risk MAP). В связи с этим в США действует программа Tysabri Outreach Unified Committee to Health TOUCH [15, 28]. Препарат был вновь разрешен к применению в мае 2006 г. с определенными ограничениями. К январю 2012 г. зарегистрировано 207 случаев ПМЛ у пациентов, получающих натализумаб. Риск развития данного осложнения у этих больных составляет 1:1000. При этом в США зарегистрировано 79 случаев развития ПМЛ, в странах Евросоюза 118 случаев, в других странах 10 случаев ПМЛ. Смертность в случае развития ПМЛ при этом составляет 21%. К февралю 2012 г. умерли 44 (21%) пациента. Большинство смертельных исходов отмечено через 2 3 мес после выявления ПМЛ. В апреле 2012 г. был описан 1 случай ПМЛ у больного РС, получающего финголимод и в анамнезе терапию натализумабом [9]. Предшествующее назначение иммуносупрессивной терапии, наличие повышенного титра антител к JC-вирусу повышают риск развития ПМЛ у пациентов, получающих иммуносупрессивную терапию длительностью более 24 мес. В настоящее время разработаны критерии включения и исключения при применении натализумаба у больных с РС [5, 12]. Индивидуальных критериев назначения моноклональных антител после той или иной терапии не разработано [13]. На сегодняшний день эффективного лечения ПМЛ не существует [8]. Используют различные классы лекарственных препаратов: противовирусные средства, цитостатики, антагонисты серотониновых рецепторов, а также трансплантацию стволовых клеток костного мозга [19, 25]. ВААРТ у ВИЧ-инфицированных больных это мультикомплексная терапия, состоящая из нуклеозидного ингибитора обратной транскриптазы (тимозид, зидовудин), ненуклеозидного ингибитора обратной транскриптазы (делавердин, рескриптор и др.), ингибитора протеаз (санвиновир, инвираза и др.). Лечение ВИЧ и ПМЛ с использованием ВААРТ увеличило выживаемость больных с 3 6 мес до 19,6 мес, снизило заболеваемость ПМЛ и другими оппортунистическими инфекциями ВИЧинфици ро ванных больных. В то же время у некоторых больных ВААРТ приводит к манифестации ПМЛ или ухудшению течения ПМЛ, что обусловлено развитием так называемого иммунного реконструктивного воспалительного синдрома (IRIS immune reconstrictution inflammatory syndrome). Предполагают, что активация инфекции связана с изменением баланса CD8+/CD4+ Т-клеток [20]. Наиболее часто при ПМЛ у не ВИЧ-инфицированных больных используют противовирусные препараты цидофир (вистид), интерферон-альфа, интерлейкин-2. Стабилизация процесса отмечалась у нескольких больных ПМЛ при лечении цитарабином (известном также как цитозар ингибитор ДНК полимеразы и репликации вируса). Современным направлением в лечении ПМЛ является использование препаратов блокаторов 5-гидрокситриптамина-2а серотониновых рецепторов, необходимых для проникновения JC-вируса в клетку. 32
Читайте также:


