Какие препараты принимают при золотистом стафилококке
По статистике, более чем у 50% здоровых людей есть золотистый стафилококк, при этом они не ощущают дискомфорта и не обращаются к врачу. Если иммунитет в порядке, микроорганизм, который считается патогенным и очень опасным, не требует медицинского вмешательства. Но при стечении нескольких неблагоприятных факторов развивается воспаление, и в этом случае необходима терапия.
Способы заражения
Существует несколько способов заражения (первыми указаны те, что встречаются наиболее часто):
· Контактный. Пренебрежение правилами гигиены приводит к тому, что бактерии стрептококки и стафилококки попадают в гортань с предметов обихода, детских игрушек, посуды. Например, подержавшись за дверную ручку, на которой есть бактерии, и поднеся руки ко рту, человек рискует заразиться.
· Воздушно-капельный. Находясь в одном помещении с больным, здоровый человек вдыхает воздух, в котором есть бактерии, и через некоторое время обнаруживает симптомы стафилококка в горле.
Стафилококк ауреус в горле может появиться даже после того, как человек вдохнет воздух с некоторым количеством микроорганизмов. Доказано, что микроб может длительное время обитать в воздухе, оставаясь жизнеспособным.
Симптомы развития стафилококковой инфекции
При стафилококке в горле могут развиться самые разные заболевания, но чаще всего врачи диагностируют стафилококковый ларингит, фарингит или тонзиллит.
Признаки, характерные для стафилококкового ларингита:
· першение и сухость в горле;
· сухой кашель, через несколько дней сменяющийся влажным, с обильным выделением мокроты;
· повышение температуры до 38,1—38,5 °C (иногда выше).
Признаки стафилококкового фарингита (диагностируется примерно в 5 случаях из 100):
· повышенная температура тела (37,5 °C и выше);
· вязкий слизистый налет на стенках горла;
· першение, вызывающее сухой кашель;
· отечность мягких тканей гортани;
· слабость, общее ухудшение самочувствия;
· боль в горле, которая усиливается при глотании;
Симптомы, характерные для стафилококкового тонзиллита:
· резкое повышение температуры (до 39—40 °C);
· боль в горле, переходящая на виски, мышцы шеи, уши;
· головная боль, слабость, головокружение, слезотечение;
· образование гноя на миндалинах;
· гиперемия слизистых оболочек миндалин и горла;
· увеличение лимфоузлов в области шеи;
· сильная боль при глотании;
Современные методы диагностики
При наличии стафилококка в горле симптомы проявляются по-другому: бактерии, попав в питательную среду, образуют колонии диаметром до 4 мм, имеющие выпуклую форму и оранжевый, белый или желтый цвет. Если нет времени ждать, пока бакпосев даст результаты, выявить болезнь может при помощи коагулазного теста. Его плюс в том, что результаты можно узнать уже через 4 часа, но если они будут отрицательными, время ожидания продлевается еще на 24 часа.
Серологический метод заключается в том, что на микробы воздействует стафилококковый бактериофаг. Их существует несколько групп, и каждая воздействует только на определенные виды патогенных микроорганизмов. Из-за невысокой точности (болезнь выявляется примерно в 60% случаев) сейчас этот способ применяется редко.
Есть допустимая норма содержания стафилококков в организме. Она выражается в микроскопических числах, которые ни о чем не скажут обычному человеку. Но пациент должен знать, что есть разница между стафилококком и стафилококковой инфекцией . В первом случае опасности нет, во втором — есть, и очень серьезная. Начинать лечение нужно немедленно, потому что появление инфекции свидетельствует о слабом иммунитете, и это значит, что организм не справится с болезнью собственными силами.
Общие принципы лечения
Результат лечения проявляется в следующем:
· укрепляется местный и неспецифический иммунитет;
· быстро заживают пораженные слизистые оболочки и мягкие ткани;
· подавляется активность болезнетворных микроорганизмов — возбудителей инфекции.
Местные антибиотики (таблетки, инъекции) помогают пациентам, у которых имеется стрептококк на миндалинах или стафилококковая инфекция в горле. Если поражены не только ткани и слизистые гортани, но и дыхательные пути (внелегочные и внутрилегочные ветвления бронхов, трахея, бронхиолы), проводят терапию сильнодействующими противостафилококовыми медикаментами и системными антибиотиками. Полезно делать полоскания препаратами Мирамистин, Фурацилин.
Важно: покупая Мирамистин, необходимо обращать внимание на концентрацию и назначение, так как данный препарат выпускается для разных целей.
Повышают эффективность лечения физиопроцедуры:
Антимикробные препараты системного действия выпускаются в виде спреев, инъекционных растворов, сиропов, таблеток, суспензий, капсул. Эффективно уничтожают золотистый стафилококк в горле у ребенка препараты, устойчивые к бета-лактамазе и пенициллиназе — ферментам, синтезируемым патогенными бактериями.
Лекарства на растительной основе
Препараты, содержащие растительные компоненты, относят к группе фитоадаптогенов. Их действие направлено на повышение сопротивляемости организма различным патогенным организмам: простейшим, вирусам, микробам, грибкам. В составе таких препаратов обычно содержатся биологически активные вещества, микроэлементы и витамины. В результате применения растительных адаптогенов снижается риск заболеть, а у тех, кто уже страдает от развившегося инфекционного заболевания, улучшается общее состояние.
Как проявляется действие лекарств:
· приходит в норму самочувствие;
· исчезает боль в горле;
· проходит отечность миндалин;
· уменьшается или полностью исчезает гиперемия.
Если до этого были другие признаки интоксикации стафилококком, они также уменьшаются. Растительные препараты полезны тем, что они способствуют скорейшему выздоровлению, предотвращают обострение болезни и снижают риск рецидива в дальнейшем.
Наиболее эффективные и недорогие фитоадаптогены:
Все препараты выпускаются в виде настоек и экстрактов. Что лучше принимать от золотистого стафилококка, подскажет лечащий врач.
Важно: у адаптогенов имеются противопоказания. В том числе, их нельзя принимать пациентам, у которых повышено артериальное давление.
При беременности экстракты и настои принимать не рекомендуется. В крайнем случае, необходимо предварительно проконсультироваться с гинекологом. Подобные средства повышают давление, при этом возможны неблагоприятные последствия как для плода, так и для самой женины. Также нежелательно давать растительные адаптогены детям: возможны побочные эффекты в виде бессонницы, отечности слизистых, кожного зуда, крапивницы.
Иммуностимулирующие препараты
Лечиться необходимо не только до исчезновения симптомов воспаления, но и в течение месяца после того, как наступит выздоровление. Такие препараты следует принимать как больным в рамках терапии при стафилококке горле, так и всем, кто страдает вторичным иммунодефицитом. Иммуностимуляторы значительно снижают риск развития инфекционных заболеваний.
Лечение народными средствами
К числу эффективных методов относят фототерапию. Но чтобы точно узнать, как вылечить больное горло и не навредить себе, предварительно нужно проконсультироваться с практикующим фитотерапевтом, которым знает, что такое золотистый стафилококк aureus. Экспериментировать с народными средствами не рекомендуется. Все же можно назвать перечень эффективных трав и плодов, которые помогают вылечить стафилококк в горле у детей и взрослых:
· мякоть абрикоса (принимать в виде пюре утром и вечером);
· плоды черной смородины (есть натощак в свежем виде);
· ванны с яблочным уксусом (50 г на ванну);
· настойка прополиса (использовать для полоскания)
· настой из смеси лекарственных трав (купить в аптеке и принимать по инструкции).
Лечение стафилококка у беременных и детей
Учитывая, что ослабленный организм хуже сопротивляется инфекции, при одинаковых обстоятельствах стафилококк в горле у ребенка или беременной женины появится с большей вероятностью, чем у остальных категорий пациентов. Однако лечить детей и будущих мам сложнее из-за большого количества противопоказаний и ограничений. Выбирая, чем лечить стафилококк, врач должен учитывать и индивидуальные особенности каждого человека. Методы борьбы с инфекцией в горле у детей подбирает педиатр, а схема лечения беременной женщины подбирается врачом-инфекционистом, при этом может потребоваться участие гинеколога, который ведет беременность.
Как лечиться тем, кто является носителем стафилококка?
Лечение стафилококка в горле не понадобится, если еще до того, как разовьется воспаление, человек будет делать следующее:
Рекомендованная продолжительность терапевтического курса, которой обычно хватает, чтобы избавиться от инфекции — 1 месяц. Затем необходимо сделать контрольный бакпосев, чтобы убедиться, что лечение золотистого стафилококка в горле дало результаты. Если носительство патогенных микроорганизмов не выявлено, можно начать принимать иммуностимуляторы. При наличии микробов в количестве, превышающем норму, следует сделать инъекцию стафилококкового анатоксина.
Вывод: быстро и эффективно вылечить золотистый стафилококк возможно только при взаимодействии с врачом и выполнении всех рекомендаций. Применять рецепты народной медицины не возбраняется, но они должны выступать не заменой полноценной терапии, а дополнением к ней.




Стерильный очищенный фильтрат фаголизатов бактерий рода Staphylococcus (с активностью по Аппельману - не менее 10 -5 ) - до 1 мл.
Представляет собой прозрачную жидкость желтого цвета различной интенсивности, возможен зеленоватый оттенок.
Препарат вызывает специфический лизис бактерий Staphylococcus.
Лечение и профилактика гнойно-воспалительных и энтеральных заболеваний, вызванных бактериями рода Staphylococcus у взрослых и детей:
заболевания уха, горла, носа, дыхательных путей и легких (воспаления пазух
носа, среднего уха, ангина, фарингит, ларингит, трахеит, бронхит, пневмония, плеврит);
хирургические инфекции (нагноения ран, ожоги, абсцесс, флегмона, фурункулы, карбункулы, гидроаденит, панариции, парапроктит, мастит, бурсит, остеомиелит);
урогенитальные инфекции (уретрит, цистит, пиелонефрит, кольпит, эндометрит, сальпингоофорит);
энтеральные инфекции (гастроэнтероколит, холецистит), дисбактериоз кишечника;
генерализованные септические заболевания;
гнойно-воспалительные заболевания новорожденных (омфалит, пиодермия, конъюнктивит, гастроэнтероколит, сепсис и др.);
другие заболевания, вызванные стафилококками.
При тяжелых проявлениях стафилококковой инфекции препарат назначается в составе комплексной терапии.
С профилактической целью препарат используют для обработки послеоперационных и свежеинфицированных ран, а также для профилактики внутрибольничных инфекций по эпидемическим показаниям.
Важным условием эффективной фаготерапии является предварительное определение чувствительности возбудителя к бактериофагу и раннее применение препарата.
Индивидуальная непереносимость или чувствительность к любому из компонентов препарата.
Целесообразно применение препарата при наличии инфекций, вызванных фагочувствительными штаммами стафилококков (по рекомендации врача).
Препарат используют для приема внутрь (через рот), ректального введения, аппликаций, орошений, введения в полости ран, вагины, матки, носа, пазух носа и дренированные полости. Перед употреблением флакон с бактериофагом необходимо взболтать и просмотреть. Препарат должен быть прозрачным и не содержать осадка.
16 августа 2016
- 9916
- 7,0
- 0
- 6
Структурная формула нового пептидного антибиотика.
Немецкие ученые обнаружили новое оружие для борьбы с больничным монстром — мультирезистентным золотистым стафилококком. Долгие годы оно скрывалось не в вечной мерзлоте или Марианской впадине, а прямо под нашим носом. Вернее — в нём.
В последние годы во всем мире увеличилось количество инфекционных заболеваний, вызванных устойчивыми к антибиотикам бактериями. Организмы с множественной лекарственной резистентностью (multidrug-resistant organisms, MDRO), такие как метициллин-резистентный золотистый стафилококк, нечувствительные к ванкомицину энтерококки или резистентные к цефалоспоринам третьего поколения грамотрицательные бактерии, в ближайшие десятилетия могут стать более частыми причинами смерти, чем рак [1].
Несколько лет назад удалось обнаружить, что представители человеческой микробиоты способны производить бактериоцины, поражающие близкородственных бактерий [2]. Например, в 2014 году из человеческого комменсала Lactobacillus gasseri выделили и описали новый синтезируемый рибосомами тиопептидный антибиотик — лактоциллин [3].
Семейные разборки
Немецкий исследователь Александр Ципперер со своими сотрудниками в июле 2016 года сообщил о том, что обнаружил в человеческом носу бактерию Staphylococcus lugdunensis IVK28, которая подавляет рост метициллин-резистентного золотистого стафилококка (methicillin-resistant Staphylococcus aureus, MRSA) [1].
Стафилококки относятся к типичным бактериям-комменсалам, колонизирующим кожу и поверхности слизистых оболочек. Staphylococcus aureus — шаровидные грамположительные бактерии, вырабатывающие каротиноидный пигмент, который придает их клеткам золотистый цвет (рис. 1). Эти микроорганизмы чрезвычайно устойчивы к внешним воздействиям и выживают в воздухе, пыли, почве, продуктах питания, на оборудовании пищевых производств и предметах быта [6], [7].
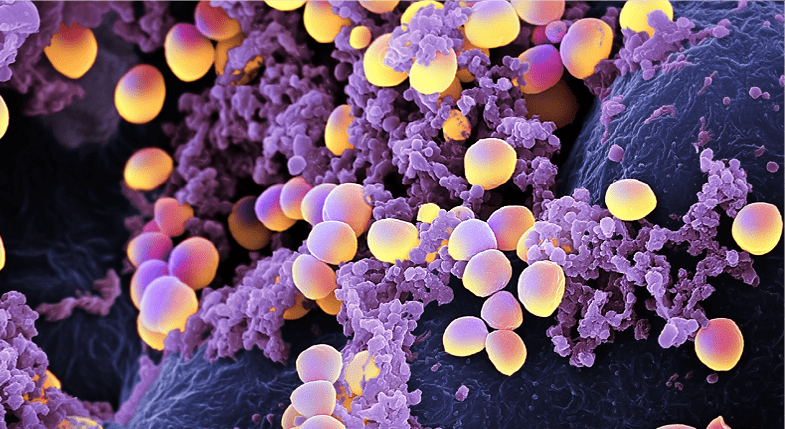
Рисунок 1. Staphylococcus aureus и лейкоциты.
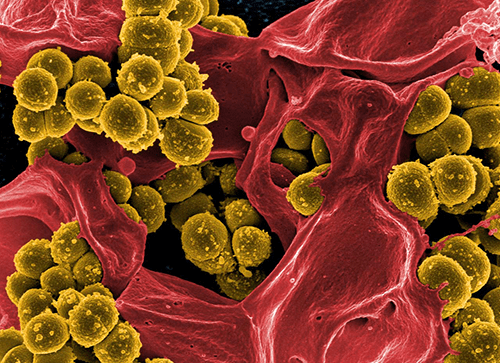
Рисунок 2. Метициллин-резистентные золотистые стафилококки.
Staphylococcus aureus — бактерия условно-патогенная, проявляющая свои патологические свойства только в благоприятных условиях, а создает их, как правило, ослабление иммунитета носителя. Активная жизнедеятельность стафилококка может привести к разнообразным заболеваниям [5], [7], [8]:
- кожи (прыщи, фурункулы, синдром ошпаренной кожи);
- органов дыхания (плеврит, пневмония);
- костной и соединительной тканей (артрит, остеомиелит);
- нервной системы и органов чувств (отит, менингит);
- сердечно-сосудистой системы (эндокардит, флебит, стафилококковая бактериемия).
Факторы патогенности S. aureus — это микрокапсула, компоненты клеточной стенки, ферменты агрессии и токсины. Микрокапсулы защищают клетки бактерий от фагоцитоза, способствуют их адгезии и распространению по организму хозяина. Составляющие клеточной стенки (например пептидогликан, тейхоевые кислоты и белок А) вызывают развитие воспаления, обездвиживают фагоциты и нейтрализуют иммуноглобулины. Коагулаза, главный фермент агрессии, вызывает свертывание плазмы крови [7], [9].
Наиболее опасны метициллин-резистентные стафилококки (methicillin-resistant S. aureus, MRSA) (рис. 2). Метициллин — это модифицированный пенициллин, с помощью которого еще недавно успешно боролись со стафилококковой инфекцией. MRSA устойчивы не только к метициллину, но и к другим антибиотикам пенициллиновой группы (диклоксациллину, оксациллину, нафциллину и др.), а также к цефалоспоринам. В последнее время выявлены штаммы и с более широким спектром устойчивости: ванкомицин-резистентные (VRSA) и гликопептид-резистентные (GISA) [6], [9], [10].
Штамм S. lugdunensis IVK28 эффективно боролся со своим вредоносным родственником лишь в условиях недостатка железа и только на твердых агаризованных средах (рис. 3, слева). Механизм противостояния был неясен, а потому Ципперер провел транспозонный мутагенез клеток выделенного штамма — чтобы выявить ген, ответственный за синтез смертельного для S. aureus вещества.

В итоге удалось получить мутанта IVK28, который не мог подавлять рост MRSA. Анализ места встройки транспозона показал, что тот нарушил структуру гена предполагаемой нерибосомной пептидсинтетазы (НРПС). Оказалось, что этот ген вместе с другими последовательностями, связанными с биосинтезом антибиотиков, входит в состав оперона размером 30 т.п.н. Это указывало на то, что предполагаемая молекула ингибитора может быть комплексом нерибосомных пептидов.
Оперон методом ПЦР обнаружили во всех культурах S. lugdunensis, а значит, он характерен для всего вида, а не только для штамма IVK28. Однако GC-состав оперона (26,9%) отличался от GC-состава остального генома S. lugdunensis (33,8%), что свидетельствовало о возможном заимствовании этого полезного генетического кластера у других видов бактерий — путем горизонтального переноса .
Оперон состоит из генов lugA, B, C и D, кодирующих пептидсинтетазные белки (см. врезку ниже), а также из других генов, чьи продукты необходимы для синтеза и транспорта нерибосомного пептида.
Чтобы окончательно вменить оперону участие в антибактериальной деятельности S. lugdunensis, наименьший ген (lugD) удалили. Мутант ΔlugD, как и ожидалось, не мог подавлять рост золотистого стафилококка, но когда в него ввели плазмиду с работающим геном lugD, агрессивный фенотип восстановился (рис. 3, в центре и справа).
Секретное оружие
Выделенный Ципперером продукт lug-оперона оказался нерибосомным циклическим пептидом, состоящим из пяти аминокислот (двух D-валинов, L-валина, D-лейцина и L-триптофана) и тиазолидинового гетероцикла (рис. 4). Назвали антибиотик лугдунином.
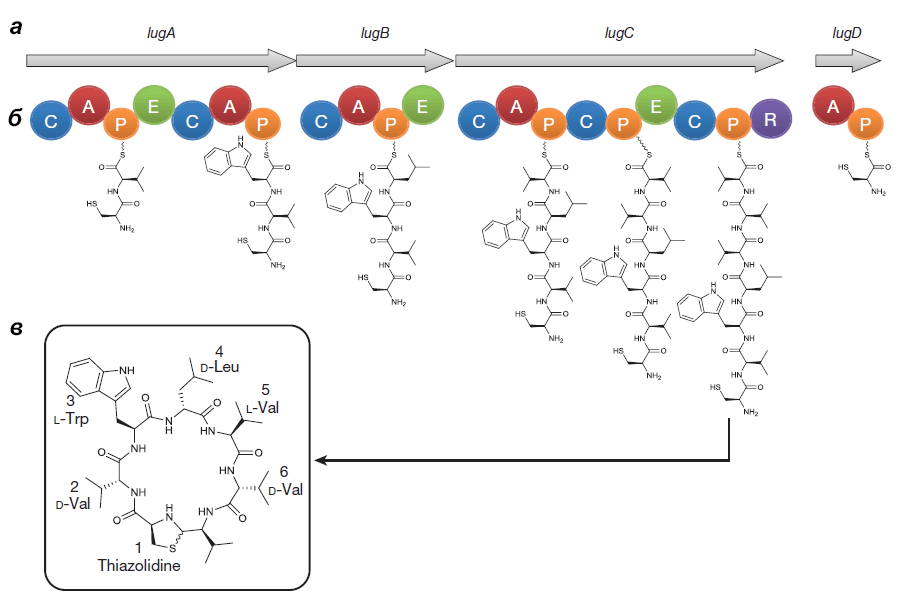
Химическим синтезом удалось получить продукт с идентичными природному лугдунину химическими свойствами и антибактериальным эффектом. Ученые предположили, что этот антибиотик ингибирует синтез бактериальных биополимеров — белков, ДНК и пептидогликанов [5].
Этот класс пептидов синтезируется в клетках низших грибов и бактерий без участия рибосом. Нерибосомные пептиды (НРП) также встречаются и у высших организмов, которые имеют бактерий-комменсалов [12].
НРП подразделяются на несколько функциональных групп [13]:
- антибиотики (ванкомицин);
- предшественники антибиотиков (ACV-трипептид — предшественник пенициллина и цефалоспорина);
- иммуносупрессоры (циклоспорин);
- противоопухолевые пептиды (блеомицин);
- сидерофоры (пиовердин);
- токсины (HC-токсин);
- сурфактанты (сурфактин).
Каждый модуль состоит как минимум из трех доменов:
- конденсирующего (принимающего пептидную цепь из предыдущего модуля);
- аденилирующего (выбирающего нужную аминокислоту);
- пептидильного (образующего пептидную связь).
Нередко модули включают и другие домены, в том числе эпимеризующий, который преобразует L-аминокислоты в D-формы [14].
По аналогии с триплетным рибосомным кодом для синтеза белка существует и нерибосомный, код НРПС, определяемый 10 остатками аминокислот в субстрат-связывающем кармане аденилирующего домена. От комбинации этих остатков зависит то, какая аминокислота будет встроена в пептид конкретным модулем НРПС. Зная этот код, можно предсказывать субстратную специфичность аденилирующих доменов и даже произвольно изменять ее посредством замены аминокислот в домене [14].
В экспериментах немецких ученых лугдунин действовал не только на метициллин-резистентных стафилококков, но и на гликопротеин-резистентных, и даже на других грамположительных бактерий типа листерии и ванкомицин-резистентного энтерококка (табл. 1). Минимальная ингибирующая концентрация (МИК) нового бактериоцина — 1,5–12 мкг × мл −1 , что говорит о высокой активности вещества. При этом такие концентрации никак не влияли на человеческую сыворотку, не вызывали лизис нейтрофилов или эритроцитов и не ингибировали метаболическую активность моноцитов. Бактериальные же клетки под действием лугдунина в концентрации даже ниже МИК прекращали синтезировать ДНК, РНК, белки и компоненты клеточной стенки. В этом отношении лугдунин напоминает даптомицин, дающий такой же эффект, но способ действия которого пока не изучен. Не было отмечено возникновения резистентности клеток S. aureus к лугдунину даже после их месячного выращивания на малых концентрациях.
| Виды и штаммы | Резистентность | МИК лугдунина (мкг × мл −1 ) |
|---|---|---|
| Staphylococcus aureus USA300 (LAC) | MRSA | 1,5 |
| + 50% человеческой сыворотки крови | 1,5 | |
| Staphylococcus aureus USA300 (NRS384) | MRSA | 1,5 |
| Staphylococcus aureus Mu50 | GISA | 3 |
| Staphylococcus aureus SA113 | 3 | |
| Staphylococcus aureus RN4220 | 3 | |
| Enterococcus faecium BK463 | VRE | 3 |
| Enterococcus faecalis VRE366 | VRE | 12 |
| Listeria monocytogenes ATCC19118 | 6 | |
| Streptococcus pneumoniae ATCC49619 | 1,5 | |
| Bacillus subtilis 168 (trpC2) | 4 | |
| Pseudomonas aeruginosa PAO1 | >50 | |
| Escherichia coli DH5α | >50 | |
| Условные обозначения: MRSA — метициллин-резистентные S. aureus; GISA — устойчивые к гликопротеинам S. aureus; VRE — ванкомицин-резистентные Enterococcus. Таблица из [1]. | ||
Испытания в боевых условиях
Как и полагается, способность лугдунина лечить стафилококковые инфекции продемонстрировали in vivo на мышиной модели (рис. 5). У шести мышей сбрили шерсть на спине и, повредив кожу многократным приклеиванием/отклеиванием пластыря, нанесли на это место золотистого стафилококка. Затем кожу обработали мазью, содержащей 1,5 мкг лугдунина, и спустя шесть часов оценили результат. Обработка новым антибиотиком сильно сокращала или даже полностью уничтожала популяцию S. aureus. Причем не только на поверхности кожи, но и в более глубоких ее слоях.
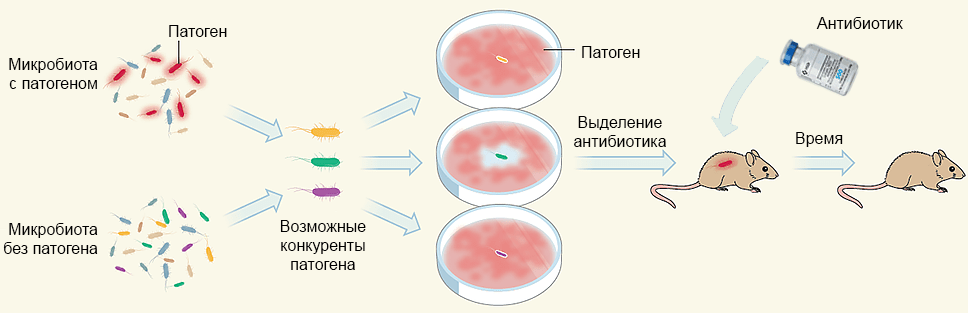
Рисунок 5. Общая схема подхода к идентификации природного антибиотика. Из бактериальных популяций человеческого тела отбирают представителей, которые не могут сосуществовать с интересующими патогенными бактериями. Этих возможных конкурентов тестируют по отдельности на средах с инфекционным агентом. Из культуры, успешно подавляющей рост патогенов, выделяют антибиотик, действие которого проверяют на животных моделях.
[5], рисунок модифицирован и адаптирован
Чтобы понять, может ли S. lugdunensis помешать колонизации носовой полости позвоночных животных золотистым стафилококком в естественных условиях, ученые провели следующий эксперимент. В носы хлопковых хомяков ввели два вида смешанных культур (S. aureus + S. lugdunensis IVK28 и S. aureus + S. lugdunensis IVK28ΔlugD) и каждую по отдельности. В контрольных случаях, когда вводили по одному штамму, все три культуры стабильно колонизировали носовую полость. Однако при введении смеси S. aureus + S. lugdunensis IVK28 количество золотистого стафилококка через 5 дней значительно уменьшилось по сравнению со смесью S. aureus + S. lugdunensis IVK28ΔlugD. Этот эксперимент показал, что продукция лугдунина позволяет штамму IVK28 эффективно конкурировать с золотистым стафилококком in vivo.
Оставалось разобраться, предотвращает ли присутствие S. lugdunensis в носу человека колонизацию бактериями S. aureus. Ципперер и его коллеги исследовали мазки из носовых ходов 187 госпитализированных больных. Из них у 60 человек (32,1%) обнаружили золотистого стафилококка и у 17 человек (9,1%) — S. lugdunensis. И только у одного пациента с S. lugdunensis в носу обитал S. aureus. У всех выделенных штаммов S. lugdunensis ПЦР-анализ продемонстрировал наличие lug-оперона, а все обнаруженные штаммы S. aureus оказались восприимчивы к лугдунину.
Перспективы
Лугдунин оказался первым обнаруженным бактериоцином нового класса — макроциклических тиазолидиновых пептидных антибиотиков. Все проверенные штаммы S. aureus (как природные, так и лабораторные) не смогли выработать резистентности к нему. Это дает надежду на то, что лугдунин в будущем станет коммерческим препаратом для борьбы с золотистым стафилококком.
И наконец, сам факт обнаружения нового антибиотика у представителя человеческой микробиоты должен послужить стимулом для активизации поиска других продуцентов бактериоцинов в составе именно таких сообществ. В дальнейшем это поможет медикам успешнее сдерживать наступление мультирезистентных патогенов.
Действующее вещество
Бактериофаг стафилококковый
Инструкция по медицинскому применению - РУ № Р N001973/01
Дата последнего изменения: 27.04.2017
Раствор для приема внутрь, местного и наружного применения.
В 1 мл лекарственного препарата содержится активного вещества - стерильного фильтрата фаголизатов бактерий рода Staphylococcus до 1 мл.
Консервант-8-гидроксихинолина сульфат - 0,0001 г/мл (содержание расчетное);
или 8-гидроксихинолина сульфата моногидрат - 0,0001 г/мл (в пересчете на 8-гидроксихинолина сульфат, содержание расчетное).
Препарат представляет собой прозрачную жидкость желтого цвета различной интенсивности.
Препарат вызывает специфический лизис бактерий Staphylococcus.
Лечение и профилактика гнойно-воспалительных и энтеральных заболеваний, вызванных бактериями рода Staphylococcus у взрослых и детей.
- заболевания уха, горла, носа, дыхательных путей и легких (воспаления пазух носа, среднего уха, ангина, фарингит, ларингит, трахеит, бронхит, пневмония, плеврит);
- хирургические инфекции (нагноения ран, ожоги, абсцесс, флегмона, фурункулы, карбункулы, гидроаденит, панариции, парапроктит, мастит, бурсит, остеомиелит);
- урогенитальные инфекции (уретрит, цистит, пиелонефрит, кольпит, эндометрит, сальпингоофорит);
- энтеральные инфекции (гастроэнтероколит, холецистит), дисбактериоз кишечника;
- генерализованные септические заболевания;
- гнойно-воспалительные заболевания новорожденных (омфалит, пиодермия, конъюнктивит, гастроэнтероколит, сепсис и др.);
- другие заболевания, вызванные стафилококками.
При тяжелых проявлениях стафилококковой инфекции препарат назначается в составе комплексной терапии.
С профилактической целью препарат используют для обработки послеоперационных и свежеинфицированных ран, а также для профилактики внутрибольничных инфекций по эпидемическим показаниям.
Важным условием эффективной фаготерапии является предварительное определение чувствительности возбудителя к бактериофагу и раннее применение препарата.
Индивидуальная непереносимость или чувствительность к любому из компонентов препарата.
Целесообразно применение препарата при наличии инфекций, вызванных фагочувствительными штаммами стафилококков (по рекомендации врача).
Препарат используют для приема внутрь (через рот), ректального введения, аппликаций, орошений, введения в полости ран, вагины, матки, носа, пазух носа и дренированные полости. Перед употреблением флакон с бактериофагом необходимо взболтать и просмотреть. Препарат должен быть прозрачным и не содержать осадка.
Рекомендуемые дозировки препарата
Доза на 1 прием (мл)
от 1 года до 3 лет
от 8 лет и старше
Лечение гнойно-воспалительных заболеваний с локализованными поражениями должно проводиться одновременно как местно, так и приемом препарата внутрь 2-3 раза в день натощак за 1 ч до приема пищи с первого дня заболевания в течение 7-20 дней (по клиническим показаниям).
В случае если до применения бактериофага для лечения ран применялись химические антисептики, рана должна быть тщательно промыта стерильным натрия хлорида раствором 0,9%.
В зависимости от характера очага инфекции бактериофаг применяют:
1. В виде орошения, примочек и тампонирования в объеме до 200 мл в зависимости от размеров пораженного участка. При абсцессе после удаления гнойного содержимого с помощью пункции препарат вводят в количестве меньшем, чем объем удаленного гноя. При остеомиелите после соответствующей хирургической обработки в рану вливают бактериофаг по 10-20 мл.
2. При введении в полости (плевральную, суставную и другие ограниченные полости) до 100 мл, после чего оставляют капиллярный дренаж, через который бактериофаг вводят в течение нескольких дней.
3. При циститах, пиелонефритах, уретритах препарат принимают внутрь. В случае если полость мочевого пузыря или почечной лоханки дренированы, бактериофаг вводят через цистостому или нефростому 1-2 раза в день по 20-50 мл в мочевой пузырь и по 5-7 мл в почечную лоханку.
4. При гнойно-воспалительных гинекологических заболеваниях препарат вводят в полость вагины, матки в дозе 5-10 мл ежедневно однократно, при кольпите - по 10 мл орошением или тампонированием 2 раза в день. Тампоны закладывают на 2 часа.
5. При гнойно-воспалительных заболеваниях уха, горла, носа препарат вводят в дозе 2-10 мл 1-3 раза в день. Бактериофаг используют для полоскания, промывания, закапывания, введения смоченных турунд (оставляя их на 1 час).
6. При энтеральных инфекциях, дисбактериозе кишечника препарат принимают внутрь 3 раза в день за 1 час до приема пищи. Возможно сочетание двукратного приема внутрь с однократным ректальным введением разовой возрастной дозы бактериофага в виде клизмы после опорожнения кишечника.
Применение бактериофага у детей (до 6 месяцев). При сепсисе, энтероколите новорожденных, включая недоношенных детей, бактериофаг применяют в виде высоких клизм (через газоотводную трубку или катетер) 2-3 раза в сутки в дозе 5-10 мл. При отсутствии рвоты и срыгивания возможно применение препарата через рот. В этом случае он смешивается с грудным молоком. Возможно сочетание ректального (в виде высоких клизм) и перорального (через рот) применения препарата. Курс лечения 5-15 дней. При рецидивирующем течении заболевания возможно проведение повторных курсов лечения. С целью профилактики сепсиса и энтероколита при внутриутробном инфицировании или опасности возникновения внутрибольничной инфекции у новорожденных детей бактериофаг применяют в виде клизм 2 раза в день в течение 5-7 дней.
При лечении омфалита, пиодермии, инфицированных ран препарат применяют в виде аппликаций ежедневно двукратно (марлевую салфетку смачивают бактериофагом и накладывают на пупочную ранку или на пораженный участок кожи).
Читайте также:


