Рецидивирующий герпетический стоматит и м рабинович

Дата публикации: 29.11.2016 2016-11-29
Статья просмотрена: 1843 раза
Хронический рецидивирующий афтозный стоматит (ХРАС) представляет серьезную проблему стоматологии в связи с ростом заболеваемости. В обзоре литературы изложены сведения касающиеся этиологии, патогенеза и современных методов лечения. Среди многочисленных патогенетических механизмов развития ХРАС, на сегодняшний день предпочтение отдают иммунологическим.
Большое внимание отводят соматическим заболеваниям, которые усугубляют течение ХРАС. Поэтому тщательное обследование пациентов и консультации специалистов является достижением в лечении больных ХРАС. Исследования доказывают, что для достижения стабильного результата в лечении необходимо индивидуальный подбор комплексной патогенетической терапии с учетом общесоматического состояния пациента. Совместно с системным лечением, которое включает гипосенсибилизирующую, общеукрепляющую, седативную, иммунокоррегирующую терапию, необходимым является и местное лечение.
Последние десятилетия в проблеме профилактики и лечения хронических заболеваний слизистой оболочки полости рта уделяется значительное внимание отечественных и зарубежных исследователей. [5, 18, 20, 19, 41, 21].
Это в первую очередь обусловлено увеличением негативного влияния на организм человека иммунодепрессивных факторов окружающей среды, широким и не всегда обоснованным использованием медикаментов с антибактериальными свойствами. [11,12, 17, 29, 23, 28].
Многие годы до сегодняшнего дня в клинической практике, пациенты, обратившиеся за стоматологической помощью с заболеваниями слизистой оболочки полости рта (СОПР), представляют одну из наиболее сложных проблем в стоматологии из-за трудностей в диагностике и лечении [35].
Проблема усложняется еще и тем, что до настоящего времени каких-либо мер коммунальной профилактики болезней СОПР не разработано [8].
По данным ВОЗ, поражает до 20 % населения. По мнению других исследователей около 20 % населения страдает афтами в тот или иной период жизни. Установлено, что возраст большинства больных колеблется от 20 до 40 лет. До полового созревания болеют лица обоего пола, но среди взрослых преобладают женщины [2].
О. Ф. Рабинович с соавт. [15] считают, что в основе этиологии и патогенеза лежит аутоиммунная теория, позволяющая связать возникновение патологических элементов с нарушением клеточного и гуморального иммунитета, как местного, так и общего.
В частности развитие хронического рецидивирующего афтозного стоматита и парестезии слизистой оболочки, связано с определенными трудностями и является одной из актуальных задач. Данные заболевания сопровождаются нарушениями микроциркуляции, которая играет основную роль в трофическом обеспечении тканей [4,13].
Одним из первых признаков нарушения микроциркуляции являются локальный спазм артериальных сосудов, застойные явления в венулярных сосудах, а также снижение интенсивности кровотока в нутритивном звене капиллярного русла [16].
В 1956 году И. Г. Лукомский и И. О. Новик смогли предположить аллергическую природу возникновения ХРАС. В качестве аллергена могут быть пищевые продукты, пыль, зубные пасты, глисты и продукты их жизнедеятельности лекарственные вещества.
Ряд авторов широко обсуждают вопрос об аллергическом генезе заболевания [25, 22].
Этиология и патогенез хронического рецидивирующего афтозного стоматита окончательно не выяснены. Установлено, что существенная роль в патогенезе хронических воспалительных процессов принадлежит состоянию микробиоценоза слизистой оболочки полости рта [6, 30, 33, 32].
Доказано его участие в процессах обмена веществ, синтеза витаминов, формировании иммунного статуса и неспецифической резистентности. О роли желудочно-кишечной патологии и заболеваний печени в патогенезе
ХРАС свидетельствуют клинические и экспериментальные данные [37, 38].
В то же время проблема свободнорадикальных процессов и антиоксидантной защиты в слюне при данной патологии остается малоизученной. Известно, что нарушения иммунологического и свободнорадикального статуса могут влиять на течение и прогноз хронических заболеваний слизистой оболочки полости рта [34, 39].
Так, Graykowski в 1966 г. с помощью кожных тестов установил у ряда больных рецидивирующим афтозным стоматитом повышенную чувствительность к различным бактериям. В дальнейшем [10] c помощью внутрикожных проб выявила у них моно- и поливалентную аллергию к протею, стафилококку, стрептококку и кишечной палочке, в связи с чем эти авторы значительную роль в патогенезе заболевания отводят бактериальной аллергии. Однако следует отметить, что вывод об инфекционно-аллергической природе рецидивирующего афтозного стоматита только на основании результатов аллергических кожных проб не может считаться достоверным.
Ряд авторов указывают, определенную роль в тканевых повреждениях при рецидивирующем афтозном стоматите играют выявленные циркулирующие иммунные комплексы [42, 27, 40].
В современных концепциях патогенеза решающее значение придается нарушениям в иммунной системе. По данным [11], у больных ХРАС выявлено угнетение клеточного иммунитета.
А. Л. Машкиллейсона и др., у 2/3 больных рецидивы афтозного стоматита возникают на фоне дефицита Т-лимфоцитов периферической крови, причем оказалось, что левамизол не у всех больных стимулировал розеткообразующую функцию Т-лимфоцитов in vitro. В патогенезе афтозного стоматита определенное значение может иметь так называемая перекрестная иммунная реакция, так как на слизистой оболочке полости рта и в кишечнике имеется бактериальная флора, и антитела, вырабатывающиеся на ее присутствие, могут по ошибке атаковать эпителиальные клетки слизистой оболочки из-за сходства их антигенной структуры с таковой некоторых бактерий. Этим вполне можно объяснить образование афт как результат проявления феномена Артюса, а также значение желудочно-кишечной патологии, сопровождающейся нарушением баланса между организмом и бактериальной флорой, в происхождении рецидивирующего афтозного стоматита. О роли желудочно-кишечной патологии и заболеваний печени в патогенезе афтозного стоматита весьма демонстративно свидетельствуют данные [3], обнаружившего его у многих больных, страдавших различными болезнями желудочно-кишечного тракта, а также экспериментальные данные В. С. Куликовой и соавт. (1977) о роли печеночной патологии.
Сторонники одной из первых теорий связывали возникновение афтозного стоматита с изменениями трофоневротического характера.
В. А. Епишев [3] наблюдал их в 15,2 % случаев, по Ship (1972), количество семейных случаев рецидивирующего афтозного стоматита достигает 80 %, по данным Г. В. Банченко [1]- лишь 12 %.
Пациенты обращаются за помощью в период обострения. Появление афт, выраженный болевой синдром, нарушение сна, головная боль, канцерофобия, что, в конечном итоге, приводит к снижению качества жизни пациентов [15].
По данным зарубежных авторов [24, 31], ХРАС имеет три основных проявления: малые афты (афты Микулича), размером не более 10 мм, большие афты (болезнь Сеттона), герпетиформные язвы — множественные афты [31]. ХРАС может быть одним из симптомов генерализованного афтоза (большой афтоз Турена) и признаком болезни Бехчета [7].
В связи с тем, что длительное течение ХРАС сопровождается сменой микробиологического статуса, показано применение эубиотиков местного действия (Ацелак, Бифилиз), а также системного действия (Хелак-форте) [9].
Таким образом, ХРАС в настоящее время представляет собой важную медицинскую и социальную проблему. На современном этапе существует большое количество средств и методов лечения ХРАС, однако полный алгоритм комплексной терапии не разработан, отсутствуют методики поддерживающей терапии, что по-прежнему остается актуальной задачей и требует дальнейших исследований.

ОГС, протекая по типу инфекционного заболевания, имеет 5 периодов развития: 1) инкубационный; 2) продромальный; 3) период развития заболевания (а - катаральный; б - высыпания элементов поражения); 4) период угасания болезни; 5) клиническое выздоровление.
Вирус остается в организме пожизненно. Перенесшие ОГС дети становятся носителями вируса или страдают рецидивирующим герпетическим стоматитом (РГС), герпесом губ. У каждого 7-8 ребенка после перенесенного ОГС развивается рецидивирующая форма болезни.. Многолетняя консультативная и лечебная работа по ведению больных с заболеваниями слизистой оболочки выявила затруднение врачей практического здравоохранения при клинической диагностике заболеваний с герпетиформными поражениями.
Целью исследования стало совершенствование клинической диагностики острого и рецидивирующего герпетического стоматита, герпеса губ у детей на основе изучения клинического течения заболевания, дифференциальной диагностики с эрозивными поражениями слизистой оболочки полости рта.
Материал и методы.
Нами проведено клиническое, лабораторное (ПЦР-диагностика) обследование и лечение 406 детей в возрасте от 2 до 16 лет: 320 детей, больных герпетическим стоматитом, герпесом губ различной степени тяжести, 32 ребенка с диагнозом герпангина, 12 детей с многоформной экссудативной эритемой , 42 - с рецидивирующим афтозным стоматитом. В статье приводятся собственные клинические случаи наблюдения больных.
Результаты и обсуждение.
Критерием ранней клинической диагностики ОГС является симптомокомплекс: подчелюстной лимфаденит, катаральный гингивит, симптомы ОРВИ. При появлении этих симптомов необходимо начать раннюю патогенетическую противовирусную общую и местную терапию. Затем возникают сгруппированные высыпания (пузырьки), быстро переходящие в эрозии на слизистой оболочке полости рта, губ, коже. Клинически заболевание протекает по типу острого инфекционного процесса в виде легкой, среднетяжелой и тяжелой формы. Тяжесть патологии определяется по степени выраженности общих симптомов и распространенности поражений на слизистой оболочке полости рта (табл. 1-3).
Таблица 1 - Клиническое течение легкой формы ОГС
Клинически отсутствует. Внешнее
отсутствие симптомов интоксикации.
Повышение температуры до 37,2-37,5 °С. Общее состояние удовловлетвори-тельное. Иногда незначительные явления катара слизистой оболочки носа, дыхательных путей. Слабый катаральный гингивит (главным образом в области десневого края нижних фронтальных зубов).
t = 37,5 °С. Общее состояние удовлетворитель-ное. Боли при приеме пищи. На фоне усиливающейся гиперемии и подъема темпера-туры в полости рта появляются сгруппированные элементы поражения (до 5).
Температура нормальная. Самочувствие хорошее. Боль при приеме пищи угасает. При своевременном и правильном лечении гингивит отсутствует (или нелеченный
Элементы поражения в стадии активной эпителизации.
Температура нормальная. Самочувствие хорошее.
Гингивит отсутствует (или нелеченный гингивит).
Высыпания однократные. Лимфаденит.
Лимфаденит сохраняется в течение 7 дней.
Продолжительность периода 1,3±0,7 дня.
Продолжитель-ность 1,0±0,7 дня.
Продолжительность 4,0±1,5 дня.
Продолжитель-ность 7 дней.
Таблица 2 - Клиническое течение среднетяжелой формы ОГС
t = 37,2-37,5°С. Общее состояние: слабость, капризы, ухудшение аппетита.
t = 38-39°С. Общее состояние средней тяжести: головная боль, тошнота рвота, бледность кожных покровов. Симптомы ОРЗ (кашель, насморк). Острый катаральный гингивит, стоматит.
Высыпания на коже лица (чаще приротовой области).
На пике подъема t усиливается гингивит и высыпают в полости рта элементы поражения от 3 до 25. Усиливается саливация, ребенок не ест, плохо спит, нарастают симптомы вторичного токсикоза (четко выражены). Высыпания часто повторные (2-3 раза). После первого высыпания элементов температура снижается до 37-37,5°С. Однако, последующие высыпания сопровождаются, как правило, ее повышением до прежних цифр. При появлении повторных высыпаний элементы поражения находятся на разных стадиях развития (ложный полиморфизм).
Температура нормальная. Самочувствие удовлетворительное: сон и аппетит восстанавливаются. Гингивит отсутствует в результате правильного и своевременного лечения или нелеченный гингивит. Элементы поражения в стадии эпителизации. Продолжительность периода угасания зависит от сопротивляемости организма ребенка, наличия в полости рта кариозных и разрушенных зубов, проводимой терапии. Нерациональная терапия способствует слиянию элементов с образованием значительных некротических поверхностей. Появляется язвенно-некротический гингивит (преимущественно в области резцов). Эпителизация затягивается.
Лимфаденит. Продолжитель-ность периода 2,5±0,5 дня.
Таблица 3 - Клиническое течение тяжелой формы ОГС
t = 38-39 °С. Общее состояние: адинамия, головная боль, кожно-мышечная гиперестезия, артралгия. Нередко брадикардия или тахикардия, артериальная гипотония, носовые кровотечения. Кашель, насморк..
Нередко заболеванию предшествует любое другое заболевание: вирусное, бактериальное
и др., сопровожда-ющееся лихорадочными состояниями.
t = 39,5-40 °С. Общее состояние: тяжелое. Резко выражены симптомы интоксикации. Насморк, кашель.
Отечные и гипере-мированные конъюнктивы глаз. Губы сухие, яркие, запекшиеся. Катарально-язвенный гингивит, стоматит.
Лимфаденит подчелюстных и шейных лимфоузлов.
t = 38-39 °С. Общее состояние: тяжелое. Отсутствует аппетит. Усиливается воспаление дыхательных путей. Выраженные носовые кровотечения. На слизистой оболочке полости рта на пике подъема температуры появляются элементы поражения до 30. Высыпания многократные, и поэтому количество элементов увеличивается до 100. Они находятся на разных стадиях развития. Элементы сливаются, образуя обширные зоны некроза. Поражаются губы, щеки, язык, мягкое и твердое нёбо, десневой край. Катаральный гингивит переходит в язвенно-некротический (чаще генерализованный). Появляется резкий гнилостный запах изо рта. Обильное слюнотечение с примесью крови. Высыпания: веки, мочки ушей, приротовая область, пальцы рук, ягодицы.
Температура нормальная. Сон и аппетит восстанавли-ваются медленно.
Остаточные явления гингивита.
Продолжитель-ность периода 3,5±0,5 дня.
Продолжительность 3,5±1,5 дня.
Лимфаденит. Продолжи-тельность 8,0±1,7 дня.
На рисунках 1, 2 представлены клинические проявления острого герпетического стоматита, герпеса губ тяжелой формы у детей, обратившихся в нашу клинику.
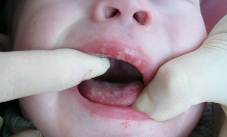
Рис. 1. ОГС, тяжелая форма.
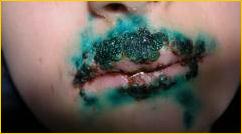
Рис. 2. ОГС, герпес губ.
Наблюдение за детьми с РГС, рецидивирующим герпесом губ показало, что степень тяжести рецидивирующего герпетического стоматита зависит от частоты рецидивов заболевания, давности рецидивирования, выраженности симптомов общего и местного характера. Легкая форма РГС характеризуется редкими (1-2 раза в несколько лет) рецидивами заболевания. При среднетяжелой форме РГС рецидивы заболевания - 1-3 раза в год. Для тяжелой формы РГС характерны частые (4 раза в год и более) рецидивы, перманентная (непрерывно-рецидивирующая) форма заболевания. Продолжительность и степень выраженности симптомов местного (гиперемия слизистой, гингивит, эрозии) и общего характера (температура, головная боль, нарушение сна, аппетита, тошнота, рвота, светобоязнь, боль в мышцах и суставах) у детей различных возрастных групп с различной давностью рецидивирования различны. Нами выявлено, что у 100% детей старшей возрастной группы, у детей с частыми рецидивами характерна неяркая выраженность местных проявлений и отсутствие общей симптоматики (рис. 3.). Поэтому критерием определения тяжести течения РГС, рецидивирующего герпеса губ должна быть частота рецидивов.
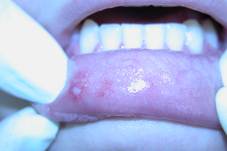
Рис. 3. Клиника тяжелой формы РГС.
Дифференциальная диагностика герпетического стоматита проводилась с герпангиной, многоформной экссудативной эритемой, рецидивирующим афтозным стоматитом.
Герпангина (Коксаки вирусный стоматит). Этиология: вирус Коксаки, ECHO. Высыпания только в области мягкого неба, на передних небных дужках, миндалинах (рис. 4). Нет высыпаний на кожных покровах, красной кайме губ. Отсутствует гингивит, нет гиперсаливации.
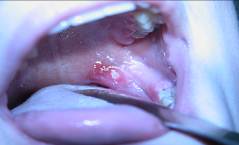
Рис. 4. Герпангина.
Многоформная экссудативная эритема (МЭЭ). Этиология: токсико-аллергическая форма или инфекционно-аллергическая. На слизистой наблюдался истинный полиморфизм элементов поражения: эритема, пузырьки, пузыри, эрозии (рис. 5). На губах - массивные кровяные корки. На коже (чаще кисти рук) у 32% детей - синюшно-красные папулы с западением (или пузырьком) в центре (кокарды), иногда одиночные вялые пузыри (рис. 6). Заболевание встречалось у детей старше 10 лет.
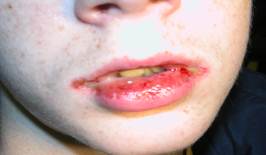
Рис. 5. МЭЭ.
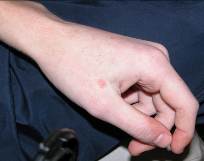
Рис. 6. МЭЭ, папулы (кокарды).
Рецидивирующий афтозный стоматит (РАС). Этиология неизвестна. Предполагаются сдвиги и заболевания в системе желудочно-кишечного тракта, пищевая аллергия, болезнь Бехчета. Характерный элемент поражения - афта - в виде поверхностного некроза эпителия овальной формы с четкими краями, диаметром 3-12 мм и более, окруженная венчиком гиперемии, имеет тенденцию к увеличению размера. У 80% больных на слизистой оболочке наблюдались одиночные элементы или несколько разбросанных (не сгруппированных), размером менее 1 см, заживающие через 10-14 суток без образования рубцов (рис. 7, 8). У 10% больных диаметр афт превышал 1 см, и они заживали с образованием рубцов (рис. 9). У 10% пациентов наблюдались множественные мелкие высыпания, отдельные из которых увеличивались в размере и рубцевались.
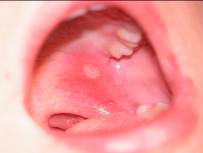
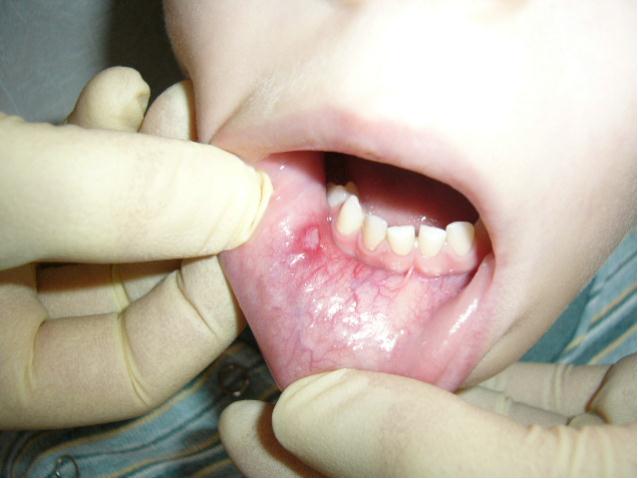
Рис. 7. РАС. Рис. 8. РАС.
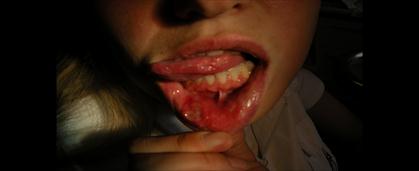
Рис. 9. РАС. Рубцующиеся афты на слизистой оболочке губ, языка.
Рецензенты:
- Фомичев Е.В., д.м.н., профессор, зав. кафедрой хирургической стоматологии и челюстно-лицевой хирургии, Волгоградский государственный медицинский университет, г. Волгоград.
- Поройский С.В., к.м.н., доцент, декан стоматологического факультета, Волгоградский государственный медицинский университет, г. Волгоград.
| >" onclick="checkLength('search_input_doc', 'SearchInDoc($(\'#search_input_doc\').val(), \'bottom\');', 150); return false;" /> | ||||
| Сочетанное применение Лейкинферона с Полиоксидонием при лечении рецидивирующего герпетического стоматита (Рабинович О. Ф., д. м. н., профессор, Рабинович И. М., д. м. н., ст. н.с., Разживина Н. В., аспирант Отделение заболеваний слизистых оболочек рта, ЦНИИ стоматологии, г. Москва) |
Для покупки документа sms доступом необходимо ознакомиться с условиями обслуживания
 | ВНИМАНИЕ! Услуга для абонентов NEO, Tele2 временно недоступна |
 | ВНИМАНИЕ! Услуга для абонентов Beeline, NEO, Tele2 временно недоступна |
Стоимость услуги - тенге с учетом комиссии.
Сочетанное применение Лейкинферона с Полиоксидонием при лечении рецидивирующего герпетического стоматита
Рабинович О. Ф., д. м. н., профессор, Рабинович И. М., д. м. н.,
ст. н.с., Разживина Н. В., аспирант
Отделение заболеваний слизистых оболочек рта, ЦНИИ стоматологии, г. Москва
Многочисленные исследования свидетельствуют о возникновении у больных с герпетическими поражениями вторичной иммунной недостаточности, которая чаще всего обусловлена снижением количества или функциональной несостоятельности клеток, либо дисбалансом компонентов систем иммунореактивности.
Поэтому целью нашего исследования является повышение эффективности комплексного лечения рецидивирующего герпеса слизистой оболочки рта с применением нового отечественного иммуномодулятора Полиоксидония.
Материалы и методы исследования
Под наблюдением находились 60 человек, страдающих РГС (25 мужчин и 35 женщин) в возрасте от 18 до 50 лет, продолжительность заболевания варьировала от полугода до 10 лет. С легкой степенью тяжести было 15 человек, со средней степенью тяжести - 25, с тяжелой степенью тяжести -20. Контрольная группа составила 15 пациентов. У всех больных исследовали иммунный статус по методологии, принятой в ГНЦИ иммунологии.
Наиболее подробно все методические подходы описаны P.M. Хаитовым и соавт., а также Б.В. Пинегиным с соавт.
Результаты и их обсуждение
Согласно существующим классификациям, основывающимся на клинико-морфологических признаках РГС, подразделяется на три степени тяжести: легкую, среднюю и тяжелую. Все больные соответственно клиническим проявлениям были распределены на соответствующие группы. При легкой степени тяжести (рис. 1) общее состояние больных характеризовалось отсутствием признаков интоксикации. При осмотре слизистой оболочки рта отмечалось: незначительная гиперемия, на фоне которой имелись герпетические высыпания с серозным содержимым: на слизистой оболочке десневого края, губ, кончике языка имелись единичные мелкоточечные эрозии полигональной формы, покрытые фибринозным налетом, незначительно болезненные при пальпации.
Легкая степень тяжести - герпетические элементы поражения с локализацией на губах и приротовой области
При средней степени тяжести (рис. 2) больные отмечали недомогание, слабость, незначительное повышение температуры тела (до 37,5°С). Клиническая картина на слизистой оболочке рта характеризовалась разлитой гиперемией, на фоне которой имеются полигональной формы эрозии, иногда сливающиеся между собой, болезненные при пальпации. Чаще патологические элементы локализовались на боковых поверхностях языка, дне полости рта, слизистой оболочке твердого неба.





Владельцы патента RU 2709842:
Изобретение относится к медицине, а именно к вирусологии, и стоматологии, и экспериментальной фармакологии, и может быть использовано для моделирования экспериментального рецидивирующего герпетического стоматита. Осуществляют дозированное введение мышам вируса простого герпеса 1 типа (ВПГ-1). Предварительно экспериментальным животным вводят 0,2 мл гидрокортизона за 2 часа до инфицирования. Затем герпесвирусную суспензию вводят внутрибрюшинно двукратно в течение 3-х недель в дозе 1LD50. Через 21 день после первичного заражения проводят повторное инфицирование мышей путем скарифицирования слизистой полости рта и внесения на поврежденную слизистую 30 мкл суспензии ВПГ-1 в дозе 1 LD50. Способ обеспечивает повышение воспроизводимости и приближение модели экспериментального рецидивирующего герпетического стоматита к клиническому течению данной патологии у человека за счет дозированного введения лабораторным мышам в течение заданного времени суспензии ВПГ-1, осуществляемого на фоне иммунодепрессии, вызываемой введением гидрокортизона. 3 табл., 3 пр.
Изобретение относится к медицине, а именно к вирусологии, стоматологии и экспериментальной фармакологии, и направлено на моделирование экспериментального рецидивирующего поражения слизистой оболочки полости рта лабораторных мышей в виде вирус-индуцированного стоматита. Может быть использовано для испытания эффективности новых противовирусных и иммуномодулирующих средств лечения герпетических стоматитов.
В настоящее время герпетическая инфекция остается наиболее распространенной и плохо контролируемой. Заболевания, обусловленные вирусом простого герпеса (ВПГ) как причина летального исхода занимают среди инфекционных заболеваний детей младшего возраста второе место (15,8%) после гриппа (35,8%) [1. Рабинович, И.М. Рецидивирующий герпетический стоматит / И.М. Рабинович, О.Ф. Рабинович, М.В. Разживина. - М.: ГЭОТАР-Медиа, 2005. - С. 64. Левончук, Е.А. Герпетическая инфекция полости рта / Е.А. Левончук // Современная стоматология. - 2005. - №1. - С. 19-22
Существующие средства и схемы терапии герпетического рецидивирующего стоматита не всегда оказываются достаточно эффективными и характеризуются большим количеством противопоказаний и побочных эффектов. Одной из возможных причин подобного состояния дел - отсутствие адекватных экспериментальных моделей рецидивирующего герпетического стоматита.
Отсутствие действенных вакцин и невозможность полного излечения в совокупности с практически 100% охватом популяции инфекцией определяют актуальность изучения герпесвирусной инфекции. Современные медико-биологические исследования заболеваний невозможно представить без применения экспериментального моделирования патологии. В качестве моделей используют как животных, так и культуры клеток - клетки различных типов, выделенных из организма и поддерживаемые в жизнеспособном состоянии в искусственных условиях.
Выбор подходящей модели для изучения инфекционного заболевания in vivo важен для адекватной экстраполяции полученных данных на процессы, протекающие в живом организме. В ряде случаев их использование не имеет альтернатив, например, при проведении доклинических исследований терапевических препаратов. Роль герпесвирусной инфекции (вируса простого герпеса 1 и 2 типов) как этиологического фактора в развитии рецидивирующего стоматита общепризнана. Однако при моделировании хронического рецидивирующего стоматита, согласно данным литературы, возникает необходимость усиливать повреждающее действие слизистой оболочки полости рта (СОПР) вирусами простого герпеса (ВПГ-1 и ВПГ-2) с помощью других иммунодепрессантов.
Существующие средства и схемы терапии рецидивирующего герпетического стоматита не всегда оказываются эффективными и характеризуются большим количеством противопоказаний и побочных эффектов. Одной из возможных причин подобного состояния дел - отсутствие адекватных экспериментальных моделей герпетических стоматитов. Наиболее близким по совокупности существенных признаков к заявляемому изобретению является способ создания модели хронической рецидивирующей герпетической инфекции у млекопитающих [Порываева А.П. Теоретические и практические аспекты моделирования хронической герпесвирусной инфекции, доктор. Дис. 03.02.02 - Вирусология 2015, 191 с.]
Недостатком данного способа моделирования является тот факт, что для оценки выраженности клинических проявлений обострений хронического герпетического стоматита необходимо наблюдение за зараженными вирусом простого герпеса (ВПГ-1) мышами не менее 320 сут. В предлагаемом нами способе время исследования можно сократить до 50-60 сут.
Наиболее близким по технической сущности к предлагаемому изобретению является [Способ получения состава для моделирования афтозного стоматита у животных Чемикосова Т.С. и соавт.; патент №2104588, G09B 23/28, опубл. 10.02.1998].
Недостатком данного способа является то, что при формировании афтозного стоматита не учитывается герпесвирусная составляющая патологического процесса.
В связи с этим задачей предлагаемого изобретения является разработка адекватной и информативной экспериментальной модели рецидивирующего герпес-индуцированного стоматита.
Техническим результатом предлагаемого нами изобретения является повышение воспроизводимости и приближение модели экспериментального рецидивирующего герпетического стоматита к клиническому течению данной патологии у человека.
Технический результат достигается тем, что в способе моделирования экспериментального рецидивирующего стоматита, включающем дозированное введение лабораторным мышам в течение заданного времени суспензии вируса простого герпеса 1 типа, осуществляют на фоне иммунодепрессии, вызываемой введением 0,2 мл гидрокортизона, вводимого экспериментальным животным за 2 часа до инфицирования, затем герпесвирусную суспензию вводят внутрибрюшинно двукратно в течение 3-х недель в дозе 1LD50, через 21 день после первичного заражения проводят повторное инфицирование мышей путем скарифицирования слизистой полости рта и внесения на поврежденную слизистую 30 мкл суспензии ВПГ-1 в дозе 1 LD50
Заявляемый способ обладает новизной в сравнении с прототипами, отличаясь от них таким существенным признаком как использование в модельных исследованиях вышеперечисленных патента - прототипа афтозной смеси, которую вводят интактным животным с целью активации аутоиммунных процессов с последующим образованием афт. При этом следует отметить, что полностью исключается основой этиологический фактор герпесвирусного рецидивирующего стоматита - герпесвирусная инфекция.
Заявляемый способ реализуют следующим образом:
Способ моделирования экспериментального рецидивирующего герпетического стоматита, включающий дозированное применение суспензии вируса простого герпеса (ВПГ-1, штамм УС). Предварительно обеспечивают иммунодепрессию, вызываемую гидрокортизоном, вводимым экспериментальным животным за 2 часа до инфицирования. Суспензию вируса вводят мышам в течение заданного времени внутрибрюшинно в дозе 1ЛД50, через 21 день после развития герпетической инфекции, не погибшим животным повторно в рану поврежденной скарификатором слизистой оболочки полости рта вносят 30 мкл суспензии ВПГ-1 в вышеназванной дозе, вызывающей развитие герпетического рецидивирующего стоматита на 6-7 сут.
Проведенные исследования иллюстрируются следующими примерами.
Для определения кратности и дозы введения суспензии вируса простого герпеса первого типа (ВПГ-1) при моделировании хронического герпетического рецидивирующего стоматита был проведен эксперимент на мелких лабораторных животных, а именно на белых беспородных мышах-самцах массой 16-18 г. Животных содержали в стандартных условиях вивария на обычном пищевом рационе, со свободным доступом к воде.
Моделирование герпетической инфекции осуществляли путем внутрибрюшинного введения животным суспензии ВПГ 1 типа или ВГП 2 типа в объеме 0,5 мл. За 2 ч перед заражением животным в целях понижения естественной резистентности внутримышечно вводили 0,2 мл гидрокортизона. Численность опытных и контрольных групп составляла по 30 мышей в каждой.
Статистический анализ результатов исследования. Определение значимости различий показателей между сравниваемыми выборками проводили с использованием параметрического критерия t-Стьюдента. Различия в сравниваемых группах считались достоверными при уровне значимости 95% (р # р Изобретение относится к медицине, а именно к экспериментальной онкологии, и касается способа ортотопической трансплантации фрагмента опухоли пищевода человека иммунодефицитным мышам для получения опухолевых моделей, более точно отражающих молекулярные, генетические и морфологические особенности развития рака пищевода человека.
Читайте также:
- У кого вич он может болеть гриппом
- Тема урока что такое вич
- Плановая операция нет анализа на вич
- Можно ли заразиться вич если прокипятить шприц
- Как болит голова при вич на начальной стадии
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции

