Правда ли что нашли вакцину от вич
1 декабря – Всемирный день борьбы со СПИДом. Каждый год к этой дате внимание учёных и людей всего мира обращается к новым достижениям в исследованиях ВИЧ.
Когда было установлено, что причиной СПИДа является вирус иммунодефицита человека (ВИЧ), казалось, что создание вакцины – дело ближайшего будущего. C тех пор прошло более 25 лет и, несмотря на огромные материальные и интеллектуальные ресурсы, затраченные за это время, вакцина против ВИЧ-инфекции все ещё не создана.
Создание вакцин – история
Чтобы понять проблемы, осложняющие разработку вакцин против ВИЧ-1, поучительно рассмотреть обстоятельства успешной разработки вакцин в прошлом. Создание вакцины против оспы – одно из наиболее ярких достижений в истории медицины. Почему 200 лет назад, в отсутствии современных знаний, создание вакцины против оспы так быстро увенчалось успехом, в то время как создание вакцины против СПИДа остается нерешённой задачей уже более четверти века? Ответ заключается в том, что сама природа дала проницательному наблюдателю чёткие указания. Эдвард Дженнер обратил внимание на то, что молочницы, ранее переболевшие коровьей оспой, не заболевали оспой натуральной. Это наблюдение позволило установить факт перекрёстной иммунологической реакции двух родственных вирусов, позволяющий использовать вирус коровьей оспы для защиты от оспы натуральной.
Известные подходы
Для создания вакцин против ВИЧ были испробованы практически все известные подходы, однако все они оказались бесперспективны.
Использование аттенуированного или инактивированного вируса связано с опасностью инфицирования, иммунитет ограничен очень узким кругом вирусных изолятов, а продолжительность иммунитета достаточна мала и не генерируется ЦТЛ.
Использование полноразмерных вирусных антигенов для создания рекомбинантных вакцин также осложнено: во-первых, требуется использование большого числа рекомбинантных антигенов ВИЧ-1, многие из которых достаточно сложно получить с использованием генноинженерных систем их синтеза; во-вторых, ВИЧ-1 имеет множество изменённых штаммовых вариантов, что также делает малоэффективным использование полноразмерных антигенов, в-третьих, полноразмерные вирусные антигены, являются потенциальными онкогенами и содержат районы, которые могут либо ингибировать протективный иммунитет, либо индуцируют развитие иммунопатологии.
Все эти проблемы ограничивают возможность использования традиционных подходов для создания вакцин против ВИЧ-1 и требуют разработки новых нетрадиционных подходов.
Новое поколение вакцин
На наш взгляд, одним из наиболее перспективных и обещающих подходов к созданию нового поколения надёжных и безопасных вакцин против ВИЧ-1 связан с созданием искусственных полиэпитопных вакцин на основе специально отобранных В- и Т-клеточных эпитопов. Такие вакцины должны содержать только те эпитопы, которые необходимы для формирования специфического иммунитета, и должны быть лишены недостатков, которые присущи субъединичным вакцинам и вакцинам, разрабатываемым на основе аттенуированного или инактивированного вируса. Искусственные полиэпитопные конструкции имеют потенциал, который позволяет улучшить иммунный ответ против ВИЧ-1 по сравнению с иммунитетом, индуцируемым при естественной ВИЧ-инфекции.
Как получают искусственные полиэпитопные иммуногены?
Вначале проводится анализ структуры вирусных белков и отбираются наиболее важные в иммунологическом плане эпитопы. При этом отбрасываются те эпитопы, которые могут вызвать нежелательные последствия. Затем осуществляется компьютерный дизайн искусственной белковой молекулы и рассчитывается соответствующая нуклеотидная последовательность искусственного гена. Ген синтезируют в пробирке путём химико-ферментативного синтеза и встраивают в подходящую векторную молекулу для его экспрессии в клетках бактерий, животных или растений. Данный подход использовался нами при конструировании двух искусственных полиэпитопных конструкций TBI и TCI.
Искусственные иммуногены - TBI и TCI
Первый полученный нами искусственный иммуноген был белок TBI. Он включает четыре Т-клеточных эпитопа и пять В-клеточных нейтрализующих эпитопов и сконструирован в виде белка с заранее заданной третичной структурой. Белок TBI прежде всего проектировался для индукции В-клеточного ответа, поэтому предсказанная структура эпитопов в составе белковой молекулы должна была обеспечить их распознавание иммунной системой и высокий уровень ответа. И действительно, созданный нами искусственный белок сохранил иммунологическую активность, поскольку его узнавали антитела из сыворотки больных ВИЧ-1. Кроме того, впервые для белка с гипотетически заданной третичной структурой были выращены кристаллы. Поскольку известно, что только природные белки способны к кристаллизации, этот факт является подтверждением того, что белок TBI по своей структуре подобен природным белкам. И самое главное – у мышей и обезьян, иммунизированных белком TBI, регистрируется появление ВИЧ-специфических антител, обладающих способностью нейтрализовать ВИЧ-1 на культуре клеток человека.
При конструировании белка TCI были выбраны эпитопы, высоко консервативные для 3-х основных субтипов ВИЧ-1, что может позволить обойти высокую вариабильность вируса. Чтобы выбранные эпитопы не обладали способностью индуцировать аутоиммунные реакции, были исключены нежелательные эпитопы, которые потенциально могут индуцировать антитела, обладающие перекрёстной специфичностью с нормальными клеточными белками. В результате белок TCI имеет более 80 оптимально отобранных эпитопов и является самым представительным среди известных полиэпитопных конструкций.
Кандидатные вакцины
КомбиВИЧвак представляет собой комбинацию двух искусственных иммуногенов, один из которых - белок TBI. Вакцина сконструирована в виде вирусоподобных частиц. На её поверхности расположено большое число молекул TBI, что позволяет значительно увеличить иммуногенность вакцинной конструкции. Один из основных показателей эффективности вакцины – способность индуцировать антитела, которые не только узнают, но и нейтрализуют вирус. Наши результаты показали, что сыворотки мышей, иммунизированных КомбиВИЧвак, эффективно подавляют репликацию вируса на культуре клеток, инфицированных вирусом ВИЧ-1, причём на том же уровне, что и сыворотки, полученные от ВИЧ-инфицированного человека. Т.о., кандидатная вакцина КомбиВИЧвак обладает рядом уникальных свойств: она объединяет В- и Т-клеточные иммуногены в одной конструкции, индуцирует как гуморальный, так и клеточный иммунный ответ, а эпитопы, входящие в состав её полиэпитопных иммуногенов, являются консервативными и представлены разными белками ВИЧ-1.
Лариса Ивановна Карпенко,
д.б.н., зав. лабораторией разработки средств иммунопрофилактики
Сергей Иванович Бажан,
д.б.н., зав. теоретическим отделом,
Александр Алексеевич Ильичёв,
д.б.н., профессор, зав. отделом иммунотерапевтических препаратов

Что покажет экспресс-тест?
Руслана Шешина: Исследования по разработке вакцины, конечно, ведутся. Но пока сложно говорить, что в ближайшее время появится прививка, помогающая защититься от ВИЧ. Вирус постоянно мутирует, появляются новые штаммы.
Но на стадии разработки и, скорее всего, лет через пять, а может, и раньше, появится инъекция, которую заразившимся ВИЧ нужно будет ставить один раз в день. Дело в том, что сейчас терапия достаточно сложная. Чтобы держать вирус под контролем, те, у кого он обнаружен, должны по несколько раз в день принимать таблетки.
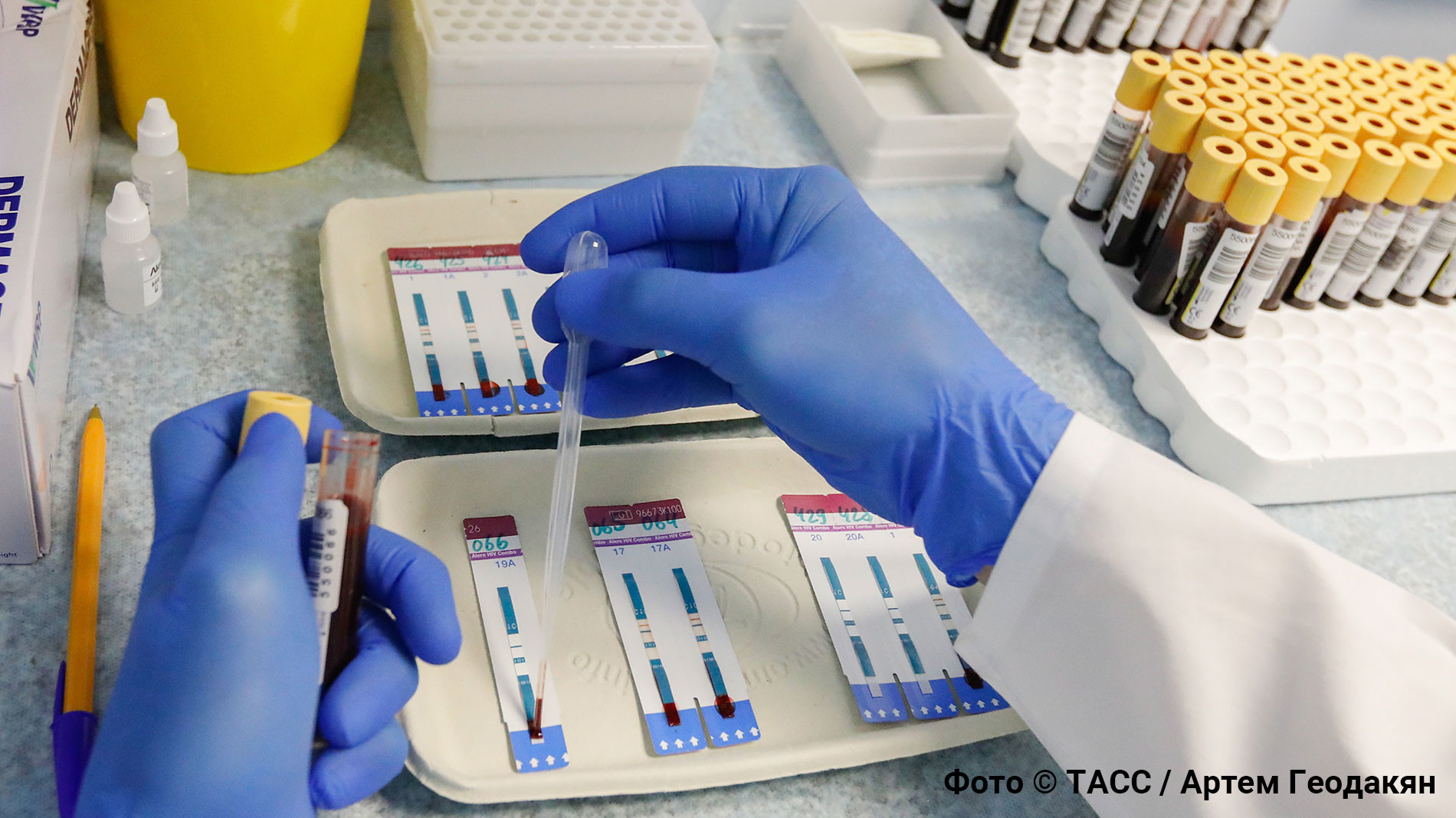
- Сейчас часто в общественных местах предлагают пройти экспресс-тест на ВИЧ. Насколько он достоверен?
- Действительно, такие экспресс-тесты мы всё чаще проводим на улице, на вокзалах, в местах большого скопления людей, разных по возрасту и социальному статусу. Это такой скрининг. Если он показывает отрицательный результат, то вируса в крови ещё три месяца назад (это такое окно, в течение которого может проявиться ВИЧ) точно не было. Если результат положительный, то мы сразу диагноз не ставим. Назначаются дополнительные лабораторные анализы. Дело в том, что плюс экспресс-тест может показать и при наличии некоторых хронических заболеваний - например, при гепатите, болезни почек.
Хочу сказать, что почти ни одна наша акция в общественных местах не прошла без того, чтобы мы не выявили ВИЧ-положительного. Как правило, потом в лабораторных условиях этот статус тоже подтверждался. Дело в том, что именно во время таких мероприятий приходят проверяться те, кто подозревал у себя наличие вируса.
Можно ли заболеть из-за маникюра?
- Как часто нужно проверяться на ВИЧ?
- Регулярно проверяться нужно тем, кто ведёт определённый образ жизни, то есть находится в группе риска: имеет беспорядочные половые контакты или принимает наркотики. Им нужно сдавать анализы раз в три месяца.
- Можно ли заразиться ВИЧ в салоне красоты, если делаешь педикюр или маникюр? Или в больнице при операции?

Также мы не скрываем, что 1% всех заражений ВИЧ носит медицинский характер. И даже при том, что с каждым годом прогресс идёт вперёд, в больницах используются самые передовые методики, кратность таких случаев увеличивается. Мы это связываем с тем, что общее количество людей с вирусом растёт.
Но всё-таки чаще всего ВИЧ заражаются при половых контактах - это 70% всех случаев. Немного меньше стали регистрировать заболевших среди наркоманов. Связываем это с тем, что сейчас больше распространены синтетические наркотики, которые не требуют инъекций.
Как жить с ВИЧ?
- Могут ли у ВИЧ-инфицированных рождаться здоровые дети?
- Мы исходим из той позиции, что у всех ВИЧ-положительных должны рождаться здоровые дети. Поэтому и назначаются необходимое обследование во время беременности. Не зря ведь не только будущие мамы, но и папы три раза до рождения ребёнка сдают анализы. А те, кто до беременности знает о вирусе, заранее её планируют. При правильной терапии вирус в организме практически блокируется и становится не опасен для других.
Также мамам с ВИЧ ребёнка грудью вскармливать не рекомендуем.

- Правда ли, что сегодня человек с ВИЧ при правильном лечении живёт долго и качественно?
- Это так. Если человек соблюдает назначенное лечение, его иммунная система сохраняется, и он практически не опасен для окружающих. Конечно, в его жизни есть некий дискомфорт, который связан с необходимостью постоянно принимать препараты. На начальных этапах может быть сложное привыкание. Бывает и головокружение, и тошнота. Но медицина не стоит на месте - препараты усовершенствуются.
Сложнее обстоит дело с теми, кто долго не знал о том, что заразился ВИЧ (долгое время вирус может никак не проявляться), когда иммунная система практически разрушилась. Если у человека уже СПИД, прогноз плохой. Но и здесь процессы бывают обратимы. Главное, получать грамотное лечение.


- На протяжении последних 40 лет мы пытаемся найти радикальное средство против вируса иммунодефицита человека. Приблизиться к этому удалось только сейчас благодаря технологиям генетического редактирования, - говорит заместитель директора Центра стратегического планирования Минздрава России Герман Шипулин. - ВИЧ встраивается в геном человека. А наша задача сегодня - "вырезать" его оттуда, "сломать" этот порочный механизм.
Почему это так важно? Недавно ВОЗ в очередной раз включил ВИЧ в список десяти самых опасных угроз для населения планеты. Только по официальной статистике, в мире инфицировано около 60 миллионов человек. Но эксперты говорят, что эту цифру можно смело умножать на два, - вот реальная картина заболевания. В год умирает около миллиона, заражается - почти вдвое больше. Многие вынуждены всю жизнь принимать препараты - "подавители" ВИЧ.


Проблема еще и в том, что они подавляют вирус не полностью - заблокировать его на 100 процентов с помощью традиционной "химии" невозможно. К тому же, в мире растет устойчивость к противовирусным препаратам. И та заместительная терапия, которая сегодня помогает продержаться, через 10 лет может быть уже не так эффективна.
Выход? Кто-то пошел по радикальному пути. Например, не так давно китайский ученый Цзянькуй Хэ объявил на весь мир о рождении генетически модифицированных детей - близнецов Лулу и Нану. Одна из девочек получила врожденный иммунитет к ВИЧ. Правда, этот эксперимент уже осудило мировое научное сообщество. "Редактирование" эмбрионов даже с благими целями признано неэтичным. Ведь никто не знает, как это отразится на потомках - а искусственно измененный геном выросшие близнецы передадут своим детям, внукам, правнукам…
Другое дело - вмешательство в ДНК уже взрослого человека: эти изменения он по-наследству не передаст. Здесь по всему миру ведутся сотни разработок: в Германии, США, Японии, России…
В чем "фишка" технологии? Если совсем просто, то ВИЧ попадает в клетку человека через две "двери" (рецепторы CCR5 и CXCR4). И если первую "дверь" с помощью специального молекулярного лекарства закрыть можно, то вторую - ни в коем случае нельзя - она играет важнейшую роль в жизни клетки. Что делать? Можно поместить внутрь нее специальный белок, который "ловит" вирус и разрушает его. Но этот метод не дает 100-процентной гарантии: позволяет "отловить" только 70-80 процентов "нарушителей".


И третий метод - самый новый и перспективный - установить на "входе" в клетку "сторожевой" пептид, который будет встраиваться в мембрану, и мешать слиянию вируса.
И если объединить все три механизма (закрыть вирусу одну из "дверей" в клетку, у второй "двери" поставить "сторожа", а внутри - специальный белок-"разрушитель"), вот тогда можно будет говорить почти о 100-процентном излечении и защите.
- Последние испытания, которые были проведены за рубежом и в нашей стране, говорят о том, что тройной механизм позволяет снизить вероятность закрепления ВИЧ в клетке человека практически до нуля, - говорит Герман Шипулин. - Это реальная перспектива именно для радикальной терапии вируса. То, о чем мы мечтаем на протяжении 40 последних лет.
Как лечение может выглядеть на практике? У человека берутся стволовые клетки: они сначала инфицируются, а потом "лечатся" генетическим препаратом прямо в пробирке, приобретая нужные терапевтические свойства. Затем эти клетки вводятся в спинной мозг человека, и начинают там размножаться, постепенно излечивая организм.
В конце февраля правительство должно утвердить Научно-техническую программу развития генетических технологий в России в 2019-2027 годах, которая сейчас разрабатывается по поручению президента. В ней отдельной строкой прописана цель - разработка генетических редакторов для борьбы с ВИЧ.
Подробный проект программы на всероссийской конференции "Путь к успеху" в сочинском центре для одаренных детей "Сириус" представил Курчатовский институт. По всей стране планируется создать около 60 геномных лабораторий. Крупных направлений работы - четыре: агроиндустрия, промышленная микробиология, биобезопасность и биомедицина. Последнее - одно из самых перспективных динамично развивающихся во всем мире: здесь больше всего разработок, больше патентов.
Например, с помощью генетического редактирования ученые пытаются лечить не только ВИЧ, но и рак. В Евросоюзе и Китае идут клинические испытания на людях иммунного препарата, который позволит организму бороться с меланомой. Некоторые клеточные препараты позволяют достичь ремиссии, к примеру, у детей с острым клеточным лейкозом, для которых не эффективны все другие методы лечения. Гемофилия, спинально-мышечная атрофия, возрастная деградация клетчатки - против всех этих заболеваний уже разработаны "генетические" препараты.
- Цель программы - разработка технологии генетического редактирования, препаратов, диагностических систем для здравоохранения, сельского хозяйства, промышленных биотехнологий, а также предупреждения чрезвычайных ситуаций биологического характера. Программа рассчитана на 9 лет, - рассказал директор Института молекулярной биологии имени В.А. Энгельгардта РАН Александр Макаров. - Что мы хотели бы сделать в этой программе. Это клеточная терапия для человека, предотвращение инфекций, гуманизированые органы, лечение наследственных болезней, безопасность и мониторинг, микроорганизмы для биотехнологий, растения и животные с улучшенными признаками.
Синтезирование этого препарата позволит избавить людей от самой страшной неизлечимой болезни. В последние несколько лет учёные начали экспериментировать с лечением ВИЧ у людей, но эффективного лекарства по-прежнему нет.
Почему это сложно?
В марте 2019 года учёные сообщили о третьем случае излечения ВИЧ. Все новостные агентства тогда пестрили заголовками о том, что после десятилетий поисков и разработки вакцины страшная инфекция наконец-то побеждена. На самом деле медикам удалось добиться лишь частичной победы над недугом с помощью повторения пересадки костного мозга от пациента с мутацией в гене CCR5. К большому сожалению, даже многие специалисты истолковали этот успех неправильно.
К массовой терапии такое лечение не имеет и не могло иметь никакого отношения. Сама по себе пересадка костного мозга — крайне дорогая операция, да и никакого избавления от ВИЧ нет: организм действительно начинает вырабатывать антитела к вирусу, но однажды попавшую в организм инфекцию нельзя убить даже с помощью дорогой операции по пересадке костного мозга.
В 2018 году руководитель Федерального научно-методического центра по борьбе и профилактике ВИЧ-инфекции ЦНИИ эпидемиологии Роспотребнадзора академик РАН Вадим Покровский отметил, что небольшая часть населения Северной Европы и России невосприимчива к заражению ВИЧ. Сейчас учёные работают над тем, чтобы научиться переносить эту невосприимчивость от одного человека к другому и искусственно создавать супериммунитет. Однако до готового к применению лекарственного препарата пройдёт ещё немало времени.
Достижение, которого нет

Китайский учёный Цзянькуй Хэ приблизился к разгадке ВИЧ ближе всех, он работал над решением проблемы много лет. Правда, и его успех (в очередной раз) приняли за достижение, которого на самом деле пока нет. Напомним, в 2018 году Цзянькуй Хэ шокировал научный мир своим рассказом о том, что редактирование генома в эмбрионах позволило наделить будущих детей устойчивостью к страшному вирусу. С помощью генетических "ножниц" — технологии CRISPR — Хэ смог удалить "брешь" в организме человека, с помощью которой вирус проникал внутрь.
И хотя рождение полностью здоровых детей от здоровой матери и заражённого вирусом отца, на первый взгляд, прошло нормально, до сих пор уникальных ГМО-близняшек так и не показали миру. И нет никакой уверенности в том, что Цзянькуй Хэ не сфальсифицировал собственные исследования. Кроме того, беспокойство учёных вызвал и другой факт — метод китайского генетика касался зародышей человека, но никакой пользы для уже инфицированных ВИЧ людей такие исследования не принесли.
Не столько лечит, сколько наоборот
Для здоровых людей проку от таких достижений практически нет, а вот вред организму нанести можно запросто. Американские генетики выяснили, что достижения китайского учёного не только не продлят жизнь трансгенным детям, но и существенно укоротят её. Исследователи пришли к выводу, что мутация в гене CCR5, дающая человеку иммунитет к вирусу, оказалась опасной для носителей. Пока организм молод и способен "обновлять" иммунную систему, никаких проблем нет. Сложности, как отмечают учёные, начнутся в преклонном возрасте — мутация гена, согласно исследованиям, увеличивает риск преждевременной смерти более чем на двадцать процентов.
В связи с этим учёные отмечают, что использование таких инструментов, как CRISPR, не только небезопасно, но и может противоречить принципам медицины и науки как таковым. По словам американских генетиков, "генетические ножницы" — настолько несовершенный инструмент для редактирования ДНК, что любое вмешательство в геном неизбежно будет сопровождаться тяжёлыми болезнями. И предсказать такое развитие событий учёные не могут просто потому, что. сама технология CRISPR так и не изучена до конца. Если говорить простым языком, то вся современная генетика на этом уровне работает по принципу "может, сработает, а может, и нет".
Несмотря на десятилетия исследований, ВИЧ по-прежнему остаётся малоизученной болезнью. После того как в начале 80-х вирус был классифицирован и зарегистрирован, стала известна его генная и клеточная структура, однако никакого эффективного лечения за (почти) 40 лет исследований придумать не удалось. Единственное, что предлагает современная медицина, — это антиретровирусная терапия, с помощью которой удаётся подавлять активность вируса. Однако полностью удалить инфекцию из организма при таком лечении всё равно нельзя. И хотя пациенты с ВИЧ могут спокойно прожить до ста лет, учёные по-прежнему упираются в "потолок знаний", который не позволяет установить природу этого заболевания и лишает учёных возможности создать эффективное лекарство.
Спасение человечества: ученые нашли средство от ВИЧ
Американские ученые вылечили мышей от ВИЧ с помощью геномного редактирования. В течение года они планируют приступить к экспериментам на людях.
Исследователи из Медицинского центра Университета Небраски и Университета Темпл в США смогли полностью вылечить мышей от ВИЧ-инфекции с помощью комбинации антиретровирусной терапии и редактирования генома. Ученые планируют в течение года улучшить результаты и приступить к экспериментам на людях. Работа была опубликована в журнале Nature Communications.
С 1980-х годов СПИД унес жизни около 35 млн человек. Носителями ВИЧ сегодня являются 37 млн. Научные исследования позволили создать препараты, способные держать болезнь под контролем, но лекарства, которое избавит пациента от вируса раз и навсегда, пока нет.
В настоящее время для борьбы с ВИЧ используется антиретровирусная терапия. Препараты подавляют репликацию вируса, но не позволяют полностью вывести его из организма. АРВТ приходится проводить пожизненно. Несмотря на то, что благодаря терапии люди с ВИЧ живут столько же, сколько и люди без вируса, АРВТ чревата побочными эффектами и требует строгого соблюдения режима приема.
Вирус иммунодефицита человека поражает клетки иммунной системы, имеющие на своей поверхности рецепторы CD4, а также Т-лимфоциты. ВИЧ вторгается в здоровые клетки и изменяет их таким образом, что они перестают бороться с заболеванием и начинают поставлять вирусу питательные вещества, необходимые для его дальнейшего размножения.
Ученые предположили, что от вируса можно избавиться с помощью технологии редактирования генома CRISPR-Cas9.
Они разработали двухступенчатую методику борьбы с ВИЧ у семи мышей, которым пересадили стволовые клетки крови человека и заразили их вирусом.
Первым этапом стало использование на протяжении месяца антиретровирусных препаратов в микроскопических жировых пузырьках, с помощью которых удалось доставлять лекарство прямо в клетки. Когда количество копий вируса упало до минимума, ученые применили CRISPR-Cas9, вырезав ДНК ВИЧ из генома клеток.
Попытки использовать CRISPR-Cas9 без АРВТ не увенчались успехом — Т-лимфоциты гибли в той же мере, что и в не получавшей лечения контрольной группе из шести грызунов, вирусная нагрузка тоже не снижалась.
Полностью избавить от ВИЧ исследователям удалось всего двух мышей — ни в крови, ни в органах следов вируса не было.
При этом также не было и серьезных побочных эффектов.
В ходе повторного эксперимента ученые смогли вылечить трех мышей из шести. Процент выздоровлений пока невелик, но исследователи акцентируют внимание на том, что это лишь начало пути и в перспективе они рассчитывают добиться более значимых результатов.
Пока что, впрочем, неизвестно, даст ли Управление по контролю за продуктами питания и медикаментами США (FDA) разрешение на эксперименты на людях. Однако случаи, когда FDA разрешало использование CRISPR-Cas9 на людях, уже были — метод был одобрен для экспериментального лечения серповидноклеточной анемии и детской слепоты.
Более ранние эксперименты по лечению ВИЧ были связаны с пересадкой стволовых клеток костного мозга. Весной 2019 года стало известно о британце, который полностью избавился от вируса, став вторым в мире человеком, вылечившимся от ВИЧ-инфекции.
Мужчина узнал о своем диагнозе в 2003 году. А в 2012 году у него развилась лимфома Ходжкина — злокачественное заболевание лимфоидной ткани. К 2016 году его состояние было настолько тяжелым, что последним шансом выжить была пересадка стволовых клеток костного мозга.
Донором стал человек с генетической мутацией CCR5 delta 32, дающей устойчивость к ВИЧ.
18 месяцев назад пациент отказался от антиретровирусной терапии. И до сих пор высокочувствительные тесты на ВИЧ не выявляют в его крови никаких следов вируса.
Большинство специалистов, впрочем, считают, что такое лечение нецелесообразно для всех ВИЧ-инфицированных.
Это дорогостоящая, сложная и рискованная процедура, кроме того, подобрать подходящего донора весьма проблематично.
Также ученые не уверены, что дело именно в защищающей от ВИЧ мутации. Они предполагают, что избавлению от вируса могла поспособствовать работа иммунной системы, стремившейся избавиться от трансплантата.

С помощью ступенчатой вакцинации иммунную систему хотят научить вырабатывать редкий тип антител, эффективно нейтрализующих ВИЧ.
По данным Всемирной организации здравоохранения, в 2016 году с ВИЧ во всем мире жили 36,7 миллионов человек, 1,8 миллиона заразилось, а 1 миллион умер от развившегося СПИДа.
К сожалению, случай с Тимоти Брауном остается исключением. У других пациентов полного избавления от вируса не случалось, к тому же замещение зараженной иммунной системы с помощью трансплантации от донора – очень сложная и рискованная процедура.
С ВИЧ также можно бороться методами генной терапии. У инфицированного человека забирают Т-клетки из крови и редактируют их геном: с помощью технологии CRISPR/Cas9 (о которой мы неоднократно писали) удаляют ген того самого рецептора, которого нет у людей с естественной устойчивостью к ВИЧ. Как несложно догадаться, на деле в этом направлении все обстоит гораздо сложнее, чем на словах, и пока что о молекулярно-генетическом лекарстве от ВИЧ говорить рано.
Но, как известно, предотвратить болезнь лучше, чем ее лечить – иными словами, против ВИЧ хорошо бы иметь вакцину. Однако, как и в случае с лекарством, 30 лет поисков вакцины против него не увенчались успехом. При вакцинировании иммунитет должен запомнить характерные молекулярные признаки вируса. Но вирусы легко мутируют, а ВИЧ мутирует особенно быстро – из-за того, что фермент, который он использует для копирования своей генетической информации, допускает много ошибок.
В течение года с момента инфицирования популяция ВИЧ может достичь такого же генетического разнообразия, какого достигает за то же время вирус гриппа в масштабе всего мира. Поэтому новая вакцина от гриппа у нас – каждый год, а вакцины от ВИЧ нету вовсе. По этой же причине организм не в состоянии победить ВИЧ самостоятельно. Иммунная система не поспевает за изменчивостью вируса: пока она изобретает антитела против одних генетических вариантов, уже вовсю плодятся другие, против которых антитела не работают.
Но сравнительно недавно надежда на создание вакцины появилась вновь, когда исследователи открыли особый тип антител – нейтрализующие антитела широкого спектра действия. Они сильно мутированы (изменены) по сравнению с обычными антителами и направлены против консервативных участков вируса (то есть таких, которые слабее всего изменяются от поколения к поколению). В исследованиях последних лет было установлено, что они способны нейтрализовать до 98% всех генетических вариантов ВИЧ. Иммунная система в какой-то момент сама начинает стабильно вырабатывать такие антитела, но этот момент наступает через несколько лет после заражения – слишком поздно.
Сотрудники Института аллергии и иммунологии в Ла-Холья и Института Скриппса разработали стратегию вакцинации, которая учит иммунную систему вырабатывать антитела широкого спектра быстро. Чтобы понять, что именно тут имеется в виду, нужно представлять, как вообще иммунные клетки начинают синтезировать антитела против патогена.
Антитела производят В-лимфоциты. При этом сами они могут взаимодействовать с чужеродными молекулами, в том числе и с вирусными белками. У нас постоянно появляются В-клетки с самыми разными рецепторами для распознавания чужаков, так что для любого вируса обязательно найдутся В-клетки, которые схватят его молекулы. Вирусный материал В-клетки поглощают, преобразуют внутри себя и выставляют наружу на своей поверхности.
Теперь В-клетки, получившие разрешение на борьбу с вирусом, пытаются сделать так, чтобы связывать его как можно точнее и прочнее. Они начинают делиться и при каждом делении мутируют, так что у каждой новой В-клетки рецептор слегка меняется, и клетки с новыми рецепторами опять проходят отбор при взаимодействии с Т-клетками.
Если слегка изменившийся рецептор распознает вирус еще лучше, то В-клетка, у которой он получился, продолжает делиться дальше. И лишь после многих раундов такого естественного отбора В-клетки с наилучшими рецепторами начинают продуцировать антитела (которые по строению идентичны рецепторам).
Роберт Эбботт (Robert K. Abbott) и его коллеги предлагают повлиять как раз на процесс отбора. Они исходят из того, что практически у всех людей в иммунной системе присутствует некое количество В-клеток широкого спектра (ранее исследователи установили, что доля таких клеток равна приблизительно одной клетке на миллион). Тогда цель вакцинации – сделать так, чтобы В-клетки широкого спектра отбирались вместо обычных, которые хоть и отшлифованы идеально под определенные вирусные генетические варианты, но очень быстро устаревают.
Сама вакцинация представляет собой многоступенчатую процедуру, в ходе которой в организм вводят вирусоподобные компоненты постепенно изменяющегося состава. Каждая ступень должна приближать иммунную систему к производству заветного типа антител. По выражению одного из исследователей, все происходящее выглядит так, как если бы В-клетки, умеющие распознавать квадраты, учили распознавать круги, но учили их этому с помощью пятиугольников.
На человеке разработанную стратегию не испытывали, пока что эксперименты ограничиваются мышами, и предварительные результаты можно узнать из статьи в Immunity. Говорить о полноценной вакцине против ВИЧ пока еще очень рано, но, по крайней мере, есть надежда, что ее действительно удастся создать.
Читайте также:




