Первичное заражение герпесом во втором триместре

Герпетическая инфекция – инфекция, вызываемая герпесвирусами 1-го и 2-го типа – хроническое рецидивирующее заболевание, входящее в группу ТОRСН – инфекций, для которого характерно поражение кожи, слизистых, глаз, нервной системы.
Инфекция, вызванная герпесвирусами, распространена повсеместно. Инфицированность населения очень высокая. По данным Всемирной организации здравоохранения (ВОЗ) герпесвирусная инфекция занимает второе место среди вирусных заболеваний человека, уступая лишь гриппу.
Восприимчивость к инфекции всеобщая, независимо от пола и возраста.
Подъемы заболевания регистрируются в осенне-зимний период.
Проведенные за последние 10 лет эпидемиологические исследования показали, что к 15-летнему возрасту инфицировано 80% детей, а к 30 годам 90% населения имеют антитела к вирусам того или иного типа.
Возбудитель инфекции – вирус простого герпеса 1 или 2 типа (ВПГ 1 или ВПГ 2). Попадая в клетку – вирус вызывает ее гибель. В отдельных клетках вирус может сохраняться длительное время, но при последующей активации вируса, клетка погибнет.
Считается, что ВПГ – 1 чаще поражает дыхательные пути, а ВПГ-2 - урогенитальную систему, но, несмотря на это, роль ВПГ-1 в развитии генитального герпеса увеличивается.
Вирусы простого герпеса неустойчивы к действию физических и химических факторов, легко разрушаются под действием ультрафиолетовых и рентгеновских лучей, чувствительны к этиловому спирту, эфиру. При низких температурах (-20-70 о С) вирус сохраняется десятилетиями.
Источники инфекции – вирусоносители и больные с различными формами болезни.
Пути передачи инфекции:
- Половой (наиболее значимый);
- Гематогенный;
- Воздушно-капельный;
- Контактно-бытовой (через игрушки, предметы обихода, одежду).
Факторами передачи вируса являются: слюна, кровь, слезная жидкость, сперма, секрет влагалища и цервикального канала, различные органы и ткани, используемые при трансплантации, моча, медицинский инструментарий.
Попадает вирус в организм через поврежденные участки кожи и слизистой, затем, в месте внедрения вируса происходит размножение вирусных частиц. Первичное инфицирование вызывает латентную (скрытую, вялотекущую) инфекцию.
Клинические проявления герпетической инфекции отличаются значительным разнообразием. Они зависят от локализации поражения, распространенности, состояния иммунной системы, типа вируса, а также от механизма заражения.
По механизму заражения герпетическая инфекция бывает первичная и рецидивирующая.
Первичная форма – остро возникающее заболевание при первом контакте с вирусом простого герпеса.
По локализации поражения:
- Кожа – простой герпес, герпетиформная экзема;
- Слизистые оболочки ротоглотки – стоматит, фарингит, тонзиллит;
- Верхние дыхательные пути – острое респираторное заболевание;
- Глаза – кератоконъюнктивит;
- Урогенитальный тракт – уретрит, цистит, вульвовагинит;
- Нервная система – менингит, энцефалит, менингоэнцефалит;
- Внутренние органы – гепатит, гломерулонефрит, пневмония.
Генитальный герпес развивается у молодых людей после начала половой жизни. Первичный генитальный герпес отличается более тяжелым и продолжительным течением. Высыпания обильные и занимают большую площадь поражения. При первичном генитальном герпесе отмечается повышение температуры, общая слабость, раздражительность. В области гениталий появляются везикулезные высыпания, сохраняющиеся до 8 суток.
Влияние вируса простого герпеса на беременность и роды.
Первичное инфицирование и рецидивы во время беременности могут привести к мертворождению, выкидышам, а также к формированию пороков у плода. Наиболее опасно заражение в третьем триместре.
При первичном инфицировании матери во время беременности инфицирование плода происходит в 5% случаев. Чаще всего инфицирование ребенка происходит во время родов (85%) или после родов (10%).
Инфицирование ребенка ВПГ во время родов может стать причиной последующего развития герпетической инфекции новорожденного.
Основную опасность представляет выделение вируса со слизистой половых органов в момент родов. Выделение вируса может сопровождаться высыпаниями в области половых органов, а может и не сопровождаться никакими симптомами.
Последствия герпесвирусной инфекции для ребенка:
- распространение вируса по всему организму с поражением головного мозга, легких, печени, надпочечников, кожи, глаз, ротовой полости;
- поражение ЦНС (снижение аппетита, судороги, повышенная возбудимость);
- поражение кожных покровов, слизистой оболочки глаз, рта.
Профилактика герпесвирусной инфекции:
Важным принципом профилактики этого заболевания является прекращение близких контактов с больным человеком в период обострения.
не пользоваться чужими предметами личной гигиены;
после контакта с пораженным герпесом участком (после нанесения противовирусного крема) необходимо тщательно вымыть руки;
Больной герпесвирусной инфекцией должен иметь отдельную посуду и пользоваться личным полотенцем;
Профилактика ВПГ-1 сводится к соблюдению общих правил предупреждения респираторных заболеваний. Профилактика ВПГ-2 соответствует профилактике инфекций передающихся половым путем ( использование презервативов во время половых контактов), использование антисептических растворов после полового акта.
Профилактика инфицирования во время беременности:
Официальный сайт
Не секрет, что беременность является серьезным испытанием для женского организма. Часто во время беременности у женщины обостряются хронические заболевания, снижается иммунитет и поэтому будущая мама становится особенно уязвимой для всякого рода инфекционных заболеваний. Среди инфекций есть относительно безобидные для матери и плода (например, ОРЗ) и очень опасные (вплоть до ВИЧ).
Но есть группа инфекций, особенность которых заключается в том, что, будучи относительно безобидными для взрослых, и даже для детей, они становятся чрезвычайно опасными для беременных.
По первым буквам латинских названий входящих в нее инфекций эту группу принято называть TORCH-инфекциями или инфекциями TORCH-комплекса.
Расшифровывается аббревиатура TORCH следующим образом:
- Т — токсоплазмоз (toxoplasmosis)
- О — другие инфекции (others)
- R — краснуха (rubella)
- С — цитомегаловирусн ая инфекция (cytomegalovirus )
- H — герпес (herpes simplex virus)
Загадочная буква О — others (другие) — подразумевает такие влияющие на плод инфекции, как гепатит В и гепатит С, сифилис, хламидиоз, гонококковая инфекция, листериоз. Недавно в этот перечень включили ВИЧ-инфекцию, ветряную оспу, энтеровирусную инфекцию.
Однако, как правило, в группу ТОРЧ-инфекций включают только четыре перечисленных заболевания: токсоплазмоз, краснуха, цитомегаловирус и герпес. При этом варианте буква О аббревиатуры расшифровывается как вторая буква слова toxoplasmosis.
Особенность ТОРЧ-инфекций в том, что при первичном заражении ими во время беременности они могут оказывать пагубное действие на все системы и органы плода, особенно на его центральную нервную систему, повышая риск выкидыша, мертворождения и врожденных уродств ребенка, формирования пороков его развития, вплоть до инвалидности.
Часто поражение беременной женщины инфекциями торч-комплекса является прямым показанием к прерыванию беременности.
Кровь на наличие антител к TORCH-инфекция м правильнее всего сдавать еще до наступления беременности, при ее планировании.
Повторим, что наиболее опасным для плода является первичное заражение торч-инфекциями на фоне беременности, особенно на ранних ее сроках, поэтому если при обследовании на torch-инфекци и до беременности в крови женщины обнаруживаются антитела к этим инфекциями, то женщина может спокойно беременеть — ее ребенку с этой стороны ничто не угрожает. Если же перед беременностью антител к инфекциям ТОРЧ-комплекса не обнаруживается, значит, беременной женщине необходимо будет принимать дополнительные меры для того, чтобы обезопасить то них себя и своего будущего малыша.
Единственная ситуация, при которой токсоплазмоз представляет собой серьезнейшую опасность — это первичное заражение токсоплазмозом во время беременности.
Важно также то, что опасность представляет только токсоплазмоз, которым женщина заразилась во время текущей беременности. Это значит, что если женщина уже переболела токсоплазмозом до беременности (не менее чем за полгода до нее) ее будущему ребенку токсоплазмоз не угрожает. Более того, в трагической ситуации, когда из-за токсоплазмоза во время беременности женщина теряет ребенка, через полгода она может беременеть, уже не опасаясь токсоплазмоза.
Если же во время беременности заражение токсоплазмозом все же произошло, то многое зависит то того, на каком сроке беременности токсоплазмы попали в организм беременной женщины. Чем более ранним был срок беременности — тем больше риск тяжелых последствий при заражении плода токсоплазмозом, но, в то же время, тем меньше вероятность того, что это заражение произойдет.
И, наоборот, на более поздних сроках беременности процент передачи токсоплазмоза плоду очень высок (около 70%), но риск тяжелых поражений плода снижается.
Коварство краснухи в том, что заражение часто происходит во время инкубационного периода, когда болезнь еще никак себя не проявляет и человек не знает о том, что он болен. Однако после перенесенного заболевания краснухой организм человека вырабатывает устойчивый иммунитет, поэтому вторичного заражения краснухой не происходит.
При заражении краснухой беременной женщины эта безобидная инфекция становится смертельно опасной для плода. В начальной стадии беременности вирус краснухи чаще всего поражает нервную ткань плода, ткани глаза, сердце. В первом триместре краснуха беременной является показанием к прерыванию беременности. Если же заражение краснухой произошло во втором или третьем триместре беременности, то таких непоправимых последствий для плода, как правило, не возникает, но, тем не менее, возможно его отставание в росте и другие нарушения. В таких случаях проводится общеукрепляющая терапия, профилактика недостаточности плаценты.
Наконец, при заражении краснухой на последнем месяце беременности ребенок может родиться с проявлениями краснухи, после чего она протекает у него так же, как у детей, заразившихся после рождения, и тяжелых последствий обычно не вызывает.
Цитомегаловирусн ая инфекция — это обнаруженное только в ХХ веке вирусное инфекционное заболевание, возбудителем которого является цитомегаловирус (ЦМВ).
Цитомегаловирус может передаваться половым путем, через кровь, при грудном вскармливании. Влияние ЦМВ на человека зависит, прежде всего, от состояния иммунной системы: при здоровом иммунитете ЦМВ практически не представляет опасности, если же иммунитет снижен, то цитомегаловирус активизируется и может поражать практически все системы и органы зараженного человека. Большинство инфицированных ЦМВ людей переносят инфекцию, даже не замечая ее. Антитела к ЦМВ устойчивы и сохраняются на всю жизнь, повторных заболеваний почти никогда не возникает.
Однако так же, как в случае с остальными торч-инфекциями, если первичное заражение цитомегаловирусо м происходит при беременности, последствия могут быть катастрофическим и. Проблема усугубляется тем, что риск внутриутробной передачи ЦМВ довольно велик — цитомегаловирусн ая инфекция занимает одно из первых мест по внутриутробно му инфицированию плода. Причем инфицирование плода может произойти разными путями, и не, только от больной матери, но и от отца во время зачатия, так как в мужской сперме тоже содержится ЦМВ.
Однако чаще всего ЦМВ попадает в организм плода либо через плаценту, либо через плодные оболочки, то есть из организма матери. Заражение ребенка может произойти и во время родов, при прохождении через инфицированные родовые пути матери, и при кормлении грудью, но этот вариант гораздо менее опасен и к тяжелым последствиям для ребенка, как правило, не ведет.
При внутриутробном заражении цитомегаловирусн ая инфекция может привести к внутриутробной гибели плода или рождению ребенка с врожденной цитомегаловирусн ой инфекцией.
Врожденная цитомегаловирусн ая инфекция может проявиться сразу после рождения ребенка такими пороками развития как недоразвитый головной мозг, водянка головного мозга, гепатит, желтуха, увеличение печени и селезенки, пневмония, пороки сердца, врожденные уродства.
Родившийся ребенок может страдать задержкой психического развития, глухотой, эпилепсией, церебральным параличом, мышечной слабостью.
Иногда врожденная цитомегаловирусн ая инфекция проявляется только на 2—5-м году жизни инфицированного ребенка слепотой, глухотой, речевым торможением, отставанием в умственном развитии, психомоторными нарушениями.
Все это приводит к тому, что первичная цитомегаловирусн ая инфекция у беременной на ранних сроках беременности является показанием к искусственному прерыванию беременности.
Если же женщина была заражена цитомегаловирусн ой инфекцией ранее, а во время беременности произошло ее обострение, то таких страшных последствий не возникает: женщине назначается лечение антивирусными препаратами и иммуномодулято рами.
Следовательно, как и в случаях всех torch-инфекций, анализ на антитела к цитомегаловиру су необходимо сдать до наступления беременности. Если антитела не будут обнаружены, то женщине будет рекомендовано проводить ежемесячное исследование крови, которое не позволит упустить первичное заражение, наиболее опасное для плода.
Последней из инфекций ТОРЧ-комплекса является герпес. Строго говоря, герпес - это даже не болезнь, а целая группа вирусных инфекционных заболеваний. Известны две группы вирусов герпеса — герпес I и II типов.
В случае запущенного хронического течения болезни герпес обоих типов может проявляться поражениями не только кожи и слизистых, но и центральной нервной системы, глаз, внутренних органов.
При первичном заражении герпесом во время беременности, особенно на начальной ее стадии, когда закладываются все органы и системы будущего ребенка, герпесная инфекция может быть смертельно опасной для плода.
В этом случае втрое повышается риск неразвивающейся беременности и выкидышей, возможно развитие уродств у плода. Если заражение генитальным герпесом происходит во второй половине беременности, то увеличивается вероятность появления врожденных аномалий плода, таких как микроцефалия, патология сетчатки, пороки сердца, врожденная вирусная пневмония. Могут произойти преждевременные роды.
Кроме того, заражение плода ВПГ во внутриутробны й период может стать причиной тяжелых ситуаций, связанных с гибелью ребенка после рождения, детского церебрального паралича, эпилепсии, слепоты, глухоты.
Ребенок может заразиться герпесом не только внутриутробно, но и во время родов, проходя родовыми путями инфицированной матери. Это происходит, если во время беременности у женщины обостряется генитальный герпес, а высыпания локализуются на шейке матки или в половых путях. В случае если за четыре недели до родов у беременной женщины обнаруживается вирус герпеса, то роды, как правило, проводятся путем планового кесарева сечения, для того чтобы свести к минимуму риск инфицирования новорожденного.
Вывод напрашивается сам собой: обследование пары, планирующей беременность, на герпес, также должно проводиться еще до наступления беременности.
Если вирус герпеса будет обнаружен, врач назначит лечение, после которого инфекция не будет беспокоить ни будущую маму, ни будущего малыша. При необходимости лечение герпеса назначается и во время беременности, для этого, как правило, используются противовирусные средства, подавляющие активность вируса герпеса, а также препараты, укрепляющие иммунитет беременной женщины, особенно стимулирующие выработку организмом интерферона.
Герпес – это инфекционное заболевание, которое вызывается вирусами герпеса разных типов. Особое значение имеют вирусы простого герпеса первого и второго типа.
Кроме того, особое место занимает вирус герпеса третьего типа, который первично вызывает ветрянку, а повторно – опоясывающий лишай. Вирус герпеса первого типа вызывает заболевания кожи и слизистых оболочек, а второго типа – герпес гениталий.
Заболевание бывает двух видов:
- первичное, когда вирус герпеса впервые проникает в организм человека;
- рецидивирующее, когда герпетическая инфекция дает клиническую симптоматику повторно. Этот феномен связан с тем, что вирус герпеса из организма не удаляется, а находится в латентном, или неактивном состоянии, в ганглионарных узлах нервной системы.
Таким образом, если заражение вирусом герпеса осуществилось, то человек становится его носителем. Около 90% населения в мире являются зараженными вирусом герпеса. У одних людей заболевание проявляется часто, протекает с затяжным течением, а другие после первичных клинических проявлений никогда больше не предъявляют жалоб на данное заболевание.
Активация вируса герпеса возникает в результате снижения иммунитета. Как правило, герпетическая инфекция сопровождает простудные заболевания, ОРВИ, может возникнуть при любом инфекционном заболевании, а также это постоянный спутник больных ВИЧ и СПИДом.
Вирус простого герпеса и беременность взаимосвязаны, так как плод для будущей матери чужероден, и организм во избежание его отторжения самостоятельно снижает материнский иммунитет.
Среди путей заражения герпесом особое значение имеют следующие:
- при вирусе простого герпеса первого типа: воздушно-капельный, контактный, половой;
- при вирусе простого герпеса второго типа, или генитальном герпесе: половой;
- при вирусе герпеса третьего типа заражение происходит от больного ветряной оспой или опоясывающем лишаем.
Во всех случаях источником заражения выступает больной человек или вирусоноситель без четкой симптоматики заболевания.
Симптомы герпеса при беременности
Симптомы герпеса при беременности совершенно не отличаются от таковых у женщин небеременных или мужчин.
Герпес во время беременности может быть первичным и рецидивирующим.
Симптоматика первичного герпеса обычно складывается из выраженного симптома интоксикации, сопровождающегося общей слабостью, разбитостью, снижением умственной и физической трудоспособности, повышением температуры тела до 38 – 38,50С. Может появиться ломота в мышцах, головные боли.
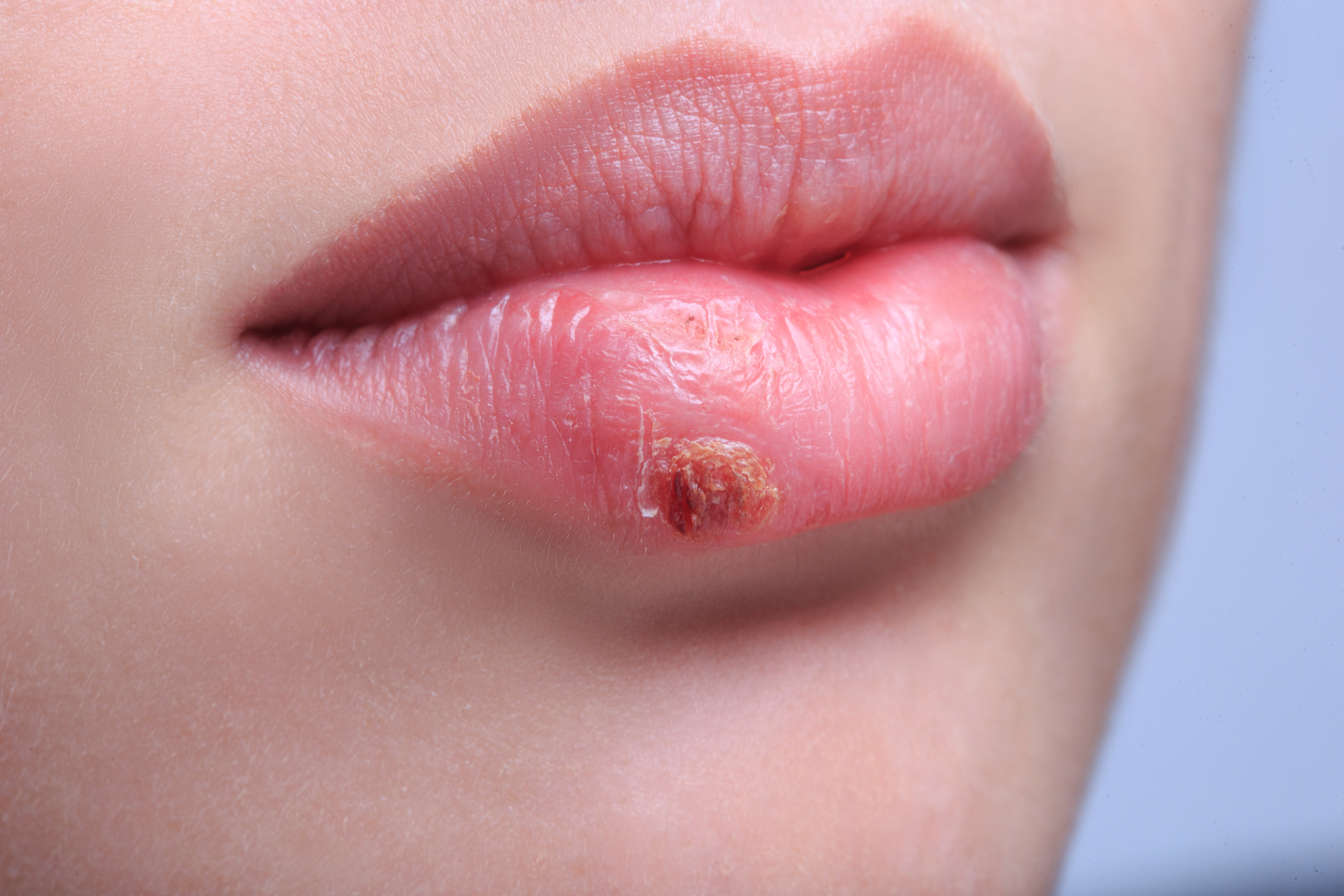
Если произошло заражение вирусом простого герпеса первого типа, то характерными признаками будут высыпания на коже и слизистых оболочках. Начинается эта реакция с чувства жжения, зуда, неприятных покалываний в области поражения. Через некоторое время на этом месте образуются пятна, переходящие в везикулы – пузырьки, наполненные жидкостью. С течением времени пузырьки лопаются, а на их месте образуются корочки. После того, как корочки отстают, на этом месте никаких следов не остается.
Если произошло первичное заражение вирусом простого герпеса второго типа, то симптомы указанные ранее, будут сохраняться, только везикулезные изменения будут находиться в области гениталий.
При рецидивирующем герпесе симптома интоксикации не бывает. Заболевший человек чувствует себя прекрасно. Только местно можно обнаружить изменения. Если же рецидив не первый, то развитие пузырьков можно предотвратить немедленным лечением.
Как правило, герпес на губах при беременности является самым частым признаком заболевания.
Вирус герпеса при беременности может оказывать негативное влияние на плод. И это зависит от того, первичный или рецидивирующий случай герпеса развился у беременной.
Герпес при беременности может протекать различными путями. Тяжесть состояния и повреждающее действие на плод оказывает тип герпетической реакции.
Так, если женщина имела контакт с вирусом герпеса, и у нее ранее были герпетические высыпания, то повреждение плода возможно лишь до 5% случаев. Если же женщина до беременности не была инфицирована вирусом герпеса, то неблагоприятное действие на плод оказывается в 90% случаев.
Кроме того, влияние герпеса на беременность зависит от того, в какой период заболела будущая мать.
Чем опасен герпес при беременности?
Еще один вопрос, который волнует молодых мам: чем опасен герпес при беременности? Герпес на ранних сроках беременности не так опасен, как во втором или третьем триместре.
Это возникает из-за того, что вирус герпеса проходит через плаценту, которая начинает формироваться только после восьмой недели беременности. Однако, и в первом триместре есть опасность развития самопроизвольного аборта. А вот в третьем триместре при первичном заражении матери вирусом простого герпеса может привести к развитию уродств плода, поражению головного мозга ребенка или к рождению мертвого плода.
При рецидивирующем герпесе заражение плода сводится к минимуму, так как в крови матери имеются специфические антитела, которые выполняют своеобразную защиту малыша от повреждений вирусом.
Герпес при беременности последствия имеет самые разнообразные. Кроме того, что ребенок может заразиться внутриутробно, он может инфицироваться и во время родов. Особенно это имеет значение при генитальном герпесе, так как при прохождении через инфицированные родовые пути матери, он подхватывает вирус. После рождения такого малыша у него может развиться герпес кожных покровов, слизистых оболочек, гениталий или же, так называемый, герпес новорожденных – распространенное поражение организма родившегося ребенка.
Лечение герпеса при беременности
Герпес во время беременности лечится такими же лекарственными препаратами, как и герпес у других людей. Единственный лекарственный препарат, который применяют для лечения герпеса – это ацикловир. Лечение герпеса при беременности проводят как местным применением мази ацикловира, так и применением этого препарата или его аналогов внутрь. При распространенном или тяжелом течении герпеса, ацикловир вводят внутривенно.
Если у женщины имеется заражение вирусом герпеса второго типа с поражением гениталий, то рекомендовано родоразрешение путем кесарево сечения, чтобы избежать заражения младенца при прохождении ребенка через инфицированные родовые пути матери. Этот аспект касается беременных, заразившихся герпесом или у которых проявились его признаки накануне родов.
Так как герпес вызывает поражение плода, то лучший вариант, если у женщины никогда не было герпеса – провести вакцинацию против него. Это создаст необходимый иммунитет, что позволит избежать заражения герпесом во время беременности. Вакцинацию проводят незадолго до планируемой беременности.
Л.А.МАРЧЕНКО, доктор медицинских наук, ведущий научный сотрудник отделения гинекологической эндокринологии. Герпетическая инфекция нередко является причиной гибели зародыша. Ее последствия могут привести к возникновению у плода пороков развития.
Вагинальные инфекции относятся к разряду наиболее часто встречающихся заболеваний нижнего отдела полового тракта. Патологические выделения из влагалища являются симптомом более 20 заболеваний, поэтому первоначально правильно установленный этиологический диагноз во многом не только определяет успех лечения, но и является гарантом отсроченных осложнений.
В последние годы наряду с общеизвестными микроорганизмами, вызывающими специфические и неспецифические инфекционные заболевания половых путей, все чаще диагностируются поражения, обусловленные вирусной инвазией гениталий, среди которых, несомненно, важная роль принадлежит вирусу простого герпеса (ВПГ).
Различают два типа ВПГ. Большинство вирусов составляет 2-ю, антигенную группу - ВПГ-2, которые преимущественно вызывают генитальную патологию, ВПМ вызывают экстрагенитальные поражения.
Пути передачи. Эпидемиология
Генитальный герпес (ГГ) относится к заболеваниям, передающимся половым путем (ЗППП).
Заражение может происходить в случае, когда у партнера, являющегося источником инфекции, на половых органах имеются типичные герпетические высыпания (рецидив заболевания) или, что особенно важно, когда он выделяет вирус, не имея при этом клинических симптомов заболевания (атипичная форма, или бессимптомное вирусоносительство).
Инфицирование возможно также при орогенитальных контактах. Бытовой путь переноса инфекции встречается крайне редко и полностью исключается, если секрет, содержащий вирус, высыхает.
Генитальный герпес может вызываться вирусом и 1-го и 2-го типа.
Известно, что степень распространенности ВПГ-2 инфекции зависит от пола обследуемых, числа их сексуальных партнеров, возраста, низкого образовательного уровня и этнической принадлежности. Исследования в 10 развитых странах показали, что серопозитивными на ВПГ-2 являются 107 млн. человек, при этом частота инфицирования в США составляет от 22 до 33%, в Европе - от 7 до 24%, в странах Индокитая - до 6%. Ситуация с инфицированием ГГ в России остается во многом крайне неясной, так как, хотя ГГ и отнесен в группу ЗППП, учет заболеваемости ведется плохо. Согласно проведенным в 1994 г. эпидемиологическим исследованиям на примере закрытой популяции в Москве, частота инфицирования генитальным герпесом составляет 19,7%. Выявлено два ее возрастных пика - 16-24 года и 35-40 лет. Женщины в 1,7 раза чаще инфицируются ВПГ-2, чем мужчины, подобных половых различий в инфицировании экстрагенитальным герпесом не выявлено.
Многие исследователи считают, что истинная ситуация в мире в отношении роста заболеваемости ГГ в достаточной мере не контролируется в связи со значительным процентом его асимптомных форм. Частота последних составляет 40-74%.
Нередко психосоциальные последствия ГГ бывают более выраженными и значимыми, чем физические страдания, связанные с частыми обострениями заболевания. ГГ, безусловно, влияет на качество жизни пациентов, т.к. уже с момента обращения к врачу перед ними возникает ряд психологических и медицинских проблем, среди которых ведущая роль принадлежит следующим: страх обнаружения вируса, депрессия; влияние на сексуальную и интимную жизнь; снижение социальной активности и изменение образа жизни; отношение к ГГ, как к болезни, передающейся половым путем; страх заразиться или быть зараженным; страх быть отвергнутым обществом; боязнь быть неизлеченным и т.д.
Клиника. Диагностические критерии
По особенностям клинических проявлений инфекции ГГ разделяют на типичный и атипичный.
Инкубационный период в среднем составляет 3-9 дней, в течение которых экспрессия вируса минимальна.
Острый период заболевания при типичной форме инфекции характеризуется обширными эрозивно-язвенными высыпаниями на слизистой больших и малых половых губ, промежности, влагалища, шейки матки. Ему всегда предшествует продромальный период, сопровождающийся субъективными ощущениями в виде боли, зуда, жжения, парестезий в области гениталий, а также общей симптоматикой - недомогание, озноб, лихорадка и т.д. При этом в 13-35% случаев наблюдается асептический менингит с тошнотой, рвотой, онемением затылка, головной болью. Все эти симптомы самостоятельно проходят с появлением высыпаний, в 10-15% отмечается фарингостоматит.
Длительность острого периода заболевания не превышает 8-10 дней, однако в редких случаях отмечается затяжной характер высыпаний. Время эпителизации эрозий, образующихся из лопнувших везикул, по мнению большинства исследователей, зависит от особенностей иммунологической реактивности организма и его репаративных возможностей. В 50-60% случаев острый период сопровождается региональным лимфаденитом.
Довольно часто при первичном эпизоде заболевания отмечается поражение мочевой системы, проявляющееся от незначительной дизурии до стойкой задержки мочеиспускания, обусловленной отеком и резкой болезненностью в области уретры в результате обширных герпетических язв или вовлечения в воспалительный процесс слизистой оболочки мочевого пузыря и уретры.
Для ГГ характерна фиксированность очагов высыпания. В зависимости от локализации последних выделяют следующие стадии поражения:
I - наружные гениталии;
II - влагалище и шейка матки;
III - матка и область придатков.
Однако подобная стадийность весьма условна. После первичного эпизода заболевания под влиянием провоцирующих факторов периодически возникают рецидивы инфекции.
Анализ провоцирующих факторов показал, что наиболее часто обострение возникает на фоне стресса (78%); переутомления (56%); менструации (50%), перенесенной простуды (24%), в то время как ультрафиолетовое облучение, физические нагрузки и употребление алкоголя встречаются, соответственно, в 12, 10 и 6% случаев.
При ГГ рецидивы возникают в 50-75% случаев, что значительно выше показателей обострения при экстрагенитальной инфекции. Это объясняется особенностями антигенной структуры вируса 2-го типа.
Частота рецидивов у многих пациентов с годами снижается. Однако довольно часто после длительной ремиссии возникает период учащения рецидивов.
В зависимости от частоты обострений выделяют три степени тяжести ГГ:
тяжелое течение - ремиссии от нескольких дней до 6 недель;
средней тяжести - ремиссии от 2 до 3 месяцев;
легкое - ремиссии не менее 4 месяцев.
Клиническая картина рецидивов хронической генитальной герпетической инфекции разнообразна. В 50-85% случаев ей сопутствует продромальный период в виде чувства жжения, зуда, болезненности в очаге поражения. В 25% случаев выявляется болевой синдром - боль иррадиирует в ногу, пах, ягодицу. В 10% случаев появляются лимфаденит, общее недомогание, озноб.
В 70% случаев во время рецидива визуализируются микроскопические везикулезно-язвенные очаги, при рецидиве не обнаруживаются какие-либо патологические изменения, и обострение бывает трудно диагностировать без дополнительных лабораторных методов исследования. Рецидив протекает, как правило, легко, продолжительность высыпаний не превышает 3-5 дней, после чего слизистые или кожные покровы полностью эпителизируются.
Диссеминация ГГ наблюдается крайне редко, только в случаях тяжелой сопутствующей инфекции либо у больных с выраженным наследственным или приобретенным иммунодефицитом.
Диагностическим критерием наличия ГГ во многом являются местные проявления заболевания. Однако при атипичных формах отсутствует манифестный признак инфекции - сгруппированные везикулы, наполненные серозной жидкостью, трансформирующиеся в эрозии и язвы, что в значительной степени затрудняет постановку диагноза. Отдует особо подчеркнуть, часто подобный тип течения ГГ характерен в значительном проценте случаев с самого начала заболевания, поэтому первичный эпизод инфекции ретроспективно выявить бывает крайне трудно.
В настоящее время в 40-75% случаев ГГ протекает атипично - без появления характерных герпетических высыпаний, включая первичный эпизод заболевания.
На основании многолетних наблюдений и соотношения жалоб с данными вирусологических исследований нами были разработаны клинические критерии, позволяющие в большинстве случаев подтвердить герпетическую природу заболевания при атипичных формах инфекции. Ведущими среди них являются стойкий зуд и жжение вульвы и влагалища; кольпиты, не поддающиеся традиционной антибактериальной терапии; рецидивирующие эрозии и лейкоплакии шейки матки; привычное невынашивание беременности; стойкий вегетативный тазовый ганглионеврит (см. рис.).
К четвертому, относительно редко встречающемуся варианту течения инфекции относят бессимптомный герпес, или вирусоносительство, при котором нет никаких клинических проявлений инфекции, однако в образцах слизи из цервикального канала или в мазках-отпечатках с половых органов выявляется вирус герпеса.
Знание этих вариантов течения инфекции важно для разработки тактики ведения беременных, страдающих ГГ.
Существует три основных механизма инфицирования плода ВПГ-2:
- вирусы из влагалища и шейки матки могут проникать к плодному яйцу восходящим путем или эмбрион может быть инфицирован во время имплантации инфицированной спермой;
- трансплацентарный переход вирусов к плоду при наличии их в крови беременных;
- заражение плода при прохождении через инфицированные родовые пути.
Последствиями герпетической инфекции являются гибель зародыша, пороки развития (микроцефалия, хориоретинит, дисплазия сетчатки, микрофтальмия, помутнение хрусталика, пороки сердца, гепатоспленомегалия, поражение отдельных органов и систем).
При ведении пациенток с генитальным герпесом врачу необходимо ставить перед собой следующие цели:
- купирование симптомов;
- проведение профилактики последствии инфекции и ее передачи половому партнеру и новорожденному.
Риск внутриутробного заражения плода ВПГ определяется совокупностью факторов - вариантом клинического течения ГГ (первичный эпизод заболевания или рецидив), особенностями клинической картины (типичное, атипичное или бессимптомное течение инфекции), продолжительностью контакта плода с инфицированными родовыми путями матери и стадией герпетических высыпаний.
При совпадении первичного эпизода заболевания ГГ с I или III триместром беременности в 40-50% случаев наблюдается либо мертворождение, либо рождение ребенка с врожденным поражением мозга (микроцефалия и другие аномалии). Поэтому, согласно рекомендациям ВОЗ, при первичном эпизоде заболевания, особенно в случае первичной инфекции в I триместре, целесообразно беременность прервать.
При рецидивирующем герпесе риск инфицирования плода составляет всего О-8%, что объясняется пассивной передачей материнских антител, более низкими титрами вируса и более коротким периодом его воздействия. В этих случаях беременность следует сохранить.
Наибольшую значимость в плане возможного инфицирования плода имеют атипично протекающие формы хронической ге-нитальной герпетической инфекции. В 70% случаев дети с неонатальным герпесом рождаются именно от матерей с атипичными или бессимптомными формами ГГ, при том, что частота бессимптомного носительства ВПГ-2 составляет в различных популяциях 0,5-8%. Смертность новорожденных от неонатального герпеса в этой группе составляет 50-70%; из выживших новорожденных здоровыми остаются только 15%.
Таким образом, становятся понятны социальная значимость для нашей страны проблемы генитальной герпетической инфекции и ее неблагоприятный вклад в заболеваемость и перинатальные потери.
Для установления нормального контакта между врачом и пациентом необходимо:
- неосуждение со стороны врача;
- вовлечение пациента в управление своей болезнью;
- возможность больного получить лучшее из доступного на текущий момент лечение.
Принципы современной терапии
К базисному виду терапии относится прежде всего комплекс противовирусного лечения - длительная блокада репродукции вируса современными химиопрепаратами, на фоне которых следует проводить стимуляцию неспецифической и специфической резистентности организма. Необходимо подчеркнуть, что лечение всегда целесообразно подбирать индивидуально и в каждом конкретном случае выбор медикаментозного комплекса определяется клинической формой инфекции, фазой заболевания (рецидив или ремиссия), иммунологическим состоянием пациента, предшествующим лечением и его эффективностью, наличием сопутствующих заболеваний (особое внимание необходимо уделять аллергоанамнезу).
Идеальный противовирусный препарат должен обладать селективным и специфическим механизмом действия, не быть токсичным (мутагенным, тератогенным, канцерогенным), не иметь побочных эффектов, не вызывать резистентность. Препарат должен характеризоваться хорошей биодоступностью, не взаимодействовать с другими лекарствами и иметь удобный режим дозирования.
Наиболее безопасным вариантом химиотерапии оказалось создание синтетических аналогов какого-либо структурного компонента (нуклеозид) герпес-вирусной ДНК, который избирательно фосфорилируется не клеткой, а вирусспецифическим ферментом - тимидинкиназой.
К наиболее широко используемым в мировой клинической практике аномальным нуклеозидам относятся ацикловир (зовиракс, виролекс), валацикловир (валтрекс), фамцикловир (пенцикловир), ганцикловир и т.д. К аналогам пирофосфата относится триаптен. К препаратам с другим механизмом действия (специфические ингибиторы) - бонафтон, алпизарин, флакозид, хелипин, флореналь.
Чаще всего для лечения генитального герпеса используют ацикловир (АЦ), обладающий высокой степенью сродства и селективности в отношении герпес-вирусов.
Ацикловир проникает преимущественно в зараженные ВПГ клетки, однако в неизмененном виде инертен и малотоксичен, прежде чем стать активным, он должен фосфорилироваться.
Существует две методики лечения рецидивирующей герпетической инфекции АЦ: эпизодическое лечение каждого обострения и продолжительная супрессивная терапия с целью предотвращения рецидивов. Выбор режима терапии определяется клиническим вариантом инфекции (первичный эпизод или рецидив) и степенью ее тяжести, а также проблемой передачи инфекции в случае, если один из партнеров серонегативен, и при планировании беременности.
В последние годы в России в качестве химиопрепарата широко использовался алпизарин. Проведенное сравнительное исследование лечебного и профилактического эффекта алпизарина и зовиракса при тяжелом течении ГГ показало, что прием зовиракса в режиме супрессивной терапии по 800 мг в сутки способствовал стойкой ремиссии у 73% больных, в то время как прием алпизарина вызывал подобный эффект только в 19% случаев. Профилактический эффект зовиракса более чем в 5 раз превосходит эффект алпизарина по восстановлению качества жизни больных.
Однако биодоступность перорально вводимого ацикловира составляет всего 15-21 %, поэтому в течение последних 10 лет с целью повышения его эффективности разрабатывались различные аминокислотные эфиры ацикловира.
Всего было синтезировано более 18 аминокислотных эфиров. Валацикловир (L-валиловый эфир) показал биодоступность, равную 63%. В отличие от ацикловира валацикловир (валтреке) под влиянием фермента валацикловиргидролазы хорошо всасывается в кишечнике и быстро метаболизируется в печени, полностью превращаясь в ацикловир. Фармакокинетика и токсические свойства валацикловира идентичны таковым для ацикловира.
В клинической практике (особенно при лечении привычного невынашивания беременности) нередко возникает необходимость одновременно проводить профилактику как генитального герпеса, так и ЦМВ-инфекции. Использование в этих случаях валтрекса в значительной степени облегчает задачу врача, так как наиболее специфичный для ЦМВ-инфекции химиопрепарат ганцикловир оказывает выраженный гепатотоксический эффект и вызывает гипоплазию костного мозга.
Более высокие концентрации ацикловира в плазме как конечного продукта введения валацикловира позволяют также использовать его в случаях инфицирования больных резистентными штаммами герпес-вируса. Поддержание высоких уровней ацикловира в плазме при лечении валацикловиром позволяет уменьшить кратность приема препарата и способствует лучшему его усвоению.
В режиме эпизодической терапии валтрекс следует назначать по 500 мг 2 раза в день в течение 5 дней. Для профилактики рецидивов инфекции - по 100 мг один раз в сутки в течение 4-6 месяцев. За безопасностью применения ацикловира и его аналогов наблюдают с 1982 года. Подобная программа принята и для валацикловира. Наиболее частыми побочными эффектами являются головная боль, тошнота, диарея. Однако они не выражены.
Высокой биодоступностью (77%) обладает и фамцикловир (диацетил-6 - дезоксипроизводное пенцикловира). Пенцикловир имеет сходный, но не аналогичный ацикловиру спектр действия, включающий вирус ветряной оспы, ВПГ-1, ВПГ-2, а также вирус гепатита В. Фамцикловир превращается в пенцикловир при всасывании и пассаже через печень, последний активируется вирусной тимидинкиназой. Фамцикловир хорошо переносится, однако в дозе в 50 мг раз выше, чем терапевтическая повышает риск развития аденокарциномы груди у мышей.
Однако ни ацикловир, ни другие противовирусные агенты - фамцикловир, валацикловир - не предотвращают ни перехода вируса в латентное состояние, ни возникновения рецидивов после их отмены, ни передачи инфекции, а также, к сожалению, не влияют на естественное течение этой инфекции в плане полного излечения. Поэтому на протяжении последних 20 лет ученые изыскивают методы непосредственного воздействия на иммунную систему больных ГГ с целью стимуляции специфических и неспецифических ее факторов, тем самым способствуя блокаде репродукции вируса. Одним из перспективных подходов профилактики и лечения герпес-вирусных заболеваний являются применение препаратов иммуноглобулинов человека и вакцинотерапия.
Читайте также:


