Нетуберкулезный микобактериоз у больных без вич инфекции

Во многих индустриально развитых странах в последнем десятилетии наблюдается рост числа больных микобактериозами. Особую актуальность эта проблема приобрела в условиях распространения ВИЧ-инфекции. В последние годы и в России среди больных ВИЧ-инфекцией тоже нарастает регистрация случаев микобактериозов, вызванных нетуберкулезными микобактериями. Проблема микобактериозов актуальна не только для ВИЧ-инфицированных, но и для других категорий больных с иммунодефицитом. Микобактериозы часто наблюдаются у больных с хроническими неспецифическими заболеваниями легких, силикозом, раком легкого. У больных с иммунодефицитом, как правило, микобактериоз носит диссеминированный характер и в значительном числе случаев приводит к смерти. Повсеместное нарастание микобактериозов в настоящее время связано с увеличением числа больных с поражением иммунной системы, с хроническими неспецифическими заболеваниями легких, с ухудшением экологической обстановки, а также с улучшением диагностики. Это группа заболеваний, вызываемых нетуберкулезными микобактериями (НТМБ), которые являются условно-патогенными микобактериями и вызывают развитие заболевания при определенных условиях, чаще всего при снижении иммунитета. У лиц, живущих с ВИЧ-инфекцией, микобактериоз относится к оппортунистическим заболеваниям [1, 2]. Но, к сожалению, эпидемиологическая ситуация по сочетанной патологии туберкулеза и ВИЧ-инфекции ухудшается. В Воронежской области с 2000 г. наблюдается рост заболеваемости и распространенности туберкулеза у ВИЧ-инфицированных [3]. В Российской Федерации нет разработанных клинических рекомендаций для ведения пациентов с микобактериозами, не имеется определенных нормативных документов для проведения диагностики и лечения данной категории больных, нет принятой клинической классификации этого заболевания. Имеющиеся данные об этиологической структуре, эпидемиологии, клинике, диагностике микобактериозов достаточно скудны ввиду того, что увеличение количества больных микобактериозами связано с нарастающей волной больных ВИЧ-инфекцией. Согласно литературным данным микобактериозы встречаются во всех экономически развитых странах. В Северной Америке распространенность микобактериозов за период с 1998 по 2010 гг. была в пределах от 5,6 (США) до 9,8 (Канада) на 100 тыс. населения. В Южной Америке (только в Бразилии) с 1996 по 2005 гг. микобактериоз устанавливался в 1,0 случае на 100. тыс. населения случаев. В Европе заболеваемость колебалась от 0,6 до 1,7 случаев на 100 тыс. населения в 1992–2010 гг., но в Шотландии заболеваемость микобактериозом достигла величины 3,1 на 100 тыс. населения с 2005 по 2010 гг. А в Японии было зарегистрировано 938 случаев легочного микобактериоза с 1970 по 2003 гг. [4–7].
К клиническим и рентгенологическим критериям для постановки диагноза микобактериоза согласно рекомендациям относятся: имеющиеся респираторные симптомы; обнаружение при рентгенографическом исследовании в легких очаговых или полостных изменений или наличие при компьютерной томографии множественных бронхоэктазов с мелкими очагами, при этом должна быть проведена дифференциальная диагностика в целях исключения других заболеваний, имеющих сходную рентгенологическую картину.
К микробиологическим критериям микобактериоза относятся:
– наличие в двух и более независимо взятых образцах мокроты нетуберкулезных микобактерий;
– не менее одного положительного результата культурального исследования материала, полученного при проведении бронхоскопии (бронхоальвеолярный лаваж [БАЛ] или промывные воды бронхов);
– морфологические изменения в тканях и органах (наличие гранулематозного воспаления или обнаружение кислотоустойчивых бактерий) и наличие роста культуры НТМБ этой ткани или не менее из одного образца БАЛ / промывных вод бронхов или мокроты,
или все вышеперечисленные критерии. В настоящее время этот вопрос является дискуссионным и широко обсуждается.
Цель исследования – изучить особенности клинических проявлений и диагностики микобактериозов у лиц, живущих с ВИЧ-инфекцией.
Результаты исследования и их обсуждение
Клиническое наблюдение 1
Пациентка Ш. (35 лет). Туберкулезом раньше не болела. Наблюдалась в Центре по борьбе со СПИД в течение 10 лет (4В стадия), получала антиретровирусную терапию. В июле 2018 г. перенесла пневмоцистную пневмонию, лечилась в стационаре, выписана с улучшением. В начале ноября состояние вновь ухудшилось, госпитализирована в стационар Центра по борьбе со СПИД. При обследовании на рентгенограмме легких выявлена патология, в мокроте обнаружены кислотоустойчивые микобактерии (КУМ), в связи с чем переведена в противотуберкулезный диспансер (ПТД) для исключения туберкулеза.
При поступлении в ПТД 22.11.2018 жалобы на кашель со слизистой мокротой до 50 мл в сутки, одышку при незначительной физической нагрузке, слабость, повышение температуры тела до 37оС, похудение на 4 кг за последний месяц. Общее состояние средней тяжести, пониженного питания, кожные покровы бледные. Дыхание жесткое с бронхиальным оттенком, гудящие хрипы в нижних отделах легких. ЧДД 24 в минуту. АД 90/55 мм рт. ст. Печень выступает на 7 см из-под подреберья.
Общий анализ крови: гемоглобин – 75 г/л; эритроциты – 2,9х1012/л; цветной показатель – 0,75; лейкоциты – 15,4х109/л; эозинофилы – 1; палочкоядерные – 16; сегментоядерные – 74; лимфоциты – 3; моноциты – 6; СОЭ – 57 мм/ч.
Общий анализ мочи: удельный вес – 1024; белок – 0,3; эритроциты – 1–2; лейкоциты – 5–6; цилиндры – 3–4.
Количество СD4+ лимфоцитов – 42 клетки/мкл.
В мокроте методом люминесцентной микроскопии выявлены кислотоустойчивые микобактерии КУМ (+) от 21.11.2018, 23.11.2018, 27.11.2018.
В мокроте методом ПЦР РВ от 26.11.2010 ДНК МБТ не выявлены; ПЦР Дженэксперт от 23.11.2018 ДНК МБТ не выявлены.
В мокроте посевом (BACTEC) от 23.11.2018, 26.11.2018 НТМБ(+). Иммунохроматографический тест на микобактерии туберкулеза TBAgMRT64 Rapid – отрицательный. Реакция на Диаскинтест отрицательная.
УЗИ органов брюшной полости: УЗ-признаки гепатоспленомегалии, диффузных изменений печени и поджелудочной железы.
Фибробронхоскопия: слева бронхи без особенностей. В просвете среднедолевого бронха (СДБ) справа густая слизисто-гнойная мокрота. По задней стенке СДБ с переходом на латеральную изъязвление, дно которого покрыто густыми массами белого цвета. Вокруг слизистая отечна, гиперемирована. Множество бугорков. За счет этих изменений БС4 сужено почти наполовину. Выше слизистая незначительно отечна. Шпора СДБ острая.
Гистологическое исследование биопсийного материала: в биоптате мелкие кусочки некротического детрита и фрагменты неспецифической грануляционной ткани с диффузной лимфоцитарной и нейтрофильной инфильтрацией, обилие мелких кровеносных сосудов.
При окраске по Цилю–Нильсену КУМ не определяются.
Заключение: морфологическая картина неспецифического воспаления.
На обзорной рентгенограмме органов грудной клетки в прямой и правой боковой проекции определяются массивное неоднородное инфильтративное затенение в средней доле правого легкого с четкой границей по междолевой борозде, неоднородное инфильтративное затенение в проекции 9-го сегмента левого легкого. Корни расширены. Тень средостения смещена влево (рис. 1, 2).
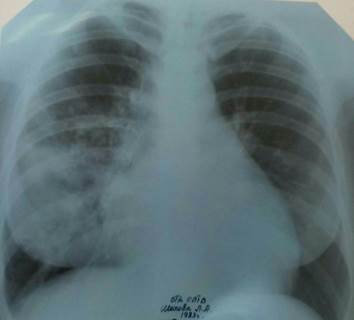
Рис. 1. Обзорная рентгенограмма органов грудной клетки в прямой проекции больной Ш.
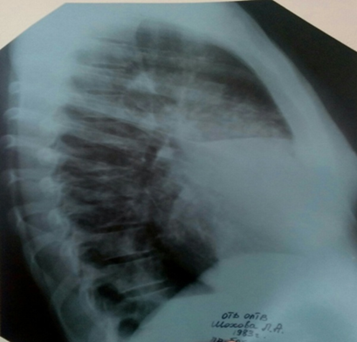
Рис. 2. Обзорная рентгенограмма органов грудной клетки в правой боковой проекции больной Ш.
Мультиспиральная компьютерная томография органов грудной полости: в верхних и средних долях правого легкого массивная инфильтрация, участки консолидации в S8 нижней доли. Множественные полиморфные очаги по всем полям, больше справа. Часть из них с деструкцией. Лимфатические узлы гиперплазированы до 12–14 мм. Сердце обычных размеров, в перикарде жидкость, толщина слоя 12 мм. Дегенеративные изменения позвоночника. Костно-деструктивных изменений не выявлено.
Таким образом, у больной были типичные клинические проявления микобактериоза: кашель, одышка, лихорадка, потеря веса, анемия. Имелись рентгенологические изменения в легких в виде фокусов и очагов и поражение внутригрудных лимфатических узлов. Диагноз верифицирован бактериологическим методом исследования мокроты (рост НТМБ в двух анализах мокроты методом ВАСТЕК).
Клиническое наблюдение 2
Пациентка М., 32 года. Из анамнеза известно, что туберкулезом раньше не болела, наблюдается в Центре по борьбе со СПИД с 2008 г. (4В стадия), получает автиретровирусную терапию (АРВТ). В августе 2018 г. перенесла менингоэнцефалит. Состояние ухудшилось в октябре 2018 г., когда стали беспокоить кашель, общая слабость, плохой аппетит. Была госпитализирована в стационар. В легких при рентгенологическом исследовании выявлена патология. Больной была назначена антибактериальная терапия. При исследовании мокроты получили КУМ(+) методом люминесцентной микроскопии. Для исключения туберкулеза пациентка направлена в противотуберкулезный диспансер.
При поступлении в противотуберкулезный диспансер: состояние относительно удовлетворительное. Кожные покровы чистые, бледные. В легких дыхание аускультативно жесткое, хрипы не выслушиваются. ЧДД – 18 в минуту. Тоны сердца ритмичные ЧСС – 78 ударов в минуту, АД 100/65 мм рт. ст. Язык влажный, с белым налетом. Живот мягкий, безболезненный.
Общий анализ крови от 28.11.2018: гемоглобин – 130 г/л; эритроциты – 3,8х10/л; цветной показатель – 1,0; лейкоциты – 8,5х109/л; эозинофилы – 2%; палочкоядерные – 3%; сегментоядерные – 76%; лимфоциты – 8%; моноциты – 11%; СОЭ – 33 мм/ч.
Общий анализ мочи от 28.11.2018: уд. вес – 1020; белок – 0,19 г/л; лейкоциты – 1–3 в поле зрения.
Количество СD4+ лимфоцитов 101 клетка/мкл от 27.11.2018.
В мокроте КУМ (+) от 28.11.2018, 05.12.2018, 06.12.2018, 14.12.2018, 18.12.2018 методом люминесцентной микроскопии.
В мокроте методом ПЦР-РВ от 04.12.2018, 20.12.2018 ДНК МБТ не выявлены.
ПЦР Дженэксперт от 03.12.2018 ДНК МБТ не выявлены.
В мокроте посевом (BACTEC) от 05.12.2018, 06.12.2018 НТМБ(+). Иммунохроматографический тест на МБТ TBAgMRT64 Rapid – отрицательный.
Реакция на Диаскинтест – отрицательная.
Фибробронхоскопия № 1: слева устье нижнедолевого бронха сужено до почти щелевидного за счет бугристой опухоли с густым налетом некроза белого цвета.
Биопсия № 1: в собственном слое слизистой обилие мелких кровеносных сосудов и диффузная воспалительная инфильтрация лимфоидного и нейтрофильного характера, на фоне которого определяются мелкие нечеткие эпителиоидно-клеточные гранулемы. При окраске по Цилю–Нильсену КУМ не определяются.
Фибробронхоскопия № 2: устье верхнедолевого бронха справа полностью стенозировано бугристой опухолью с густым налетом фибрина белого цвета.
Биопсия № 2: в биоптате – мелкие фрагменты слизистой, местами покрытые многослойным плоским эпителием, местами – слоем некротического детрита. В слизистой – диффузная нейтрофильная и лимфоцитарная инфильтрация, на фоне которой местами определяются нечеткие мелкие эпителиоидно-клеточные гранулемы. В центре некоторых гранулем – скопление ядерного детрита. При окраске по Цилю–Нильсену КУМ не обнаружены.
МСКТ ОГК: в верхней доле S1, S2 справа и нижней доле S6 и базальной пирамиде левого легкого определяются очаговые изменения, деструкция четко не видна. Гиперплазированы бронхопульмональные лимфатические узлы. Средостение структурно не смещено.
В представленном случае клинические проявления микобактериоза (кашель, общая слабость, потеря веса) были мало выраженными. Это можно объяснить количеством СД4+ лимфоцитов (101 кл/мкл). Диагноз микобактериоза поставлен своевременно благодаря бактериоскопическому исследованию мокроты больной, консультации фтизиатра и комплексу обследований в противотуберкулезном диспансере.
1. В настоящее время наблюдается рост заболеваемости микобактериозами у лиц, живущих с ВИЧ-инфекцией. Для своевременного выявления микобактериозов у врачей различных специальностей должна быть настороженность.
2. Диагноз микобактериоза следует устанавливать на основании комплексного клинико-рентгенологического и микробиологического обследования. Главными критериями при постановке данного диагноза должны быть выделение культуры НТМБ и гистологическая верификация.
Полный текст:
Цель: провести анализ случаев микобактериоза в популяции людей, живущих с ВИЧ, выявленных в инфекционном стационаре города Санкт-Петербурга за последнее десятилетие.
Результаты. С 2012 года фиксируется увеличение частоты выявления микобактериоза у пациентов с ВИЧ-инфекцией: прирост нозологии за последние пять лет в среднем составлял 57% в год. Группа пациентов с микобактериозом, вызванным Mycobacterium avium complex, характеризовалась преимущественно половым путем инфицирования (68,7%); средний возраст составил 35 лет; треть пациентов были трудоустроены на момент выявления болезни (35%). Анамнестически о пребывании в местах лишения свободы сообщало 11 человек (13,3%), лишь 4 (4,8%) пациента активно употребляло психоактивные вещества. В группе пациентов с микобактериозом, вызванным прочими нетуберкулезными микобактериями, преобладал гемоконтактный путь передачи ВИЧ-инфекции (57,1%), пенитенциарный анамнез имело 28,6%. Более чем в половине случаев ведущим источником бактериовыделения стал материал верхних дыхательных путей.
Заключение. Наблюдается неуклонный рост микобактериозов в структуре вторичных инфекций при ВИЧ-инфекции. Ведущим этиологическим агентом является M. avium. Пациенты с данной патологией отличаются сохранным социальным статусом, половым путем инфицирования. Наиболее часто развивались генерализованные формы процесса; самым частым источником бактериовыделения, по данным этой выборки, был материал респираторного тракта.
1. Thomson R.M. and NTM working group at Queensland TB Control Centre and Queensland Mycobacterial Reference Laboratory. Changing epidemiology of pulmonary nontuberculous mycobacteria infections. Emerg. Infect. Dis., 2010, Vol. 16, No. 10, pp. 1576–1583. URL: DOI:10.3201/eid1610.091201.
2. Shah N.M. et al. Pulmonary Mycobacterium avium-intracellulare is the main driver of the rise in non-tuberculous mycobacteria incidence in England, Wales and Northern Ireland, 2007–2012. BMC Infect. Dis., Vol. 16, No. 195, 6 May, 2016, URL: DOI:10.1186/s12879-016-1521-3.
3. Namkoong Ho et al. Epidemiology of pulmonary nontuberculous mycobacterial disease, Japan (1). Emerg. Infect. Dis., 2016, Vol. 22, No. 6, pp. 1116–1117.
4. Zweijpfenning S.M.H., van Ingen J., Hoefsloot W. Geographic distribution of nontuberculous mycobacteria isolated from clinical specimens: a systematic review. Semin. Respir. Crit. Care Med., 2018, Vol. 39, No. 03, pp. 336–342. URL: DOI: 10.1055/s-0038-1660864.
5. Yaoju Tan et al. Epidemiology of pulmonary disease due to nontuberculous mycobacteria in Southern China, 2013–2016. BMC Pulm. Med., 2018, Vol. 18, No. 1, pp. 168. URL: DOI:10.1186/s12890-018-0728-z.
6. Hirokazu Y. et al. Population structure and local Aaaptation of MAC lung disease agent Mycobacterium avium subsp. hominissuis. Genome Biol. Evol., 2017, Vol. 9, No. 9, pp. 2403–2417.
7. Пантелеев А.М., Драчева М.С., Никулина О.В., Соколова О.С., Зонова А.В. Клинико-лабораторные особенности микобактериоза у больных ВИЧ-инфекцией // Журнал инфектологии. 2016. Т. 8, № 3. С. 40–45. [Panteleev А.M., Drachevа, M.S., Nikulina O.V., Sokolova O.S., Zonova A.V. Clinical and laboratory features of mycobacteriosis in patients with HIV infection. J. Infectol., 2016. Vol. 8, No. 3, pp. 40–45 (In Russ.)].
9. Актуальные проблемы ВИЧ-инфекции в России. Роль медицинских работников в профилактике ВИЧ-инфекции. 10.12.2013. М.: ФНМЦ по профилактике и борьбе со СПИДом ФБУН ЦНИИЭ Роспотребнадзора. [Actual problems of HIV-infection in Russia. The role of health workers in HIV prevention. 10.12.2013. Moscow: Federal scientific and methodological center for prevention and control of AIDS of the Central Research Institute of Epidemiology of Rospotrebnadzor (In Russ.)].
10. ВИЧ-инфекция в Санкт-Петербурге по состоянию на 01.01.2016 г. / Информационный бюллетень. СПб.: Санкт-Петербургский центр по профилактике и борьбе со СПИД и инфекционными заболеваниями, 2016. [HIV infection in Saint-Petersburg as of 01.01.2016 / Newsletter. Saint-Petersburg: Saint-Petersburg center for the prevention and control of AIDS and infectious diseases, 2016 (In Russ.)].
11. Зимина В.Н., Дегтярева С.Ю., Белобородова Е.Н., Кулабухова Е.И., Русакова Л.И., Фесенко О.В. Микобактериозы: современное состояние проблемы // Клиническая микробиология и антимикробная химиотерапия. 2017. Т. 19, № 4. С. 276–282 [Zimina V.N., Degtyareva S.Yu., Beloborodova E.N., Kulabukhova E.I., Rusakova L.I., Fesenko O.V. Mycobacterioses: the current state of the problem. Clinical Microbiology and Antimicrobial Chemotherapy, 2017, Vol. 19, No. 4, pp. 276–282 (In Russ.)].
12. Pettipher A.C., Karstaedt A.S. and Hople M. Prevalence and Clinical Manifestations of Disseminated Mycobacterium avium Complex Infection in South Africans with Acquired Immunodeficiency Syndrome Clive. Clin. Infect. Dis., 2001, Vol. 33, pp. 2068–2071. URL: DOI: 10.1086/323979.
13. Shafran S.D., Singer J., Zarowny D.P., Phillips P., Salit I., Walmsley S.L., Fong I.W., Gill M.J., Rachlis A.R., Lalonde R.G., Fanning M.M., Tsoukas C.M. A comparison of two regimens for the treatment of Mycobacterium avium complex bacteremia in AIDS: rifabutin, ethambutol, and clarithromycin versus rifampin, ethambutol, clofazimine, and ciprofloxacin. Canadian HIV Trials Network Protocol 010 Study Group. N. Engl. J. Med., 1996, Aug 8, Vol. 335, No. 6, pp. 377–383.
14. Barreto J., Palaci M., Ferrazoli L., Martins M.C., Suleiman J., Lorenç R., Ferreira O.C. Jr., Riley L.W., Johnson W.D. Jr., Galvão P.A.A. Isolation of Mycobacterium avium Complex from Bone Marrow Aspirates of AIDS Patients. J. Infect. Dis., 1993, Vol. 168, No. 3, pp. 777–779.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
1 Нетуберкулезный микобактериоз у больных ВИЧ инфекцией: особенности клинических проявлений, диагностика, лечение ГКУЗ Московский научно практический центр борьбы стуберкулезомдзм В.Н. Зимина
2 Нетуберкулезный микобактериоз (НТМБ) инфекционное заболевание, вызываемое нетуберкулезными микобактериями (МКБ 10: А 31; В 20.0) Практическая важность НТМБ как клинической проблемы обозначилась в течение первых лет эпидемии ВИЧ инфекции, когда значительное число больных пациентов умерли от генерализованной МАС инфекции * Практически одновременно с начала 1990 х гг. в экономически развитых странах отмечается неуклонный рост (в разы) заболеваемости НТМБ и у людей с ВИЧ негативным статусом ** *Daley C.L., Griffith D.E. Pulmonary non tuberculous mycobacterial infections // Int. J. Tuberc. Lung Dis Vol. 14, 6. Р **Falkinham J.O. Nontuberculous mycobacteria in the environment. // Clin Chest Med Vol.23. P
3 Причины стремительного роста клинической значимости и интереса к НТМБ Увеличение числа больных с иммунодефицитными состояниями: больные ВИЧ инфекцией пациенты с трансплантированными органами другие вторичные иммунодефициты состояния Рост числа людей с хроническими неспецифическими заболеваниями легких (отмечена предрасположенность к НТМБ лиц с ХОБЛ, бронхоэктазами, кистозным фиброзом, пневмокониозами и т.д.) Улучшение методов диагностики! Вероятно ранее большинство нетуберкулезных микобактериозов, были ложно признаны как туберкулез Литвинов В.И., Макарова Н.В., Краснова М.А. Нетуберкулезные микобактерии. М.: МНПЦБТ с. Оттен Т.Ф., Васильев А.В. Микобактериоз. СПб: Медицинская пресса, с.
4 Контагиозность микобактериозов (1) По способности вызывать заболевание у человека и животных все микобактерий можно разделить на три группы: безусловно патогенные (опасные) для человека и животных виды микобактерий М. tuberculosis и M. Bovis, M. leprae возбудитель заболевания проказы; условно патогенные микобактерий (около 40 видов), которые при определенных условиях могут вызвать заболевания человека. Наиболее клинически значимые из них: M. avium, M.intracellulare, M. kanssasii, M. malmoense, M. xenopi, M. fortuitum, M. chelonai; сапрофитные микобактерии, которые свободно живут в окружающей среде и, как правило, не опасны для человека: M. Terrae, M. phlei, M. gordonae/aqual, M. triviale, M. flavescens, M. Gastri David L., Heyman М. Diseases due to other mycobacteria. Washington: American Public Health Association Р Daley C.L., Griffith D.E. Pulmonary non tuberculous mycobacterial infections // Int. J. Tuberc. Lung Dis Vol. 14, 6. Р
6 Нетуберкулезный микобактериоз у больных ВИЧ инфекцией Говоря об нетуберкулезном микобактериозе у больных ВИЧинфекцией при иммунодефиците, обычно подразумевают заболевание, вызванное Mycobacterium avium intracellulare (другое название Mycobacterium avium complex, МАС). МАС инфекция является истинно оппортунистическим СПИДиндикаторным заболеванием и развивается при тяжелом иммунодефиците (чаще при снижении CD4+лимфоцитов менее 50 клеток/мкл)* *Horsburgh CR Jr. The pathophysiology of disseminated Mycobacterium avium complex disease in AIDS. J Infect Dis 1999, Suppl 3: S
7 Нетуберкулезный микобактериоз у больных ВИЧ инфекцией В эру до АРВТ, в благополучных странах (где низкий уровень заболеваемости туберкулезом), МАС инфекцию регистрировали почти у 40% больных СПИДом* Частота возникновения оппортунистических заболеваний, США, Bucharz K et al. AIDS defining opportunistic illnesses in US patients, : a cohort study. AIDS; 2010, 24:
8 Нетуберкулезный микобактериоз у больных ВИЧ инфекцией По оценочным данным НТМБ среди заболеваний вызванных микобатериальной инфекцией (В20.0) у больных ВИЧ инфекцией в РФ составляет 3 7% У больных ВИЧ инфекцией в период относительной компенсации Т клеточного иммунитета или у длительно получающих АРВТ, могут развиться микобактериозы других видов НТМБ (стакойже частотой как и в популяции в целом) *Nightingale SD, Byrd LT, Southern PM, et al. Incidence of Mycobacterium avium intracellulare complex bacteremia in HIV positive patients.j Infect Dis 1992, 165:
9 Клиника МАС инфекции у больных ВИЧинфекцией Симптомы МАС инфекции неспецифичны и схожи с туберкулезом: лихорадка, потеря веса, слабость При МАС инфекции часто поражается ЖКТ, поэтому наиболее встречаемые симптомы это диарея, боли в животе При генерализации процесса наиболее уязвимы костный мозг, печень, селезенка Характерно поражение лимфатических узлов (внутригрудных, забрюшинных) с формированием абсцессов К. Хоффман, 2011
10 Диагностика: Дифференциальная диагностика в основном с туберкулезом и лимфомой ОАК часто выраженная анемия, цитопения При наличии цитопении, анемии помогает пункция костного мозга с идентификацией возбудителя Лучевая диагностика неспецифична: поражение ВГЛУ, инфильтраты, диссеминация, нередко образование полостей распада УЗИ ОБП увеличение печени, селезенки, мезентериальных лимфатических узлов. В отличие от туберкулеза поражение серозных оболочек нехарактерно К. Хоффман, 2011
11 Схема выявления микобактерий классическими микробиологическими методами (бактериологическая лаборатория фтизиатрической службы) 1 2 дня Микроскопия Диагностический материал Иммунохроматографи я или б/х тесты МБТ Посев Определение ЛЧ НТМБ 3 18 недель Твердые среды Жидкие среды день Лабораторная диагностика туберкулеза. Методические материалы к проведению цикла тематического усовершенствования. М.: Р. Валент 2012 г,
12 Видовая идентификация возбудителя, выросшего на средах Микобактерии туберкулезного комплекса (МТК) Быстрая дифференциация МТК от НТМ: ПЦР IS6110 TBc-ID (Becton Dickinson) (референс лаборатория) МИКРОСКОПИЯ КИСЛОТОУСТОЙЧИВЫЕ ПАЛОЧКИ Нетуберкулезные микобактерии (НТМ) Идентификация НТМ до вида: технология ДНК-стрипов (Hain-test) масс-спектрометрия Лабораторная диагностика туберкулеза. Методические материалы к проведению цикла тематического усовершенствования. М.: Р. Валент 2012 г, 704 с.
13 Генерализованная МАС инфекция с поражением мезентериальных лимфатических узлов с абсцедирование и костного мозга у ВИЧинфицированного больного (количество CD4+лимфоцитов 28 клеток/мкл) Обзорная рентгенограмма ОГК Срез КТ ОБП: пакеты увеличенных мезентериальных Из личного архива клинических наблюдений В.Н. Зиминой (неопубликованные)
14 Окраска по Цилю-Нильсену (кислотоустойчивые бактерии в количестве, не поддающемся подсчету, локализованы в макрофагах)
15 Тест-система система для обнаружения ДНК Mycobacterium avium и Mycobacterium tuberculosis при исследовании тканей (ФГУН ЦНИИ Эпидемиологии Роспотребнадзора) ДНК Mycobacterium avium ОБНАРУЖЕНА ДНК МБТ не обнаружены
16 Критерии диагноза НТМБ (для больных с ВИЧ инфекцией) Абсолютные: Многократное выделение одного и того же вида НТМБ с учетом соответствующей клинико рентгенологической картины заболевания Выделение НТМБ из закрытого очага, при получении пробы в стерильных условиях (абсцесс, биопсия, операционный материал, ликвор, экссудат) Относительные: Диагноз НТМБ можно ставить и по однократному выделению нетуберкулезных микобактерий, если имеются клинико рентгено лабораторные признаки заболевания
17 Лечение НТМБ Лечение нетуберкулезного микобактериоза очень длительное, поликомпонентное Терапия высокозатратная Источник финансирования на проблему не ясен (бюджет? ОМС? другие источники?)
18 Лечение НТМБ сложное и достаточно длительное Поликомпонентная антбактериальная терапия (комбинация антибиотиков и противотуберкулезных препаратов) К сожалению спектр ПТП ограничен из за устойчивости НТМБ к большинству ПТП An Official ATS/IDSA Statement: Diagnosis, Treatment and Prevention of Nontuberculous Mycobacterial Diseases Am J Respir Crit Care Med Vol
19 Лечение НТМБ с доказанной эффективностью Вид НТМБ Режим антибактериальной терапии МАС Кларитромицин мг/день или азитромицин 600 мг день; этамбутол 15 мг/кг; рифампин 600 мг/рифабутин 300 M. kansasii Рифампин 600 мг; этамбутол (15 мг/кг); изониазид 300 мг Срок мес Кларитромици н +/- Степень доказательности 12 + A II 12 - A II An Official ATS/IDSA Statement: Diagnosis, Treatment and Prevention of Nontuberculous Mycobacterial Diseases Am J Respir Crit Care Med Vol
20 Диссеминированная MAC инфекция Кларитромицин + этамбутол (35 больных с МАС инфекцией) или Азитромицин + этамбутол (24 больных с МАС инфекцией) Рандомизированное open label исследование, 10 центроввсша, гг. 59 пациентов Исследование прекращено досрочно в связи с появлением существенного различия между группами в связи с исчезновением бактериемии. Исчезновение бактериемии на 16 й неделе лечения: Кларитромицин + этамбутол у 85,7% пациентов Азитромицин + этамбутол у 37,5% пациентов Время (медиана) до исчезновения бактериемии: Кларитромицин + этамбутол 4,38 недель Азитромицин + этамбутол более 16 недель Нежелательные эффекты: Кларитромицин + этамбутол 9% (3/35) пациентов Азитромицин + этамбутол 8% (2/24) пациентов P = 0,007 P = 0,0018 Ward TT. et al. Randomized, Open Label Trial of Azithromycin Plus Ethambutol vs. Clarithromycin Plus Ethambutol as Therapy for Mycobacterium avium Complex Bacteremia in Patients with Human Immunodeficiency Virus Infection. Clinical Infectious Diseases 1998;27:
21 Кларитромицин обеспечивает более высокую концентрацию в альвеолоцитах, в сравнении с азитромицином (данные по однодозовым исследованиям, пероральный прием) LConte J. et al. Single Dose Pulmonary Pharmakokinetics of azithromycin, clarithromycin, ciprofloxacin and cefuxime in volunteer subjects. Antimicrob Agents and Chemotherapy 1996;40(7); p
22 Выживаемость среди пациентов, которые получали лечение MAC инфекции различными схемами полихимиотерпии Дизайн: многоцентровое, рандомизированное open label исследование III фазы исследование 3 режимов терапии MAC инфекции у пациентов со СПИДом. 160 пациентов с диссеминированной формой MAC инфекции, лечение в течение 48 недель Кол во пациентов и время (недели) между рандомизацией и смертельным исходом указаны под графиком. P = 0,02. C, кларитромицин; E, этамбутол; R, рифабутин. Benson C A et al. Clin Infect Dis. 2003;37:
23 MAC инфекции, комбинированное лечение (1?; 2; 3; 4?) MAC инфекция с образованием очагов/бронхоэктазов 1. Макролид Кларитромицин 1000 мг 3 р/нед ИЛИ Азитромицин мг 3 р/нед MAC инфекция с образованием полостей в легких Кларитромицин 1000 мг 1 р/день ИЛИ Азитромицин мг 1 р/день Тяжелая или ранее леченная MACинфекция Кларитромицин 1000 мг 1 р/день ИЛИ Азитромицин мг 1 р/день 2. Этамбутол 25 мг/кг 3 р/нед 15 мг/кг 1 р/день 15 мг/кг 1 р/день 3. Рифамицин Рифампин 600 мг 3 р/нед Рифампин мг 1 р/день 4.Аминогликозид в/в НЕ НАЗНАЧАЕТСЯ Амикацин или стрептомицин 25 мг/кг 2 3 р/нед ИЛИ без их добавления Рифабутин мг 1 р/день или Рифампин мг 1 р/день Амикацин или стрептомицин 25 мг/кг 2 3 р/нед Griffith et al. ATS/IDSA Statement Diagnosis, Treatment, and Prevention of Nontuberculous Mycobacterial Diseases 2007 Am J Respir Crit Care Med 2007 Vol 175. pp ,
24 Длительность терапии при МАС инфекции у больных ВИЧинфекцией (рекомендации CDC, 2013 г.) Терапия МАС инфекции у ВИЧ инфицированных двухэтапная (фаза индукции и фаза поддерживающая) Критерии для прекращения терапии (AII): Длительность терапии не менее 12 месяцев И Отсутствие признаков MAC инфекции И Количество CD4 > 100 клеток/мл на фоне АРВТ более 6 месяцев *Panel on Opportunistic Infections in HIV Infected Adults and Adolescents. Guidelines for the prevention and treatment of opportunistic infections in HIV infected adults and adolescents:recommendations from the Centers for Disease Control and Prevention, the National Institutes of Health, and the HIV Medicine Association of the Infectious Diseases Society of America.Available at Accessed ( ) [pp ]
25 Макролиды и антиретровирусные препараты (лекарственные взаимодействия) При назначении кларитромицина для лечения МАС инфекции наиболее предпочтительно включить в качестве третьего препарата ИП ВИЧ. В этом случае нет необходимости коррекции дозы у пациентов без нарушения функции почек. При назначении кларитромицина и препаратов группы ННИОТ происходит снижение дозы кларитромицина. Значение взаимодействия препаратов на эффективность лечения неизвестно. Желательно воздержаться от совместного назначения. Одно из свойств азитромицина отсутствие действия на систему цитохрома P450. Азитромицин характеризуется низким потенциалом взаимодействия с другими препаратами. Поэтому, при наличии клинически значимых лекарственных взаимодействий кларитромицина и АРВТ (например при выраженном нарушении функции почек) принимается решение о возможности замены кларитромицина на азитромицин. Panel on Opportunistic Infections in HIV Infected Adults and Adolescents. Guidelines for the prevention and treatment of opportunistic infections in HIV infected adults and adolescents:recommendations from the Centers for Disease Control and Prevention, the National Institutes of Health, and the HIV Medicine Association of the Infectious Diseases Society of America.Available at Accessed ( ) [pp ]
26 Клинико экспертные проблемы микобактериозов Сходство клинико рентгенологических проявлений и обнаружение в мокроте кислотоустойчивых микобактерий часто приводит больных микобактериозами во фтизиатрические учреждения Однако, исходя из имеющихся представлений об заболевании, пребывание больных НТМБ в противотуберкулезном учреждении небезопасно Высока вероятность заражения туберкулезом, особенно для больных ВИЧ инфекцией Нормативная и клинико экспертная база (длительность временной нетрудоспособности, критерии стойкой нетрудоспособности) по нозологии в РФ сегодня отсутствует Не определено кто осуществляет диспансерное наблюдение больных НТМБ (пульмонолог? фтизиатр? инфекционист? ) Отсутствуют национальные протоколы ведения таких пациентов
27 Благодарю за внимание! Зимина Вера Николаевна: vera
Читайте также:


