Хламидийный бронхит у беременной
Специфические инфекционные заболевания полового тракта у беременных значительно увеличивают частоту материнских и перинатальных осложнений. Такая инфекция, как хламидиоз, ассоциированная с микоплазмами, цитомегаловирусная, герпесвирусная инфекции, а такж
Специфические инфекционные заболевания полового тракта у беременных значительно увеличивают частоту материнских и перинатальных осложнений. Такая инфекция, как хламидиоз, ассоциированная с микоплазмами, цитомегаловирусная, герпесвирусная инфекции, а также их сочетание с бактериальными поражениями являются одной из ведущих причин перинатальной смертности (Королева А. И., 2000; Стрижаков А. Н. и соавт., 2003). В последние годы возросло число хламидийной, вирусной, микоплазменной и смешанной инфекций, борьба с которыми представляет значительные сложности в связи с развивающейся устойчивостью микроорганизмов к антибиотикам и особенностями ответных реакций организма (Глазкова Л. К., 1999; Рюмин Д. В., 1999; Семенов В. М., 2000; Хрянин А. А., 2001; Johnson R. A., 2000).
По-прежнему высокой остается частота урогенитального хламидиоза у беременных, колеблющаяся от 3% до 74% по данным различных авторов (Асцатурова О. Р., 2001; Прилепская В. Н. и соавт., 1998; Семенов В. М., 2000; Hiltunen-Back E., 2001; Stamm W. E., 1999).
В настоящее время доказано, что Chlamydia trachomatis является облигатным паразитом человека. Заражение происходит при половом контакте, редко — бытовым путем (Плиева З. А., 2000; Morion R. S., Kinghom G. R., 1999).
Хламидийная инфекция ведет к прерыванию беременности, невынашиванию, развитию фетоплацентарной недостаточности, внутриутробному инфицированию (ВУИ) плода, послеродовым воспалительным заболеваниям, неонатальным инфекциям.
В I триместре беременности наиболее характерным осложнением является угрожающий выкидыш, неразвивающаяся беременность и спонтанный аборт. Во II и III триместрах угроза прерывания беременности имеет длительное течение, а токолитическая терапия дает, как правило, нестойкий эффект. Это связано с инфицированием амниона хламидиями, которое встречается у 65% беременных. Тельца Chlamydia trachomatis выявлены во всех тканевых структурах плаценты женщин с генитальным хламидиозом. Отмечено, что пораженные хламидиями клетки обнаружены в просвете капилляров ворсин хориона, что указывает на возможный гематогенный путь передачи инфекции от матери к плоду. В плацентах женщин с генитальным хламидиозом происходит нарушение иммунного гомеостаза с образованием патогенных иммунных комплексов (ПИК), включающих IgM, IgG, IgA и фиксирующих С3-фракцию комплемента как маркер патогенности. Показано, что фиксация ПИК на мембранных структурах плаценты приводит к разрушению мембран синцития и плацентарного барьера. Последнее вызывает развитие плацентарной недостаточности и повреждение фето-плацентарной системы.
В случаях инфицирования амниотических оболочек может развиться многоводие, специфическое поражение плаценты (плацентит), плацентарная недостаточность, гипотрофия и гипоксия плода. Истинные пороки развития плода не являются патогномоничными для хламидийной инфекции.
Следует отметить, что при наличии более двух эхографических маркеров у новорожденного в 82% наблюдений постнатально диагностируется внутриутробная инфекция.
Для беременных с хламидийной инфекцией и фетоплацентарной недостаточностью первичными ее проявлениями являются нарушения внутриплацентарного кровотока.
Механизмы ВУИ при хламидийной инфекции включают следующие пути распространения инфекции:
- восходящий — при наличии специфического поражения нижних отделов полового тракта;
- нисходящий — при локализации воспалительного очага в области придатков матки;
- трансдецидуальный — при наличии инфекции в эндометрии;
- гематогенный — в большинстве случаев обусловлен способностью хламидий длительно персистировать в лимфоцитах периферической крови;
- контагиозный — прямая контаминация новорожденного при прохождении через родовой канал.
При отсутствии гипоксии плода и аспирации инфицированного содержимого родового канала риск развития тяжелой инфекции у новорожденного ниже, чем при длительном контакте плода с инфицированной средой во время беременности. Так, почти половина новорожденных от матерей с хламидиозом имеют клинически выраженную инфекцию.
К неонатальным проявлениям хламидийной инфекции относятся поражения кожи и слизистых (конъюнктивит), пневмония, отит, вульвит, уретрит. У недоношенных детей возможно развитие специфического миокардита после хламидийной пневмонии, описаны случаи хламидийного менингита и энцефалита.
В зависимости от пути заражения и инфицирующей дозы, проявления перинатальной хламидийной инфекции могут встречаться не только в первые 168 ч жизни новорожденного (ранний неонатальный период), но и реализовываться в течение первых месяцев жизни ребенка.
Основным методом борьбы с подобными осложнениями является своевременное проведение рациональной этиотропной антибиотикотерапии.
В то же время подавляющее большинство (62–84%) генитальных инфекций имеют смешанную этиологию. Среди сопутствующих возбудителей наиболее часто выявляются микоплазмы и уреаплазмы, вирусы, анаэробы и грибы (возбудители нарушений микроценоза влагалища). В связи с этим для лечения инфекций, передаваемых половым путем (ИППП), должны использоваться антибактериальные препараты с высокой биодоступностью и активностью в отношении других бактериальных возбудителей с внутриклеточной персистенцией. Различный спектр осложнений беременности, ассоциированных с инфекционным процессом и многоочаговость поражений, присущая хламидиозу, требует комплексных подходов к терапии.
Пациенткам с бактериальными ИППП чаще всего назначают системную терапию антибактериальными препаратами с учетом предполагаемой или определяемой чувствительности возбудителя.
Общими положениями являются преимущественное использование макролидов как препаратов выбора для лечения хламидийной, микоплазменной и уреаплазменной инфекций у беременных, начало лечения после 20 нед гестации или в III триместре беременности.
Для лечения урогенитального хламидиоза в гинекологической практике используют тетрациклины, фторхинолоны и макролиды. Применение тетрациклинов и фторхинолонов во время беременности и лактации противопоказано из-за наличия неблагоприятных эффектов для эмбриона, плода и новорожденного.
Для лечения беременных с генитальными инфекциями применяются такие антибиотики группы макролидов, как эритромицин, спиромицин и джозамицин, использование которых с учетом срока гестации безопасно для матери и плода.
Одним из наиболее изученных с точки зрения безопасности у беременных является макролидный антибиотик джозамицин (Вильпрафен). Важное клиническое значение имеет его высокая активность против таких внутриклеточных патогенов, как C. trachomatis, M. hominis, M. genitalium, U. Ureallyticum. Джозамицин быстро и полностью всасывается из желудочно-кишечного тракта (ЖКТ), создавая максимальную концентрацию в плазме крови уже через 1 ч. Важным аспектом, определяющим успех лечения, является достижение высоких концентраций препарата в тканях по сравнению с плазмой крови. Способность джозамицина накапливаться преимущественно в фагоцитирующих клетках особенно важна для элиминации внутриклеточных возбудителей. Доказано, что фагоциты доставляют джозамицин в места локализации инфекционного агента, где действующее вещество освобождается в процессе фагоцитоза, причем концентрация джозамицина в очаге инфекции на 30% выше, чем в здоровых тканях. В отличие от ряда препаратов данного класса джозамицин не стимулирует двигательную функцию кишечника и не ингибирует такие важнейшие компоненты метаболической системы печени, как цитохром Р 450 и НАДФ-цитохром С-редуктазу. Таким образом, джозамицин отличают оптимальный спектр активности в отношении урогенитальных патогенов, благоприятная фармакокинетика и высокая безопасность, в том числе у беременных.
Следует отметить, что в настоящее время бактериостатический антибиотик эритромицин практически не используется для лечения урогенитального хламидиоза, так как его микробиологическая эффективность зачастую не превышает 30% (Асцатурова О. Р. и соавт., 2001; Страчунский Л. С., 1998; Ridgway G. L., 1995).
С целью выявления частоты генитальных инфекций, факторов риска их развития, приводящих к осложнениям беременности, родов и их исходов для новорожденного, было проведено обследование 5430 беременных на базе родильного дома и консультативно-диагностического центра при ГКБ № 7 с 1997 по 2005 г.
Контрольную группу составили 200 женщин с отсутствием генитальных инфекций в анамнезе и во время беременности, у детей которых не были диагностированы инфекционно-воспалительные заболевания в раннем неонатальном периоде.
Частота встречаемости заболеваний, передаваемых половым путем, составила 17,85% (969). Структура ИППП у беременных была представлена хламидийной (24,56%), микоплазменной (8,36%), уреаплазменной (3,1%), трихомонадной (4,85%), смешанной (59,13%) инфекциями.
Острые и обострения хронических вирусных заболеваний наблюдались в 10,24% (556 случаев) и были представлены герпетическими поражениями в 8,34%, цитомегаловирусной инфекцией — в 0,78% и папилломавирусной инфекцией — в 1,12%.
Высокая частота смешанных инфекций при хламидиозе, наличие малосимптомного и латентного его течения приводит к необходимости комплексной диагностики ИППП и нарушений микроценоза влагалища.
Ни один из современных методов диагностики хламидиоза не обеспечивает 100% надежности. Поэтому лабораторная диагностика должна основываться на сочетании минимум двух методов, одним из которых должен являться метод полимеразной цепной реакции (ПЦР).
Непосредственная идентификация элементарных телец (ЭТ) и ретикулярных телец (РТ) хламидий возможна при микроскопии мазков, окрашенных по Романовскому–Гимзе. Цитоплазматические включения определяются в виде микроколоний, окрашенных в темно-синий или розовый цвет (тельца Гальберштадтера–Провачека). Чувствительность цитологического метода обнаружения хламидий не превышает 10–12%. Метод позволяет оценить состояние микроценоза влагалища, количество лейкоцитов, выявить наличие дрожжеподобных грибов, влагалищных трихомонад.
Наиболее распространенный метод диагностики хламидийной инфекции — иммуноцитологический — основан на реакции прямой или непрямой иммунофлюоресценции (определение антигена С. trachomatis).
При его использовании к биологическому материалу добавляются меченые флюоресцинами моноклональные антитела. Полученные мазки оценивают под люминесцентным микроскопом. Чувствительность метода колеблется в пределах 65–90%, а специфичность — 85–90%. Главными недостатками метода являются его субъективность и низкая чувствительность.
Иммуноферментный анализ основан на идентификации антигенов хламидий путем связывания их антителами. Количественная оценка комплексов антиген-антитело проводится с помощью автоматизированного определения выраженности цветной реакции. Преимуществом метода является возможность определять растворимые антигены, время проведения (4–6 ч), недостатком — возможность получения ложноотрицательных и ложноположительных реакций.
ПЦР обладает преимуществами по сравнению с иммунологическими методами: высокая специфичность — 95%; максимальная чувствительность; быстрота проведения (4–5 ч). Недостатком ПЦР-диагностики хламидиоза является то, что метод амплификации ДНК не позволяет оценить жизнеспособность клетки, дает положительные результаты при малых количествах возбудителя и наличии отдельных фрагментов его генома. Несмотря на это первичным способом оценки элиминации хламидий должна являться ПЦР. При получении положительного результата показано проведение микробиологического исследования, а при невозможности последнего — повторная ПЦР через 5–6 нед.
Наиболее достоверным методом диагностики хламидиоза является сочетание культурального исследования и ПЦР.
К методам непрямой диагностики хламидийной инфекции относится определение уровня специфических антител. Накопление антител классов М, G и А происходит через разные промежутки времени и зависит от характера инфицирования (первичная инфекция, реинфекция). При первичном инфицировании вначале появляются IgM, затем — G, потом — А. При вторичном инфицировании отмечается быстрое нарастание антител классов G и А на фоне отсутствия IgM. Этот метод исследования позволяет определить стадию заболевания, оценить эффективность проводимого лечения, доказать хламидийную этиологию экстрагенитальных поражений.
У 238 беременных острая хламидийная инфекция (длительность заболевания менее 2 мес) имелась у 79 (33,19%), хроническая (более 2 мес) — у 159 (66,8%). У большинства пациенток с хронической инфекцией (62%) имелись анамнестические данные, свидетельствующие о длительности заболевания более полугода и неадекватной предшествующей терапии.
Под нашим наблюдением в ходе проспективной части исследования находились 72 беременные со сроком гестации 29–41 нед, у 33 (45,83%) из которых предшествующая этиологическая терапия острой или хронической хламидийной инфекции была неэффективна, а также 28 (38,89%) женщин с хронической рецидивирующей инфекцией и 11 (15,28%) беременных, преждевременно прекративших ранее начатую терапию. До включения в исследование больные получали различную антибиотикотерапию: в первой подгруппе 16 (57,14%) беременных по поводу хламидийной инфекции принимали эритромицин по 1–3 г/сут, 9 — азитромицин по 0,25 г/сут, 8 — спирамицин по 9 млн ЕД/сут. Необходимо отметить неадекватность суточной дозы эритромицина и азитромицина для лечения хламидиоза.
Всем пациенткам после разъяснения особенностей течения хламидийной инфекции, ее опасности для беременной и плода, необходимости проведения антибактериальной терапии и лечения, направленного на купирование осложнений беременности, действия препарата джозамицина (Вильпрафен) и схемы его применения была назначена терапия, включавшая прием 1 таблетки (500 мг) Вильпрафена 3 раза/сут на протяжении 10 дней. Всем половым партнерам больных проводилось обследование и лечение генитальных инфекций. После терапии Вильпрафеном беременные в течение 3-х дней фиксировали возможные побочные эффекты препарата (тошнота, рвота, боль в животе, изменение характера стула, метеоризм, сыпь, кожный зуд).
Контроль за эффективностью терапии осуществляли на основании результатов ПЦР через 4 нед после приема Вильпрафена. Лечение считали эффективным при отсутствии обнаружения генома Chlamydia trachomatis. При положительных результатах первой ПЦР выполняли культуральное исследование (или ПЦР через 5–6 нед).
Микробиологическая эффективность применения джозамицина у беременных с хламидийной инфекцией по результатам первого контрольного обследования составила 93,06%. В трех наблюдениях при положительных результатах первой ПЦР не обнаружено роста C. trachomatis на культуре клеток McCoy. В течение 3 мес наблюдения микробиологически верифицированная персистенция хламидий после лечения сохранялась у 2 женщин (2,78%).
По сравнению с данными, полученными в контрольной группе, при хламидиозе имеются значимые отличия в частоте акушерско-гинекологической патологии во время беременности (рис. 1).
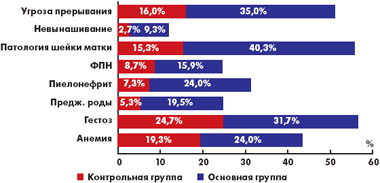 |
| Рис. 1. Осложнения беременности у женщин контрольной группы и с хламидийной инфекцией |
Осложнениями гестационного процесса, связанными с хламидийной инфекцией, считали угрозу прерывания беременности, преждевременные роды, фетоплацентарную недостаточность и задержку роста плода, эхографические маркеры внутриутробного инфицирования (изменение эхогенности плаценты, много- и маловодие, структурные дефекты развития плода). Кроме того, отмечена высокая частота сочетания хламидиоза с патологией шейки матки и инфекцией мочевыводящих путей.
После проведения лечения Вильпрафеном по указанной схеме (1500 мг/сут в течение 10 дней) зарегистрировано существенное снижение частоты осложнений беременности, родов, общей и инфекционной заболеваемости новорожденных (рис. 2).
 |
| Рис. 2. Частота осложнений беременности, родов и неонатальной заболеваемости после лечения хламидиоза Вильпрафеном |
Применение Вильпрафена для лечения урогенитального хламидиоза во время беременности, в том числе после неэффективной терапии другими антибиотиками, приводит к микробиологической излеченности у 97,22% пациенток. Важно отметить, что такие высокие показатели эффективности лечения достигнуты в группе женщин с рецидивирующей и хронической хламидийной инфекцией. Кроме того, применение джозамицина возможно вне зависимости от срока беременности.
Особенностью хронической хламидийной инфекции является скудная симптоматика или полное отсутствие клинических проявлений заболевания, что приводит к поздней диагностике. В то же время нерациональная антибиотикотерапия не только обусловливает возникновение резистентности возбудителя, но и приводит к позднему началу адекватного лечения. Высокая частота ассоциированных с инфекцией осложнений требует проведения высокоинформативных методов диагностики хламидиоза и назначение этиотропной терапии в комплексном лечении беременных.
Частота перинатальных инфекций после использования Вильпрафена во время беременности снизилась в 2,4 раза. Не было отмечено случаев хламидийной пневмонии и генерализованной инфекции у новорожденных, матери которых получали терапию джозамицином.
Таким образом, у беременных с ИППП эхографические маркеры инфекции обнаруживаются почти в 30%. Частота фетоплацентарной недостаточности у этих женщин возрастает почти в 2 раза. Гемодинамические нарушения у беременных с восходящим инфицированием плода преимущественно регистрируются в плодово-плацентарном звене кровообращения.
Так как хроническая и рецидивирующая хламидийная инфекция приводит к изменениям фетоплацентарного комплекса, необходимо своевременно диагностировать хламидийные поражения и осуществлять комплексную терапию с учетом степени распространения процесса, срока беременности и наличия сопутствующих осложнений.
Лечение хламидийной инфекции у беременных с помощью джозамицина (Вильпрафена) уменьшает частоту материнских и перинатальных осложнений, имеет хорошую переносимость, обладает высоким удобством для соблюдения режима приема и психологического комфорта пациенток.
По вопросам литературы обращайтесь в редакцию.
П. В. Буданов, кандидат медицинских наук, доцент
ММА им. И. М. Сеченова, Москва
Многие будущие мамы недоумевают, когда им назначают анализы на инфекции, передающиеся половым путем, среди которых значится и хламидиоз: зачем их сдавать, если ничего не беспокоит?
Однако, несмотря на отсутствие проявлений, хламидиоз может отрицательно повлиять на течение беременности, здоровье малыша и роды.

Хламидиоз – это инфекционное заболевание, вызываемое хламидиями. Это совсем обычные микроорганизмы, живущие внутри клеток. Долгое время из-за очень маленького размера их считали вирусами, затем нашли сходство с бактериями, а в настоящее время и вовсе отнесли к одноклеточным паразитам. Хламидии внедряются в клетки орга- низма человека и разрушают их. Попав однажды в организм, они способны жить в нем долгие годы, зачастую не вызывая никаких проявлений, но, тем не менее, подрывая изнутри работу легких, кишечника, суставов, мозга, глаз и других органов.
Они вызывают воспалительные реакции, ведущие к спаечным процессам и истощению иммунной системы. Примерно в половине случаев хламидиоз про- текает бессимптомно, но довольно часто он дает о себе знать болями внизу живота и воспалением канала шейки матки.
Нередко при хламидиозе ак- тивизируются другие болезнетворные микроорга- низмы: золотистый стафилококк, энтеробактерии, грибковая флора, что вызывает различные, часто гноевидные выделения из половых органов.
• полимеразная цепная реакция (ПЦР) является наиболее чув- ствительным методом диагностики заболевания – взятый на анализ материал сканируется на наличие ДНК хламидии. При этом возможно исследование целого семейства хламидий, а не одного вида. Поэтому перед анализом важно узнать, покажет ли исследование тех хламидий, которые вызывают орнитоз и другие болезни, передающиеся от птиц и животных;
• иммуноферментный метод (определение антител в крови);
• иммунофлюоресцентный метод (исследование соскоба под флуо- ресцентным микроскопом с обнаружением антигена хламидий);
• посев на культуре клеток (взятый материал размещают в особой среде и через несколько дней смотрят, есть ли хламидии) и не- которые другие методы.
На этот счет у специалистов единого мнения нет. Одни считают, что последствия этой инфекции ми- нимальны за счет работы фетоплацентарного ба- рьера, защищающего малыша от болезнетворных агентов, другие – что возможны очень серьезные нарушения. Например, развитие плацентарной не- достаточности, когда плацента не справляется со своей работой и плод не получает достаточного количества кислорода и питательных веществ. Помимо этого, хламидиоз может привести к преждевременному излитию околоплодных вод и слабости родовой деятельности.
Во время беременности обследование на хламидиоз не является обязательным, но будущим ма- мам с воспалительными заболеваниями половых органов, особенно в сочетании с проблемами в мочеполовой системе, его рекомендуется прой- ти. Также необходимо оно женщинам с невына- шиванием (предшествующими выкидышами), у которых были внематочные беременности и пре- ждевременные роды.
Если у будущей мамы найден хламидиоз, то требует- ся обязательное его лечение. Хронический хламиди- оз (в крови обнаружены антитела типа G) лечат в 20 и 30 недель беременности. Если же процесс острый (в крови обнаружены антитела типа М), лечение на- значают после 12 недель беременности.
Для борьбы с хламидиями используют антибиотики, разре- шенные для беременных женщин. Также врач может назначить препараты для поддержания иммунитета.
Мало кто знает, что хламидиоз передается не только половым путем. Существует множество видов хламидий, поражающих практически всех животных, птиц, рыб, амфибий, рептилий, мол- люсков и даже насекомых, и многие из этих воз- будителей передаются человеку, вызывая пнев- монии, бронхиты, болезни желудочно-кишечного тракта, глаз, рождение ослабленных деток и даже прерывание беременности. И неважно, под ка- ким названием скрывается хламидиоз: псит- такоз, орнитоз, попугайная болезнь или что-то иное.
Птицы, в част- ности, городские голуби, разносят заболевание буквально по всему свету. В организм человека инфекция проникает через дыхательные пути или рот. Очень часто хламидии ютятся на частичках пыли, с которыми и путешествуют по миру, ища но- вых хозяев.
Очень быстро хламидии проникают в кровь, вызывая симптомы общей интоксикации и поражение различных органов – легких, печени, селезенки, нервной системы и матки. При воз- никновении заболевания у беременной женщи- ны внутриутробного заражения малыша не про- исходит и пороков развития у него не возникает.
Однако болезнь может осложнить течение бере- менности. Тяжелые формы орнитоза, особенно в первые месяцы беременности, могут привести к ее самопроизвольному прерыванию. Кроме того, влияние на плод могут оказать антибиотики, на- значаемые для лечения, которое, кстати, прово- дят в инфекционном отделении стационара. Так что если в вашей семье есть домашний пи- томец, его диагностика на хламидиоз является важной частью спокойного протекания беремен- ности.
Для диагностики хламидиоза у животных применяются те же методы, что и для человека. А основой профилактики будет ограничение кон- тактов с домашними животными и соблюдение правил личной гигиены после общения с ними. Также надо следить, чтобы ваши питомцы не кон- тактировали с дикими и бродячими особями, не позволяйте им ловить птиц и лягушек.
Все права защищены и охраняются законом. Товарный знак №395740 от 2008 г. ООО "ШАНС БИО"
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
ММА имени И.М. Сеченова
П о данным ВОЗ, частота обнаружения Chlamydia trachomatis у беременных колеблется в очень широких пределах (от 2 до 37%), в среднем составляя 6-8% [11]. С. trachomatis передается преимущественно половым путем и обладает выраженным тропизмом к цилиндрическому эпителию. Поэтому наиболее частыми клиническими проявлениями являются уретрит и слизисто-гнойный цервицит. При распространении инфекционного процесса могут наблюдаться бартолинит, эндометрит, сальпингит, иногда проктит и некоторые другие более редкие формы заболевания [19]. Однако у 60% женщин хламидиоз протекает абсолютно бессимптомно [20].
Данные о возможном влиянии хламидийной инфекции на течение и исход беременности чрезвычайно противоречивы. Одни авторы указывают на увеличение частоты невынашивания беременности и мертворождаемости, другие категорически отрицают это [1,3,9,16]. Что не подлежит сомнению, так это тот факт, что урогенитальный хламидиоз беременных является существенным фактором риска развития хламидийной инфекции у новорожденных. Заражение происходит в 60-70% случаев, преимущественно интранатально при прохождении плода через инфицированные родовые пути. При этом у 20-50% детей, рожденных женщинами с хламидиозом, в первые две недели жизни развивается конъюнктивит, а у 10-20% на 1-3 месяц жизни хламидийная пневмония [17, 25].
В результате, учитывая высокую распространенность урогенитального хламидиоза беременных и его значительную роль в развитии осложнений у матери и плода, целесообразность антибактериальной терапии хламидийной инфекции в настоящее время не вызывает сомнений. Однако выбор препаратов для лечения инфекции, вызванной Chlamydia trachomatis, у беременных значительно ограничен, так как многие из них могут вызывать тератогенный эффект или оказывать эмбрио- и фетотоксическое действие [19].
Поскольку известны противопоказания к применению во время беременности высокоэффективных в отношении Chlamydia trachomatis антибиотиков тетрациклинового ряда и хинолонов, чаще всего для лечения беременных используется эритромицин [24]. Эффективность эритромицина достаточно высока - 83-95% [8,13]. Однако, по данным различных авторов, побочные эффекты со стороны желудочно-кишечного тракта наблюдаются у 38-58% пациенток, что нередко приводит к отказу от приема этого препарата. Кроме того, высокая курсовая доза и необходимость многократного приема значительно ограничивают применение эритромицина [5, 23].
Американский центр по профилактике и контролю за заболеваниями (CDC) рекомендует проводить начальный курс терапии эритромицином, а в качестве препарата второй линии, в случае неэффективности проведенного лечения, использовать амоксициллин [8]. Этот препарат показал себя безопасным во время беременности и эффективным для лечения хламидийной инфекции - в нескольких исследованиях он продемонстрировал эффективность 85-99% в сочетании со снижением частоты побочных эффектов (1,5-12,8% в сравнении с таковой при приеме эритромицина 23,1-31,6%) [6, 12].
Антибактериальная терапия хламидиоза у беременных
CDC, Sexually transmitted diseases, 2002
Эритромицин 500 мг х 4 раза в сутки - 7 дней перорально или амоксициллин 500 мг х 3 раза в сутки - 7 дней перорально.
Эритромицин 250 мг х 4 раза в сутки - 14 дней перорально или азитромицин 1 г однократно перорально.
Однако следует отметить, что in vitro пенициллины оказывают неполный ингибирующий эффект по отношению к Chlamydia trachomatis, в связи с чем возникает необходимость в повторном культуральном исследовании с целью установления излеченности через 3-4 недели после окончания терапии амоксициллином [22]. Кроме того, пенициллины воздействуют на жизненный цикл хламидий в фазу превращения метаболически активных ретикулярных телец в элементарные тельца, вызывая при этом образование аномальных включений с последующей продукцией белков теплового шока (HSP60). Данные вещества, в свою очередь, активируют дендритные клетки и запускают иммунологический ответ. Лечение больных пенициллинами, таким образом, не только недостаточно эффективно, но и чаще приводит к развитию синдрома Рейтера [14].
W.J. Hueston и соавт. [10], проводившие анализ по выбору антибактериальной терапии хламидийной инфекции во время беременности, считают рекомендуемую схему экономически невыгодной и приводящей к наиболее низкому уровню эффективности лечения (13,6 случаев безуспешной терапии на 1000 пролеченных пациенток). При оценке лекарственных средств с этой точки зрения авторами учитывалась общая стоимость лечения, включая затраты на культуральное исследование до и после проведения терапии, на курсовые дозы антибиотиков, а также процент случаев неудач.
Наиболее эффективной и экономичной признана следующая стратегия терапии: начальный курс амоксициллина по 500 мг три раза в сутки в течение семи дней с последующим однократным приемом азитромицина в дозе 1 г для пациенток с персистирующей хламидийной инфекцией. Уровень неизлеченности при применении данной схемы составляет 4,8 на 1000 пациенток.
Использование азитромицина представляется сейчас наиболее перспективным направлением в терапии урогенитального хламидиоза беременных. Этот антибиотик группы макролидов обладает уникальными характеристиками: высоким уровнем всасывания и устойчивостью в кислой среде, высокой концентрацией в тканях, продолжительным периодом полувыведения, возможностью проникновения внутрь клетки, где локализуется возбудитель хламидиоза, и способностью блокировать фазу превращения элементарных телец хламидий в метаболически активные ретикулярные тельца [14].
Ряд сравнительных рандомизированных исследований подтверждают высокую эффективность азитромицина при однократном пероральном приеме в дозе 1 г (97-100%), значительное снижение частоты побочных эффектов со стороны желудочно-кишечного тракта (7,4% в сравнении с таковой при использовании эритромицина 38,8%), отсутствие неблагоприятного влияния на плод [5, 23]. В многоцентровом исследовании, включавшем 347 пациенток, микробиологическая излеченность при применении азитромицина была достигнута в 97% случаев, а клиническая излеченность в 86% случаев. В то же время, по данным Stamm и соавт. [21], у 3 беременных через 5 недель после окончания терапии вновь была выделена Chlamydia trachomatis. Однако в данном случае нельзя однозначно говорить о рецидиве инфекций, так как невозможно достоверно исключить факт реинфецирования. Тем не менее, максимальная (из имеющихся в наличии в настоящее время лекарственных средств) терапевтическая и экономическая эффективность в сочетании с хорошей переносимостью, удобством применения и безопасностью позволяют рассматривать азитромицин, как препарат выбора в лечении урогенитального хламидиоза беременных.
Из макролидов, помимо эритромицина и азитромицина, для лечения хламидийной инфекции во время беременности G. Rigway [18] предлагает использовать джозамицин по 500 мг 2 раза в сутки в течение 7 дней. Данные российских ученых (Ю.К. Скрипкин и соавт. [4], Н.С. Потекаев и соавт. [2]) демонстрируют клиническую эффективность препарата от 97,2% до 100%, которая гарантируется высокой концентрацией джозамицина в тканях, а также его безопасность для беременных женщин и детей. Однако представленные исследования не являются плацебо-контролируемыми, что снижает их достоверность, а главное - малочисленность групп беременных женщин не позволяет оценить реальную безопасность этого препарата. Клинический же опыт применения джозамицина для лечения хламидиоза во время беременности весьма ограничен, поэтому немногочисленные неблагоприятные перинатальные исходы могут остаться незамеченными.
Опубликованные в последнее время отдельные сообщения об использовании в терапии урогенитальной хламидийной инфекции у беременных рокситромицина по 300 мг в сутки и кларитромицина по 250 мг 2 раза в сутки в течение 7 дней также требуют подтверждения крупномасштабными рандомизированными исследованиями с использованием значимых критериев эффективности и безопасности [18].
Ряд работ посвящен опыту применения клиндамицина для терапии урогенитального хламидиоза во время беременности. По эффективности и безопасности этот препарат сопоставим с амоксициллином. Использование клиндамицина для курса инициальной терапии с приемом азитромицина, как препарата резерва, продемонстрировало низкий уровень неизлеченности (4,2 случая на 1000 пациенток), но данная стратегия оказалась значительно более дорогой в сравнении с остальными комбинациями и потому менее целесообразной [10, 15].
Обобщенные данные по проблеме терапии хламидийной инфекции у беременных представлены в систематическом Кокрановском обзоре, включающем 11 рандомизированных контролируемых исследований по анализу сравнительной эффективности применения эритромицина, амоксициллина и азитромицина у пациенток с хламидиозом во время беременности. Показатель микробиологической излеченности, свидетельствующий о ликвидации возбудителя и об отсутствии риска заболевания новорожденного или матери, составляет около 90% для всех исследованных антибиотиков (при применении плацебо - 12%).
Препаратом первого выбора назван эритромицин. Амоксициллин и азитромицин весьма перспективны, демонстрируют большую клиническую эффективность и меньшую частоту побочных реакций в сравнении с эритромицином, однако отсутствие долгосрочных крупномасштабных рандомизированных исследований эффективности и безопасности применения этих препаратов во время беременности ограничивает их широкое внедрение в рутинную клиническую практику [7].
Приоритетным направлением фармакотерапии урогенитального хламидиоза в настоящее время является определение соответствия воздействия антибиотиков характеристикам внутриклеточного жизненного цикла хламидий. Примечательно, что Chlamydia trachomatis завершает свой цикл развития, находясь в составе вакуоли инфицированной эпителиальной клетки и оставаясь, по-видимому, недоступной для воздействия большинства клеточных и гуморальных механизмов защиты. Неизвестно, способны ли антибиотики, проникающие внутрь клеток, уничтожать хламидий в вакуолях или их бактерицидная активность направлена на элементарные тельца, высвобождающиеся при естественной гибели инфицированных клеток. В частности, нет сомнений в том, что азитромицин и рокситромицин проникают в клетки, в особенности в макрофаги, и накапливаются здесь в высоких концентрациях. Однако до сих пор не имеется убедительных доказательств того, что эти препараты обладают более выраженной внутриклеточной активностью по отношению к хламидиям, чем другие антибиотики или факторы иммунной защиты. Фармакокинетические исследования в данном направлении особенно актуальны для решения вопроса о латентной хламидийной инфекции, имеющей место примерно у 4-11% беременных и требующей более интенсивного и длительного лечения [14].
1. Евсюкова И.И., Кошелева Н.Г., Башмакова М.А., Савичева А.М. и соавт. Хламидийная инфекция в акушерстве и перинатологии (диагностика, профилактика, лечение). // СПб. -1995. С. 9.
2. Потекаев Н.С., Пашинян М.Г., Пашинян А.Г., Потекаев Н.Н. Джозамицин(вильпрафен) в терапии урогенитального хламидиоза. // Вести. Дерматол. Венерол. -2000. №1 С.48-50.
3. Савичева А.М., Башмакова М.А. Урогенитальный хламидиоз у женщин и его последствия. // Медицинская книга. Москва - 1998, С.65-87.
4. Скрипкин Ю.К., Пашинян М.Г. Лечение джозамицином больных урогенитальным хламидиозом. // Вести. Дерматол. Венерол. -2000 №2 С.49-50.
5. Adair C.D., Gunter M., Stovall T.G. et al. Chlamydia in pregnancy: a randomized trial of azithromycin and erythromycin. // Obstet.Gynecol. -1998, Feb.; 91(2): 165-168.
6. Alary M., Loey J.R., Moutquih J.M. et al. Randomized prospective study comparing erythromycin and amoxycillin in the treatment of genital chlamydial infection in pregnancy//Lancet -1994.344: 1461-1465.
7. Brocklehurst P. Update on the treatment of sexually transmitted infections in pregnancy. //Int.J.STD AIDS 1999. 10:571-580.
8. Centers for Disease Control and Prevention Guidelines for treatment of sexually transmitted diseases // MMWR -2002, v-51, N-RR-6, P.34.
9. Fiest A., Sydler Т., Gebbers S.S. et al. No association of Clamydia with abortion. //J.Soc.Med. -1999, 92(5);237-238.
10. Hueston W.J., Lenhart J.G., A decision analysis to guide antibiotic- selection for Chlamydia infection during pregnancy. // Arch.Fam.Med -1997, 6(6): 551-555.
11. Kovacs L., Nagy E., Berbik I. Et al. The frequency and the role of Chlamydia trachomatis infection in premature labor. // Int/J/Gynaecol.Obstet. 1998. 62:47-54.
12. Magat A.H., Alger L.S., Nagey D.A., Hatch C., Lavchik J.C. Double-blinded randomized study comparing amoxicillin and erythromycin for treatment of Chlamydia trachomatis in pregnancy. // Obstet.Gynecol. -1993, 81: 745-749.
13. Miller J.M., Martin D.H. Treatment of Chlamydia trachomatis infections in pregnant women. // Drugs -2000. 60(3): 597-605.
14. Morton R.S., Kinghorn G.R. Genitourinary Chlamydial infection: a reappraisal and hypothesis. // Int/J/STD AIDS 1999. 10:765-775.
15. Nuovo J., Melnikow J., Paliescheskey M., King J., Mowers R. Cost-effectiveness analysis of five different antibiotic regimens for treatment of uncomplicated Chlamydia trachomatis cervicitis. // J. Am. board. Fam.Pract. -1995,8:7-16.
16. Rastogi S., Kapur S., Salhan S. et al. Chlamydia trachomatis infection in pregnancy: Risk factor for an adverce outcome. // Brit.J.Biomed.Scien. 1999. 56:94-98.
17. Ratelle S., Keno D., Hardwood M. et al. Neonatal chlamydial infections in Massachusetts, 1992-1993//Am. J.Prev.Med. 1997. 13: 221-224.
18. Rigway G. Treatment of Chlamydia trachomatis Infections. // Abstracts of Proceeding of the 4th Meeting jf the European Society for Chlamydia research. August 2000. Helsinki, Finland. 28-32.
Читайте также:


