Цитотоксические т-лимфоциты при вич
По функциональным признакам различают три типа лимфоцитов: B-клетки, T-клетки, NK-клетки.
- В-лимфоциты распознают чужеродные структуры (антигены) вырабатывая при этом специфические антитела (белковые молекулы, направленные против чужеродных структур).
- Т-лимфоциты выполняют функцию регуляции иммунитета. Т-помощники стимулируют выработку антител, а Т-супрессоры тормозят ее.
- NK-лимфоциты осуществляют контроль над качеством клеток организма. При этом NK-лимфоциты способны разрушать клетки, которые по своим свойствам отличаются от нормальных клеток, например, раковые клетки. Содержание Т-лимфоцитов в крови составляет 65-80 % от общего количества лимфоцитов, В-лимфоцитов — 8-20 %, NK-лимфоцитов — 5-20 %. В образовании антител центральная роль принадлежит B-лимфоцитам. При этом B-лимфоциты обеспечивают специфический приобретенный иммунитет совместно с другими малыми лимфоцитами — T-лимфоцитами, используя разнообразные механизмы, направленные в большинстве случаев на расширение пределов эффективности врожденного иммунитета.
Третья группа T-лимфоцитов распознает и разрушает клетки, инфицированные вирусами или иными внутриклеточно размножающимися патогенами. Этот тип CD8 T-лимфоцитов назван цитотоксическими T-лимфоцитами. Как правило, распознавание антигена T-клетками происходит только при условии его презентации на поверхности других клеток в ассоциации с молекулами MHC. В распознавании участвует специфичный к антигену T-клеточный рецептор, функционально и структурно сходный с тем поверхностным иммуноглобулином sIg, который у B-клеток служит антигенраспознающим рецептором. Свои функции воздействия на другие клетки T-лимфоциты осуществляют путем выделения цитокинов, которые передают сигналы другим клеткам, или в результате прямых межклеточных контактов. Как и в случае B-лимфоцитов, отбор и активация T-лимфоцитов происходят после контакта с антигеном, затем они проходят стадию клональной экспансии и превращаются в зрелые T-хелперы и цитотоксические T-лимфоциты, а также формируют обширную популяцию клеток памяти.
Одна из важных регуляторных функций T-лимфоцитов — это их способность стимулировать B-клетки к пролиферации и дифференцировке. Другая важная регуляторная функция T-клеток состоит в их способности угнетать иммунный ответ. При этом T-хелперы и T-супрессоры обнаруживают комплексный тип антигенной специфичности. Фундаментальным свойством T-клеток является их специфичность по отношению к продуктам главного комплекса гистосовместимости). Специфическое иммунологическое распознавание патогенных организмов — это всецело прерогатива лимфоцитов, поэтому именно они инициируют реакции приобретенного (специфического) иммунитета. В обычном мазке крови лимфоциты различаются как по размерам (диаметр 6-10 мкм), так и по морфологии. Варьирует отношение величины ядра к величине цитоплазмы (Я:Ц), а также форма самого ядра. В цитоплазме некоторых лимфоцитов могут содержаться азурофильные гранулы. При световой микроскопии мазков крови, окрашенных, например, гематологическим красителем Гимза, можно обнаружить два морфологически различных типа циркулирующих лимфоцитов: — относительно мелкие клетки, в типичном случае лишенных гранул и с высоким соотношением Я:Ц и — более крупные клетки с меньшим содержанием Я:Ц и содержащие гранулы в цитоплазме, известные как большие гранулярные лимфоциты.
Различают абсолютное и относительное увеличение числа лимфоцитов в крови (лимфоцитоз) . В последнем случае имеется лишь увеличение процента лимфоцитов в лейкоцитарной формуле без повышения их общего количества. Чаще встречается относительный лимфоцитоз, который наблюдается при всех лейкопениях, зависящих от нейтропении. Это имеет место при брюшном тифе, при анемии Бирмера, гриппе, некоторых хронических спленомегалиях, некоторых эндокринных заболеваниях (базедова болезнь, аддисонова болезнь и др.), алейкии, некоторых авитаминозах, голодании, алиментарной дистрофии, в период выздоровления после перенесенных острых инфекционных заболеваний, после различных профилактических прививок.
Увеличение процента лимфоцитов в крови одновременно с абсолютным лимфоцитозом наблюдается при доброкачественном течении туберкулеза, при хроническом и доброкачественном течении сифилиса, после подкожного впрыскивания адреналина, при коклюше (одновременно с выраженным лейкоцитозом).
Лимфоцитоз отмечают при некоторых редких формах язвенной ангины, так называемой лимфоцитарной ангины, при которой помимо высокого процента лимфоцитов в крови могут встречаться и юные формы их вплоть до лимфобластов, при лимфатических лейкемиях (лейкемических лимфаденозах), когда общее количество лейкоцитов может доходить до 300 000-500 000 и больше в 1 мм3 крови, а процент лимфоцитов достигать 90-95. При этом заболевании микроскопическое исследование крови обнаруживает в каждом поле зрения почти исключительно одни лимфоциты, причем наряду со зрелыми лимфоцитами встречаются в большом количестве более молодые формы их вплоть до лимфобластов.
Уменьшение количества лимфоцитов (лимфопения, или лимоцитопения) чаще всего является относительным и выражается низким процентом лимфоцитов в лейкоцитарной формуле при одновременном нейтрофильном лейкоцитозе. В этих случаях абсолютное количество лимфоцитов может быть нормальным или даже повышенным. Такая относительная лимфопения наблюдается при лейкемическом миелозе, при котором процент лимфоцитов может равняться 1-2 и даже меньше, но абсолютное количество их нередко значительно увеличено; при значительных нейтрофильных лейкоцитозах, например, при крупозной пневмонии, сепсисе и т. д. При острых инфекционных заболеваниях начинающееся повышение количества лимфоцитов наряду с появлением эозинофилов является благоприятным признаком, предвещающим выздоровление.
Абсолютная лимфопения, выражающаяся низким процентом лимфоцитов в лейкоцитарной формуле при нормальном или уменьшенном общем количестве лейкоцитов, встречается редко. Она может наблюдаться при тяжелых острых инфекционных заболеваниях, особенно при остром сепсисе, протекающем с лейкопенией, часто при кори, иногда во время приступа пароксизмальной гемоглобинурии, в случаях обширной деструкции лимфоидной ткани, например, при саркоме, раке, туберкулезе лимфатических узлов.
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Лимфоцитах или же Вам необходим осмотр? Вы можете записаться на прием к доктору – клиника Eurolab всегда к Вашим услугам! Лучшие врачи осмотрят Вас, проконсультируют, окажут необходимую помощь и поставят диагноз. Вы также можете вызвать врача на дом. Клиника Eurolab открыта для Вас круглосуточно.
Как обратиться в клинику:
Телефон нашей клиники в Киеве: (+38 044) 206-20-00 (многоканальный). Секретарь клиники подберет Вам удобный день и час визита к врачу. Наши координаты и схема проезда указаны здесь. Посмотрите детальнее о всех услугах клиники на ее персональной странице.
Если Вами ранее были выполнены какие-либо исследования, обязательно возьмите их результаты на консультацию к врачу. Если исследования выполнены не были, мы сделаем все необходимое в нашей клинике или у наших коллег в других клиниках.
Необходимо очень тщательно подходить к состоянию Вашего здоровья в целом. Есть много болезней, которые по началу никак не проявляют себя в нашем организме, но в итоге оказывается, что, к сожалению, их уже лечить слишком поздно. Для этого просто необходимо по несколько раз в год проходить обследование у врача, чтобы не только предотвратить страшную болезнь, но и поддерживать здоровый дух в теле и организме в целом.
Исследование включает в себя определение абсолютных и относительных значений субпопуляционного состава Т-лимфоцитов (CD3, CD4, CD8, CD45), количества Т-регуляторных лимфоцитов ( T-reg. Cells) соотношения Т – хелперы/Т – цитотоксические клетки и Т-клеток, несущих на своей поверхности маркеры активации CD38, HLA-DR. Рекомендуется к назначению для контроля показателей клеточного звена иммунной системы в динамике после комплексного иммунологического обследования.
Иммунофенотипирование, клеточный иммунитет, многоцветный клеточный анализ методом проточной цитометрии, Т-клетки, Т-хелперы, Т-цитотоксические клетки, Т-регуляторных лимфоциты.
Human Immune System, Immunophenotyping, Multicolor Flow Cytometry Cell Analysis, Human Leukocyte Differentiation Antigens, Human T cells, T helper cells, Cytotoxic T cells, T-reg Cells, Activation markers.
Метод исследования
Какой биоматериал можно использовать для исследования?
Общая информация об исследовании
Оценка клеточного состава (иммунофенотипирование) лимфоцитов крови человека - основной компонент в оценке иммунного статуса - выполняется методом проточной цитофлуориметрии.
Иммунофенотипирование - характеристика клеток при помощи моноклональных антител или каких-либо других зондов, позволяющих судить об их типе и функциональном состоянии по наличию того или иного набора клеточных маркеров.
Иммунофенотипирование лейкоцитов заключается в обнаружении на их поверхности маркеров дифференциации, или CD-антигенов. Лейкоциты экспрессируют ряд поверхностных и цитоплазматических антигенов, уникальных для своей субпопуляции и стадии развития. CD-антигены (англ. cluster of differentiation antigens) - это антигены на поверхности клеток, маркеры, отличающие одни типы клеток от других. Дифференциации этих антигенов изучены и стандартизованы, им присвоены определенные номера. CD могут быть распознаны с помощью соответствующих моноклональных антител. Используя флюоресцентно-меченые моноклональные антитела, связывающиеся с определенными CD, можно с помощью метода проточной цитометрии произвести подсчёт содержания лимфоцитов, относящихся к различным по функции или стадии развития субпопуляциям.
В основе проточной цитофлуориметрии лежит проведение фотометрических и флюоресцентных измерений отдельных клеток, пересекающих одна за другой вместе с потоком жидкости луч монохроматического света, обычно света лазера.
СD3
Этот маркер позволяет идентифицировать зрелые покоящиеся (интактные) Т-клетки и подсчитать общее количество Т-лимфоцитов. Количественная оценка субпопуляции CD3+ лимфоцитов имеет диагностическую значимость в следующих случаях:
- первичные и вторичные иммунодефициты;
- острые вирусные инфекции, включая ВИЧ;
- внутриклеточные бактериальные и паразитарные инфекционные заболевания (например, туберкулез, лепра, лейшманиоз);
- реакции отторжения трансплантатов и болезни "трансплантат против хозяина";
- лимфопролиферативные расстройства (острый Т-лимфобластный лейкоз).
При сахарном диабете довольно часто наблюдается снижение у больных процентного содержания и абсолютного числа СD3+ лимфоцитов.
СD4
Использование МКА к CD4 антигену дает возможность количественно охарактеризовать особый клон клеток, получивших название Т-хелперов/индукторов. СD4+ клетки в функциональном отношении делятся на два вида хелперных лимфоцитов: Т-хелперы 1-го порядка (Th1-клетки) и 2-го порядка (Th2-клетки). Различные CD4+ Т-клетки продуцируют разные наборы цитокинов. Th1-клетки (их называют еще клетками гиперчувствительности замедленного типа – ГЗТ) – цитокины для клеточного иммунного ответа: интерлейкин 2 (IL-2), IL-3, g-IFN, TNF-a, TNF-b, - среди которых дискриминантным цитокином является g-IFN. Th2 секретируют набор цитокинов, необходимый для гуморального иммунного ответа: IL-3, 4, 5, 6, 10, 13, TNF-b, - среди которых дискриминантным цитокином является IL-4.
Определение количества CD4+ клеток имеет значение в диагностике состояний, связанных с дефектами антителопродукции и реакций клеточноопосредованного иммунитета. Показателю числа CD4+ клеток отводится решающая роль для прогноза течения ВИЧ-инфекции.
Функциональное состояние CD4+ лимфоцитов тестируют по цитокиновому профилю: функциональная полноценность Th1-клеток подтверждается по секреции g-IFN, а Th2-клеток – по секреции IL-4.
СD8
Дифференцировочная молекула CD8 представляет собой гликопротеин, обнаруживаемый на поверхности тимоцитов и Т-лимфоцитов и участвующий в распознавании антигенных пептидов в контексте с молекулами главного комплекса гистосовместимости (MHC) класса I.
Клиническая значимость определения количества СD8+ лимфоцитов:
- вирусные инфекции (при определенной модификации имеется возможность количественной оценки вирусоспецифических цитолитических CD8+ Т-лимфоцитов);
- при ряде заболеваний большое прогностическое значение имеет соотношение между CD4- и CD8-субпопуляциями Т-лимфоцитов (иммунорегуляторный индекс CD4/CD8); например, прогрессирующее снижение иммунорегуляторного индекса у ВИЧ-инфицированных больных может свидетельствовать о переходе в СПИД;
- злокачественные новообразования;
- оценка эффективности проведенной вакцинации (в особенности противовирусными вакцинами).
До недавнего времени приписываемая субпопуляции CD8+ клеток супрессорная активность сейчас практически полностью отвергается. По данным большинства экспериментальных и клинических исследований считается, что существование какой-либо отдельной популяции Т-супрессорных клеток, даже без привязки к CD8-маркеру, маловероятно.
При аутоиммунных тиреоидитах, в частности при диффузном токсическом зобе (ДТЗ), в реакциях клеточного иммунитета отмечается снижение субпопуляции CD8+ лимфоцитов и снижение функциональной активности цитотоксических лимфоцитов.
При сахарном диабете также отмечается уменьшение функциональной активности и количества CD8+ лимфоцитов.
Снижение фракции СD8+ лимфоцитов наблюдается также у больных с первичной хронической недостаточностью коры надпочечников (болезнь Аддисона).
Анти-HLA-DR
Молекула HLA-DR также является маркером активации и принадлежит к МНС II класса. Она представляет собой трансмембранный гликопротеин, состоящий из a- и b-субъединиц, имеющих молекулярный вес 36 и 27 кД. Анти-HLA-DR реагирует только с эпитопом HLA-DR и не имеет перекрестных реакций с молекулами HLA-DQ и HLA-DP. Он экспрессируется на В-лимфоцитах, моноцитах, макрофагах, активированных Т-лимфоцитах.
Имеются данные о том, что молекула HLA-DR экспрессируется примерно на 10 % Т-лимфоцитах ПК, однако при активации клеток митогеном количество и плотность ее экспрессии резко возрастает. Существует предположение, что молекула HLA-DR на Т-клетках может выступать в качестве рецептора, участвующего в трансдукции сигнала активированными Т-лимфоцитами. Это наводит на мысль о ее возможной роли в качестве "профессиональной" АПК, участвующей в поддержании иммунной памяти.
HLA-DR также может присутствовать на клетках эпителия тимуса, на клетках В-лимфоцит-зависимых полей селезенки и лимфатических узлов, В-клеточной лимфомы. Этот антиген имеет коэкспрессию с CD1а антигеном на клетках Лангерганса.
CD25
Антиген CD25 известен как низкоаффинный рецептор ИЛ2, имеющий молекулярную массу 55 кД.
Молекула CD25, ассоциированная с b-цепью (CD122) и общей g-цепью (CD132), формирует высокоаффинный комплекс рецептора ИЛ-2. В процессе воспаления может вырабатываться растворимая форма ИЛ-2R. Маркер CD25 присутствует на субпопуляцях Т- и В-лимфоцитов периферической крови, в том числе на активированных макрофагах, НK. Его экспрессия резко возрастает при активации ФГА и КонА на поверхности CD3-активированных Т-лимфоцитов, на Т-клетках из смешанной культуры лимфоцитов, на инфицированных HTLV Т-лимфоцитах лейкемической линии при Т-лимфоцитарной лейкемии.
Метод позволяет определить количественное соотношение основных популяций Т-лимфоцитов:
- Т-лимфоциты (CD3 + CD19 - );
- Т-хелперы/индукторы ( CD3 + CD4 + CD45 + );
- Т-цитотоксические лимфоциты (Т-ЦТЛ) ( CD3 + CD8 + CD45 + );
- соотношение Т-хелперы / Т-цитотоксические лимфоциты (CD3 + CD4 + / CD3 + CD8 + ).
малые клеточные популяции, а также изучить их функциональную активность:
- активированные Т-лимфоциты (CD3 +HLA-DR + CD45 + );
- регуляторные Т-хелперные клетки (CD4 +CD25brigCD45 + ), выполняющие иммуносупрессорную функцию
- активированные цитотоксические Т-лимфоциты (CD3 +CD8brightCD38 + ) (% от всех Т-лимфоцитов)
- активированные Т-лимфоциты, экспрессирующие a-цепь рецептора ИЛ-2 (CD3 +CD25 +CD45 + ).
Когда назначается исследование?
Являясь реальными супрессорами, Т-регуляторные клетки играют ведущую роль во многих иммунологических процессах: регулируют Т-клеточный гомеостаз, предотвращают аутоиммунные заболевания, аллергии, гиперчувствительность, реакцию "трансплантат против хозяина". Вместе с тем регуляторные Т-клетки снижают противоопухолевый иммунитет и иммунитет к инфекциям.
Особый интерес представляют исследования, связанные с изучением соотношения аутоактивных клонов В-клеток и регуляторных Т-клеток при различной патологии воспалительного генеза. Так, при осложненном течении ряда патологических воспалительных процессов сохранение высокого уровня Т-reg и В1- клеток к 30-м суткам характеризует сохранение напряженности воспалительного процесса и, возможно, начало формирования дефекта функционирования Т-reg клеток, которое впоследствии может привести к хронизации воспаления и к развитию аутоиммунного процесса.
Таким образом, наличие и количественные характеристики этой популяции служат важным диагностическим признаком.
Рекомендовано для комплексного обследования пациентов, входящих в группу риска по четырем основным иммунопатологическим синдромам.
С инфекционным синдромом:
- частые ОРВИ, хронические инфекции ЛОР-органов (гнойные синуситы, отиты, периодически встречающиеся лимфадениты, пневмонии с тенденцией к рецидивированию, бронхоплевропневмонии);
- бактериальные инфекции кожи и подкожной клетчатки (пиодермии, фурункулез, абсцессы, флегмоны, септические гранулемы, рецидивирующий парапроктит у взрослых);
- урогенитальные инфекции;
- грибковые поражения кожи и слизистых оболочек, кандидоз, паразитарные инвазии;
- рецидивирующий герпес различной локализации;
- гастроэнтеропатия с хронической диареей неясной этиологии, дисбактериозом;
- длительный субфебрилитет, лихорадка неясной этиологии;
- генерализованные инфекции (сепсис, гнойные менингиты).
С аллергическим (атопическим) синдромом:
- атопический дерматит;
- нейродермит;
- экзема с инфекционным компонентом;
- тяжелая атопическая бронхиальная астма, поллиноз, хронический астматический бронхит.
С аутоиммунным синдромом:
- ревматоидный артрит;
- рассеянный склероз;
- диффузные заболевания соединительной ткани (системная красная волчанка, склеродермия, дерматомиозит);
- аутоиммунный тиреоидит;
- неспецифический язвенный колит;
С иммунопролиферативным синдромом:
- опухолевые процессы в иммунной системе (лимфомы, болезнь Ходжкина, острый и хронический лимфолейкоз, саркома Капоши).
Что означают результаты?
Изменения различных клеточных популяций лимфоцитов в сторону повышения или понижения развиваются при различных патологических процессах в организме, таких как инфекции, аутоиммунные и онкологические заболевания, иммунодефициты, в постоперационном периоде, при трансплантации органов.
Ниже представлена таблица с клиническими ситуациями, которые могут приводить к изменениям в субпопуляционном составе лимфоцитов.
Субпопуляция лимфоцитов
Повышение показателя
Снижение показателя
T-лимфоциты (CD3 + CD19 - )
• Острые и хронические инфекции;
• длительный прием лекарственных препаратов (особенно монотерапия);
• прием биологически активных добавок;
• интенсивные занятия спортом;
• Некоторые виды инфекций;
• алкогольный цирроз печени;
• прием иммуносупрессивных препаратов.
Т-хелперы (CD3 + CD4 + CD45 + )
• Ряд аутоиммунных заболеваний;
• отдельные Т-клеточные лейкозы;
• отравление солями бериллия.
• Иммунодефицитные состояния (основной лабораторный признак вторичного иммунодефицита);
• алкогольная болезнь печени;
• прием иммуносупрессивных препаратов или стероидов.
Т-цитотоксические лимфоциты (CD3 + CD8 + CD45 + )
• Некоторые вирусные инфекции;
• ряд Т-клеточных лейкозов;
• острая фаза аллергии;
• ряд аутоиммунных патологий.
• Некоторые виды аутоиммунных, аллергических заболеваний;
T-reg. (регуляторные Т-клетки (CD4+CD25brightCD45+)
(сахарный диабет 1-го типа, рассеянный склероз, ревматоидный артрит, аутоиммунный тиреоидит, неспецифический язвенный колит, болезнь Крона, миастения);
• аллергические заболевания (бронхиальная астма, атопический дерматит, пищевая аллергия).
Активированные Т-лимфоциты (CD3+HLA-DR+CD45+)
• алкогольный цирроз печени;
Не имеют диагностического значения.
В совокупности с клиническими данными, симптоматикой, другими методами лабораторных исследований вышеуказанные изменения являются диагностическим признаком возникновения этих патологических процессов в организме человека.
- Результаты данного исследования необходимо сопоставлять с клиническими данными и показателями других лабораторных анализов.
- Оценка показателей в динамике существенно повышает клиническую значимость исследования.
При ВИЧ-инфекции пациент регулярно сдает анализы крови.
Изначально они сдаются, чтобы подтвердить факт болезни. В дальнейшем – с целью её контроля.
Основные показатели – это:
- вирусная нагрузка (этот показатель меняется, в зависимости от прогрессирования болезни или успешности лечения);
- количество CD4 и соотношение CD4/ CD8 (отражает состояние иммунитета ВИЧ-инфицированных пациентов).
Проводятся также общеклинические исследования. Они нередко указывают на сопутствующие заболевания или побочные эффекты, развивающиеся в результате противовирусной терапии.
Общий анализ крови при ВИЧ: показатели
На основании ОАК при ВИЧ диагноз не ставится. Исследование имеет лишь вспомогательное значение.
Изменения наблюдаются в острой фазе ВИЧ. Снижается количество лейкоцитов. В наибольшей мере уменьшается концентрация в крови лимфоцитов. Но постепенно эти показатели восстанавливаются.
Следующие значительные изменения показателей ОАК можно будет выявить только на стадии СПИД.
В общеклиническом анализе крови может обнаруживаться:
- дефицит лейкоцитов;
- низкий уровень тромбоцитов;
- может понижаться гемоглобин и количество эритроцитов (хотя они обычно не опускаются ниже нормы);
- в лейкоцитарной формуле отмечается низкое содержание нейтрофилов и лимфоцитов.
Показатель СОЭ при ВИЧ
СОЭ – показатель, который возрастает при воспалительных реакциях в организме.

В норме он не должен превышать 10 мм/ч.
При недавнем заражении ВИЧ этот показатель может значительно возрастать. Дальше он постепенно приходит в норму.
СОЭ отражает активность иммунитета. Этот показатель соответствует уровню цитокинов. В том числе интерлейкина-6 и фактора некроза опухолей α. В дальнейшем по увеличению уровня СОЭ можно предположить повышение активности ВИЧ-инфекции. Потому что данный показатель возрастает в тот период, когда отмечается уменьшение числа CD4 клеток.
Но на практике СОЭ не имеет большого значения в диагностике. Потому что всем пациентам регулярно определяют уровень CD4 лейкоцитов. Их количество проверяется через каждые несколько месяцев.
СОЭ не является маркером острых интеркуррентных патологий при ВИЧ. Нередко даже значительное возрастание показателя до 100 мм в час и более не сопровождается никакими инфекциями или симптомами.
Биохимия крови при ВИЧ: показатели
Данный анализ не имеет большого значения в диагностике ВИЧ-инфекции. Он необходим в основном для оценки функции внутренних органов: почек, печени, поджелудочной железы и т.д.
Установлено, что у пациентов, страдающих ВИЧ, при снижении уровня CD4 в крови повышается уровень белка и альбумина. Остальные базовые показатели биохимического анализа крови у них в норме.
Однако на организм пациента влияет не только болезнь. Он постоянно принимает несколько антиретровирусных препаратов. Они могут оказывать побочные эффекты, влияя на функцию печени и почек.
В таких случаях возможно повышение в крови ряда показателей:

Чаще всего поражается печень. Потому что многие пациенты с ВИЧ наркозависимые. А наркотические вещества сами по себе оказывают гепатотоксическое действие.
Некоторые страдают также вирусным гепатитом С. В этом случае вероятность побочных эффектов со стороны печени возрастает.
Другие факторы риска:
- ожирение;
- пожилой возраст;
- высокий уровень трансаминаз на момент начала лечения;
- алкоголизм;
- низкий уровень тромбоцитов в крови;
- высокая вирусная нагрузка;
- недостаточность функции почек.
Признаки нарушения работы печени в биохимическом анализе крови при ВИЧ встречаются достаточно часто. Но тяжелая печеночная недостаточность развивается очень редко.
Такие случаи зафиксированы при использовании препаратов:
Иногда страдает функция почек. В этом случае возрастает уровень сывороточного креатинина. Причиной становится нарушение его секреции в проксимальных канальцах почек.
Такие побочные эффекты возможны при приеме:
- тенофира;
- атазанавира;
- индинавира (устаревший препарат, который почти не используется).
После отмены препаратов нефротоксические эффекты исчезают.
Вирусная нагрузка при ВИЧ: показатели
При острой ВИЧ-инфекции обычно отмечается стремительное увеличение виремии. Она достигает больше 100 миллионов копий РНК в мл.
Большинство патогенетических процессов происходят именно в эту фазу заболевания. Однако высокая вирусная нагрузка сохраняется недолго. Срабатывает иммунитет человека. А клетки, обеспечивающие репликацию вируса, погибают. Поэтому виремия начинает снижаться.
В течение нескольких недель она достигает значения, которое называют установочной точкой. Чем выше эта точка, тем хуже прогноз заболевания.
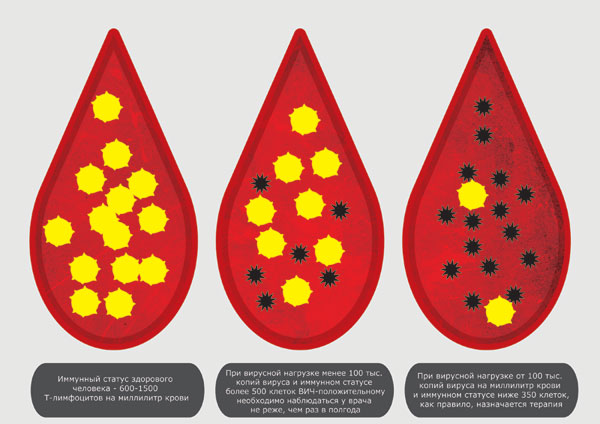
На величину установочной точки влияет:
- репликационная способность вируса;
- генетические факторы;
- врожденные особенности иммунитета.
В среднем после острого периода вирусная нагрузка составляет лишь 1% от исходного значения.
В дальнейшем она длительное время остается стабильной. Определяя уровень виремии через определенные промежутки времени, можно прогнозировать развитие заболевания. Исследования показывают, что если через 2 года вирусная нагрузка не превышает 1000 копий РНК в мл, то через 12 лет при естественном течении болезни у человека все ещё не будет стадии СПИДа.
Но если вирусная нагрузка через 2 года после инфицирования превышает 100 тысяч копий в мл, то 80% из них уже имеют СПИД-индикаторные заболевания.
От величины установочной точки зависит скорость падения уровня CD4-лимфоцитов. В норме этот показатель составляет от 435 до 1600 копий РНК в мл. В дальнейшем вирусная нагрузка возрастает.
Существует условная градация, когда её следует считать высокой, а когда – низкой.
Расшифровка – в таблице.
| Показатель | Вирусная нагрузка |
| До 10 000 копий РНК | Низкая |
| От 10 до 100 тысяч копий РНК | Средняя |
| Более 100 000 копий РНК | Высокая |
Обычно вирусная нагрузка коррелирует с уровнем CD4. Чем она выше, тем количество клеток иммунной системы в крови ниже. Вирусная нагрузка определяется регулярно. Она является показателем успешности лечения. Целью антиретровирусной терапии является достижение неопределяемого уровня виремии. То есть, тест ПЦР должен показывать отрицательные результаты.
Такие результаты могут быть достигнуты через 3-6 месяцев после начала лечения. Обычно неопределяемой считают нагрузку ниже 50 копий РНК в мл. Это граница чувствительности большинства тестов.
Показатели анализов при ВИЧ инфекции
При ВИЧ также сдают некоторые общеклинические анализы. Однако они нужны в большей мере для оценки функции внутренних органов, нежели для диагностики ВИЧ. Помимо общего и биохимического анализов крови сдаются анализы мочи.

Они помогают своевременно обнаружить поражение почек.
Некоторые препараты для антиретровирусной терапии способны спровоцировать почечную недостаточность. В этом случае уменьшается объем диуреза. Повышается плотность мочи.
Нефротоксические препараты также могут вызывать отложение конкрементов. В этом случае возможно появление солей в анализе мочи. Иногда в ней определяются эритроциты. Это происходит чаще после приступов почечной колики.
Иммунный статус при ВИЧ: показатели
При ВИЧ-инфекции страдают прежде всего показатели иммунитета.
В острой фазе заболевания происходит резкое снижение уровня CD4-лимфоцитов. Затем, после снижения виремии, количество этих клеток начинает постепенно восстанавливаться.
Однако без антиретровирусной терапии оно никогда не достигнет исходного уровня. Через неделю после заражения запускается каскад цитокиновых реакций. Наблюдается значительное возрастание количества цитокинов в крови. Они помогают держать под контролем инфекцию.
В этот же период увеличивается количество Т-лимфоцитов CD8. Они играют основную роль в сдерживании инфекции. А именно, убивают клетки, пораженные ВИЧ, с помощью цитолиза. Также они воздействуют они опосредованно, за счет увеличения продукции цитокинов.
На период возрастания популяции CD8-лимфоцитов приходится первичное уменьшение вирусной нагрузки. Т-клетки способны уничтожать вирус. Но он достаточно быстро мутирует, защищаясь от иммунитета. В дальнейшем иммунограмма для диагностики ВИЧ становится малоинформативной. Потому что показатели приближаются к нормальным значениям.
Если отклонения от нормы есть, то они незначительные. Обычно снижается общее число CD4-лимфоцитов.
Количество CD8-лимфоцитов может быть повышенным. Соотношение CD4/ CD8 уменьшается.
При ВИЧ оно составляет меньше единицы. Через несколько лет наступает стадия выраженного иммунодефицита (СПИД).
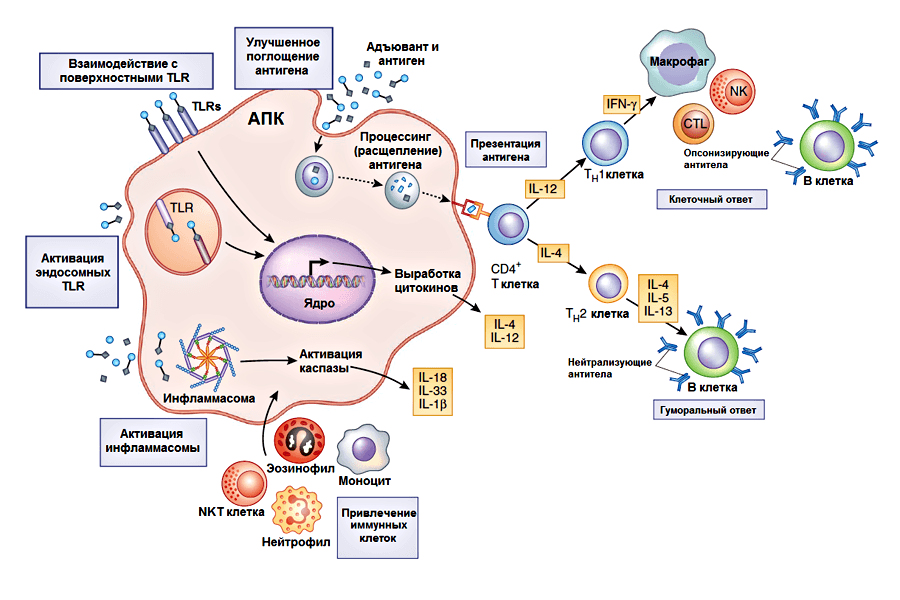
В этом случае в крови резко снижается количество CD4. В среднем у здорового человека их 800 до 1050 в мкл. Нормой считается содержание в крови CD4 от 500 до 1600 в мкл.
При ВИЧ их количество может снижаться до 200 в мкл и меньше. Общее количество Т-лимфоцитов уменьшается до 1000 и меньше в мкл.
Количество CD8 остается в пределах нормы. Поэтому соотношение CD4/ CD8 значительно уменьшается. В норме оно составляет 0,9-1,9. То есть, CD4 лимфоцитов должно быть в полтора-два раза больше, чем CD8. Но при ВИЧ их становится значительно меньше.
Антиретровирусную терапию обычно начинают при уровне CD4 ниже 350 в мкл.
Может также использоваться другой показатель для определения уровня иммунодефицита при ВИЧ. Это процент CD4 в общем количестве Т-лимфоцитов. Критическим значением является показатель 15%. Это означает, что следует начинать агрессивную антиретровирусную терапию. В том числе в случае, когда общее количество CD4 в иммунограмме остается высоким.
Существует прямая зависимость между вирусной нагрузкой и содержанием CD4 в крови. В среднем у человека на момент инфицирования этих клеток около 1000 в мл.
На пике острой фазы ВИЧ, когда вирусная нагрузка максимальная, количество CD4 снижается до 500 в мкл или меньше. Это происходит в среднем через 6 недель после инфицирования. Затем в течение последующих 9-12 месяцев начинается постепенное повышение CD4.
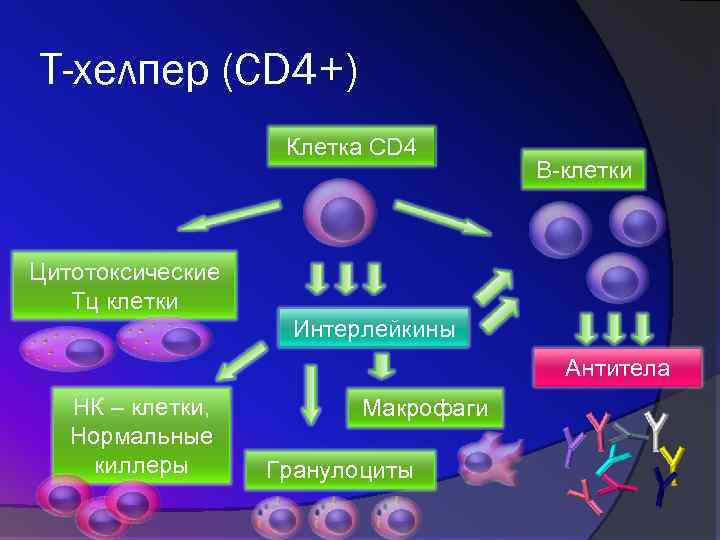
Оно достигает значения в 600-700 клеток в мл. Но затем снова начинает опускаться.
Снижение уровня CD4 происходит медленно, но неуклонно. В среднем через 5 лет после начала заболевания их уровень ниже 400 в мкл. Через 7 лет их уже меньше 200 в мкл.
По количеству этих клеток можно прогнозировать различные оппортунистические болезни. В прогностическом отношении имеет значение динамика изменения количества CD4.
В группу высокого риска входят пациенты, у которых число этих клеток уменьшается на 100 и более в мкл за 6 месяцев. Если за год их число снижается на 20-50 клеток в мкл, это средний риск.
Читайте также:


