Стрептококковый бактериофаг при мазке у женщин
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Инфекционная патология женских половых органов является наиболее актуальной проблемой акушерства, гинекологии и перинатологии, т. к. именно с ней связаны воспалительные заболевания гениталий, привычное невынашивание беременности, бесплодие, хронические тазовые боли, внутриутробная инфекция плода и новорожденного [1–4].
Этиологическая структура воспалительных заболеваний половых органов женщины крайне разнообразна. Спектр возбудителей включает в себя десятки видов всех классов микроорганизмов — бактерии, вирусы, простейшие и грибы [5, 6]. Преобладают смешанные инфекции, в составе которых частота бактериальных агентов и их ассоциаций превышает 60%. При внутриутробной инфекции резко увеличивается частота осложнений беременности, ассоциированных с бактериальными поражениями. Преобладают потери беременности и плацентарная недостаточность [3, 7, 8]. Среди инфекционных причин антенатальной смертности смешанные инфекции составляют 75% [2, 3, 7].
В последнее время стало понятно, что без использования современных достижений фундаментальной и клинической микробиологии решить проблему инфекционной патологии практически невозможно. Успехи в области молекулярной и биохимической вирусологии связаны с раскрытием стратегии вирусного генома, выявлением особенностей биосинтеза облигатных для бактерий паразитов — бактериофагов. Тем не менее, проблема профилактики и лечения различных острых и хронических, персистирующих бактериальных инфекций, до сих пор далека от окончательного разрешения [4, 5].
Важными вопросами являются выбор метода контроля за эффективностью лечения, определение критериев бактериологической излеченности, безопасность терапии [2, 4, 6, 9]. Неадекватная оценка тяжести течения инфекционного процесса и неправильно разработанная стратегия терапии приводят к развитию аутоиммунной патологии и хронизации воспалительных заболеваний [9–11].
В структуре патологии, связанной с персистирующими, рецидивирующими инфекциями, глобальной проблемой являются нарушения иммунитета. В настоящее время более 1/3 всей патологии человека протекает в сочетании с клиническими признаками иммунной недостаточности, что определяет тяжесть клинических проявлений заболевания, развитие осложнений и ухудшение прогноза. Именно снижение локальной и общей резистентности организма приводит к длительно существующим заболеваниям.
Изменение парадигмы иммунитета беременности создает длительно существующее повышение риска манифестации и рецидивирования персистирующих инфекций у беременных и новорожденных [1–3, 7].
В настоящее время основой правильной врачебной деятельности является использование принципов доказательной медицины, основывающейся на знании сочетания доказанной эффективности лечебных воздействий и подтверждения их безопасности. Именно оценка соотношения предполагаемой пользы и прогнозируемого (ожидаемого) риска является краеугольным камнем качественной клинической практики [2, 4]. Особенно высокие требования к безопасности назначаемого медикаментозного лечения предъявляются в акушерстве и педиатрии.
Широкое распространение антибиотикотерапии в середине XX в. имело свои преимущества за счет универсальности воздействия антибиотиков (широкого спектра их действия), возможности проведения эмпирической терапии и отсутствия устойчивых штаммов микроорганизмов.
В настоящее время проблема антибиотикорезистентности имеет критическое значение для всех областей клинической медицины. Полимикробная этиология инфекционных заболеваний в акушерстве и гинекологии, селекция резистентных штаммов возбудителей приводят к резкому снижению эффективности антибактериальных препаратов первого ряда выбора. Существующие рекомендации для лечения воспалительных заболеваний включают уже и применение нескольких антибактериальных препаратов [12].
Антибактериальная терапия может явиться причиной развития дисбактериоза. В случае применения антибиотиков на фоне дисбактериоза может усиливаться степень его выраженности. Кроме того, антибиотики снижают колонизационную резистентность влагалища и кишечника, увеличивают проницаемость слизистой оболочки, способствуя тем самым проникновению микроорганизмов в кровяное русло, внутренние органы и развитию вторичного очага инфекции и аллергизации организма [12, 13].
Назначение бактериофагов можно без преувеличений назвать высокоспецифичной антибактериальной терапией. Исторически единственными лекарственными средствами, подавляющими рост бактерий, были антибактериальные вирусы — бактериофаги. Препараты бактериофагов имеют хорошие перспективы в качестве альтернативы химиотерапевтической антибактериальной терапии. В отличие от антибиотиков они обладают строгой селективностью действия, не подавляют нормальную микрофлору, стимулируют факторы специфического и неспецифического иммунитета, что особенно значимо при лечении хронических воспалительных заболеваний или бактерионосительства.
бактериофаги содержат поликлональные вирулентные бактериофаги широкого диапазона действия, активные и в отношении бактерий, устойчивых к антибиотикам [18]. Фаготерапия может успешно сочетаться с назначением антибиотиков [19].
Для приготовления препаратов бактериофагов используют вирулентные фаги, выделенные из окружающей среды и адаптированные к гомологичным возбудителям [20].
В настоящее время в Российской Федерации зарегистрированы бактериофаги для лечения и профилактики кишечных инфекций — дизентерийный поливалентный, сальмонеллезный групп, А, В, С, D, Е, брюшнотифозный; против основных возбудителей заболеваний — стафилококковый, стрептококковый, клебсиеллезный, протейный, синегнойный, а также комбинированные препараты из нескольких видов бактериофагов: колипротейный, пиобактериофаг поливалентный, содержащий стафилококковый, стрептококковый, клебсиеллезный, протейный, синегнойный и коли бактериофаги, , включающий дизентерийный, сальмонеллезный, стафилококковый, энтерококковый, протейный, синегнойный и коли бактериофаги (табл. 1, 2).
Достоинство поливалентных (монокомпонентных) препаратов заключается в строгой специфичности действия, поскольку они вызывают гибель только своего конкретного вида бактерий и в отличие от антибиотиков не влияют на нормальную микрофлору влагалища и кишечника больного. Использование бактериофагов показало хорошие результаты при лечении и профилактике кишечных инфекций, дисбактериозов, заболеваний при хирургической, педиатрической, гинекологической, ЛОР и офтальмологической патологии. Отечественными неонатологами показана высокая эффективность фаготерапии инфекций у детей раннего возраста.
Поликомпонентные препараты бактериофагов наиболее удобны в клинической практике врача , принимая во внимание постоянное существование смешанных бактериальных ассоциаций [11, 17, 22].
После определения чувствительности бактерий к конкретному фагу можно использовать монокомпонентные поливалентные бактериофаги. Разнообразие механизмов резистентности к антибиотикам обусловливает возможность комбинированного применения химиопрепарата с антибактериальной активностью в сочетании с бактериофагом (). Особенно эффективна такая комбинация для разрушения микробных биопленок.
Препараты бактериофагов могут назначаться для профилактики и лечения инфекционных заболеваний, нарушений микроценоза, а также для предотвращения колонизации слизистых оболочек женских половых органов бактериями. В условиях роста антибиотикорезистентности можно рассматривать бактериофаги как успешную альтернативу антибиотикам [14, 15, 17, 22].
Комбинированные препараты фагов имеют более высокую активность литического действия на бактериальную клетку за счет синергизма действия отдельных фагов и обеспечивают получение лечебного эффекта при инфекциях, вызванных ассоциациями микробов.
Существуют разнообразные лекарственные формы бактериофагов: жидкие, таблетированные, гели. Хранятся бактериофаги при температуре от 2 до 10°С в сухом темном месте в течение лет. Важным условием, обеспечивающим результативность лечения фаговыми препаратами, является определение чувствительности к ним возбудителя [21].
Вирулентные бактериофаги, адсорбируясь на поверхности гомологичной микробной клетки, инъецируют свой генетический материал в ее цитоплазму, где интенсивно размножаются, используя структурные компоненты клетки, и разрушают ее. Далее зрелые фаговые частицы готовы к новому заражению, и литический процесс повторяется с новыми и новыми бактериальными клетками. Скорость инфицирования бактериальных клеток может достигать 1023 за 1 секунду [21].
Методика определения чувствительности микроорганизмов к бактериофагам
Определение фагочувствительности проводят на 1,5% агаре или агаре Хоттингера (для стафилококков и стрептококков в питательный агар добавляют 0,4% глюкозы). Дно чашки Петри с обратной стороны предварительно расчерчивают соответственно используемым фаговым препаратам.
Бактериальную суспензию суточной агаровой культуры (5 ед. по ОСО П) выделенного бактериального штамма равномерно распределяют по поверхности чашки Петри с хорошо подсушенной питательной средой. Излишек жидкости удаляют пастеровской пипеткой и подсушивают в зоне пламени горелки в течение 20–30 с.
На поверхность агара с впитавшейся культурой пастеровской пипеткой с тонко оттянутым концом наносят по 1 капле (0,03 мл) образца препарата бактериофагов. После подсыхания капель фагов чашки инкубируют в термостате при температуре 37°С в течение 18–20 ч, для бактерий рода Proteus — в течение 4–6 ч.
Учет и регистрация результатов проводятся по схеме:
+++ — полусливной лизис (незначительный рост культуры в зоне лизиса);
++ — наличие в месте нанесения капли фага более 50 колоний фага (пятна лизиса);
+ — от 20 до 50 колоний фага;
± — менее 20 колоний фага;
— полное отсутствие лизиса. Наличие зон лизиса ++++ и +++ свидетельствует о высокой чувствительности изучаемого штамма к фагу, ++ — умеренной, + — слабой чувствительности. Предпочтение должно быть отдано бактериофагам, вызывающим лизис с интенсивностью ++++ и +++ [17].
Являясь безвредным биологическим методом лечения, фаготерапия может применяться во время беременности, в периоде новорожденности и у детей раннего возраста.
В настоящее время в клинической медицине используют только литические формы бактериофагов, которые обладают бактерицидным действием и четким механизмом саморегуляции собственной популяционной активности.
Для получения положительных результатов использования бактериофагов необходимо предварительное исследование чувствительности к ним микроорганизмов. При использовании бактериофагов в крупных клиниках, больницах целесообразно включать их в состав производственных штаммов, на которых готовятся коммерческие препараты, госпитальные штаммы возбудителей заболеваний, характерных для данного стационара.
Всего в исследование включили 136 женщин. С воспалительными заболеваниями органов малого таза (ВЗОМТ) были 73 пациентки, 32 из которых получали стандартную антибактериальную терапию в сочетании с пероральным приемом Секстафага®, 41 — только противомикробные препараты. Критериями исключения явились тяжелое и осложненное течение инфекции.
Больных с рецидивирующими нарушениями микроценоза влагалища (63) также разделили на две группы: 28 женщин получали только Секстафаг®, 35 — только метронидазол интравагинально. Критерием исключения служило обнаружение вульвовагинального кандидоза.
Внутри подгрупп не было достоверных отличий по возрасту и соматической патологии. Наблюдение за пациентами продолжали на протяжении 6 мес.
Пиобактериофаг поливалентный (Секстафаг®) обладает способностью специфически лизировать микроорганизмы (стафилококки, стрептококки, патогенные кишечные и синегнойные бактерии), Proteus mirabilis, Proteus vulgaris, Klebsiella pneumoniae. Перорально препарат поливалентного бактериофага пациенты получали по 20,0 мл 2 р./сут на протяжении 10 дней. Пероральный прием предваряли приемом щелочной минеральной воды или раствором пищевой соды.
Интравагинально Секстафаг® вводили по 10,0 мл 2 р./сут на тампоне с экспозицией 60 мин на протяжении 10 дней.
В результате проведения исследования отмечено, что у больных ВЗОМТ, получавших комбинированную фагоантибиотикотерапию, продолжительность лечения сократилась в среднем до 5,8 cут, в то время как у пациентов только с антибиотиками продолжительность эффективного курса составила 8,7 сут.
Среди пациенток с рецидивирующими нарушениями микроценоза влагалища эффективность монотерапии в виде интравагинального введения полифага составила 85,7% (24 из 28). При назначении метронидазола интравагинально микробиологическая эффективность достигала 71,4% (25 из 35). Частота рецидивов бактериального вагиноза и неспецифического кольпита на протяжении 6 мес. наблюдения снизилась в 4,2 раза после применения поливалентного бактериофага.
Во время назначения препарата бактериофага не было отмечено аллергических реакций, немотивированного отказа от лечения. На фоне антибиотикотерапии только у одной пациентки развились диспептические явления, не потребовавшие дополнительного лечения и отказа от основной терапии.
Изолированно от проведения настоящего исследования выполнена оценка эффективности профилактического использования препарата с бактериофагами для профилактики рецидивирования вагинальных инфекций.
Принимая во внимание, что целевую когорту пациентов составили 32 женщины, демонстрируем предварительные результаты наблюдений, длившихся на протяжении не более 7 мес.
Антибактериальное средство Фагогин предназначено для профилактики вульвовагинальных инфекций и инфекционных заболеваний половых органов, а также является средством интимной гигиены. Использование средства Фагогин как средства профилактики особенно актуально у беременных для снижения риска манифестации и рецидивирования персистирующих инфекций.
Гель Фагогин вводился интравагинально по 5 мл 2–3 р./сут на протяжении 3–4 недель. Обязательной рекомендацией являлось использование геля Фагогин в качестве гигиенической процедуры после полового контакта.
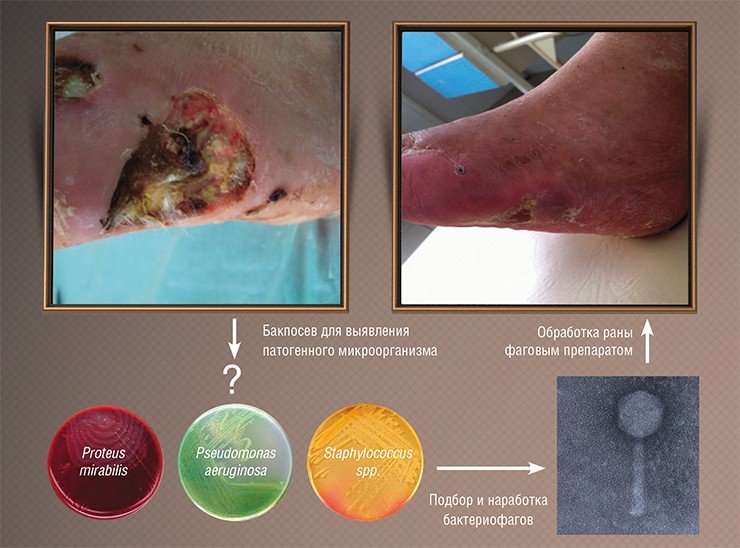
После 3 нед. терапии у 87,5% пациенток жалобы купировались. Явления посткоитального цистита регрессировали у 8 (66,7%) женщин. Принципы клинических решений применения бактериофагов в гинекологии представлены на рисунке 1.
На данном этапе накопленных знаний фундаментальной и клинической микробиологии и вирусологии, имеющегося клинического опыта необходимо выделить доказанные преимущества фаготерапии:
- строгая специфичность: бактериофаги воздействуют только на чувствительные к ним бактерии, в то время как антибиотики поражают бактерии без специфичности, вызывая угнетение нормальной микрофлоры и формирование резистентности;
- быстродействие и глубокое проникновение в очаг инфекции: при пероральном приеме через 1 ч бактериофаги попадают в кровь, через 1–1,5 ч выявляются из бронхолегочного экссудата и с поверхности ожоговых ран, через 2 ч — из мочи, а также из ликвора больных с травмами;
- самовоспроизведение: ДНК бактериофага встраивается в хромосому бактерии, вследствие чего бактериальная клетка начинает продуцировать сотни бактериофагов, поражающих бактерии до их полного уничтожения;
- саморегуляция: в отсутствие бактерий, необходимых для размножения, бактериофаги быстро и полностью удаляются из организма;
- безопасность и отсутствие противопоказаний: препараты бактериофагов можно назначать беременным, кормящим матерям и детям любого возраста, включая недоношенных;
- полная совместимость с любыми лекарственными средствами: доказанная эффективность препаратов бактериофагов как при монотерапии, так и в комбинации с антибиотиками;
- стимуляция специфического и неспецифического иммунитета: фаготерапия особенно эффективна при лечении хронических воспалительных заболеваний на фоне иммунодепрессивных состояний;
- постоянная актуализация фаговых клонов: препараты бактериофагов соответствуют современной этиологической структуре возбудителей.
В настоящее время имеется ограниченное количество сообщений о применении фаготерапии в акушерстве и гинекологии. Распространение применения бактериофагов требует накопления базы качественных рандомизированных мультицентровых клинических исследований. Тем не менее, очевидными являются возможности и перспективы применения бактериофагов в акушерстве и гинекологии:
- монотерапия нарушений микроценоза влагалища;
- монотерапия или комбинация с антибиотиками при лечении ВЗОМТ, хронического эндометрита;
- профилактика и лечение инфекций во время беременности с экстрагенитальной локализацией первичного очага;
- профилактика и лечение внутриутробной инфекции;
- профилактика и лечение послеоперационных осложнений при гинекологических вмешательствах и кесаревом сечении.
Таким образом, в условиях формирования антимикробной резистентности, формирования устойчивых бактериальных пленок необходимость в новых альтернативных лечебных технологиях и антимикробных препаратах приобретает все большую значимость. Перспективы применения бактериофагов касаются не только антимикробной терапии, но и высокоточной диагностики, а также онкологии. Проведенное исследование показало, что поливалентный пиобактериофаг в виде монотерапии и сочетанной с антибиотиками терапии повышает эффективность лечения, уменьшает частоту рецидивов и обладает высокой комплаентностью.
Первые клинические эксперименты с бактериофагами начались сто лет назад, и казалось, что этот новый метод терапии обречен на успех: с научной точки зрения он выглядел безупречным, и результаты применения выглядели многообещающими.
Почему же в последующие десятилетия интерес к терапевтическому применению бактериофагов в мире упал? Почему он возник вновь, и почему эта замечательная идея до сих пор не реализована в полной мере? И практические врачи, и их пациенты сегодня должны четко представлять не только суть, но и все сильные и слабые стороны этого перспективного вида терапии
Бактериофаги – это не обычные лекарства. Они не являются простыми химическими веществами, как антибиотики и большинство других препаратов, но их вряд ли можно считать и полноценными живыми организмами, так как они, как и все остальные вирусы, могут размножаться только в клетке-хозяине. По сути, это нанороботы с генетической программой, способные проникнуть внутрь бактериальной клетки и там размножиться, разрушив ее.
Поэтому к бактериофагам не всегда применимы стандартные для фармакологии нормы и подходы. И хотя фаговые препараты сегодня производятся и используются в медицине, наши знания о многообразии этих вирусов, механизмах их взаимодействия с бактериями и конкуренции с себе подобными пока недостаточны, чтобы в полной мере использовать их мощный терапевтический потенциал.
Безопасно и эффективно
Фаготерапия родилась едва ли не сразу после открытия самих бактериофагов, однако широкие испытания этих противобактериальных средств начали проводиться в СССР только в конце 1930-х гг. В результате была доказана эффективность препаратов бактериофагов как профилактического средства при борьбе с эпидемиями дизентерии и холеры, а использование их при лечении ран и гнойно-воспалительных процессов показало их потенциал как альтернативы антибиотикам.
Однако результаты исследований тех времен были зачастую противоречивы: иногда фаги сразу подавляли развитие инфекционных процессов, но иногда оказывались бесполезными. Специалисты сразу поняли, в чем причина: лечение было успешным лишь тогда, когда использовались фаги, способные инфицировать именно тот бактериальный штамм, который и вызвал заболевание. Поэтому при возникновении эпидемии требовалось выделить инфекционный агент, проверить на нем имеющиеся фаговые препараты и запустить в производство в качестве препарата наиболее эффективный бактериофаг.
К сожалению, результаты подобных исследований, проводившихся в СССР, не были должным образом документированы и описаны в научной литературе, к тому же они проводились по схемам, не соответствующим принятым на сегодня протоколам клинических испытаний. Тем не менее главные результаты этой работы были бесспорны: фаги доказали свою безопасность и высокую эффективность в реальных условиях и с тех пор используются в нашей стране в клинической практике наряду с обычными лекарственными средствами.

С появлением антибиотиков интерес к фагам на Западе был утрачен, но после появления антибиотикоустойчивых штаммов бактерий в разных странах начали разрабатывать фаговые препараты и проводить испытания, которые, по сути, повторяли исследования, уже проведенные в СССР. Результаты этих работ вновь подтвердили безопасность препаратов бактериофагов, что, в частности, отметило и Управление по контролю за качеством пищевых продуктов и лекарственных препаратов США (FDA).
В Великобритании успешно проведены эксперименты по лечению бактериофагами хронического отита, вызванного нечувствительной к антибиотикам синегнойной палочкой Pseudomonas aeruginosa, а в рамках проекта Phagoburn семь медицинских центров Франции, Бельгии и Швейцарии проводят клинические испытания коктейля фагов для предотвращения инфекций при ожогах. Об испытаниях собственных оригинальных коктейлей фагов для лечения широкого спектра заболеваний сообщает и ряд американских фирм (Intralytix, Enbiotix, AmpliPhi). Правда ни одно из этих масштабных клинических испытаний пока не доведено до конца.
В России препараты бактериофагов можно приобрести в обычной аптеке. Но при этом нужно понимать, что в отличие от других лекарств с точной химической формулой и концентрацией действующих компонентов препарат бактериофага представляет собой нестандартный раствор, содержащий живые вирусные частицы. Даже препарат с одним и тем же названием, но произведенный на разных предприятиях или в разное время, может содержать отличающиеся комбинации и (или) пропорции фагов.
Поэтому покупать препарат бактериофага, чтобы лечиться самостоятельно, не стоит. Назначить лечение и выбрать лекарство должен специалист. Спектр заболеваний, которые можно лечить бактериофагами широк: трофические язвы, ожоговые и раневые инфекции, инфекции органов дыхания, мочеполовой системы и желудочно-кишечного тракта, остеомиелит и т. п. Возбудителями болезней во всех этих случаях служат такие печально известные бактерии, как золотистый стафилококк, включая лекарственно устойчивые штаммы, синегнойная палочка, патогенные формы кишечной палочки, сальмонеллы, протеи, стрептококки и др. В принципе в природе можно найти бактериофаг против любой бактерии, включая возбудителей чумы и сибирской язвы. Можно применять бактериофаги и для профилактики бактериальных инфекционных болезней, например, они были успешно использованы в детских садах и школах для предотвращения эпидемии дизентерии.

Основная же и главная причина неудач – неумелый подбор фагов для лечения конкретных пациентов. Каждый конкретный фаг эффективен против одного или максимум нескольких штаммов бактерий, а у разных пациентов схожая по внешнему проявлению инфекция, например, ангина может быть вызвана разными штаммами стрептококка. Чтобы вылечить больного, необходимо выделить культуру патогена и протестировать ее на чувствительность к конкретным фагам. То есть терапия бактериофагами должна проводиться с использованием принципов персонализированной медицины, к чему современная медицина практически не готова.

На пути к персонализированной Фаготерапии
Опыт СССР, Грузии и Польши показал, что для успешного применения бактериофагов нужны не только клиника, но и производственно-лабораторный участок, располагающий коллекцией фагов и специалистами, способными идентифицировать бактерии, подбирать и выделять бактериофаги для конкретного пациента.
Но в таком случае имеет ли смысл масштабное производство фаговых препаратов? Ответ – да, потому что проблема узкой специфичности фагов частично решается производством фаговых коктейлей из нескольких (иногда десятков) разных фагов, поражающих разные штаммы целевого возбудителя. Ведь подобрать для больного нужный фаговый коктейль быстрее и проще, чем тестировать отдельные фаги из большой коллекции.
И все же не надо думать, что бактериофаги полностью заменят антибиотики – эти препараты дополняют друг друга, и применяться они должны в разных ситуациях. Когда больной находится в тяжелом состоянии, и есть уверенность, что причиной служит бактериальная инфекция, времени на эксперименты и подбор препаратов нет. Единственно правильное решение в этой ситуации – антибиотик широкого спектра действия.
Но в ситуации хронической инфекции или инфекции, вызванной бактериями со множественной устойчивостью к антибиотикам, предпочтение следует отдавать бактериофагу. В случае таких затяжных болезней, как отит, у врача есть время, чтобы использовать фаговый коктейль или специально подобрать фаг. Или же, когда после операции больной поражается антибиотикоустойчивым бактериальным штаммом, и его состояние быстро ухудшается, фаготерапия может стать единственным спасением.
Богатый опыт применения бактериофагов в клинической практике, накопленный за последние сто лет, свидетельствует о перспективности фаговых медицинских технологий. Дальнейшая работа специалистов из множества компаний, работающих сегодня в этой области, и применение методов синтетической биологии обязательно приведут к созданию препаратов с несравненно большей эффективностью по сравнению с современными фаговыми коктейлями.
Тем не менее, биотехнологи, также как ученые и медики, надеются, что безвредные и эффективные препараты все же займут свое законное место в арсенале терапии инфекционных заболеваний.
Алешкин А. В. Бактериофаги в инфекционной патологии: прошлое, настоящее и будущее // Лекции по исследованию и применению бактериофагов. 2016. Ульяновск. С. 11—51.
Козлова Ю. Н., Репин В.Е., Анищенко В.В., Власов В.В. и др. Штамм бактериофага Pseudomonas aeruginosa, используемый в качестве основы для приготовления асептического средства против синегнойной палочки. // Патент РФ №2455355. 2012.
Козлова Ю. Н., Морозова В. В., Тикунова Н. В. и др. Штамм бактериофага Staphylococcus aureus SA20, обеспечивающий разрушение биопленок, образуемых бактериями рода Staphylococcus // Патент РФ № 2565824. 2015.
Морозова В. В., Козлова Ю. Н., Тикунова Н. В. и др. Штамм бактериофага Citrobacter freundii CF17, способный лизировать патогенные штаммы Citrobacter freundii // Патент РФ № 2565559. 2015.
Тикунова Н. В., Морозова В. В. Фаговый дисплей на основе нитчатых бактериофагов: применение для отбора рекомбинантных антител // Аcta Naturae. 2009. № 3. С. 6—15.
Тикунова Н. В. и Власов В. В. Бактериофаги – враги наших врагов // Наука из первых рук. 2013. № 2(50). С. 58—69.
Покровская М. П. Каганова Л. С., Морозенко М. А. и др. Лечение ран бактериофагом. М.: НАРКОМЗДРАВ СССР, МЕДГИЗ. 1941. 57 с
Górski A. et al. Phages targeting infected tissues: novel approach to phage therapy. // Future Microbiol. 2015. V. 10. P. 199—204.
Międzybrodzki R. et al. Clinical aspects of phage therapy // Adv. Virus. Res. 2012. V. 83. P. 73—121.
В публикации использованы иллюстрации из книги Лечение ран бактериофагом. М.: НАРКОМЗДРАВ СССР, МЕДГИЗ. 1941. 57 с.
Информация об исследовании
Биологический материал: Мазки в пробирки с транспортной средой и на стекла (3 пробирки + 3 стекла)
Внимание! С 01.01.2013 г. при выявлении в посеве возбудителей семейства Streptococcaceae, чувствительность к стрептококковому бактериофагу определяться не будет в связи с тем, что данный реагент снят с производства.
При обнаружении роста нормальной или условно-патогенной флоры в низком титре и не имеющей диагностического значения определение чувствительности к антибиотикам/бактериофагам не проводится.
Данное исследование позволяет составить целостное представление о микрофлоре урогенитального тракта. Оно состоит из 3-х бактериологических посевов и микроскопии мазков, взятых из 3-х точек (уретра, цервикальный канал и влагалище).
Микроскопия мазка позволяет оценить воспалительную реакцию слизистой уретры, цервикального канала или влагалища (по уровню лейкоцитов) и диагностировать такие заболевания как кандидоз (молочница), трихомониаз, гонорея, бактериальный вагиноз. Бактериологический метод – это посев материала на питательные среды и выделение чистых культур микробов с их последующей идентификацией. При обнаружении патогенных микроорганизмов определяется чувствительность выделенных микроорганизмов к антибиотикам. При высеве патогенных микроорганизмов определяется чувствительность к антибиотикам, таким образом данный анализ позволяет подобрать самое сложное и точное лечение.
Мазок из уретры берут не ранее 3-4 ч после мочеиспускания и обязательно до начала антибактериальной терапии. Аккуратно ватным тампоном забирается материал со слизистой уретры и помещается в пробирку с транспортной средой, доставляемую в лабораторию. Пациенток просят в течение 24 часов до исследования не прибегать к спринцеванию.
Бактериальная флора уретры здорового человека имеет смешанный характер: основным видом уретральных сапрофитов является негемолитический коагулазонегативный стафилококк (Staph. Epidermidis) и коринобактерии (Согуnеbacterium). Этот вид стафилококка, обычно локализующийся в передней части уретры, не являясь патогенным, участвует в антимикробной защите слизистой оболочки, выделяя вещества, подавляющие рост патогенных микроорганизмов. К патогенным микроорганизмам, вызывающим инфекцию мочевых путей, относятся: стафилококки: золотистый (S.aureus), эпидермальный (S.epidermidis) в количестве более 10 7 КОЕ/мл, сапрофитный (S.saprophyticus), энтерококки (Enterococcus), кишечная палочка (E.coli), цитобактер (Citrobacter), энтеробактер (Enterobacter), протей (Proteus vulgaris), дрожжевой грибок (Candida albicans). В выдаваемом результате, указывается преобладающая микрофлора, количество патогенных микроорганизмов и чувствительность к различным группам антибиотиков. Мазок из влагалища и цервикального канала берут в течение 24 часов после спринцевания, данная процедура уменьшает количество микроорганизмов для посева. В норме флора может содержать лактобактерии до 10 7 , энтерококки до 10 2 , кишечную палочку до 10 2 , дрожжевой грибок до 10 2 КОЕ/мл. При посеве могут определяться патогенные штаммы стрептококка (S. agalactinаe, S. pyogenes), стафилококка (S. Aureus), повышенное количество кишечной палочки (E. Coli). Иногда во влагалище размножаются бактерии, которые не вызывают воспаление, но потенциально опасны такие как гарднереллы (Gardnerella vaginalis), вызывающие вагиноз. Заболевание может протекать незаметно, Лишь изредка вагиноз проявляется зудом и обильными выделениями из влагалища, которые имеют рыбный запах. Ко всем выделенным патогенным штаммам производится подбор чувствительных антибиотиков.
Выделяемые возбудители (условно-патогенные бактерии):
энтеробактерии, неферментирующие грамотрицательные бактерии, стрептококки, энтерококки, стафилококки, коринеформные бактерии, гемофилы и дрожжеподобные грибы.
Специфические возбудители: Хламидии (Chlamydia trachomatis), влагалищная трихомонада (Trichomonas vaginalis), бледная спирохета (Treponema pallidum), гонококк (Neisseria gonorrhoeae) в данном исследовании не определяются.
Показания к назначению исследования
- Определение этиологии инфекционного заболевания, установление конкретного вида возбудителя
- Определение рациональной антимикробной терапии.
- Оценка эффективности проводимой терапии
Подготовка к исследованию
Женщинам рекомендуется сдавать анализ до менструации или через 2 дня после ее окончания.
За 24-48 час исключить -половой контакт, местные(влагалищные) процедуры- введение свечей, спринцевания, УЗИ вагинальное и кольпоскопия
Проводить исследование не ранее чем через 14 дней после применения антибактериальных препаратов.
За 2 часа до взятия мазков не мочиться.
Результаты исследования
Референсные значения для различных видов микроорганизмов зависят от их локализации (точки взятия биологического материала).
В результате исследования указывается наличие или отсутствие роста микроорганизмов, степень бактериурии, выраженная в КОЕ/мл, наименование возбудителя. Также определяется чувствительность штаммов к препаратам (при заказе соответствующих позиций).
Читайте также:


