Стрептококки группы а пожирающие плоть
Среди 18 видов и 8 родственных групп бактерий, причисленных к важнейшим патогенам человека, особую роль играют стрептококки. По медицинской значимости они занимают второе место после стафилококков. Из числа стрептококков, патогенных для человека, с середины 80-х гг. ХХ столетия во многих странах мира наблюдается рост заболеваемости, обусловленной β-гемолитическими стрептококками группы А (БГСА, S.pyogenes).
β-гемолитический стрептококк группы А (пиогенный стрептококк, БГСА S.pyogenes) - грамположительный, неспорообразующий, неподвижный микроорганизм. Растёт на кровяном агаре, обладает выраженной гемолитической активностью, каталазанегативный, чувствителен к бацитрацину. Встречается повсеместно, часто колонизирует кожные покровы и слизистые оболочки человека. Главными путями передачи являются воздушно-капельный, контактный и пищевой. Патогенез заболеваний связан с продукцией токсинов: гемолизин, стрептолизин, стрептокиназы А и В, дезоксирибонуклеаза, гиалуронидаза. Основные нозоформы представлены поверхностными (ангины, фарингит, импетиго, рожа), инвазивными (некротизирующий фасциит, миозит, менингит, эндокардит, пневмония, послеродовой сепсис) и токсин-опосредованными инфекциями (скарлатина, синдром токсического шока). Со стрептококковой инфекцией связано также возникновение неврологических расстройств у детей, проявляющихся обсессивно-компульсивными расстройствами (PANDAS-синдром).
Streptococcus pyogenes сохраняет 100% чувствительность к β-лактамным антибиотикам (пенициллинам, цефалоспоринам, карбапенемам). Они остаются единственным классом антибиотиков, к которым у S.pyogenes не развилась резистентность. Актуальной проблемой является устойчивость к макролидам, которая в некоторых регионах мира превышает 30%. Многоцентровое исследование резистентности клинических штаммов S.pyogenes, проведённое в 2000-2001 гг., позволило изучить распространенность устойчивости, прежде всего к макролидам, в различных регионах России. Частота резистентности к эритромицину варьировала и достигала 11,4%, при этом не было обнаружено штаммов, устойчивых к телитромицину, представителю нового класса антибиотиков - кетолидов. Почти в 90% случаев резистентность к макролидам была обусловлена метилированием рибосом, в остальных случаях она была связана с активным выведением (эффлюксом) антибиотика из клетки.
Стрептококковый тонзиллофарингит
Стрептококковый тонзиллофарингит (ангина) - острое общее инфекционное заболевание с преимущественным поражением лимфоидного аппарата и слизистой оболочки глотки, вызванное БГСА. Под рецидивирующим стрептококковым тонзиллофарингитом следует понимать множественные эпизоды заболевания в течение нескольких месяцев с положительными результатами бактериологических и/или экспресс-методов диагностики БГСА, отрицательными результатами исследований между эпизодами заболевания, повышением титров противострептококковых антител после каждого случая болезни.
Этиология: среди бактериальных возбудителей острого тонзиллофарингита наибольшее значение имеет БГСА.
Эпидемиология. В США ежегодно диагностируется 1-1,4 млн. случаев тонзиллофарингита БГСА-этиологии. Передача осуществляется воздушно-капельным, контактным и пищевым путями. Источниками инфекции являются больные, реже - бессимптомные носители. Вероятность заражения увеличивается при высокой обсемененности и тесном контакте. БГСА может вызывать крупные вспышки тонзиллофарингита в организованных коллективах. Чаще болеют дети в возрасте 5-15 лет. Наибольшая заболеваемость - в зимне-весенний период.
Клиническая картина: Инкубационный период составляет от нескольких часов до 2-4 дней. Характерно острое начало с повышения температуры тела до 37,5-39°С, выражена общая интоксикация. Боль в горле бывает так сильно выражена, что у больного нарушается глотание. При осмотре выявляется покраснение нёбных дужек, язычка и задней стенки глотки. Миндалины гиперемированы, отёчны, часто с гнойным налётом желтовато-белого цвета. Налёт рыхлый, пористый, легко удаляется шпателем с поверхности миндалин без кровоточащего дефекта. У всех больных отмечается регионарный лимфаденит.
Кровь: лейкоцитоз, сдвиг лейкоцитарной формулы влево, увеличение СОЭ, появление С-реактивного белка.
Длительность периода разгара (без лечения) составляет 5-7 дней. В дальнейшем, при отсутствии осложнений, основные клинические проявления болезни быстро исчезают.
Осложнения. Особую опасность представляют осложнения стрептококкового тонзиллофарингита, которые делятся на:
- ранние (гнойные), развивающиеся на 4-6-й день от начала заболевания,- отит, синусит, мастоидит, паратонзиллярный абсцесс, шейный лимфаденит, менингит, бактериемия, эндокардит, пневмония;
- поздние (негнойные): постстрептококковый гломерулонефрит, токсический шок, развивающиеся в стадии реконвалесценции (на 8-10-й день от начала болезни) и острая ревматическая лихорадка, развивающаяся через 2-3 нед после купирования симптомов заболевания - опасные, часто приводящие к инвалидизации заболевания.
Диагностика. Чрезвычайно важно своевременно установить этиологию тонзиллофарингита, поскольку, за редким исключением, только ангина стрептококковой этиологии требует антибактериальной терапии. Диагностика включает микробиологическое исследование мазка с поверхности миндалин и/или задней стенки глотки. За рубежом широкое распространение получили методы экспресс-диагностики, основанные на прямом выявлении стрептококкового антигена в мазках с поверхности миндалин и/или задней стенки глотки. Современные тестовые системы позволяют получать результат через 15-20 мин с высокой специфичностью (95-100%), но меньшей, чем при культуральном исследовании, чувствительностью (60-95%), в связи с чем отрицательный результат экспресс-теста всегда должен подтверждаться культуральным исследованием.
Целью антибиотикотерапии острых стрептококковых ангин является эрадикация БГСА, что ведёт не только к ликвидации симптомов инфекции, но и предупреждает ранние и поздние осложнения, а также предотвращает распространение инфекции.
Выбор антибиотиков. Препаратами I ряда для лечения острого стрептококкового тонзиллита являются пенициллин (феноксиметилпенициллин), аминопенициллины и оральные цефалоспорины. У пациентов с доказанной аллергией на β-лактамные антибиотики следует применять макролиды, а при непереносимости последних - линкозамиды.
Носительство БГСА. В среднем около 20% детей школьного возраста являются носителями БГСА в весенне-зимнее время. Учитывая низкий риск развития гнойных и негнойных осложнений, а также незначительную роль в распространении БГСА, хронические носители, как правило, не нуждаются в антибактериальной терапии.
Острая ревматическая лихорадка
Острая ревматическая лихорадка (ОРЛ) может возникать как после тонзиллофарингита с типичной клинической картиной, так и после перенесённой бессимптомной или малосимптомной инфекции. ОРЛ возникает только после инфекций глотки, и никогда после инфекций кожи и мягких тканей. Предположительное объяснение этого феномена состоит в различии иммунного ответа на кожную и глоточную инфекцию и в отсутствии ревматогенного потенциала у штаммов, вызывающих кожные инфекции. Риск развития ОРЛ после нелеченного тонзиллофарингита составляет 1%. К ревматогенным М-серотипам стрептококка относятся 1, 3, 5, 6, 18, 19, 24.
В настоящее время в развитых странах острая ревматическая лихорадка встречается с частотой 0,5 на 100000 детей школьного возраста. В развивающихся странах заболеваемость составляет от 100 до 200 на 100000 детей школьного возраста, ежегодно регистрируется от 10 до 15 млн. новых случаев ОРЛ, которая является основной причиной смерти от сердечно-сосудистой патологии.
Следует отметить, что немотивированная задержка восстановления трудоспособности, слабость, нестойкий субфебрилитет, артралгии, сердцебиение и нерезко повышенная СОЭ, сохраняющиеся после перенесенной ангины, в сочетании с ростом титров противострептококковых антител (антистрептолизин О, антистрептокиназа, антистрептогиалуронидаза, анти-ДНКаза В) могут свидетельствовать о дебюте острой ревматической лихорадки.
В соответствии с рекомендациями ВОЗ для диагностики острой ревматической лихорадки в качестве международных применяются критерии Джонса, пересмотренные Американской кардиологической ассоциацией в 1992 г. (см. табл.). Наличие двух больших критериев или одного большого и двух малых в сочетании с данными, документированно подтверждающими предшествующую БГСА-инфекцию, свидетельствует о высокой вероятности ОРЛ. Однако ни один диагностический критерий не является строго специфичным для ОРЛ, поэтому трудности в раннем распознавании заболевания и дифференциальной диагностике с другими нозологиями сохраняются по-прежнему.
Критерии Джонса, применяемые для диагностики первой атаки ревматической лихорадки (по состоянию на 1992 г.)

Адрес: г. Смоленск, пл. Ленина, д. 1
Телефоны: (4812)29-22-01, 29-22-02
Территориальный орган федеральной службы по надзору в сфере здравоохраненияпо Смоленской области
Территориальное управление федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека по Смоленской области










Телефон доверия Смоленской областной клинической психиатрической больницы:
Рабочие дни: с 15:00 до 18:00
Выходные дни: с 8:00 до 20:00
Телефон горячей линии Благотворительного фонда реабилитации больных наркоманией "Нарком":
Профилактика стрептококовой (группы А) инфекции

Стрептококковые инфекции – группа заболеваний, включающая инфекции, вызываемые стрептококковой флорой разных видов и проявляющихся в виде поражения дыхательных путей и кожных покровов. К стрептококковым инфекциям относят стрептококковое импетиго, стрептодермию, стрептококковый васкулит, ревматизм, гломерулонефрит, рожу, ангину, скарлатину и другие заболевания. Стрептококковые инфекции опасны склонностью к развитию постинфекционных осложнений со стороны различных органов и систем. Поэтому диагностика включает не только выявление возбудителя, но и инструментальное обследование сердечно-сосудистой, дыхательной и мочевыделительной систем.
Streptococcus – род факультативно-анаэробных грамположительных шаровидных микроорганизмов, устойчивых в окружающей среде. Стрептококки устойчивы к высушиванию, сохраняются в высушенных биологических материалах (мокрота, гной) несколько месяцев. При температуре 60 °С. погибают через 30 минут, под действием химических дезинфицирующих средств - через 15 минут.
Источник стрептококковой инфекции – носитель стрептококковых бактерий или больной одной из форм инфекции человек.
Механизм передачи – аэрозольный. Возбудитель выделяется больным при кашле, чихании, во время разговора. Заражение происходит воздушно–капельным путем, поэтому основными источниками заражения являются люди с преимущественным поражением верхних дыхательных путей (ангина, скарлатина). При этом на расстоянии более трех метров заразиться уже нельзя. В некоторых случаях возможна реализация алиментарного и контактного путей передачи (через грязные руки, зараженную пищу). Для стрептококков группы А при попадании в благоприятную питательную среду некоторых пищевых продуктов (молоко, яйца, моллюски, ветчина и др.) характерно размножение и длительное сохранение вирулентных свойств.
Вероятность возникновения гнойных осложнений при инфицировании стрептококками высока у лиц с ожогами, ранениями, беременных, новорожденных, больных после операций. Стрептококки группы В обычно вызывают инфекции мочеполовой сферы и могут передаваться при половых контактах. Новорожденные зачастую получают инфекцию в результате инфицирования околоплодных вод и при прохождении родовых путей. Естественная восприимчивость человека к стрептококковым бактериям высокая, иммунитет типоспецифический и не препятствует заражению стрептококками другого вида.
Симптоматика стрептококковых инфекций крайне многообразны ввиду большого количества вероятных локализаций очага инфекции, видов возбудителя. Кроме того, интенсивность клинических проявлений зависит от общего состояния организма инфицированного. Стрептококки группы А склонны к поражению верхних дыхательных путей, слухового аппарата, кожи (стрептодермия), к этой группе относятся возбудители скарлатины и рожи.
Заболевания, развившиеся в результате поражения этими микроорганизмами, можно разделить на первичные и вторичные формы. Первичные формы представляют сбой воспалительные инфекционные заболевания органов, ставших воротами инфекции (фарингит, ларингит, ангина, отит, импетиго и т. д.). Вторичные формы развиваются в результате включения аутоиммунных и токсико-септических механизмов развития воспаления в различных органах и системах. К вторичным формам стрептококковых инфекций с аутоиммунным механизмом развития относятся ревматизм, гломерулонефрит и стрептококковый васкулит. Токсино-инфекционный характер носят некротические поражения мягких тканей, мета- и перитонзиллярный абсцессы, стрептококковый сепсис.
Редкие клинические формы стрептококковых инфекций: некротическое воспаление мышц и фасций, энтерит, синдром токсического шока, очаговые инфекционные поражения органов и тканей (например, абсцесс мягких тканей). Стрептококки группы В в подавляющем большинстве вызывают инфекции у новорожденных, хотя встречаются в любом возрасте. Это связано с преимущественным поражением данным возбудителем мочеполовых путей и заражением новорожденных интранатально.
Стрептококковые инфекции группы В нередко являются причиной послеродовых эндометритов, циститов, аднекситов у родильниц и осложнений в послеоперационном периоде при проведении кесарева сечения. Стрептококковая бактериемия кроме того может отмечаться у лиц с выраженным ослаблением иммунных свойств организма (пожилые люди, больные сахарным диабетом, синдромом иммунодефицита, злокачественными новообразованиями). Нередко на фоне протекающей ОРВИ развивается стрептококковая пневмония. Зеленящий стрептококк может быть причиной развития эндокардитов и последующих клапанных дефектов. Стрептококки группы mutans вызывают кариес.
Осложнения стрептококковых инфекций – это аутоиммунные и токсикосептические вторичные поражения органов и систем (ревматизм, гломерулонефрит, некротические миозиты и фасциты, сепсис и т. д.).
Этиологическая диагностика стрептококковой инфекции слизистой оболочки глотки и кожных покровов требует бактериологического исследования с выделением и идентификацией возбудителя. Исключением можно считать скарлатину. Поскольку в настоящее время многие виды стрептококковых бактерий приобрели определенную устойчивость к антибиотикам некоторых групп, необходимо тщательное микробиологическое исследование и осуществления теста на чувствительность к антибиотикам. Диагностика, произведенная в достаточном объеме, способствует выбору эффективной тактики лечения.
Экспресс-диагностика стрептококков группы А позволяют установить возбудителя в течение 15-20 минут с момента взятия анализа без выделения чистой культуры. Однако выявление присутствия стрептококков не всегда означает, что именно они являются этиологическим фактором патологического процесса, этот факт может говорить и об обычном носительстве. Ревматизм и гломерулонефрит практически всегда характеризуются повышением титра антител к стрептококкам уже с первые дни обострения. Титр антител к внеклеточным антигенам определяют с помощью реакции нейтрализации. При необходимости проводится обследование пораженных стрептококковой инфекцией органов: осмотр отоларинголога, рентгенография легких, УЗИ мочевого пузыря, ЭКГ и др.
В зависимости от формы стрептококковой инфекции лечение проводит гинеколог, уролог, дерматолог, пульмонолог или другие специалисты. Патогенетическое и симптоматическое лечение зависит от клинической формы заболевания.
Профилактика заражения стрептококковой инфекцией:
- меры личной гигиены
- индивидуальная профилактика при контактах в узком коллективе с лицами, имеющими респираторные заболевания: ношение маски, обработка посуды и поверхностей, на которые могли попасть микроорганизмы, мытье рук с мылом.
Общая профилактика заключается в осуществлении планомерного контроля над состоянием здоровья коллективов: профилактические осмотры в школах и детских садах, изоляция выявленных больных, адекватные лечебные мероприятия, выявление скрытых форм носительства стрептококковой инфекции и их пролечивание.
Особое внимание необходимо уделять профилактике внутрибольничного инфицирования стрептококковой инфекцией, поскольку заражение в стационаре пациента, находящегося в ослабленном состоянии, в разы вероятнее, и течение инфекции у таких больных заметно тяжелее. Предупреждение заражения рожениц и новорожденных заключается в тщательном соблюдении санитарно-гигиенических норм и режима, разработанных для отделений гинекологии и родильных домов.
Ангина - инфекционно–аллергический процесс, локальные изменения при котором затрагивают глоточное лимфоидное кольцо, чаще всего небные миндалины. Течение ангины характеризуется повышением температуры тела, общеинтоксикационным синдромом, болью в горле при глотании, увеличением и болезненностью шейных лимфоузлов. При осмотре выявляется гиперемия и гипертрофия миндалин и небных дужек, иногда – гнойный налет. Ангина диагностируется отоларингологом на основании данных фарингоскопии и бактериологического посева из зева. При ангине показано местное лечение (полоскание горла, промывание лакун, обработка миндалин препаратами), антибиотикотерапия, физиотерапия.
Ангина – группа острых инфекционных заболеваний, которые сопровождаются воспалением одной или нескольких миндалин глоточного кольца. Как правило, поражаются нёбные миндалины. Реже воспаление развивается в носоглоточной, гортанной или язычной миндалинах. Возбудители болезни проникают в ткань миндалин извне (экзогенное инфицирование) или изнутри (эндогенное инфицирование). От человека человеку ангина передается воздушно-капельным или алиментарным (пищевым) путем. При эндогенном инфицировании микробы попадают в миндалины из кариозных зубов, придаточных пазух (при синуситах) или носовой полости. При ослаблении иммунитета ангина может вызываться бактериями и вирусами, которые постоянно присутствуют на слизистой рта и глотки.





Рожа (рожистое воспаление) представляет собой инфекционное заболевание, вызываемое стрептококком группы А, преимущественно поражающее кожные покровы и слизистые оболочки, характеризующееся возникновением ограниченного серозного или серозно-геморрагического воспаления, сопровождающегося лихорадкой и общей интоксикацией. Рожа входит в число самых распространенных бактериальных инфекций. Характеристика возбудителя



214025, г. Смоленск,
ул. Нормандия-Неман, 37
Бактерии способные сгноить заживо, снять кожу с костей или убить за 24 часа. Самые опасные и самые хищные.
Наше любопытство завораживают хищники. Мы любим шоу о дикой природе, об акулах, больших кошках, мы всегда с упоением наблюдаем противостояние убийцы и его жертвы. Мы переживаем за антилопу, пришедшую на водопой, и нильского крокодила, сосредоточенно ждущего её под мутными водами древней реки, чтобы в нужный момент, выверенный эволюцией, сам естественный отбор свершился и сравнил, кто из них всё же сильнее, быстрее, проворнее, кто будет жить, а кто будет съеден. С таким же гипнотическим интересом мы завороженно читаем о болезнях и эпидемиях, унесших жизни людей или угрожающих им сейчас. Эбола, Марбург , лихорадка Зикка, Дэнге, малярия, сотни смертельных патогенов. нам интересно – кто же самый опасный из них?
Мы боимся. Мы смотрим сериалы про зомби и пандемии, проецируя возможные последствия глобальных катастроф на нашу реальность. Мы боимся. Но мы обманываем себя каждый божий день. Мы врем себе, делая вид, что не замечаем войны, которая идёт каждую секунду. Войны нашего тела с миллионами хищников, готовых нас сожрать. И они не прячутся где-то под водой или в далеких джунглях, они – повсюду. Они прямо на вашей коже. Всегда. С самого рождения они ждут, когда вы ослабнете и позволите им войти. И они всегда побеждают, даже если ждать придется всю вашу жизнь. Потому что они – гнилостные бактерии, микромир гниения, тлена и разложения. А мы – всего лишь часть этой экосистемы.
Сегодня о бактериях – пожирателях плоти рассказывает ваш непопулярный ScientaeVulgaris.
Некроз и пингвиний суп
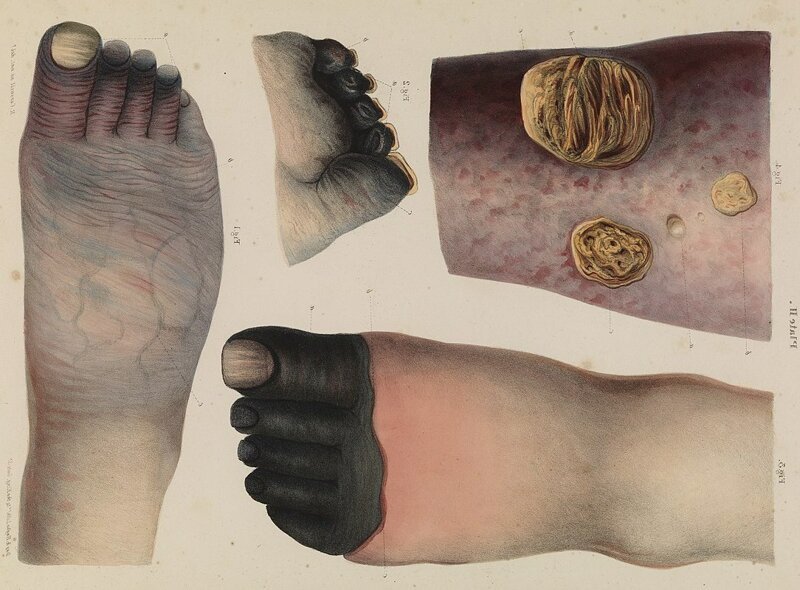
Гангрена – это, прежде всего, некроз. Где-то что-то в организме начало умирать - пока не вы лично, но ваше тело. Чаще всего это связано с тем, что доступ крови к участку вашей тушки прекратился. Клетки лишились кислорода, питательных веществ и стали массово откидывать клеточные копытки и отходить к клеточным божкам. Это может быть обморожение, сильный ожог, атеросклероз, тромбоз или ещё какая неприятность, в результате которой какая-то часть вашего тела внезапно стала холодеть, обрела бледный, а затем и мраморно-синий цвет, и в итоге с жуткими болями и запахом тухлого мяса потемнела.
Характерный пример – "траншейная стопа", когда солдаты успевают намокнуть в около-нулевую температуру, но не успевают просушить портянки.

И вот, перед вами – та самая киношная картинка с черными пальцами. Знакомьтесь – это сухая гангрена, и она представляет собой медленно растущий некроз. Обескровленный участок продолжает чернеть и усыхать. Напоминает он по цвету вяленое мясо. Это, собственно, и есть процесс мумификации, но только частично и на ещё живом теле. Дальше умирающие клетки выделяют токсины, отравляющие соседние ткани, и черная иссохшая плоть расползается, медленно поглощая остальное тело, превращая его в почерневшую мумию.
Смерть наступает, когда гангрена доходит до внутренних органов или заражение переходит на другой, более активный уровень. Изредка она двигается настолько медленно, что организм успевает её изолировать, и сам отсекает гниющую плоть, и тогда вы как гигантская ящерица просто теряете конечность, а культя медленно заживает. Но сухая гангрена – это практически невозможный вариант. Если бы всё было так просто, то и Людовик XIV и Юлия Началова были бы живы. Реальность несколько сложнее.

Некроз – это ведь, как правило, следствие травмы, болезни или других проблем. Не важно, что вызвало его – закупорка сосуда в стопе диабетика или тромб. Важно то, что любой некроз, как и обычный порез, укус мухи, царапина, ссадина, или игла шприца, катетер в вене. любое лишнее отверстие в вашем тельце – да хотя бы банальное пулевое ранение – открывают двери настоящим хищникам. В ткани попадает инфекция. И если ваша иммунная система не справится, развивается сепсис, а время для вас начинает лихорадочно ускоряться. При сепсисе смерть может наступить в течение 24 часов. То же происходит и с гангреной: как правило, организм не успевает её изолировать, к мумификации присоединяются патогены, а заражение становится системным.
Продолжим разделяться – сепсис не болезнь. Это воспаление, ответ вашего организма на вброс в него огромного количества токсинов и продуктов жизнедеятельности гноеродных бактерий. И именно сепсис – одна из самых частых причин смерти при экстренной госпитализации, и бич систем здравоохранения многих стран. Только США потратили за 2013 год 23,6 млрд. долларов на 1,3 миллиона пациентов с диагнозом “сепсис”. Тяжелый сепсис может привести к летальному исходу примерно у 20–35% людей, а септический шок – к летальному исходу у 30–70% людей. Это выше, чем у некоторых штаммов Эболы. И вызывает его не вирус из джунглей, а банальное население поверхностей вашей кожи и ваших слизистых.
Лицо бедности
К примеру, Prevotella intermedia – население биопленки полости рта – вызывает пародонтоз. При наличии гемина (смесь соляной кислоты с гемоглобином), метадиона и некоторых гормонов начинает бурно расти. Иначе говоря, если ваша ротовая полость, населенная биопленкой с десятками разных видов бактерий, выбросит игральные кости химического состава отрыжек, остатков еды, полового созревания и ферментов в пользу P. intermedia – начнётся пародонтоз. Можно, конечно, просто чаще чистить зубы или использовать агрессивную зубную пасту с фтором, и избежать его развития, но это слишком просто. Сегодня исследования зависимости пародонтоза и роста разных биопленок – настоящий темный лес: с одной стороны отмечен рост P. intermedia в период беременности, с другой – аналогичное действо происходит при недостаточном/скудном питании у беднейших слоев населения в Африке.
Но что нужно, чтобы обычный пародонтоз превратился в фильм ужасов? Компания.

Добавьте к парондотозной падле (Prevotella intermediа) Fusobacterium necrophorum – этого обычного обитателя желудочно кишечного тракта, ответственного за 10% всех случаев ангин. Потом ещё немного Fusobacterium nucleatum, живущего в составе зубного налета. И тот, и другой – жесткие веретенообразные прилипалы, они собирают вокруг себя всё, что только можно, создавая бляшки-поселения из микроорганизмов. В итоге получите что-то вроде отдельной экосистемы, куда при отсутствии контроля и наличии доступа к вашей плоти на огонек собираются все остальные злодеи, что есть в округе: родственник боррелиоза или болезни Лайма - Borrelia vincentii (процветает при дефиците витаминов, длительном отсутствии чистки зубов и формирует мощные биопленки, вызывающие гингивит и воспаление дёсен); Porphyromonas gingivalis (специалист по проникновению в соединительную ткань десны, разваливает молекулы коллагена и устойчив к антибиотикам); и, например, золотистый стафилококк, вездесущий, всеобъемлющий, всегниющий. К ним присоединяется ещё с десяток бактерий, каждая из которых берёт на себя одну из функций. И все вместе они, наконец, справляются со своей главной задачей – выходом на новый уровень роста: размножение не на поверхности вашей кожи, а под ней.
В медицине конкретно эта картина заболевания получила название Нома. Для вас всё выглядит гораздо проще – у вас просто жрут лицо. Вся эта братия микроорганизмов переварят кожу, мышцы, нервы, оголятся кости. Глазные яблоки сначала утратят поддержку, затем включатся в процесс и, превратившись в гной, вытекут. Выпадут зубы. Растворится язык.
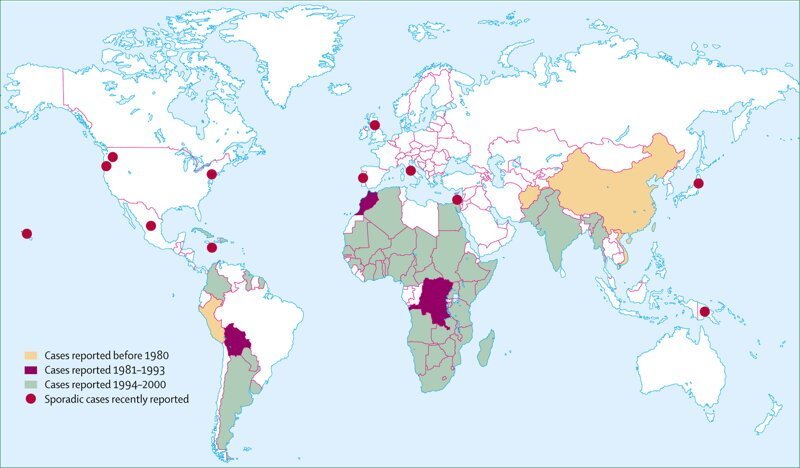
Смертность почти 100%. В некоторых источниках вы встретите указание на 80-85%, однако это статистика тех, кто попал в больницу и получил помощь. Но ведь речь идет о беднейшем населении планеты - какая, к черту, помощь? И какая, к черту, больница? Нома – это настоящее лицо бедности, самое дикое и самое страшное из всех, что только бывают. А ведь всего лишь простая регулярная гигиена полости рта и достаточное питание ставят эту болезнь в категорию исчезнувших. В Европе в 1649 году Арнольд Бутия описал в своем Observationes Medicae de Affectibus Omissis (медицинский обзор вымерших болезней) Ному как исчезнувшую редкую болезнь региона Сахары. Но прошло почти 400 лет, а она вполне себе жива, и всё там же. От 40 000 до 140 000 человек заболевают Номой каждый год. При этом общее количество выживших после Номы на сегодня оценивается в 210 000. И это несмотря на статистику смертности и социальную стигматизацию - когда детей с таким заболеванием изолируют, приписывая болезни мистические или религиозные свойства.
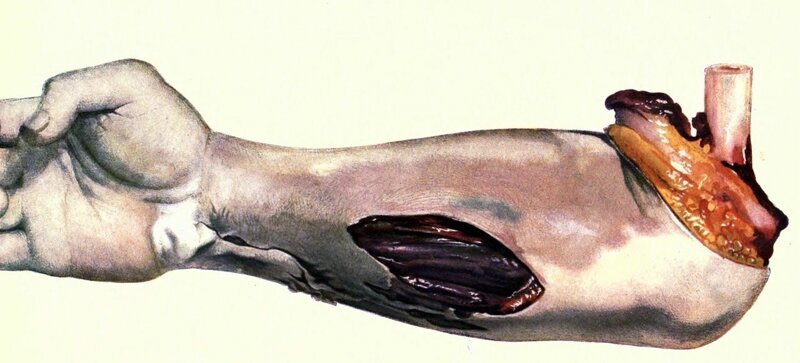
Этому описанию – две с половиной тысячи лет! Так что говорить, что “некротический фасциит – новая угроза” – дело неблагодарное. Но Гиппократ называл её рожей, а это не то, скажете вы. Поражения лобка и половых органов вообще выделены в отдельный тип гангрен - гангрены Фурье. Быстро разрастающиеся, они требуют операций по вскрытию ран, установке дренажа для оттока гноя. Открытые половые органы и иссеченная гниющая брюшная полость с вкраплениями подкожного жира – визитная карточка жуткого состояния, из-за близости к жизненно-важным органам весьма опасного и нередко ведущего к смерти.
Но старина Гиппо не был так уж не прав на счет патогена. Так что продолжим разделяться! Мухи налево, котлеты направо, кетчуп прямо, а SV за добавкой. Прежде чем сразу пугать вас жуткими фотографиями разложившихся мышц и плоти, сползающей лоскутами с костей, давайте вспомним более популярные и частые формы инфекций мягких тканей. Это рожа, упомянутая Гиппократом, и целлюлит. На последнем слове, боюсь, многие подпрыгнули. Но не надо путать аппетитные апельсиновые попки на пляжах “ол инклюзив” с их липодистрофией (целлюлитом) и cellulitis – гнойное воспаление клетчатки. И рожа, и cellulitis могут со временем перерасти в полномасштабный фасциит. И те и другие вызываются стрептококками группы А. Кто есть кто?
Справа cellulitis, слева Рожа:
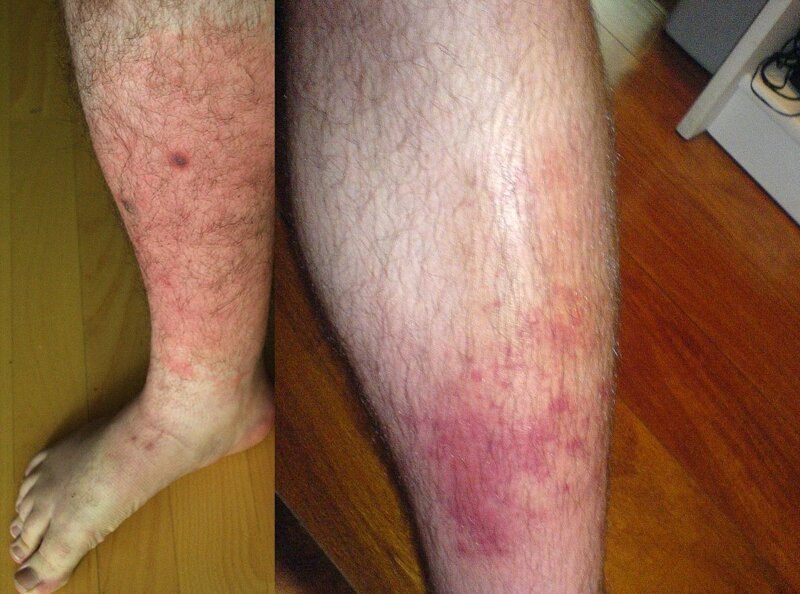
Большинство из тех, кто перешел черту – от обычной сыпи к ужасам фасциита, имели хронические системные заболевания, страдали алкоголизмом, наркоманией, диабетом, у них был подавлен иммунитет бесконечными таблетками от аллергии или ВИЧ. Но при этом каждый третий из заболевших был абсолютно здоров, – в их случае так совпало, что в одном месте оказался нужный набор случайностей. Судьба микромира бросила кости и под кожу попала смертельная комбинация патогенов. Одновременно.
Кто они? В первую очередь стрептококки группы А. Почему А? Классификация создана на основании полисахаридов, по характерным молекулам в оболочке стрептококков. Стрептококки группы А – коренные паразиты слизистых путей, особенно носа и рта. Возглавляет их S.pyogenes, ответственный за многие ваш ЛОР болезни - от фарингитов до скарлатины. Лечится мощными дозами пенициллина. Случаи резистентности пока не подтверждались. Иногда к нему присоединяется S. aureus – золотистый стафилококк, живущий на кожных покровах и в верхних дыхательных путях. Он отвечает за десятки инфекций и заболеваний – от гнойных прыщей до пневмонии и остеомиелита. Но в отличии от pyogenes, aureus лечат со времен открытия пенициллина, и он успешно мутировал, научившись производить пенициллиназу (фермент) для переваривания оного. Та же история повторяется для более современных антибиотиков метициллина и ванкомицина.

Остальные попутчики фасциита зависят от конкретных обстоятельств. Если, например, сожрать сырую морскую мидию, можно познакомиться с Vibrio vulnificus – обитателем морей и океанов, вызывающим гастроэнтерит. Но если жрать сырых мидий вместе с раковинами или иметь в анамнезе язву желудка, можно получить внутреннюю некротическую инфекцию, которая развиваться будет с невероятной скоростью и с бешеными последствиями. Некроз, перфорация - и с десяток сопутствующих штаммов бактерий из пищеварительной системы будет следовать сквозь вас как сепсис-бронепоезд по маршруту пляж – крематорий.
Но даже не строя из себя идиота и не пожирая сырые мидии, добытые с волнорезов на спор, а банально загорая в стационаре, имея ослабленный иммунитет и неуемные загребущие руки, можно легко встретить возбудителя вентилятор-ассоциированной пневмонии Pseudomonas aeruginosa, занести его с расчесыванием катетера в микро-ранку и получить абсцесс, сепсис и – сползающее с костей мясо. Что, с учетом невероятной живучести патогена против большинства антибиотиков, вылечить будет очень сложно.
Безусловно, самые удачливые из нас могут встретить не абы кого, а славный род клостридий. В нем есть совершенно особенный чемпион, Clostridium perfringens. Обитает бактерия везде, вплоть до почвы, умеет формировать споры, анаэробна (не требует кислорода), толстокожа (грамположительна) – имеет самое быстрое время репродуцирования из всех организмов на планете - 6,3 минуты, растет даже в присутствии формальдегида и в ходе размножения производит крайне интересный альфа-токсин. Интересен он в первую очередь тем, что проникает в плазматическую мембрану клеток, провоцирует разрывы в мембранах и вызывает газовую гангрену.
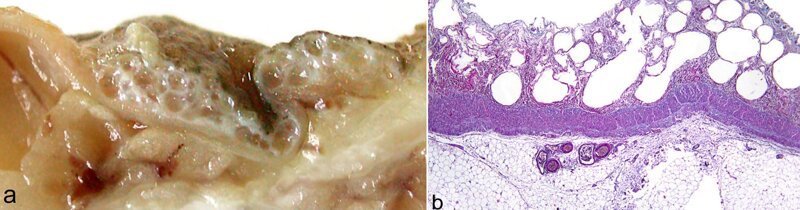
Лично я не знаком ни с одним человеком, кто её наблюдал бы вживую. Но одного описания хватает, чтобы обойтись без ужина. За 6 часов вы переходите от царапины до лихорадки и кожных покровов серо-синего цвета вчерашнего зомби. При надавливания на края первичной раны из тканей и слизистой массы выделяются мелкие пузырьки газа с неприятным, сладковато-гнилостным запахом. При прощупывании конечности и пораженных участков определяется крепитация (похрустывание пузырьков газа, разрывающих клеточные мембраны). Дополняется это всё разрушением сосудов, заполнением полостей кровью и появлением фиолетовых пузырей, напоминающих обратные ожоги. Из лечения – дозы антибиотиков на грани смертельных и экстренная ампутация пораженных конечностей гильотинным типом (это не присказка, а способ экстренного отрезания конечности по кругу и за один раз).
Что же мы имеем в итоге? Бесконечный список бактерий вокруг нас? Быстрое устаревание лекарств? Жуткие болезни, снимающие мясо и кожу с костей? Неотвратимость вымирания? И единственную преграду между ними - нашу иммунную систему.
Читайте также:


