Легионеллез у детей клинические рекомендации
Основные факты
- Бактерия L. pneumophila была впервые выявлена в 1977 году. Она явилась причиной вспышки тяжелой формы пневмонии в одном центре конгрессов в США в 1976 году.
- Наиболее распространенные формы передачи Legionella — это вдыхание зараженных аэрозолей, которые образуются в условиях распыления воды, образования струй или водяного тумана. Инфицирование может также произойти в результате аспирации заряженной воды и льда, в особенности в случае восприимчивых пациентов, находящихся на лечении в больницах.
- Инкубационный период болезни легионеров составляет 2–10 дней (однако в случае ряда вспышек, имевших место, он может составлять до 16 дней).
- Смерть наступает в результате прогрессивной пневмонии с расстройством и/или остановкой дыхания и полиорганной недостаточностью.
- Если болезнь легионеров не лечить, то она обычно ухудшается в течение первой недели.
- По сообщениям, 75–80% больных — это люди старше 50 лет и 60–70% из них — мужчины.
Легионеллез варьируется по степени тяжести от легкого лихорадочного заболевания до серьезной и иногда фатальной формы пневмонии и вызывается воздействием разновидности бактерии Legionella, которая встречаются в воде и почвенных смесях.
Случаи болезни легионеллеза зачастую классифицируют с учетом типа воздействия (приобретенная на уровне сообщества, во время поездки или в условиях стационарного лечения).
Самой распространенной причиной заболевания, включая вспышки, является бактерия Legionella pneumophila. Legionella pneumophila и связанные с ней разновидности обычно встречаются в озерах, реках, ручьях, горячих источниках и других водоемах. Другие разновидности, включая L. longbeachae, можно обнаружить в почвенных смесях.
Бактерия L. pneumophila была впервые выявлена в 1977 году. Она явилась причиной вспышки тяжелой формы пневмонии в центре конгрессов в США в 1976 году. С тех пор она ассоциируется с вспышками, связанными с низкокачественным техническим обслуживанием искусственных водных систем, в особенности в стояках водяного охлаждения и испарительных конденсаторах, используемых в системах кондиционирования воздуха и промышленного охлаждения, системах горячего и холодного водоснабжения в общественных и частных зданиях и в гидромассажных ваннах.
Доза инфицирования неизвестна, однако в случае восприимчивых лиц она, как можно предположить, низка, поскольку симптомы болезни проявляются после непродолжительного воздействия и на расстоянии 3 км и более от источника вспышек. Вероятность болезни зависит от концентрации Legionella в водном источнике, образования и распространения аэрозолей, таких характеристик инфицированного человека, как возраст и предшествующее состояние здоровья, а также вирулентность конкретного штамма Legionella. В большинстве случаев инфицирования болезнь не проявляется.
Причина
Причинными факторами являются бактерии Legionella, находящиеся в водяных или почвенных смесях. Наиболее распространенной причиной болезни является пресноводная разновидность L. pneumophila,которая распространена в естественных акватических условиях во всем мире. Однако наиболее вероятным источником болезни являются искусственные водные системы, которые создают условия, способствующие размножению и распространению Legionella.
Эти бактерии живут и размножаются в водных системах при температуре 20-50 градусов Цельсия (оптимальная температура – 35 градусов Цельсия). Legionella может выживать и размножаться в качестве паразитов в одноклеточных простейших организмах и биопленках, которые образуются в водных системах. Они могут вызывать инфекцию посредством инфицирования клеток человека, механизм которого аналогичен механизму в случае инфицирования простейших микроорганизмов.
Передача
Наиболее распространенной формой передачи Legionella — вдыхание зараженных аэрозолей. Источники аэрозолей, которые ассоциируются с передачей Legionella, включают стояки охлаждения систем кондиционирования воздуха, системы горячего и холодного водоснабжения, увлажнители и гидромассажные ванны. Инфицирование - особенно среди уязвимых пациентов больниц - может также произойти при аспирации загрязненной воды и льда, и при воздействии бактерии на новорожденных детей во время родов в воде. Инфекция не передается непосредственно от человека человеку.
Распространение
Предполагается, что болезнь легионеров распространена во всем мире.
Степень заболеваемости
Степень распространенности известных случаев заболеваемости инфекцией легионеров варьируются в широких пределах в зависимости от уровня эпиднадзора и отчетности. Поскольку во многих странах надлежащие методы диагностики этой инфекции или достаточно развиты системы эпиднадзора отсутствуют, показатели заболеваемости неизвестны. В Европе, Австралии и США в расчете на миллион жителей приходится около 10-15 случаев в год.
По сообщениям, 75-80% больных — это люди в возрасте старше 50 лет и 60-70% из них — мужчины. Другие факторы риска внебольничного легионеллеза, не связанного с поездками, включают: курение, неумеренное потребление спиртных напитков, болезнь легких, нарушение иммунитета и хронические респираторные или почечные болезни.
Факторы риска больничной пневмонии включают следующие: недавно перенесенная хирургическая операция, интубация, которая представляет собой процесс введения трубки в трахею, механическая вентиляция, аспирация, наличие назогастральных трубок и использование оборудования респираторной терапии. Наиболее восприимчивыми субъектами являются пациенты с нарушенной иммунной системой, включая пациентов, перенесших операцию по трансплантации органов, и онкологических больных, а также пациентов, принимающих кортикостероиды.
Прогностическими факторами смерти вследствие болезни легионеров является поздняя диагностика и позднее назначение надлежащего лечения с помощью антибиотиков, преклонный возраст и наличие сопутствующих болезней.
Симптомы
Легионеллез является общим термином, который описывает легочные и нелегочные формы инфекции Legionella.
Нелегочная форма (болезнь Понтиака) представляет собой острую самоизлечивающуюся гриппоподобную болезнь, которая обычно длится от 2 до 5 дней. Инкубационный период составляет от нескольких часов до 48 часов. Основные симптомы: жар, озноб, головная боль, недомогание и мышечная боль (миалгия). Этот тип инфекции к летальному исходу не приводит.
Продолжительность инкубационного периода легочной формы болезни легионеров составляет от 2 до 10 дней (однако в ряде имевших место случаев вспышек, он составлял до 16 дней). Вначале симптомы проявляются в виде жара, потери аппетита, головной боли, недомогания и летаргии. У некоторых пациентов могут наблюдаться боли в мышцах, диарея и состояние спутанности. Обычно также наблюдается легкий кашель, однако до 50% пациентов могут выделять мокроту. Мокрота со следами крови или кровохарканье может наблюдаться приблизительно у одной трети пациентов. Тяжесть этой болезни варьируется от легкого кашля до быстротекущей летальной пневмонии. Смерть наступает в результате прогрессивной пневмонии с расстройством и/или остановкой дыхания и полиорганной недостаточностью.
Если болезнь легионеров не лечить, то она обычно ухудшается в течение первой недели. Подобно другим факторам риска, вызывающим тяжелую форму пневмонии, наиболее частыми осложнениями в случае легионеллеза является легочная недостаточность, шок и острая недостаточность почек и других органов. Восстановление функций во всех случаях нуждается в лечении с помощью антибиотиков и обычно занимает нескольких недель или месяцев. В редких случаях тяжелая прогрессивная пневмония или неэффективное лечение пневмонии может дать осложнение на мозг.
Показатели смертности в результате болезни легионеров зависят от тяжести заболевания, соответствия первоначального лечения с помощью противомикробных препаратов, места инфицирования легионеллой и характеристик больного (это означает, что данная болезнь обычно протекает в более серьезной форме в случае пациентов с нарушенным иммунитетом). Показатель смертности может достигать 40-80% среди пациентов, которые не проходят лечения в связи с ослабленным иммунитетом, и может быть снижена до 5-30% за счет надлежащего ведения больного и в зависимости от тяжести клинических показаний и симптомов. В целом показатель смертности обычно составляет 5–10%.
Деятельность ВОЗ
В настоящее время никакой вакцины против болезни легионеров не существует.
Угрозу легионнелеза в области общественного здравоохранения можно снять посредством осуществления планов по обеспечению безопасности воды на уровне органов, ответственных за безопасность строительных объектов или водных систем. Эти планы должны носить конкретный характер применительно к строениям или водным системам и предусматривать введение в действие и регулярное отслеживание мер по борьбе с выявленными рисками, включая наличие бактерии Legionella. Хотя искоренить источник инфекции не всегда возможно, тем не менее существенно снизить уровень риска вполне возможно.
Профилактика болезни легионеров зависит от принятия мер по контролю в целях сведения до минимума размножения легионеллы и распространения аэрозолей. Эти меры включают надлежащее техническое обслуживание соответствующих устройств, включая регулярную чистку и дезинфекцию и применение других физических (температура) или химических (биоциды) мер с целью свести их размножение до минимума. В качестве примеров можно привести следующие:
- регулярное техническое обслуживание, чистка и дезинфекция стояков охлаждения, а также частое или постоянное добавление биоцидов;
- установка каплеуловителей для предотвращения распространения аэрозолей из стояков охлаждения;
- поддержание адекватного уровня таких биоцидов, как хлор, в бассейнах наряду с полным дренажем и чисткой всей системы не реже 1 раза в неделю;
- поддержание систем горячего и холодного водоснабжения в чистоте и либо поддержание температуры горячей воды на уровне более 50 °C (для этого необходимо, чтобы температура воды, вытекающей из нагревательного устройства, была на уровне не менее 60 °C) и холодной ниже 25 °C, а в идеале ниже 20 °C, и альтернативная обработка этих систем подходящим биоцидом для ограничения размножения бактерии, особенно в больницах и других медицинских учреждениях и в домах престарелых;
- уменьшение застоя путем еженедельного слива воды из неиспользуемых кранов в зданиях.
Применение таких видов контроля существенно снижает риск заражения легионелой и позволяет предотвратить возникновение спорадических случаев заболевания и вспышек. В случае весьма восприимчивых пациентов в стационарных условиях лечения, в том числе тех, которые подвергаются риску аспирации (например, генераторы льда могут быть источниками Legionella и не должны использоваться такими пациентами).
Меры борьбы и профилактики должны приниматься в условиях надлежащей бдительности со стороны врачей общей практики и медико-санитарных служб на местном уровне в целях выявления случаев заболевания.
ВОЗ предоставляет технические ресурсы для содействия в области ведения пациентов и борьбы с легионеллезом, а также рекомендации государствам-членам по конкретным вопросам.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Государственный институт усовершенствования врачей МО РФ, Москва
Воспаление легких, вызываемое M.pneumoniae, наиболее часто диагностируется у детей и лиц молодого возраста, достигая среди указанных контингентов 20–30% от числа всех этиологически верифицированных внебольничных пневмоний. Напротив, в старших возрастных группах микоплазменная пневмония диагностируется, как исключение (1–3%). Наряду со спорадическими случаями наблюдаются и групповые (эпидемические) вспышки заболевания – в основном в организованных коллективах (школьники, военнослужащие).
Микоплазменная пневмония, как правило, сопровождается ознобом, мышечными и головными болями, симптомами инфекции верхних дыхательных путей. Напротив, кровохарканье и боли в груди весьма нетипичны.
При стетоакустическом обследовании удается получить зачастую весьма скудную информацию: локально выслушиваются мелкопузырчатые хрипы или незвучная инспираторная крепитация при отсутствии укорочения (притупления) перкуторного звука. Нередко определяются шейная лимфаденопатия, полиморфные кожные сыпи, гепатоспленомегалия.
При рентгенографии органов грудной клетки обнаруживается неоднородная инфильтрация легочной ткани, локализующаяся преимущественно в нижних долях легких, причем в 10–40% случаев процесс имеет двусторонний характер. Массивная очагово–сливная инфильтрация, полостные образования, плевральный выпот для микоплазменной пневмонии не характерны. Нередко даже в случаях своевременно назначенной адекватной антибактериальной терапии пневмоническая инфильтрация разрешается спустя многие недели, существенно отставая от клинического выздоровления.
Известно, что M.pneumoniae инициирует выраженную поликлональную пролиферацию лимфоцитов. Именно этим обстоятельством можно объяснить многообразие внелегочных иммунологически опосредованных проявлений заболевания – кожных, суставных, гематологических, гастроинтестинальных, неврологических и др. В свое время особое внимание в диагностике микоплазменной инфекции уделялось феномену высокого титра холодовых гемагглютининов с субклиническим гемолизом (положительная проба Кумбса, ретикулоцитоз). Однако, как было установлено в последующем, данная лабораторная находка не является специфичной для микоплазмоза и с разной частотой обнаруживается при цитомегаловирусной инфекции, легионеллезе, эпидемическом паротите и особенно при инфекционном мононуклеозе.
Выделение культуры Mycoplasma pneumoniae – чрезвычайно трудоемкий и длительный процесс (микроорганизм растет крайне медленно, требует 7–14 сут., часто и гораздо более длительных сроков инкубации, а также специальных сред, содержащих все предшественники, необходимые для синтеза макромолекул, способных обеспечить микоплазмы источниками энергии) – см. табл. 2.
Определение антигена микоплазмы может быть достигнуто несколькими методами. Использование поликлональной антисыворотки характеризуется очень малой специфичностью, поскольку значительное число индивидов являются здоровыми носителями инфекции. Обнаружение антигена в мокроте с использованием реакции иммуноферментного анализа (ИФА) демонстрирует вариабельную чувствительность (40–81%) и специфичность (64–100%), если при этом в качестве референс–метода рассматривается выделение культуры возбудителя. Имеющиеся в арсенале современных лабораторий коммерческие ДНК–РНК–пробы, дающие возможность идентифицировать M.pneumoniae в мазках из зева, характеризуются высокой специфичностью, но низкой чувствительностью. В настоящее время все большее внимание привлекает технология полимеразной цепной реакции (ПЦР), однако для дифференциации активной и персистирующей инфекции необходимо проведение серологических тестов.
Тест холодовой агглютинации ввиду его низкой чувствительности и специфичности в настоящее время в клинической практике не используется. Реакция связывания комплемента демонстрирует вариабельную чувствительность (50–90%) и субоптимальную специфичность. Наиболее приемлемым стандартом серологической диагностики микоплазменной инфекции сегодня является ИФА с обнаружением специфических IgG и IgM. ИФА демонстрирует высокую чувствительность и специфичность – 92% и 95% соответственно. Время сероконверсии, т.е. четырехкратного возрастания титра антимикоплазменных антител при последовательном исследовании проб крови, взятых в остром периоде заболевания и в периоде реконвалесценции, обычно составляет 3–8 недель.
Каждый из трех известных в настоящее время видов хламидий способен вызывать воспаление легких: Chlamydia trachomatis – отдельные случаи пневмонии у новорожденных; Chlаmydophila psittaci – поражение легких при пситтакозе (орнитозе); Chlamydophila pneumoniae – весьма распространенный возбудитель пневмонии и острого бронхита у взрослых и детей. Собственно C.pneumoniae, как уже говорилось выше, и рассматривается как один из актуальных возбудителей атипичной пневмонии. Этиологический вклад Chlamydia pneumoniae в развитие внебольничной пневмонии, преимущественно у лиц молодого возраста, составляет 3–10%.
Клиническая картина респираторного хламидиоза, ввиду его недостаточной изученности, представляется менее определенной, нежели, например, микоплазменной инфекции. Установлено весьма распространенное бессимптомное или малосимптомное течение С.pneumoniae–инфекции. Так, при обследовании военнослужащих–новобранцев было подтверждено, что только у 10% из числа лиц с серологически верифицированной активной хламидийной инфекцией обнаруживались клинико–рентгенологические признаки пневмонии. Наверное, именно этот факт и объясняет значительную частоту бессимптомных серопозитивных лиц (25–86%), причем с возрастом частота циркуляции антихламидийных антител в популяции возрастает. Бессимптомное назофарингеальное носительство C.pneumoniae определяется примерно у 5–7% обследуемых здоровых детей, что предполагает возможность передачи инфекции от человека к человеку с респираторными секретами.
Клиническая картина хламидийной пневмонии часто оказывается схожей с таковой при микоплазменной пневмонии. Лихорадка и малопродуктивный приступообразный кашель встречаются в 50–80% случаев. Выраженная гиперемия зева и боли при глотании, часто сопровождаемые осиплостью голоса, наблюдаются более чем у трети больных, нередко являясь дебютными и/или наиболее демонстративными признаками заболевания.
При рентгенографии органов грудной клетки чаще визуализируется мелкоочаговая (размером 2–3 см), нередко многофокусная инфильтрация. Лобарная инфильтрация, образование полостей в легких и плевральный выпот нетипичны для хламидийной пневмонии. Количество лейкоцитов и лейкоцитарная формула в периферической крови обычно нормальные.
Хламидийная пневмония характеризуется, как правило, нетяжелым, но нередко затяжным течением.
Первоначально для выделения культуры C. pneumoniae использовались 6–7–дневные куриные эмбрионы (возбудитель наиболее интенсивно размножается в эктодермальных клетках оболочки желточного мешка). Впрочем, затем выяснилось, что этот метод демонстрирует низкую чувствительность. В конечном счете выбор был сделан в пользу перевиваемой линии клеток человека (Hеlа, La 229), до того использовавшейся для выделения респираторного синцитиального вируса (табл. 3).
Обычно вначале проводят определение IgG, предваряя этим тестом определение IgM. Таким образом, исключается ложноположительное определение IgM в случаях наличия ревматоидного фактора, особенно у пожилых пациентов. Свидетельствами активной хламидийной инфекции являются четырехкратное нарастание титров IgG или IgA в парных сыворотках крови, взятых с 2–4–недельным интервалом в остром периоде заболевания и в периоде реконвалесценции, или однократно определяемый высокий титр антихламидийных антител (например, IgG>=1:512).
В настоящее время активно обсуждается перспектива клинического применения ПЦР в диагностике хламидийной инфекции. Однако относительная сложность в проведении и высокая цена сдерживают масштабное распространение этой диагностической технологии. Впрочем, ПЦР позволяет осуществить быструю диагностику, что может в части случаев оказаться полезным в плане выбора соответствующей антимикробной химиотерапии.
Физическая симптоматика легионеллезной пневмонии, как правило, убедительна: локальная крепитация, признаки консолидации легочной ткани (бронхиальное дыхание, укорочение перкуторного звука). Рентгенологические данные неспецифичны – визуализируется очаговая пневмоническая инфильтрация, локализующаяся обычно в пределах одной доли легких. Нередко одновременно обнаруживается и ограниченный плевральный выпот и, напротив, нечасто, обычно на поздних стадиях болезни, формируются полостные образования в легких. Процесс нормализации рентгеновской картины занимает обычно длительное время, иногда несколько месяцев.
Данные лабораторных исследований, хотя и несут неспецифическую информацию, но, указывая на полисистемность поражения, могут быть использованы, как определенный диагностический критерий. Так, в анализах мочи определяется гематурия и протеинурия; в крови часто выявляются повышенная активность щелочной фосфатазы, креатинфосфокиназы, аминотрансфераз, гипербилирубинемия. В клинической гемограмме обнаруживаются лейкоцитоз с нейтрофилезом и абсолютная лимфопения, значительное увеличение СОЭ.
L.pneumophila – чрезвычайно трудный для культивирования микроорганизм (табл. 4). Метод выделения культуры возбудителя демонстрирует широкий диапазон чувствительности – от 11 до 80% (в сравнении с детекцией антигена).
Тест прямой иммунофлюоресценции наиболее популярен в клинической практике. Он очень быстр в выполнении, но его чувствительность вариабельна и относительно невысока (18–75%). Чувствительность прямой иммунофлюоресценции возрастает до 80%, если этот метод подкрепляется культуральным или если респираторные секреты (трахеальный аспират или жидкость бронхоальвеолярного лаважа) предварительно обработаны. Специфичность теста может достигать 94%. Спустя 4–6 дней после начала адекватной антибактериальной терапии определение антигена становится невозможным.
Антиген L.pneumophila может быть также обнаружен в моче радиоиммунологически, с использованием ИФА или в реакции латексной агглютинации. Однако следует иметь в виду, что легионеллезный антиген может персистировать в течение многих месяцев после выздоровления, а ИФА пригоден только для идентификации L.pneumophila, 1–й серогруппы.
Наиболее популярная сегодня диагностика легионеллеза предполагает идентификацию специфических антител – непрямая иммунофлюоресценция, ИФА и микроагглютинация. В типичных случаях сероконверсия (четырехкратное нарастание титра специфических антител) наблюдается через 4–8 недель, однако у лиц старших возрастных групп этот временной интервал может достигать 14 недель. Следует также учитывать тот факт, что 20–30% пациентов, переносящих острую легионеллезную инфекцию, не демонстрируют нарастания титра антител. ИФА характеризуется высокой специфичностью (95%) и приемлемой чувствительностью (85%) при определении специфических IgG и IgM. Описываются отдельные наблюдения перекрестных реакций с Pseudomonas aeruginosa, Chlamydia/Chlamydophila spp., Mycoplasma pneumoniae и Campylobacter spp.
Лечение атипичной пневмонии
Рис. 1. Алгоритм эмпирической антибактериальной терапии нетяжелой внебольничной пневмонии (по A.Ortqvist, 2002 [4], с изменениями)
При нетяжелом течении атипичной пневмонии (вероятнее всего, микоплазменной или хламидийной этиологии) макролиды следует назначать внутрь в среднетерапевтических дозах – эритромицин по 250–500 мг каждые 6 часов; кларитромицин по 250 мг каждые 12 часов; азитромицин по 500 мг 1 раз в день в течение 3–х дней или по 250 мг 2 раза в день в 1–й день и по 250 мг 1 раз в день со 2–го по 5–й дни.
В последние годы была показана и высокая клиническая эффективность новых фторхинолонов в лечении легионеллезной пневмонии (левофлоксацин, 500 мг один раз в сутки в течение 10–14 дней) [8].
Продолжительность антибактериальной терапии атипичной пневмонии составляет не менее 2–3–х недель; минимизация сроков лечения несет в себе реальный риск рецидива инфекции. При этом следует еще раз напомнить, что зачастую клиническое выздоровление при микоплазменной, хламидийной или легионеллезной инфекциях нижних дыхательных путей существенно опережает более позднее рентгенологическое, которое порой затягивается на многие недели или даже месяцы.
1. Niederman M.S., Mandell L.A., Anzueto A. et al. Guidelines for the management of adults with community–acquired pneumonia. Diagnosis, assessment of severity, antimicrobial therapy, and prevention. Am J Respir Crit Care Med 2001; 163: 1730–1754.
2. British Thoracic Society Guidelines for the management of community–acquired pneumonia in adults. Thorax 2001; 56 Suppl. 4: 1–64.
3. M.J.Fang, M.Fine, J.Orloff et al. New and emerging etiologies for community–acquired pneumonia with implications for therapy: a prospective multicenter study of 359 cases. Medicine 1990; 69:307–316.
4. Ortqvist A. Treatment of community–acquired lower respiratory tract infections in adults. Eur Respir J 2002; 20: Suppl. 36, 40s–53s.
5. И.С.Тартаковский. Современные подходы к диагностике атипичных пневмоний. Клиническая микробиология и антимикробная химиотерапия 2000; 1: 60–68.
6. Reese R.E., Betts R.F., Gumustop B. Handbook of antibiotics. 3rd ed. Philadelphia:Lippincott Williams & Wilkins; 2000
7. File T.M., Tan J.S. Plouffe J. F. The role of atypical pathogens: Myciplasma pneumoniae, Chlamydia pneumoniae, and Legionella pneumophila in respiratory infections. Infect Dis Clin North Am 1998; 12: 569–592.
8. Chidiac C. Legionella pneumophila effectively managed by levofloxacin. Abstracts of 7th International Symposium of New Quinolones. Edinburgh, UK, 2001; 57.









Основные ссылки
Вы здесь


Артикул: 852-000
Производитель: Alere Inc., США 
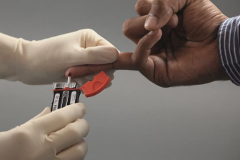
Экспресс-тест для определения антигена L.pneumophila (возбудителя Легионеллёза) в моче иммунохроматографическим методом.
Регистрационное удостоверение
ИХА тест "Binax NOW® Legionella" входит в стандарт оказания медицинской помощи, приказ МЗ РФ №741н от 9.11.2012 "Об утверждении стандарта специализированной медицинской помощи при пневмонии тяжелой степени тяжести с осложнениями": А26.28.010 Определение антигена возбудителя легионеллеза (Legionella pneumophila) в моче.
ИХА тест "Binax NOW® Legionella" входит в стандарты диагностики пневмонии, утвержденные в России:
В связи со сходством клинических проявлений и симптоматики легионеллезной и пневмококковой пневмонии быстрая и эффективная лабораторная диагностика приобретает решающее значение для выбора тактики этиотропной терапии больных.
В 1999 г. ВОЗ и в 2002 г. Европейской рабочей группой по легионеллезу в качестве диагностических критериев приняты стандарты, в соответствии с которыми диагноз легионеллеза в случае острой инфекции нижних дыхательных путей (клинически и рентгенологически подтвержденной) считается установленным:
1) при выделении культуры легионелл из отделяемого респираторного тракта или легочной ткани;
2) при 4-кратном или более нарастании титра специфических антител к Legionella pneumophila серогруппа 1 в реакции непрямой иммунофлюоресценции;
3) при определении растворимого антигена Legionella pneumophila серогруппа 1 в моче иммуноферментным (ИФА) или иммунохроматографическим методом (ИХА)
ИХА тест рекомендован Роспотребнадзором для установления диагноза легионеллёза с 2008 года:
"Выявление антигена бактерий Legionella pneumophila серогруппы 1 в клиническом материале иммунохроматографическим методом" Методические рекомендации, утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом РФ Г.Г. Онищенко 09 декабря 2008 N 01/14633-8-34 и введены в действие.
Тесты Бинакс одобрены FDA (Администрация по пищевым продуктам и лекарственным средствам США), и в настоящее время в более чем 90% случаев окончательного диагноза внебольничной пневмонии в мире устанавливается данным методом.
Выявление возбудителя пневмоний в моче ИХА методом включено в руководства по пневмонии Америки, Британии, Бразилии, Франции, Европы, Швеции, Испании, Канады:
Общество инфекционных болезней Америки/Руководства американского торакального общества по управлению внебольничной пневмонией у взрослых
Руководства британского торакального общества по управлению внебольничной пневмонией у взрослых:
Бразильские руководства по внебольничной пневмонии у имуннокомпетентных взрослых
Французские Руководства Лечение инфекций нижних дыхательных путей у иммунокомпетентных взрослы х
Европейские Руководства по управлению инфекциями нижних дыхательных путей у взрослых
Шведкие руководства по управлению внебольничной пневмонией у имуннокомпетентных взрослых
Руководства Испанского общество пульмонологии и торакальной хирургии
Канадские руководства по начальному управлению внебольничной пневмонии.
Предназначение:
Тест для определения возбудителя легионеллёза Binax NOW® Legionella – быстрый in vitro иммунохроматографический анализ для качественного определения антигена Legionella pneumophila серогруппы 1 в образцах мочи у пациентов с симптомами пневмонии. Он предназначен для помощи в постановке предположительного диагноза легионеллезной инфекции (болезнь легионеров), вызванной L. pneumophila серогруппы 1, в сочетании с культуральным и другими методами.
Аналогов данного теста нет ни Российского, ни Зарубежного производства.
В дополнение к быстрому тесту выпускается ИФА тест на легионеллу Binax® Legionella Urinary Antigen EIA для классического иммуноферментного анализа. ИФА тест-система на легионеллёз Binax® Legionella Urinary Antigen EIA предназначена для качественного определения Legionella pneumophila серогруппы 1 в образцах мочи, как дополнение к культуральному методу для постановки предположительного диагноза прошедшей или текущей болезни легионеров.
Binax NOW® Legionella – один из наиболее широко известных быстрых иммунохроматографических тестов для определения антигена возбудителя легионеллеза (Legionella pneumophila) в моче, благодаря его чувствительности, специфичности и простоте использования.
Время постановки: 15 минут
Чувствительность: 95%
Специфичность: 95%
Исследуемый образец: Моча
Количество тестов: 22
Индивидуальный анализ: Есть
Еще в начале 80-х годов прошлого века было показано, что в самом начале болезни (2-3-е сутки) антиген возбудителя можно обнаружить в моче больного легионеллезом, причем сам возбудитель в моче отсутствует. Антиген термастабилен и может быть выявлен в течение примерно 30 дней после начала заболевания. В 1989 г. метод был стандартизован компаниями Binax (США) и Biotest (Германия), испытан 14 лабораториями Европейских стран (включая лабораторию легионеллеза ГУ НИИЭМ им. Н.Ф. Гамалеи РАМН) и был рекомендован в качестве высокоспецифичного и чувствительного метода, позволяющего поставить окончательный диагноз на первой неделе заболевания.
Если непосредственно после введения стандарта определения антигена L. pneumophila в моче данный метод использовали для диагностики менее чем в 5% случаев, то в настоящее время метод применяют для постановки окончательного диагноза более чем в 90% подтвержденных случаев легионеллезной инфекии. Превосходство данного метода над традиционными, включенными в стандарт бактериологическим и серологическим методами состоит, прежде всего, в сроках исследования. Бактериологический метод занимает не менее 4-5 суток, причем требуются инвазивные процедуры для получения материала (бронхоскопия, биопсия), так как из мокроты, особенно после начала элютропной терапии, возбудитель удается выделить далеко не всегда. Выявление диагностического нарастания титров антител в реакции непрямой иммунофлюоресценции возможно лишь на третьей неделе заболевания, когда проведен курс антибиотикотерапии и исход заболевания обычно уже ясен. Необходимость, исследования парных сывороток определяет ретроснективный характер диагностики легионеллеза данным методом.
Читайте также:




