Кто вылечил стрептококк влагалища отзывы
Среди 18 видов и 8 родственных групп бактерий, причисленных к важнейшим патогенам человека, особую роль играют стрептококки. По медицинской значимости они занимают второе место после стафилококков. Из числа стрептококков, патогенных для человека, с середины 80-х гг. ХХ столетия во многих странах мира наблюдается рост заболеваемости, обусловленной β-гемолитическими стрептококками группы А (БГСА, S.pyogenes).
β-гемолитический стрептококк группы А (пиогенный стрептококк, БГСА S.pyogenes) - грамположительный, неспорообразующий, неподвижный микроорганизм. Растёт на кровяном агаре, обладает выраженной гемолитической активностью, каталазанегативный, чувствителен к бацитрацину. Встречается повсеместно, часто колонизирует кожные покровы и слизистые оболочки человека. Главными путями передачи являются воздушно-капельный, контактный и пищевой. Патогенез заболеваний связан с продукцией токсинов: гемолизин, стрептолизин, стрептокиназы А и В, дезоксирибонуклеаза, гиалуронидаза. Основные нозоформы представлены поверхностными (ангины, фарингит, импетиго, рожа), инвазивными (некротизирующий фасциит, миозит, менингит, эндокардит, пневмония, послеродовой сепсис) и токсин-опосредованными инфекциями (скарлатина, синдром токсического шока). Со стрептококковой инфекцией связано также возникновение неврологических расстройств у детей, проявляющихся обсессивно-компульсивными расстройствами (PANDAS-синдром).
Streptococcus pyogenes сохраняет 100% чувствительность к β-лактамным антибиотикам (пенициллинам, цефалоспоринам, карбапенемам). Они остаются единственным классом антибиотиков, к которым у S.pyogenes не развилась резистентность. Актуальной проблемой является устойчивость к макролидам, которая в некоторых регионах мира превышает 30%. Многоцентровое исследование резистентности клинических штаммов S.pyogenes, проведённое в 2000-2001 гг., позволило изучить распространенность устойчивости, прежде всего к макролидам, в различных регионах России. Частота резистентности к эритромицину варьировала и достигала 11,4%, при этом не было обнаружено штаммов, устойчивых к телитромицину, представителю нового класса антибиотиков - кетолидов. Почти в 90% случаев резистентность к макролидам была обусловлена метилированием рибосом, в остальных случаях она была связана с активным выведением (эффлюксом) антибиотика из клетки.
Стрептококковый тонзиллофарингит
Стрептококковый тонзиллофарингит (ангина) - острое общее инфекционное заболевание с преимущественным поражением лимфоидного аппарата и слизистой оболочки глотки, вызванное БГСА. Под рецидивирующим стрептококковым тонзиллофарингитом следует понимать множественные эпизоды заболевания в течение нескольких месяцев с положительными результатами бактериологических и/или экспресс-методов диагностики БГСА, отрицательными результатами исследований между эпизодами заболевания, повышением титров противострептококковых антител после каждого случая болезни.
Этиология: среди бактериальных возбудителей острого тонзиллофарингита наибольшее значение имеет БГСА.
Эпидемиология. В США ежегодно диагностируется 1-1,4 млн. случаев тонзиллофарингита БГСА-этиологии. Передача осуществляется воздушно-капельным, контактным и пищевым путями. Источниками инфекции являются больные, реже - бессимптомные носители. Вероятность заражения увеличивается при высокой обсемененности и тесном контакте. БГСА может вызывать крупные вспышки тонзиллофарингита в организованных коллективах. Чаще болеют дети в возрасте 5-15 лет. Наибольшая заболеваемость - в зимне-весенний период.
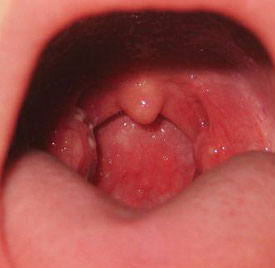
Клиническая картина: Инкубационный период составляет от нескольких часов до 2-4 дней. Характерно острое начало с повышения температуры тела до 37,5-39°С, выражена общая интоксикация. Боль в горле бывает так сильно выражена, что у больного нарушается глотание. При осмотре выявляется покраснение нёбных дужек, язычка и задней стенки глотки. Миндалины гиперемированы, отёчны, часто с гнойным налётом желтовато-белого цвета. Налёт рыхлый, пористый, легко удаляется шпателем с поверхности миндалин без кровоточащего дефекта. У всех больных отмечается регионарный лимфаденит.
Кровь: лейкоцитоз, сдвиг лейкоцитарной формулы влево, увеличение СОЭ, появление С-реактивного белка.
Длительность периода разгара (без лечения) составляет 5-7 дней. В дальнейшем, при отсутствии осложнений, основные клинические проявления болезни быстро исчезают.
Осложнения. Особую опасность представляют осложнения стрептококкового тонзиллофарингита, которые делятся на:
- ранние (гнойные), развивающиеся на 4-6-й день от начала заболевания,- отит, синусит, мастоидит, паратонзиллярный абсцесс, шейный лимфаденит, менингит, бактериемия, эндокардит, пневмония;
- поздние (негнойные): постстрептококковый гломерулонефрит, токсический шок, развивающиеся в стадии реконвалесценции (на 8-10-й день от начала болезни) и острая ревматическая лихорадка, развивающаяся через 2-3 нед после купирования симптомов заболевания - опасные, часто приводящие к инвалидизации заболевания.
Диагностика. Чрезвычайно важно своевременно установить этиологию тонзиллофарингита, поскольку, за редким исключением, только ангина стрептококковой этиологии требует антибактериальной терапии. Диагностика включает микробиологическое исследование мазка с поверхности миндалин и/или задней стенки глотки. За рубежом широкое распространение получили методы экспресс-диагностики, основанные на прямом выявлении стрептококкового антигена в мазках с поверхности миндалин и/или задней стенки глотки. Современные тестовые системы позволяют получать результат через 15-20 мин с высокой специфичностью (95-100%), но меньшей, чем при культуральном исследовании, чувствительностью (60-95%), в связи с чем отрицательный результат экспресс-теста всегда должен подтверждаться культуральным исследованием.
Целью антибиотикотерапии острых стрептококковых ангин является эрадикация БГСА, что ведёт не только к ликвидации симптомов инфекции, но и предупреждает ранние и поздние осложнения, а также предотвращает распространение инфекции.
Выбор антибиотиков. Препаратами I ряда для лечения острого стрептококкового тонзиллита являются пенициллин (феноксиметилпенициллин), аминопенициллины и оральные цефалоспорины. У пациентов с доказанной аллергией на β-лактамные антибиотики следует применять макролиды, а при непереносимости последних - линкозамиды.
Носительство БГСА. В среднем около 20% детей школьного возраста являются носителями БГСА в весенне-зимнее время. Учитывая низкий риск развития гнойных и негнойных осложнений, а также незначительную роль в распространении БГСА, хронические носители, как правило, не нуждаются в антибактериальной терапии.
Острая ревматическая лихорадка
Острая ревматическая лихорадка (ОРЛ) может возникать как после тонзиллофарингита с типичной клинической картиной, так и после перенесённой бессимптомной или малосимптомной инфекции. ОРЛ возникает только после инфекций глотки, и никогда после инфекций кожи и мягких тканей. Предположительное объяснение этого феномена состоит в различии иммунного ответа на кожную и глоточную инфекцию и в отсутствии ревматогенного потенциала у штаммов, вызывающих кожные инфекции. Риск развития ОРЛ после нелеченного тонзиллофарингита составляет 1%. К ревматогенным М-серотипам стрептококка относятся 1, 3, 5, 6, 18, 19, 24.
В настоящее время в развитых странах острая ревматическая лихорадка встречается с частотой 0,5 на 100000 детей школьного возраста. В развивающихся странах заболеваемость составляет от 100 до 200 на 100000 детей школьного возраста, ежегодно регистрируется от 10 до 15 млн. новых случаев ОРЛ, которая является основной причиной смерти от сердечно-сосудистой патологии.
Следует отметить, что немотивированная задержка восстановления трудоспособности, слабость, нестойкий субфебрилитет, артралгии, сердцебиение и нерезко повышенная СОЭ, сохраняющиеся после перенесенной ангины, в сочетании с ростом титров противострептококковых антител (антистрептолизин О, антистрептокиназа, антистрептогиалуронидаза, анти-ДНКаза В) могут свидетельствовать о дебюте острой ревматической лихорадки.
В соответствии с рекомендациями ВОЗ для диагностики острой ревматической лихорадки в качестве международных применяются критерии Джонса, пересмотренные Американской кардиологической ассоциацией в 1992 г. (см. табл.). Наличие двух больших критериев или одного большого и двух малых в сочетании с данными, документированно подтверждающими предшествующую БГСА-инфекцию, свидетельствует о высокой вероятности ОРЛ. Однако ни один диагностический критерий не является строго специфичным для ОРЛ, поэтому трудности в раннем распознавании заболевания и дифференциальной диагностике с другими нозологиями сохраняются по-прежнему.
Критерии Джонса, применяемые для диагностики первой атаки ревматической лихорадки (по состоянию на 1992 г.)
Стрептококк ( лат. Streptococcus) – это бактерия шарообразной или яйцеподобной формы, принадлежащая к семейству Стрептококковые (Streptococcaceae).
Стрептококки являются анаэробными паразитами не только человека, но и животных. Местом обитания и размножения стрептококковой инфекции являются органы дыхания, желудочно-кишечного тракта и мочеполовой системы мужчин и женщин, может находиться на коже. Преобладающее же количество бактерий стрептококк обычно оседает в носу, ротовой полости, горле и толстом кишечнике, иногда встречается в уретре мужского органа и влагалище женщины.
В природе, данный вид бактерий также существует в земле, на поверхности растений, грибов.
Стрептококковая инфекция является условно-патогенной микрофлорой, — она практически всегда присутствует в организме человека и не несет в себе какую-либо опасность, поскольку ее количество и пребывание в человеке контролирует иммунная система. Однако, как только человеку стоит ослабеть (стрессы, переохлаждение организма, гиповитаминоз и т.д.), бактерии сразу же начинают активно размножаться, выделять в организм большое количество продуктов своей жизнедеятельности, отравляя его, и провоцировать развитие различных заболеваний, как написано выше, преимущественно – дыхательной, пищеварительной и мочеполовойсистем. И потому, основным превентивным действием против развития стрептококковой инфекции в организме, и связанных с ней заболеваний, является укрепление и поддержание нормального функционирования иммунитета. Однако не следует считать все виды стрептококков патогенными, — некоторые из них являются полезными бактериями, например — Streptococcus thermophilus, которые применяются при производстве кисло-молочной продукции – йогуртов, сметаны, моцареллы и других.
Основные способы заражения стрептококковой инфекцией – воздушно-капельный и контактно-бытовой путь.
Заболевания, которые способны вызвать стрептококки
- Абсцесс;
![]()
- Бронхит;
- Васкулит;
- Гломерулонефрит;
- Импетиго;
- Лимфаденит;
- Менингит;
- Остеомиелит;
- Острый тонзиллит (ангина);
- Пародонтит;
- Пневмония;
- Ревматизм;
- Рожистое воспаление (рожа);
- Сепсис;
- Скарлатина;
- Стрептодермия;
- Фарингит;
- Хейлит, заеды;
- Эндокардит;
- Заболевания мочеполовой системы.
Кроме того, стрептококковая инфекция может стать вторичной инфекцией, присоединяясь, например к стафилококковой, энтерококковой и другим видам инфекции.
Наиболее часто, заболеваниями стрептококковой этиологии болеют дети, люди преклонного возраста, а также офисные работники.
Давайте немного рассмотрим краткую характеристику бактерий – стрептококк.
Стрептококк представляет собой типичные клетки, диаметр которых составляет менее 1 мкм, располагающиеся попарно или цепочками, образуя вытянутую палочку с утолщениями и утончениями, по форме напоминающую бусинки, нанизанные на цепочку. Из-за этой формы они и получили свое название. Стрептококковые клетки образуют капсулу, и способны легко превратиться в L-форму. Бактерии неподвижны, за исключением штаммов группы D. Активное размножение происходит при контакте с частичками крови, асцитической жидкости или углеводами. Благоприятная температура для нормальной жизнедеятельности инфекции +37°С, кислотно-щелочный баланс (рН) – 7,2-7,4. Живут стрептококки преимущественно колониями, образуя как бы сероватый налет. Перерабатывают (ферментируют) углеводы, образовывая кислоту, расщепляют аргинин и серин (аминокислоты), в питательной среде синтезируют внеклеточно такие вещества, как — стрептокиназа, стрептодорназа, стрептолизины, бактериоцины и лейкоцидин. Некоторые представители стрептококковой инфекции – группы В и D образовывают красные и желтые пигменты.

Стрептококковая инфекция включает в себя около 100 видов бактерий, наиболее популярными из которых являются – пневмококки и гемолитические стрептококки.
Как инактивировать стрептококк?
Бактерии стрептококки погибают при:
— их обработке растворами антисептиков и дезинфектантов;
— пастеризации;
— воздействии антибактериальных средств – тетрациклинов, аминогликозидов, пенициллинов (не применяется при инвазивной стрептококковой инфекции).
Как передается стрептококк? Рассмотрим наиболее популярные пути заражения стрептококковой инфекцией.
Условия, при которых человек начинает заболевать стрептококковыми болезнями, обычно состоят из двух частей – контакт с данной инфекцией и ослабленный иммунитет. Однако, человек может серьезно заболеть и при обычном контакте с данным видом бактерий.
Как стрептококк может попасть в организм?
Воздушно-капельный путь. Риск заражения стрептококковой инфекцией обычно возрастает в период простудных заболеваний, когда концентрация различной инфекции (вирусы, бактерии, грибок и другие) в воздухе, преимущественно в закрытых помещениях существенно возрастает. Пребывание в офисах, общественном транспорте, выступлениях и других местах с большим скоплением людей, особенно в период ОРЗ-болезней, является основным способом заражения данными бактериями. Чиханье и кашель – это основные сигналы, которые предупреждают, что из этого помещения лучше удалиться, или хотя бы тщательно его проветривать.
Воздушно-пылевой путь. Пыль обычно состоит из мелких частичек тканей, бумаги, слущенной кожи, шерсти животных, пыльцы растений и различных представителей инфекции – вирусов, грибков, бактерий. Пребывание в запыленных помещениях, еще один фактор, повышающий риск попадание в организм стрептококковой инфекции.
Контактно-бытовой путь. Заражение происходит при совместном, вместе с болеющим человеком, использовании посуды, предметов личной гигиены, полотенца, постельного белья, кухонных принадлежностей. Риск заболевания повышается при травмировании слизистой оболочки носовой или ротовой полости, а также поверхности кожи. Очень часто, на работе, люде заражаются через использование одной чашки на несколько человек, или же питье воды из горла, из одной бутылки.
Половой путь. Инфицирование происходит при интимной близости с человеком, который болеет стрептококками, или же просто является их носителем. Данный вид бактерий имеет свойство жить и активно размножаться в органах мочеполовой системы мужчин (в уретре) и женщин (во влагалище).
Фекально-оральный (алиментарный) путь. Инфицирование стрептококками происходит при несоблюдении правил личной гигиены, например, при употреблении пищи немытыми руками.
Медицинский путь. Заражение человека происходит, в основном при его осмотре, хирургическом или стоматологическом вмешательстве не продезинфицированными медицинскими инструментами.
Как стрептококк может серьезно навредить здоровью человека, или что ослабляет иммунную систему?
Наличие хронических болезней. Если у человека присутствуют хронические заболевания, это обычно свидетельствует об ослабленном иммунитете. Чтобы не усложнять течение болезней, и стрептококковая инфекция не присоединилась к уже имеющимся болезням, обратите должное внимание и сделайте акцент на их лечение.
Наиболее распространенными заболеваниями и патологическими состояниями, при которых стрептококк часто атакует больного, являются: переохлаждение организма, ОРВИ, грипп, ОРЗ, тонзиллит, туберкулез, сахарный диабет, ВИЧ-инфекция, заболевания эндокринной и других систем организма, травмирование слизистых оболочек ротовой и носовой полости, горла, органов мочеполовой системы.
Кроме того, риск заражения стрептококком повышают:
- Вредные привычки: употребление алкоголя, курение, наркотики;
- Отсутствие здорового сна, стрессы, хроническая усталость;
- Употребление пищи, преимущественно малополезного характера;
- Малоподвижный образ жизни;
- Недостаточность в организме витаминов и микроэлементов (гиповитаминозы);
- Злоупотребление некоторыми лекарственными препаратами, например – антибиотиками, сосудосуживающими препаратами;
- Посещение салонов красоты сомнительного характера, особенно процедур маникюра, педикюра, пирсинга, набивке татуировки;
- Работа в загрязненных помещениях, например, на предприятиях химической или строительной промышленностей, особенно без средств защиты дыхательных путей.
Клиническая картина (симптомы) стрептококка весьма разнообразна, и зависит от локализации (органа), который поражает данный род бактерий, штамма инфекции, состояния здоровья и иммунной системы, возраста человека.
Общими симптомами стрептококка могут быть:
- Боль в горле, изменение тембра голоса;
- Образование налета, часто гнойного характера на миндалинах больного;
- Увеличение лимфатических узлов;
- Общая слабость, недомогание, боль в мышцах и суставах;
- Повышенная и высокая температура тела, от 37,5 до 39 °С;
- Озноб;
- Покраснение кожи, а также зуд и появление на ней пузырьков или бляшек;
- Боль в животе, отсутствие аппетита, тошнота, рвота, диарея, холецистит;
- Чувство болезненности и зуда в органах мочеполовой системы, выделения из них;
- Синуситы – ринит (насморк), этмоидит, гайморит, сфеноидит и фронтит;
- Затрудненное дыхание, кашель, чиханье, одышка;
- Нарушение чувства обоняния;
- Болезни дыхательных путей: ангина, ларингит, фарингит, трахеит, бронхит и пневмония (воспаление легких);
- Головные боли, головокружения, нарушение сознания;
- Бессонница;
- Обезвоживание организма;
- Нарушение нормального функционирования некоторых органов и тканей, которые стали очагом оседания бактерии.
- Гломерулонефрит;
- Менингит;
- Воспаление сердечной мышцы — миокардит, эндокардит, перикардит;
- Васкулит;
- Гнойный отит;
- Потеря голоса;
- Абсцесс легких;
- Ревматизм;
- Ревматоидный артрит;
- Пульпит;
- Тяжелые формы аллергии;
- Хронический лимфаденит;
- Рожа;
- Сепсис.

Всего известно около 100 видов стрептококков, каждый из которых характеризуется своей патогенностью.
Для удобства, данный род бактерий, в зависимости от типа гемолиза эритроцитов, выделили в 3 основные группы (классификация Брауна):
- Альфа-стрептококки (α) , или зеленящие стрептококки — вызывают неполный гемолиз;
- Бета-стрептококки (β) — вызывают полный гемолиз, и являются наиболее патогенными бактериями;
- Гамма-стрептококки (γ) – являются негемолитическими бактериями, т.е. они не вызывают гемолиза.
Классификация Лансфилда (Lancefield), в зависимости от строения карбогидрата C клеточной стенки бактерии, также выделяет 12 серотипов β-стрептококков: А, В, С… до U .
Streptococcus pneumoniae (Пневмококк). Является основным возбудителем таких болезней, как – пневмония (воспаление легких), менингит, бронхит, ларингит, средний отит, ринит, остеомилит, септический артрит, перитонит, эндокардит, сепсис и другие. Место оседания – дыхательные пути человека.
Streptococcus thermophilus (Стрептококк термофильный). Синонимы: Streptococcus salivarius thermophilus, Streptococcus salivarius subsp. thermophilus. Является полезной бактерией. Используется для приготовления полезных молочных продуктов – йогуртов, сметаны, ряженки, различных сыров (например – моцареллы), используется в БАДах.
Streptococcus mutans (Стрептококк мутанс). Способствует развитию таких заболеваний, как – кариес зубов. Развитие кариеса из-за данной вида бактерии происходит из-за ее свойства переводить сахарозу, глюкозу, фруктозу и лактозу в молочную кислоту, благодаря которой происходит постепенной разрушение зубной эмали. Streptococcus mutans имеет также свойство прилипать к зубной эмали, поэтому тщательная чистка зубов и полоскание ротовой полости специальными средствами являются профилактической мерой против данного вида инфекции.
Streptococcus salivarius (Слюнной стрептококк). Обычно обитает в ротовой полости и верхних дыхательных путях человека – в носу, в горле. Как и предыдущий тип, Streptococcus salivarius способен ферментировать сахарозу в молочную кислоту, однако не имеет такой же патогенности, как первый. В современном мире, некоторые штаммы слюнного стрептококка используют в качестве пробиотика. Его используют для производства специальных сосательных леденцов, способных предохранять полость рта с более опасными типами стрептококков. Замечено, что присутствие в полости рта слюнного стрептококка способствует снижению риска заразиться ангиной, фарингитом и другими инфекционными болезнями верхних дыхательных путей.
Streptococcus sanguis (ранее — Streptococcus sanguis). Является обычным обитателем зубного налета, однако имеет интересное свойство – он предотвращает прилипание к зубам streptococcus mutans, косвенно способствующего развитию кариеса.
Streptococcus mitis (ранее — Streptococcus mitior). Обычно оседают в верхних дыхательных путях – носовой и ротовой полости, горле. Этот вид бактерии является одним из возбудителей такого заболевания сердца, как — инфекционный эндокардит.
Бета-гемолитические стрептококки обычно несут в себе наибольшую опасность для здоровья человека. Это связано с их способность разрушать эритроциты (красные кровяные тельца). При этом во время своей жизнедеятельности, бета-стрептококки выделяют большое количество различных токсинов (ядов), распространение по организму которых приводит к различным сложным, а иногда и смертельно-опасным болезням и патологическим состояниям. Рассмотрим их более подробно.
Яды, вырабатываемые жизнедеятельностью бета-стрептококков в организме:
Стрептолизин – нарушает целостность клеток крови и сердца;
Лейкоцидин – фермент, разрушающий лейкоциты (иммунные клетки крови);
Скарлатинозный эритрогенин – способствует расширению капилляров, что приводит к кожной сыпи при болезни скарлатина;
Стрептокиназа, гиалуронидаза, протеиназа и амилаза – ферменты, которые способствуют распространению стрептококковой инфекции по всему организму, а также пожиранию здоровых тканей;
Некротоксин и летальный токсин – яды, которые способствуют омертвлению тканей.
Все вышеприведенные вещества, разносятся по организму через кровь.
Кроме того, попадая бактерий в организм, иммунитет начинает вырабатывать по отношению к ним антитела. Опасным положением является, когда антитела не могут признать измененные клетки и ткани организма, тогда они начинают их атаковать, поражая, фактически свой же организм. Таким образом, развиваются аутоиммунные заболевания.
Кольпит: откуда он берется? Как с ним бороться? А главное - как не допустить его повторного появления?
Проблема лечения воспаления женских половых органов всегда занимала центральную позицию в гинекологии. Такие болезни на первом месте по встречаемости у женщин, и они опасны своими последствиями.
Что такое кольпит в гинекологии?
Диагноз кольпит (вагинит) в гинекологии ставят на основании осмотра, лабораторных исследований, а также клинической картины, которая отличается в зависимости от формы заболевания (острый или хронический кольпит).
При остром кольпите все симптомы проявляются ярче, тогда как хроническая форма характеризуется менее явными признаками. Однако, несмотря на умеренную выраженность неприятных явлений, заболевание хронический кольпит это очень обманчивая, а от того и опасная форма воспалительного процесса в слизистой оболочке половых органов женщины. Для предотвращения нежелательных проблем со здоровьем очень важно обсудить со своим гинекологом - что такое кольпит и как его лечить.
Важным этапом в лечении любой болезни является правильная диагностика. От того, какой именно возбудитель вызвал инфицирование, напрямую зависит курс лечения:
- вагинит, вызванный возбудителями половых инфекций, называется специфическим;
- если же причиной воспаления стали стафилококки и стрептококки, значит это неспецифический кольпит.
Симптомы, причины и формы кольпита
Чем отличаются острый и хронический кольпит и симптомы у женщин и у девушек? Вагинит - заболевание, поражающее все возрастные группы. Ведущие симптомы кольпита у девушек, у женщин и у девочек имеют одинаковые проявления.
Признаки, указывающие на воспаление слизистой оболочки влагалища:
- чувство тяжести в нижних отделах живота;
- обильные выделения с неприятным запахом;
- жжение и боль при мочеиспускании;
- повышение температуры тела.
Зачастую, к перечисленным симптомам присоединяются недомогание, общая слабость, нарушение сна, раздражительность, болезненные ощущения во время полового акта (у женщин).
Основные причины кольпита у женщин:
- нарушение интимной гигиены;
- травмы половых органов (послеродовые разрывы, внутриматочная спираль, травмы в процессе полового акта);
- гормональные изменения;
- аллергические заболевания;
- нарушение менструальной функции;
- неконтролируемый приём медикаментов.
Зная причины и признаки кольпита неспецифического, женщина, страдающая дискомфортными ощущениями, должна обратиться за помощью к врачу. Гинеколог проведёт тщательный осмотр и назначит анализы необходимые для дифференцировки того, неспецифическое это или специфическое воспаление влагалища. Для этого из влагалища, мочеиспускательного и цервикального канала берут мазок на флору. Данное исследование поможет определить вид инфекции, вызвавшей вагинит, а также выявить все сопутствующие инфекции, которые могут видоизменять клиническую картину, служить препятствием для появления положительных результатов терапии и стать причиной возникновения параллельной патологии.
Кроме разделения по этиологическому признаку (по возбудителям), вагиниты делят на гнойный и гранулёзный. Их отличает вид и характер выделений.
Основные методы лечения кольпита
Комплексное лечение воспалительного процесса – обязательное условие на пути к выздоровлению. Самолечение или игнорирование симптомов вагинита может перевести заболевание из острой фазы в хроническую, а это грозит опасными последствиями. Это же относится и к таким смежным болезням, как хронический сальпингоофорит или хронический эндометрит матки.
При отсутствии должного лечения, хронический кольпит имеет свойство распространяться на соседние органы: яичники, маточные трубы и матку.
Заболевание опасно серьёзными последствиями, к ним относятся:
- нарушение менструального цикла;
- бесплодие;
- внематочная беременность;
- невынашивание беременности;
- развитие внутриутробных инфекций и патологий плода.
- другие воспалительные заболевания органов малого таза.
В виду того, что существует большая угроза развития осложнений и отрицательных последствий, болезнь кольпит и её лечение – объекты повышенного внимания акушеров-гинекологов всего мира:
- разрабатываются новые методы диагностики заболевания на самых ранних стадиях;
- совершенствуются подходы к лечению, с учётом разных форм вагинитов.
Врачи ставят перед собой задачу: как вылечить кольпит гнойный и гранулёзный, выявить этиологию, определить специфический ли это вагинит или неспецифический.
Лечение неспецифического кольпита основывается на подборе этиотропного препарата, т.е. антибиотика, действие которого направлено на борьбу с конкретным видом микроорганизмов. Такой подход осуществляется с помощью определения чувствительности возбудителя к антибактериальным препаратам. Выбранное лекарство гинеколог назначает в таблетированной форме или в виде мазей или кремов.
Помимо методов, направленных на борьбу с инфекций, лечение хронического кольпита включает в себя симптоматическую терапию. С целью уменьшения и исключения неприятных ощущений, сопровождающих воспаление слизистой оболочки влагалища, назначают:
- антигистаминные препараты;
- дезинфицирующие растворы;
- антисептики местного применения.
Внимательное отношение к собственному здоровью и регулярное посещение гинеколога – залог раннего выявления, эффективного лечения и предотвращения последствий кольпита.
Акушерство, гинекология и репродукция. 2015; N2: c.19-23
Целью исследования явилось определение частоты встречаемости стрептококка группы В у рожениц и новорожденных. Материалы и методы. Проспективное исследование включило две группы наблюдения: 1-я группа пациенток (n=35) с доношенной беременностью и срочными родами, 2-я группа пациенток (n=22) с преждевременными родами в сроке от 34 до 37 нед. Всем пациенткам при поступлении и всем новорожденным был проведен экспресс-тест на стрептококк группы В. Результаты исследования. В 1-й группе тест был положительным у 25,7% женщин и у 8,6% новорожденных. Во 2-й группе тест был положительный у 18,2% женщин и у 22,7% новорожденных.
Статья поступила: 30.03.2015 г.; в доработанном виде: 08.04.2015 г.; принята к печати: 17.06.2015 г.
Конфликт интересов
Авторы заявляют об отсутствии необходимости раскрытия финансовой поддержки или конфликта интересов в отношении данной публикации.
Все авторы сделали эквивалентный вклад в подготовку публикации.
Для цитирования
Леваков С.А., Боровкова Е.И. Контаминация родовых путей у беременных стрептококком группы В: актуальность внедрения скрининговых программ. Акушерство, гинекология и репродукция. 2015; 2: 19-23.
Streptococcus Group B contamination of the birth canal in pregnant women: the relevance of the introduction of screening programs
Levakov S.A., Borovkova E.I.
First Moscow State Medical Sechenov University of the Ministry of Health Russian Federation
Summary
The aim of the study was to determine the frequency of occurrence of group B Streptococcus in women in labour and newborn babies. Materials and methods. prospective study included two groups: group 1 patients (n=35) with full-term pregnancy and term birth, group 2 patients (n=22) with preterm birth in the period from 34 to 37 weeks. All patients upon admission and all newborns was carried out rapid test for Streptococcus group B. Results. in the 1st group, the test was positive in 25.7% of women and 8.6% of newborns. In the 2nd group, the test was positive in 18.2% of women and 22.7% of newborns.a prospective study was conducted of contamination of the genital tract in pregnancy Streptococcus group B. We have formed 2 groups: group 1 patients (n=35) with full-term pregnancy and term birth, group 2 (n=22) patients with preterm birth in the period from 34 to 37 weeks. All patients upon admission and all newborns was conducted rapid test for Streptococcus group B. In the 1st group, the test was positive in 25.7% of women and 8.6% of newborns. In the 2nd group, the test was positive in 18.2% of women and 22.7% of newborns.
Key words
Pregnancy, group b Streptococcus, preterm birth, intrapartum infection of the fetus.
Received: 30.03.2015; in the revised form: 08.04.2015; accepted: 17.06.2015.
Conflict of interests
The authors declared that they do not have anything to disclosure regarding funding or conflict of interests with respect to this manuscript.
All authors contributed equally to this article.
For citation
Levakov S.A., Borovkova E.I. Streptococcus group B contamination of the birth canal in pregnant women: the relevance of the introduction of screening programs. Akusherstvo, ginekologiya i reproduktsiya / Obstetrics, gynecology and reproduction. 2015; 2: 19-23 (in Russian).
Ключевые слова: Беременность, стрептококк группы В, преждевременные роды, интранатальное инфицирование плода.
Концептуальной основой для решения этих задач является раннее выявление и предупреждение репродуктивных нарушений, охрана здоровья женщин, оптимизация организации и качества оказания акушерско-гинекологической помощи.
Стрептококк группы В (СГВ, Streptococcus agalactiae) – это грамположительный диплококк рода Streptococcus, семейства Streptococcaceae. Он относится к условно-патогенной флоре, обитающей в кишечнике человека, колонизирует слизистые влагалища и верхних дыхательных путей у детей и подростков. У беременных СГВ диагностируется в 15-40% случаев [1].
Во время беременности СГВ часто является причиной развития бессимптомной бактериурии, гестационного пиелонефрита, внутриутробного инфицирования плода и хореонамнионита. Восходящее инфицирование матки повышает риск спонтанных выкидышей ранних сроков и преждевременных родов. В послеродовом периоде СГВ является причиной развития послеродового эндометрита (8%), пневмонии и сепсиса новорожденных (2%), а также бактериемии без очага поражения (31%) [1,4].
Инфицирование плода происходит интранатально, кроме того, возможно антенатальное заражение при восходящем распространении возбудителя и внутриутробном инфицировании.
В патогенезе развития стрептококковой инфекции у плода и новорожденного имеет значение массивность колонизации Streptococcus agalactiae. При отсутствии проведения лечебных и профилактических мероприятий заболеваемость новорожденных достигает 2% [7].
Согласно рекомендациям Всемирной организации здравоохранения скрининг на наличие бета-гемолитического стрептококка проводится всем беременным в 36 нед. или (если не был выполнен ранее) в родах в случае развития преждевременных родов, лихорадки или длительности безводного промежутка более 12 ч [5].
Абсолютным и доказанным является риск интранатального инфицирования плода, которое происходит в 80-90% случаев. Выделяют две формы неонатальных и перинатальных инфекций: ранняя инфекция (развивается в первые 24-48 ч) и поздняя инфекция (проявляется через 8-10 дней после родов). Наиболее опасной является ранняя инфекция в связи с более острым характером ее течения. Поздняя форма заболевания может быть вызвана внутрибольничной инфекцией (при родах в медицинском учреждении) и очень редко связана с осложнениями при родовспоможении. Заражаемость стрептококками группы B составляет от 1 до 5% (для всех рождений живого плода), смертность от развивающейся инфекции колеблется от 22 до 80% [2,6].
В Российской федерации специфического обследования на бета-гемолитический стрептококк не проводится. Косвенно о контаминации организма можно судить по результатам культурального исследования мочи (проводится после 14 нед. беременности) и отделяемого влагалища.
Целью исследования явилось определение частоты встречаемости СГВ у рожениц и новорожденных.
Материалы и методы
Для достижения поставленной цели было проведено проспективное исследование, включившее 57 рожениц, на базе филиала №2 больницы им. А.К. Ерамишанцева.
При поступлении в родильный дом всем пациенткам проводилось стандартное клинико-лабораторное обследование, включающее УЗИ плода, допплерометрию, кардиотокографию, определение группы крови, резус-фактора, клинического анализа крови и показателей гемостаза.
Кроме того, всем пациенткам и новорожденным, включенным в исследование, проводилось исследование на контаминацию стрептококком группы В с помощью качественного иммунохроматографического экспресс-теста для определения антигена стрептококков группы В во влагалищных мазках.
Метод определения основан на использовании специфического комплекса конъюгированных с красителем мышиных моноклональных антител к стрептококку В и иммобилизованных в тестовой зоне кассеты поликлональных мышиных антител к стрептококку В для его избирательного определения в тестируемых пробах с высокой степенью чувствительности. При прохождении пробы через слой адсорбента меченый конъюгат антител с красителем связывается с присутствующим в пробе стрептококковым антигеном, образуя комплекс антиген-антитело. Этот комплекс связывается с иммобилизованными на мембране в тестовой зоне кассеты поликлональными антителами к антигену стрептококков группы B, образуя в нем пурпурно-розовую полосу, если в пробе присутствует стрептококковый антиген. Если же стрептококки группы B в пробе отсутствуют, окрашенной полосы в тестовой зоне не образуется. Несвязанный конъюгат, продолжая продвигаться по слою адсорбента, достигает контрольной зоны (C), где осаждается с образованием контрольной полосы, подтверждающей качественность применяемых в тесте реагентов.
Статистическая обработка полученных результатов проводилась по стандартным методам описательной и вариационной статистики с применением линейного регрессионного анализа.
Были сформированы две группы: 1-ю группу составили 35 рожениц с доношенной беременностью (37-41 нед.), 2-ю группу – 22 роженицы с преждевременным родами в сроках от 35 до 37 нед.
85% всех пациенток были в возрасте от 24 до 35 лет. В структуре экстрагенитальных заболеваний значимых различий в группах выявлено не было. НЦД по гипертоническому типу встречалось у 14,3 и 13,6% пациенток, варикозное расширение вен нижних конечностей – у 11,4 и 9%, хронический гастрит – у 22,8 и 22,7%, ЖКБ – у 8,6 и 4,5%, железодефицитная анемия – у 11,4 и 13,6% соответственно. В структуре заболеваний органов мочевыводящих путей хронический цистит (14,3 и 18,2%) и МКБ (8,6 и 9%) выявлялись с одинаковой частотой.
Средний возраст менархе в обеих группах составил 11,6 лет (от 10,5 до 14 лет). 89% женщин имели регулярный менструальный цикл. Среди гинекологических заболеваний наиболее распространенными были инфекции, передаваемые половым путем (37,1 и 36,4%), дисфункция яичников (7,7 и 4,5%), эктопия шейки матки (48,6 и 45,5%), миома матки (5,7% в 1-й группе) и полип эндометрия (2,9 и 9%).
Все пациентки были первородящими. 82% пациенток в 1-й группе и 72,7% во 2-й группе были первобеременными. Среди повторнобеременных предыдущие беременности закончились медикаментозным абортом (5,7 и 4,5%), самопроизвольным выкидышем в сроке до 12 нед. (8,6 и 13,6%) и артифициальным абортом (2,8 и 9,1%).
Течение первого триместра настоящей беременности осложнялось развитием раннего токсикоза легкого и среднетяжелого течения (77,1 и 86,4%) и угрозы прерывания беременности, диагностированной в 14,4 и 40,9% случаях соответственно группам. По поводу угрозы прерывания беременности пациентки получали спазмолитическую (дротаверин 120 мг в сут., препарат магния 300 мг в сут.) и гормональную терапию (дидрогестерон 20 мг в сут., натуральный микронизированный прогестерон 400 мг в сут.) до 16-20 нед.
Во II триместре у беременных выявлена железодефицитная анемия (14,3 и 13,6%), угроза прерывания беременности (8,6 и 36,4%), бессимптомная бактериурия (5,7 и 9%) и острый цистит (0 и 4,5%). По поводу развившихся осложнений пациентки получали антианемическую терапию (препараты железа в суточной дозе до 300 мг), спазмолитическую терапию (дротаверин, свечи с гиосцина бутилбромидом), антибактериальную терапию в течение 5-7 дней (защищенные пенициллины, цефалоспорины 2-3-го поколения).
В III триместре беременности умеренная преэклампсия диагностирована у 11,4% пациенток 1-й группы и у 9% 2-й группы, задержка роста плода по асимметричному типу выявлена у 5,7 и 4,5% женщин, угроза преждевременных родов – у 5,7% и 90,9% женщин, частота инфекций нижних отделов мочевыводящих путей составила 11,4 и 22,7% соответственно.
Пациентки, включенные в исследование, поступали в родильный дом с регулярной родовой деятельностью. Из них в 1-й группе с излитием околоплодных вод было 10 (28,5%) пациенток, во 2-й группе – 11 (50%) пациенток. Средняя продолжительность родов у пациенток 1-й группы составила 9±1,2 ч, безводного промежутка – 10,5±1,7 ч. Средняя продолжительность родов у пациенток 2-й группы составила 7,5±2,3 ч, безводного промежутка – 12,2±1,5 ч.
Все дети родились живыми, из них недоношенными 22 ребенка, незрелыми 27 детей. Средняя масса новорожденных в 1-й группе составила 3369±81 г, во 2-й группе – 2725±54 г.
С признаками морфофункциональной незрелости было рождено 27 детей, гипоксически-ишемическое поражение ЦНС выявлено у 8,6 и 9,1% детей, а острую асфиксию в родах перенесли 2,8 и 9,1% детей соответственно. Врожденная пневмония развилась в 2,8 и 18,2% случаев, а проведения интубации трахеи и искусственной вентиляции легких потребовалось в 2,8 и 22,7% случаев.
Всем роженицам при поступлении и их новорожденным был проведен экспресс-тест на наличие СГВ (см. табл. 1). Материалом для исследования у женщин были мазки из заднего свода влагалища и перианальной области, а у новорожденных – мазки из носоглотки и ротовой полости. При получении положительного результата, по данным экспресс-диагностики, пациенткам было проведено профилактическое введение цефазолина 2 г в/в однократно.
Таблица 1. Результаты экспресс-теста на стрептококк группы В.
 |
Из 35 пациенток 1-й группы у 9 (25,7%) был получен положительный результат теста. При этом пять пациенток ранее получали терапию во II и III триместрах в связи с бессимптомной бактериурией или острым циститом. Аналогичная ситуация прослеживается и у пациенток 2-й группы: из четырех женщин с положительным экспресс-тестом у троих были выявлены и пролечены ранее инфекции нижних отделов мочевыводящих путей.
У 1 (2,8%) новорожденного из 1-й группы и у 5 (22,7%) новорожденных из 2-й группы была диагностирована врожденная пневмония. При этом у ребенка из 1-й группы тест на СГВ был отрицательный, у детей из 2-й группы положительный тест был только в двух случаях. Ни одного случая развития сепсиса у новорожденных выявлено не было.
Целесообразность проведения скрининга заключается в выявлении контаминированных пациенток и проведении специфической антибактериальной терапии для снижения риска развития интранатального инфицирования и сепсиса у новорожденного. Внедрение программы обследования и антибиотикопрофилактики позволяет снизить данную частоту в 3 раза [2,3].
Всем беременным в сроке 35-37 нед. необходимо проводить культуральное исследование из влагалища и кишечника на определение стрептококка группы В с использованием селективных сред. Исключение составляют пациентки, у которых была диагностирована бессимптомная бактериурия и женщины, в анамнезе у которых были случаи рождения детей с подтвержденной стептококковой инфекцией. Данным пациенткам не проводится скрининговое обследование, но интранатально проводится антибактериальная профилактика [2].
Антибактериальная профилактика в родах показана женщинам с подтвержденной контаминацией СГВ, пациенткам с рождением в предыдущей беременности ребенка с СГВ-инфекцией, наличием бессимптомной стрептококковой бактериурии в данной беременности, а также при отсутствии данных о контаминации СГВ и наличии в родах лихорадки, длительности безводного промежутка 18 ч и более и преждевременных родах [3].
Антибактериальная профилактика в родах не проводится при отрицательном скрининге на СГВ, проведении кесарева сечения в случае отсутствия дородового излития околоплодных вод.
При подозрении на инфицирование новорожденного проводят быстрые тесты на определение стрептококков группы В (микроскопия желудочного секрета и мазки из носоглотки) и культуральное исследование на селективной среде (материалом для посева служит желудочный сок, кровь, спинномозговая жидкость, моча, эндобронхиальный аспират).
В связи с тем, что стрептококковая инфекция у новорожденных рассматривается как одна из основных причин тяжелых перинатальных осложнений, в странах западной Европы и США беременным в обязательном порядке проводят профилактическое лечение при отсутствии лабораторно исключенной стрептококковой инфекции [3].
Проведенное нами исследование позволило выявить, что почти каждая 5-я пациентка, вне зависимости от срока гестации, контаминирована стрептококком группы В и теоретически входит в группу высокого риска по реализации интранатального инфицирования плода.
Внедрение скрининга на СГВ в программу ведения беременности и применение экспресс-тестов в родильном доме позволит снизить частоту передачи возбудителя интранатально и улучшит перинатальные исходы.
Читайте также: