Антитоксин дифтерийный регистрационное удостоверение

- Форма выпуска: 1 ампула / 2 дозы №10.
- Схема вакцинации: профилактика дифтерии согласно Национального календаря прививок у детей с 6-летнего возраста, подростков и взрослых.
Инструкция по применению
НПО МИКРОГЕН, ФГУП (Россия)
Код ATX: J07AF01 (Diphtheria toxoid)
АНАТОКСИН ДИФТЕРИЙНЫЙ ОЧИЩЕННЫЙ АДСОРБИРОВАННЫЙ С УМЕНЬШЕННЫМ СОДЕРЖАНИЕМ АНТИГЕНА ЖИДКИЙ (АД-М АНАТОКСИН)
сусп. д/в/м и п/к введения 0.5 мл/1 доза: амп. 1 доза 10 шт.
Суспензия для в/м и п/к введения
0.5 мл
0.5 мл (1 доза) - ампулы (10) - пачки картонные.
Клинико-фармакологическая группа: Иммунологический препарат. Анатоксин
Фармако-терапевтическая группа: МИБП-анатоксин
Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата.
Формирует специфический иммунитет против дифтерии.
профилактика дифтерии у детей с 6-летнего возраста, подростков и взрослых.
Коды МКБ-10
В/м в верхний наружный квадрант ягодицы или передне-наружную часть бедра или глубоко п/к (подросткам и взрослым) в подлопаточную область в разовой дозе 0.5 мл. Перед прививкой ампулу необходимо тщательно встряхнуть до получения гомогенной взвеси.
Для плановых возрастных ревакцинаций лицам, получивших прививку столбнячным анатоксином в связи с экстренной профилактикой столбняка препарат вводят однократно.
Редко (в первые 2 сут) - гипертермия, недомогание, местные реакции (болезненность, гиперемия, отечность); в единичных случаях - аллергические реакции (ангионевротический отек, крапивница, полиморфная сыпь), незначительное обострение аллергических заболеваний.
- гиперчувствительность.
Беременным прививки проводят по эпидпоказаниям.
Лиц, перенесших острые заболевания, прививают через 2-4 нед после выздоровления. При легких формах заболеваний прививки допускаются после исчезновения клинических симптомов.
Больных хроническими заболеваниями прививают после достижения полной или частичной ремиссии. Лиц с неврологическими изменениями прививают после исключения прогрессирования процесса. Больным аллергическими заболеваниями прививки проводят через 2-4 нед после окончания обострения, при этом стабильные проявления заболевания (локализованные кожные явления, скрытый бронхоспазм и т.п.) не являются противопоказаниями к вакцинации, которая может быть проведена на фоне соответствующей терапии.
Иммунодефициты, ВИЧ-инфекция, а также поддерживающая курсовая терапия (в т.ч. ГКС и нейротропными ЛС) не являются противопоказаниями к прививке.
С целью выявления противопоказаний врач в день прививки проводят опрос родителей и осмотр прививаемых с обязательной термометрией. При вакцинации взрослых допускается предварительный отбор лиц, подлежащих прививке, с их опросом медицинским работником в день прививки, проводящим вакцинацию. Лица, временно освобожденные от прививки, должны быть взяты под наблюдение и учет и своевременно привиты.
При эпидемиологической необходимости препарат можно вводить на фоне острого заболевания.
В случае сильной реакции на предыдущую дозу этого препарата повторная доза вводится на фоне применения ГКС (преднизолон внутрь 1-1.5 мг/кг/сут за день до и сразу после прививки).
Препарат можно вводить спустя месяц или одновременно с полиомиелитной вакциной и др. ЛС национального календаря прививок.
Учитывая возможность развития аллергических реакций немедленного типа у особо чувствительных лиц, за привитыми необходимо обеспечить медицинское наблюдение в течение 30 мин. Места проведения прививок должны быть обеспечены средствами противошоковой терапии.
Лицам, давшим на введение препарата тяжелые формы аллергических реакций, дальнейшие плановые прививки препарата прекращают.
Не пригоден к применению препарат в ампулах с нарушенной целостностью, отсутствием маркировки, при изменении физических свойств (изменение цвета, наличие неразбивающихся хлопьев), неправильном хранении.
Вскрытие ампул и процедуру вакцинации осуществляют при строгом соблюдении правил асептики и антисептики. Препарат во вскрытой ампуле хранению не подлежит.
Введение препарата регистрируют в установленных учетных формах с указанием номера серии, срока годности, предприятия изготовителя, даты введения.
Фармакологическое действие
Применение при беременности и кормлении грудью
Показания
— профилактика дифтерии у детей с 6-летнего возраста, подростков и взрослых. Коды МКБ-10| Код МКБ-10 | Показание |
| A36 | Дифтерия |
| Z23.8 | Необходимость иммунизации против другой одной бактериальной болезни |
Владелец регистрационного удостоверения:
Режим дозирования
В/м в верхний наружный квадрант ягодицы или передне-наружную часть бедра или глубоко п/к (подросткам и взрослым) в подлопаточную область в разовой дозе 0.5 мл. Перед прививкой ампулу необходимо тщательно встряхнуть до получения гомогенной взвеси.
Для плановых возрастных ревакцинаций лицам, получивших прививку столбнячным анатоксином в связи с экстренной профилактикой столбняка препарат вводят однократно.
Побочное действие
Лекарственная форма
| АНАТОКСИН ДИФТЕРИЙНЫЙ ОЧИЩЕННЫЙ АДСОРБИРОВАННЫЙ С УМЕНЬШЕННЫМ СОДЕРЖАНИЕМ АНТИГЕНА ЖИДКИЙ (АД-М АНАТОКСИН) | сусп. д/инъекц. 0.5 мл/1 доза: амп. 10 шт. рег. №: Р N002665/01-2003 от 01.07.08 - Бессрочно |
Форма выпуска, состав и упаковка
| Суспензия для инъекций | 0.5 мл |
| дифтерийный анатоксин | 1 доза |
0.5 мл - ампулы (10) - пачки картонные.
Клинико-фармакологическая группа: Иммунологический препарат. Анатоксин Фармако-терапевтическая группа: МИБП-анатоксин Открыть описание активных компонентов препарата АНАТОКСИН ДИФТЕРИЙНЫЙ ОЧИЩЕННЫЙ АДСОРБИРОВАННЫЙ С УМЕНЬШЕННЫМ СОДЕРЖАНИЕМ АНТИГЕНА ЖИДКИЙ (АД-М АНАТОКСИН) (ANATOXINUM DIPHTHERICUM PURIFICATUM ADSORPTUM CUM QUANTITALE MINORE ANTIGENORUM FLUIDUM (AD-M ANATOXINUM)) Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата.
Особые указания
Лиц, перенесших острые заболевания, прививают через 2-4 нед после выздоровления. При легких формах заболеваний прививки допускаются после исчезновения клинических симптомов.
Больных хроническими заболеваниями прививают после достижения полной или частичной ремиссии. Лиц с неврологическими изменениями прививают после исключения прогрессирования процесса. Больным аллергическими заболеваниями прививки проводят через 2-4 нед после окончания обострения, при этом стабильные проявления заболевания (локализованные кожные явления, скрытый бронхоспазм и т.п.) не являются противопоказаниями к вакцинации, которая может быть проведена на фоне соответствующей терапии.
Иммунодефициты, ВИЧ-инфекция, а также поддерживающая курсовая терапия (в т.ч. ГКС и нейротропными ЛС) не являются противопоказаниями к прививке.
С целью выявления противопоказаний врач в день прививки проводят опрос родителей и осмотр прививаемых с обязательной термометрией. При вакцинации взрослых допускается предварительный отбор лиц, подлежащих прививке, с их опросом медицинским работником в день прививки, проводящим вакцинацию. Лица, временно освобожденные от прививки, должны быть взяты под наблюдение и учет и своевременно привиты.
При эпидемиологической необходимости препарат можно вводить на фоне острого заболевания.
В случае сильной реакции на предыдущую дозу этого препарата повторная доза вводится на фоне применения ГКС (преднизолон внутрь 1-1.5 мг/кг/сут за день до и сразу после прививки).
Препарат можно вводить спустя месяц или одновременно с полиомиелитной вакциной и др. ЛС национального календаря прививок.
Учитывая возможность развития аллергических реакций немедленного типа у особо чувствительных лиц, за привитыми необходимо обеспечить медицинское наблюдение в течение 30 мин. Места проведения прививок должны быть обеспечены средствами противошоковой терапии.
Лицам, давшим на введение препарата тяжелые формы аллергических реакций, дальнейшие плановые прививки препарата прекращают.
Не пригоден к применению препарат в ампулах с нарушенной целостностью, отсутствием маркировки, при изменении физических свойств (изменение цвета, наличие неразбивающихся хлопьев), неправильном хранении.
Вскрытие ампул и процедуру вакцинации осуществляют при строгом соблюдении правил асептики и антисептики. Препарат во вскрытой ампуле хранению не подлежит.
Введение препарата регистрируют в установленных учетных формах с указанием номера серии, срока годности, предприятия изготовителя, даты введения.
Владелец регистрационного удостоверения:
Произведено:
Лекарственная форма
рег. №: ЛС-000331 от 21.04.10 - БессрочноФорма выпуска, упаковка и состав препарата Анатоксин дифтерийно-столбнячный очищенный адсорбированный жидкий (АДС-анатоксин)
| Суспензия для инъекций | 0.5 мл | 1 амп. |
| анатоксин дифтерийно-столбнячный | 1 доза | 2 дозы |
1 мл (2 дозы) - ампулы (10) - пачки картонные.
Фармакологическое действие
Показания активных веществ препарата Анатоксин дифтерийно-столбнячный очищенный адсорбированный жидкий (АДС-анатоксин)
- профилактика дифтерии и столбняка у детей с 6-летнего возраста, подростков и взрослых.
| Код МКБ-10 | Показание |
| A35 | Другие формы столбняка |
| A36 | Дифтерия |
| Z27.8 | Необходимость иммунизации против других комбинаций инфекционных болезней |
Режим дозирования
В/м в верхний наружный квадрант ягодицы или передне-наружную часть бедра или глубоко п/к (подросткам и взрослым) в подлопаточную область в разовой дозе 0.5 мл.
Перед введением препарат необходимо тщательно встряхнуть до получения гомогенной взвеси.
Для плановых возрастных ревакцинаций в 7 и 14 лет, затем каждые последующие 10 лет без ограничения возраста - однократно.
Для вакцинации детей 6 лет и старше , ранее непривитых против дифтерии и столбняка - курс вакцинации состоит из двух прививок с интервалом 30-45 дней. Сокращение интервала не допускается. При необходимости увеличения интервала очередную прививку следует проводить в возможно ближайший срок. Первую ревакцинацию проводят через 6-9 мес после законченной вакцинации однократно, вторую ревакцинацию - с интервалом в 5 лет. Последующие ревакцинации осуществляют каждые 10 лет без ограничения возраста.
В качестве замены коклюшно-дифтерийно-столбнячной вакцины (АКДС-вакцины) или дифтерийно-столбнячного анатоксина со стандартной концентрацией антигенов (АДС-анатоксина) у детей с сильными общими реакциями (гипертермией до 40°С и выше) или поствакцинальными осложнениями на указанные препараты. Если реакция развилась на первую вакцинацию АКДС (АДС), то АДС-М анатоксин вводят однократно не ранее, чем через 3 мес, если реакция развилась на вторую вакцинацию, то курс вакцинации против дифтерии и столбняка считают законченным. В обоих случаях первую ревакцинацию АДС-М анатоксином проводят через 9-12 мес. Если реакция развилась на третью вакцинацию АКДС (АДС), первую ревакцинацию АДС-М анатоксином проводят через 12-18 мес.
Для проведения курса вакцинации взрослых, которые ранее достоверно не были привиты против дифтерии и столбняка, проводят полный курс иммунизации (две вакцинации АДС-М анатоксином с интервалом 30 дней и ревакцинация через 6-9 мес).
В очагах дифтерии профилактические прививки проводят в соответствии с инструктивно-методическими документами Минздрава России.
Побочное действие
Противопоказания к применению
- гиперчувствительность;
- беременность.
Применение при беременности и кормлении грудью
Противопоказан к применению при беременности.
Применение у детей
Применение возможно согласно режиму дозирования.
Детей с неврологическими нарушениями прививают после исключения прогрессирования процесса.
Особые указания
Лиц, перенесших острые заболевания, прививают через 2-4 нед после выздоровления. При легких формах заболеваний прививки допускаются после исчезновения клинических симптомов.
Больных хроническими заболеваниями прививают по достижении полной или частичной ремиссии. Детей с неврологическими нарушениями прививают после исключения прогрессирования процесса. Больным аллергическими заболеваниями прививки проводят через 2-4 нед после окончания обострения, при этом стабильные проявления заболевания (локализованные кожные явления, скрытый бронхоспазм) не являются противопоказаниями к вакцинации, которая может быть проведена на фоне соответствующей терапии.
Иммунодефициты, ВИЧ-инфекция, а также поддерживающая курсовая терапия (в т.ч. ГКС ) не являются противопоказаниями к прививке.
С целью выявления противопоказаний врач в день прививки проводит опрос родителей и осмотр прививаемых с обязательной термометрией. При вакцинации взрослых допускается предварительный отбор лиц, подлежащих прививке, с их опросом медицинским работником в день прививки, проводящим вакцинацию. Лица, временно освобожденные от прививки, должны быть взяты под наблюдение и учет и своевременно привиты.
При эпидемиологической необходимости АДС-М анатоксин можно вводить на фоне острого заболевания. В случае сильной реакции не предыдущую дозу этого препарата повторная доза вводится на фоне применения ГКС (преднизолон внутрь - 1-1.5 мг/кг/сут за день до и сразу после прививки).
Лиц, привитых столбнячным анатоксином, между ревакцинациями прививают дифтерийным анатоксином.
АДС-М анатоксин можно вводить спустя месяц или одновременно с полиомиелитной вакциной и другими вакцинами национального календаря прививок.
Учитывая возможность развития аллергических реакций немедленного типа у особо чувствительных лиц, за привитыми необходимо обеспечить медицинское наблюдение в течение 30 мин. Места проведения прививок должны быть обеспечены средствами противошоковой терапии.
Лицам, давшим на введение АДС-М анатоксина тяжелые формы аллергических реакций, плановые прививки препаратом прекращают.
Не пригоден к применению в ампулах с нарушенной целостностью, отсутствием маркировки, при изменении физических свойств (изменение цвета, наличие неразбивающихся хлопьев), неправильном хранении.
Вскрытие ампул и процедуру вакцинации осуществляют при строгом соблюдении правил асептики и антисептики. Препарат во вскрытой ампуле хранению не подлежит.
Введение препарата регистрируют в установленных учетных формах с указанием номера серии, срока годности, предприятия-изготовителя, даты введения.
1.1. В методических рекомендациях (далее - МР) представлена рациональная и эффективная тактика использования серологических методов диагностики и мониторинга иммунитета к дифтерийной инфекции.
1.2. В настоящих МР описаны используемые в последние годы международные и отечественные методы определения противодифтерийных антител, а также предложен наиболее надежный и перспективный метод иммуноферментного анализа (далее - ИФА) для определения суммарных и высокоавидных антител, его стандартное применение, в том числе предложены надежные критерии оценки защитных уровней, необходимые для выявления среди детей и взрослых групп повышенного риска и оценки напряженности индивидуального и коллективного иммунитета к дифтерийной инфекции.
1.3. Настоящие МР предназначены для врачей-эпидемиологов и микробиологов и носят рекомендательный характер.
2.1. Несмотря на высокие показатели привитости населения от дифтерии в разных регионах России периодически регистрируются случаи заболевания дифтерией или носительства Corynebacterium diphtheria, особенно среди лиц в закрытых коллективах [3, 4, 8].
2.2. В настоящее время, спустя 15 лет после прошедшей эпидемии дифтерии, повсеместно отмечается снижение внимания клиницистов к этой инфекции. Профилактические и диагностические обследования проводятся, но не в полном объеме [12].
2.3. Как известно, защищенность от дифтерии в нашей стране определяется с помощью реакции прямой гемагглютинации (РПГА) [13]. Однако результат реакции, выражаемый в титрах, не позволяет точно определить количество антитоксических антител (АТ-АТ), а, значит, и оценить состояние иммунитета против дифтерии. Разработка и повсеместное внедрение в практику оценочной шкалы защищенности от дифтерии на основании определения количества АТ-АТ позволили контролировать качество вакцинации 1 [14]. Однако информация о количестве вырабатываемых противодифтерийных антител не всегда дает достоверный ответ на вопрос о степени защищенности от дифтерии. Это было продемонстрировано во время последней эпидемии дифтерии в России и после нее, когда у заболевших (до 40 % случаев) находили в крови АТ-АТ зашитых уровней [9, 10]. Проведенными исследованиями установлена определяющая роль высокоавидных АТ-АТ в защите от дифтерии, которые могут быть определены наряду с количеством суммарных АТ-АТ в иммуноферментном анализе [2, 5, 6, 16]. При этом была показана динамика формирования и утраты АТ-АТ, равно как и показателя их авидности, изучены особенности специфического иммунитета к дифтерии среди различных групп населения [1, 7, 11, 15]. Тем не менее, отсутствие программ и схем исследования при диагностике дифтерии и изучении напряженности иммунитета у населения, содержащих новые аргументированные данные, не позволяют полноценно и качественно проводить бактериологический и иммунологический контроль в отношении защищенности к дифтерии на местах.
0,01 МЕ/мл - минимальная степень защиты,
0,01 - 0,09 МЕ/мл - некоторая степень защиты,
0,1 - 0,9 МЕ/мл - защитный уровень антител,
1,0 и > МЕ/мл - стойкая длительная невосприимчивость к дифтерии.
3.2. Список оборудования и материалов, необходимых для проведения исследования, представлен в прилож. 1.
4.1. Серологический контроль состояния иммунитета
у детей и подростков
4.1.1. Серологический контроль иммунитета в различных группах позволяет представить иммунологическую структуру населения и выявить группы повышенного риска, определить состояние вакцинального иммунитета как в ранние, так и в отдаленные сроки после вакцинации.
4.1.2. Серологический контроль состояния и длительности сохранения вакцинального иммунитета необходимо осуществлять систематически методом выборочного серологического обследования (мониторинга) различных групп населения в городах и сельских районах каждой области, края.
4.1.3. Обследованию подлежат привитые против дифтерии дети и подростки от 3 до 18 лет каждой возрастной группы (3 года, 4 года, 5 лет и т.д., особое внимание следует обратить на детей 9 - 13 лет).
4.1.4. Серологический контроль следует проводить, начиная с групп детей 3 лет не ранее, чем через 6 месяцев после последней прививки. К этому возрасту должен быть закончен первичный вакцинальный комплекс против дифтерии, включающий вакцинацию и первичную ревакцинацию (V и RV).
4.1.5. В случае отсутствия материально-технических возможностей обследования каждой возрастной группы детей и подростков можно отобрать возрастные группы, подлежащие очередной ревакцинации (4 - 5 лет, 9 - 10 лет, 14 - 15 лет).
4.1.6. При получении неудовлетворительных иммунологических показателей в этих группах контроль за иммунитетом следует провести в каждой возрастной группе.
4.2. Серологический контроль состояния иммунитета у взрослых
4.2.2. Особое внимание должно уделяться лицам в закрытых коллективах.
5.1. Реакция пассивной гемагглютинации (РПГА)
Для постановки реакции используется диагностикум дифтерийный эритроцитарный антигенный. Поскольку срок годности эритроцитарных диагностикумов составляет 1 год, необходимо перед каждым проведением серологического исследования сывороток проверять активность препарата. Проверка проводится с контрольным антитоксином, приложенным к комплекту, либо используется национальный препарат дифтерийного антитоксина, очищенного ферментолизом и специфической сорбцией, диагностический сухой. Допускается исследование контрольной сыворотки (лабораторный образец) с известным титром дифтерийных антител. Если диагностикум выявляет в сыворотке антитела в концентрации на 2 - 3 разведения ниже, чем они в ней содержатся, то такой препарат не пригоден для дальнейшего исследования.
РПГА ставят в два этапа согласно инструкции, прилагаемой к препарату: 1-й - подготовка к реакции; 2-й - основной опыт. Ответ может быть получен на 2-е сутки с момента получения исследуемого материала лабораторией.
Однако ряд зарубежных исследователей отмечает возможность получения ложноположительных данных и несовпадение результатов, полученных в реакции нейтрализации in vivo и методах in vitro. По данным ряда авторов коэффициент корреляции между результатами, полученными в РПГА и PH, составляет всего 0,6.
5.2. Реакция нейтрализации (PH) в культуре клеток Vero
Поэтому в качестве второго стандарта была принята реакция нейтрализации (PH) в культуре клеток Vero, поскольку она лишена недостатков биологического теста, более стандартна и наглядна. Коэффициент корреляции результатов, полученных в PH в культуре клеток Vero, с результатами, полученными в классическом методе (на лабораторных животных), составляет 0,98. Этот метод гораздо экономичнее, быстрее и проще в постановке. Однако достоверность результатов PH во многом определяется стандартностью культуры клеток и всех контролей (токсинов и антитоксинов).
В реакции используется цветная проба, основанная на способности токсина изменять метаболическую активность зараженных клеток, что определяют по цвету индикатора, содержащегося в питательной среде. В не пораженных токсином культурах клеток под влиянием выделяющихся продуктов клеточного метаболизма pH питательной среды сдвигается в кислую сторону, вызывая изменение цвета индикатора. В пораженных токсином культурах в результате дегенерации клеток их метаболическая активность подавляется, и цвет фенолового красного не изменяется или изменяется частично.
В реакции используется токсин 0,0002 Lf/мл и антитоксин 0,032 МЕ/мл (National Collection of Type Cultures Diphtheriae Reference Laboratory, Central Health Laboratory (CPHL), London, UK). При постановке реакций применяют культуру клеток Vero, получаемую из лаборатории детских вирусных инфекций НИИЭМ им. Пастера, в концентрации 2,5 ⋅ 10 5 клеток/мл. Содержание антитоксических антител определяют от 0,000125 МЕ/мл и выше,
5.3. Иммуноферментный анализ (ИФА)
Тест-система для ИФА представляет собой набор, предназначенный для определения суммарных антитоксических антител, и включает следующие реагенты: иммуносорбент 1-96-луночный полистироловый или хлорвиниловый планшет для иммунологических реакций, в лунках которого сорбирован анатоксин дифтерийный очищенный; конъюгат - иммуноглобулины (F(аb')2-фрагменты) диагностические против IgG человека, аффинноочищенные, меченные пероксидазой; контрольный положительный образец (К+) - сыворотка или плазма крови человека с известным титром дифтерийных антител; контрольный отрицательный образец (К-) - сыворотка или плазма крови человека, не содержащая дифтерийных антител; концентрат фосфатно-солевого буферного раствора с твином (ФСБ-Т×25); блокатор - белково-солевой раствор (Б); цитратно-фосфатный буферный раствор с перекисью водорода (ЦФБР); хромоген - тетраметилбензидин (ТМБ); стоп-реагент (СР) - 5 %-ый раствор серной кислоты. Специальная компьютерная программа, прилагаемая к набору, дает возможность производить перерасчет показателей оптической плотности в показатели антитоксических международных единиц.
Для определения индекса авидности противодифтерийных антитоксических антител в сыворотке (плазме) крови человека разработано дополнение к набору, которое включает в себя следующие ингредиенты: контрольный положительный образец высокоавидных антител (КА+) - сыворотка крови человека с известным индексом авидности противодифтерийных антитоксических антител (индекс авидности сыворотки указан на этикетке флакона); контрольный отрицательный образец низ-коавидных антител (КА-) - сыворотка крови человека, содержащая противодифтерийные антитоксические антитела низкой авидности; фосфатно-солевой буфер, содержащий 3М калия роданистого для определения авидности противодифтерийных антитоксических антител (ФСБ-3МКрод). Набор рассчитан на исследование 29 образцов сыворотки (плазмы) крови для определения индекса авидности противодифтерийных антитоксических антител.
Тест-система укомплектована национальным стандартом антитоксина, измеряемым в МЕ/мл. Расчет концентрации АТ проводится с учетом коэффициента по калибровочной кривой, что делает результаты более достоверными. Сравнительный анализ нейтрализующего эффекта испытуемых сывороток людей в клеточной культуре Vero и других линиях показал хорошую корреляцию (r = 0,91) с результатами, полученными в модифицированных вариантах ИФА, что подтверждает адекватность применения ИФА для измерения уровня антитоксического иммунитета к дифтерии у здоровых людей.
5.3.1. Определение уровня противодифтерийных АТ
с помощью тест-системы ИФА
1. Приготовить разведения исследуемых сывороток 1:20, 1:200, 1:2000 на буферном растворе № 1 (содержимое флакона концентрата ФСБ-Т×25 развести в 600 мл дистиллированной вода, содержимое флакона с блокатором растворить в 5,0 мл дистиллированной воды, полученный раствор добавить в емкость с раствором ФСБ-Т и тщательно перемешать) в макропланшете непосредственно перед использованием.
2. Приготовить непосредственно перед использованием рабочие разведения: отрицательной сыворотки - 1:20, добавляя в содержимое флакона (0,2 мл) 3,8 мл буферного раствора; положительной сыворотки - 1:200 (отмерить 0,01 мл растворенного К+ и добавить 2,0 мл раствора № 1), из которого затем приготовить отдельно каждое разведение - 1:2, 1:4, 1:8 и 1:16 (в итоге получить пять разведений К+ - 1:200, 1:400, 1:800, 1:1 600 и 1:3200).
3. Полистироловые планшеты с иммунобилгоированным антитоксином трижды отмыть буферным раствором (в объеме 0,3 мл в каждую лунку), удалить буферный раствор, постукивая по сложенной в несколько слоев фильтровальной бумаге, помещенной на поддон.
7. Удалить жидкость из лунок, планшеты промыть, как указано в пункте 5.
8. Внести в каждую лунку планшета по 0,2 мл раствора ТМБ (готовят непосредственно перед внесением в лунки планшетов). Для этого содержимое флакона с ТМБ перенести во флакон с ЦФБР и тщательно перемешать. Раствор готовить в защищенном от прямых солнечных лучей месте. Планшет выдержать при температуре (20 ± 2) °С в течение 20 мин в защищенном от света месте.
9. Реакцию остановить добавлением в каждую лунку по 0,1 мл стоп-реагента (СР).
5.3.2. Определение индекса авидности противодифтерийных
антитоксических антител
1. Внести контрольные и исследуемые образцы. После внесения контролем К+, К- и раствора № 1 добавить КА+, КА- и все испытуемые сыворотки в двух повторностях (одну повторность КА+, КА- и рабочие сыворотки промыть раствором № 1, а вторую - 3М раствором калия роданистого). Планшет герметично закрыть и выдержать (60 ± 5) мин при температуре (37 ± 1) °С. следуя инструкции к набору дата ИФА. Затем содержимое лунок собрать в сосуд с дезинфицирующим раствором (5 - 6 % раствор монохлорамина).
2. Первая промывка планшета.
Контроли К+, К- и первую повторность КА+, КА- и рабочих сывороток промыть 5 раз раствором № 1, вторую повторность КА+, КА- и рабочих сывороток промыть 4 раза 3МКрод, а 5-й раз - раствором № 1.
3. Далее все этапы реакции выполнить согласно основной инструкции к набору.
Регистрация и оценка результатов
Результаты ИФА регистрируют на спектрофотометре при двух длинах волн 450/620 нм.
Индекс авидности (ИА) рассчитывают по формуле:
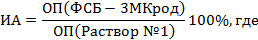
ОП(ФСБ - 3МКрод) - оптическая плотность в лунках, обработанных раствором детергента (ФСБ-3МКрод), ОП(Раствор № 1) - оптическая плотность в лунке, обработанной обычным промывочным раствором, используемым в тест-системе (раствор № 1).
КА+ должен содержать высокоавидные противодифтерийные антитоксические антитела с индексом авидности не менее 90 %. КА- должен содержать низкоавидные противодифтерийные антитоксические антитела с индексом авидности не более 10 %.
Индекс авидности рабочих сывороток более 30 % соответствует вероятности защиты от заболевания дифтерией на 95 %, а индекс авидности 10 % является показателем критического уровня, ниже которого вероятность заболевания возрастает до 99 %.
1. Показатель ОП рабочей сыворотки в лунке, обработанной ФСБ-3МКрод, равен 0,24, а в лунке, обработанной раствором № 1, равен 0,37. Индекс авидности, рассчитанный по приведенной формуле, равен 65 %, что соответствует высокой степени защиты от дифтерии (более 30 %).
2. Показатель ОП рабочей сыворотки в лунке, обработанной ФСБ-3МКрод, равен 0,05, а в лунке, обработанной раствором № 1, равен 0,62. Индекс авидности, рассчитанный по приведенной формуле, равен 8 %, что соответствует низкой степени защиты от дифтерии (менее 10 %).
6.1. Оценка индивидуальной защищенности
от дифтерийной инфекции
Этап 1. Отобрать кровь у обследуемого в пробирку с активатором свертывания. Внести в систему баз данных информацию об обследуемом по форме (табл. 1).
Профессия или учебное заведение
Наличие хронического или острого заболевания
Есть или нет подозрение на дифтерию
Этап 2. Определить с помощью ИФА тест-системы и 3М роданистого калия количество противодифтерийных антитоксических антител, выраженное в МЕ/мл, и индекс авидности антител, выраженный в %. Количество антител рассчитать по данным оптической плотности в лунках планшета с помощью компьютерной программы, входящей в качестве приложения к тест-системе. Индекс авидности (ИА) антител рассчитать по формуле;
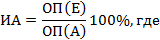
ОП(Е) - оптическая плотность в лунке, обработанной детергентом, ОП(А) - оптическая плотность в лунке, обработанной обычным промывочным раствором, используемым в тест-системе.
Этап 3. Сделать прогноз защищенности обследуемого на будущее. Поскольку авидность антител, защищающая от заболевания дифтерией, снижается быстрее, чем количественный показатель суммарных антител, то в прогнозе необходимо ориентироваться на индекс авидности антител. Для этого найти на графике (рис. 1) значение, наиболее приближенное к полученному индексу авидности антител (с учетом прошлой вакцинации, если она была проведена в ближайший год), и определить по графику, через сколько месяцев индекс авидности снизится до критической отметки (10 %). Очередную ревакцинацию (или повторное исследование) рекомендуется пройти до этой даты.
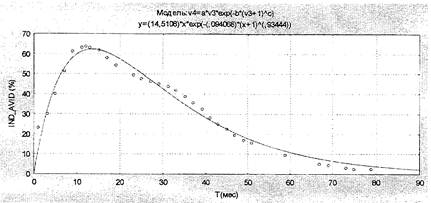
Рис. 1. Математическая модель из исходных данных
о динамике индексов авидности после ревакцинации
Примечания. IND_AVID (%) - индексы авидности (%), Т (мес.) - время после ревакцинации (месяцы). Средняя погрешность модели = 5 %.
6.2. Оценка коллективной защищенности
от дифтерийной инфекции
Этап 1. Определить контингент для изучения напряженности иммунитета к дифтерии с учетом групп риска. Исследование лучше проводить спустя 3 - 5 лет после очередной ревакцинации. Отобрать кровь для исследования. Заполнить индивидуальную информацию в базе данных для каждого обследуемого
Этап 2. Определить индивидуальные показатели защищенности от дифтерии и рассчитать вероятность заболевания на момент обследования. Затем определить средние показатели для всей группы обследованных.
Этап 3. Определить прогноз для всего коллектива в отношении динамики авидности антитоксических антител. Рассчитать сроки очередного обследования или вакцинации.
Все рекомендуемые мероприятия не идут в разрез с нормативными документами по вакцинопрофилактике и контролю иммунитета, а предполагают индивидуальный подход ко всем обследуемым лицам и повышенное внимание к представителям из групп риска.
1. Стандартное оборудование клинических лабораторий для взятия крови.
2. Стандартное оборудование для проведения серологических реакций.
3. Ламинарный или настольный бокс, ТУ 9452003-215-04087-5.
4. Фотометр микропланшетный (ридер).
1. Алексеева Е.А. Оптимизация мониторинга противодифтерийного иммунитета детей в Вологодской области/Е.А. Алексеева, Д.А. Краева, Г.Я. Ценева, Г.И. Беспалова//Материалы X Съезда ВНПОЭМП, Инфекция и иммунитет. Москва, 2012. № 2. С. 77 - 78.
2. Алексеева Е.А. Эффективность высокоавидных антитоксических антител в оценке невосприимчивости к дифтерийной инфекции/Е.А. Алексеева, Л.А. Краева. Г.Я. Ценева, А.М. Николаева//Профилактическая и клиническая медицина. 2011. № 1. С. 38.
4. Краева Л.А. Качественные показатели антитоксических антител в оценке противодифтерийного иммунитета/Л.А. Краева, Ф.С. Носков, Г.Я. Ценева//Ж. мед. иммунол. С.-Пб., 2005. Т. 7. № 2 - 3. С. 274.
7. Краева Л.А. Роль высокоавидных антитоксических антител в оценке невосприимчивости к дифтерийной инфекции/Л.А. Краева, Г.Я. Ценева, А.М. Николаева, Е.А. Алексеева//Эпидемиология и инфекционные болезни. 2011. № 4. С. 20 - 24.
12. Ценева Г.Я. Уровень антитоксического противодифтерийного иммунитета у населения Северо-Западного окрута РФ и пути оптимизации мониторинга инфекции/Г.Я. Ценева, Л.А. Краева, Е.Е. Щедеркина//Эпидемиология и вакцинопрофилактика. 2010. № 5 (54). С. 51 - 54.
14. Efsltatiou A., Maple Р.А.С. Manual for the laboratory diagnosis of diphtheria. Copenhagen//The Expanded Programme on Immunization in the European Region of WHO. 1994 (ICP/EPI038).
Читайте также:


